文档内容
考点 42 分子结构与性质
【基础过关】
1.下列关于σ键和π键的理解不正确的是( )
A.含有π键的分子在进行化学反应时,分子中的π键比σ键活泼
B.在有些分子中,共价键可能只含有π键而没有σ键
C.有些原子在与其他原子形成分子时只能形成σ键,不能形成π键
D.当原子形成分子时,首先形成σ键,可能形成π键
【答案】B
【解析】同一分子中的π键不如σ键牢固,反应时比较容易断裂,A项正确;在共价单键中只含有σ
键,而含有π键的分子中一定含有σ键,B项错误、D项正确;氢原子、氯原子等跟其他原子形成分子时
只能形成σ键,C项正确。
2.下列反应中既有离子键、极性共价键、非极性共价键的断裂又有其形成的反应是( )
A.NH Cl NH ↑+HCl B.2NaO+2H O = 4NaOH+O ↑
4 3 2 2 2 2
C.2Al+2NaOH+2H O=2NaAlO +3H ↑ D.2NaOH+Cl =NaCl+NaClO+H O
2 2 2 2 2
【答案】B
【解析】A项,该反应中没有非极性共价键的断裂,A项不符合题意;B项,该反应中钠离子和过氧
根之间的离子键断裂,钠离子和氢氧根之间的离子键形成,过氧根中非极性键断裂,氧气中非极性键形成,
水中极性键断裂,氢氧根中极性键形成,B项符合题意;C项,该反应中没有非极性共价键的断裂,C项
不符合题意;D项,该反应中没有非极性共价键的形成,D项不符合题意;故选B。
3.下列有关化学键知识的比较肯定错误的是( )
A.键能:C—N<C===N<C≡N
B.键长:I—I>Br—Br>Cl—Cl
C.分子中的键角:HO>CO
2 2
D.相同元素原子间形成的共价键键能:σ键>π键
【答案】C
【解析】C、N原子间形成的化学键,三键键能最大,单键键能最小,A正确;原子半径:I>Br>
Cl,则键长:I—I>Br—Br>Cl—Cl,B正确;HO分子中键角是105°,CO 分子中键角是180°,C错误;
2 2
相同元素原子之间形成的σ键的键能比π键的大,D正确。
4.NF 是微电子工业中一种优良的等离子蚀刻气体,可通过电解熔融氟化氢铵(NH HF )制得。下列有
3 4 2
关说法错误的是( )
A.NF 的空间构型为平面三角形
3
B.相关元素电负性由大到小的顺序为F>N>H
C.NF 和NH HF 中N原子的杂化方式均为sp3
3 4 2
资料整理【淘宝店铺:向阳百分百】D.NH HF 晶体中微粒间的作用有离子键、共价键、配位键、氢键
4 2
【答案】A
【解析】A项,NF 分子中N的周围形成3个σ键,孤电子对数= ,故其价层电子对为4,
3
故其的空间构型为三角锥形,A项错误;B项,同一周期从左往右元素的电负性依次增大,同一主族从上
往下依次减小,故相关元素电负性由大到小的顺序为,B项正确;C项,NF 分子中N的周围形成3个σ键,
3
孤电子对数= ,故其价层电子对为4,NH HF 中NH +周围有4个σ键,孤电子对数=
4 2 4
,故其价层电子对为4,NF 和NH HF 中N原子的杂化方式均为sp3,C项正确;D项,
3 4 2
NH HF 晶体中NH +与HF -微粒内存在共价键和配位键,微粒间存在离子键,且HF -与HF -微粒间存在氢
4 2 4 2 2 2
键,D项正确;故选A。
5.一定条件下发生反应:Fe+6HCN+2KCO=K [Fe(CN) ]+H↑+2CO↑+2HO。下列说法正确的是
2 3 4 6 2 2 2
( )
A.K[Fe(CN) ]的中心原子的核外电子排布式为[Ar]3d5
4 6
B.该反应中只存在离子键和共价键的断裂和形成
C.HCN、CO、CO2-中碳的杂化方式和空间构型均相同
2 3
D.HCN 水溶液中存在 4 种氢键
【答案】D
【解析】A项,K[Fe(CN) ]的中心原子为Fe,核外电子排布式为[Ar]3d64S2,A错误;B项,反应存在
4 6
离子键、共价键的断裂和形成,还有配位键的形成,B错误;C项,HCN为 sp杂化,CO 为 sp杂化,碳
2
酸根离子中心原子属于sp2杂化,C错误;D项,HCN 水溶液中存在 4 种氢键,H-CN······H-CN、
HO········H-CN、H-CN·········H-O-H、HO·······H-O-H ,D正确;故选D。
2 2
6.甲醛分子式为CHO,有强烈刺激性气味,甲醛在常温下是气态,已被世界卫生组织确定为致癌和
2
致畸形物质。下列关于其结构及性质的分析正确的是( )
A.C原子采取sp3杂化,O原子采取sp杂化
B.甲醛分子中中心原子价层电子对数为4,含有一对孤电子对,是三角锥形结构
C.一个甲醛分子中含有3个σ键和1个π键
D.甲醛分子为非极性分子
【答案】C
【解析】一个甲醛分子中含有两个碳氢键,一个碳氧双键,C原子采取sp2杂化,氧原子形成一个碳氧
双键,含有2对孤电子对,O原子采取sp2杂化,A项错误;甲醛分子中中心原子价层电子对数为3,不含
资料整理【淘宝店铺:向阳百分百】孤电子对,是平面三角形结构,B项错误;一个甲醛分子中含有两个碳氢键、一个碳氧双键,双键含有一
个σ键和一个π键,所以共含有3个σ键和1个π键,C项正确;甲醛分子为平面三角形结构,碳原子位于
三角形内部,空间结构不对称,所以为极性分子,D项错误。故选C。
7.CHOH、NH 和(CH)NNH 均为常见的燃料,关于这三者的结构与性质,下列说法错误的是(
3 2 4 3 2 2
)
A.CHOH的电子式为
3
B.NH 空间结构为平面形
2 4
C.CHOH、NH 和(CH)NNH 都易溶于水
3 2 4 3 2 2
D.CHOH和(CH)NNH中C、O、N杂化方式均相同
3 3 2
【答案】B
【解析】A项,甲醇可看成是甲烷中的一个氢原子被羟基取代得到的,CHOH的电子式为 ,
3
A正确;B项,NH 中N原子的杂化方式为sp3,不是平面形,B错误;C项,CHOH、NH 和(CH)NNH
2 4 3 2 4 3 2 2
都能和水分子形成氢键,都易溶于水,C正确;D项,CHOH为四面体结构,-OH结构类似于水的结构,
3
(CH)NNH 的结构简式为 ,两者分子中C、O、N杂化方式均为sp3,D正确;故选B。
3 2 2
8.徐光宪在《分子共和国》一书中介绍了许多明星分子,如 HO 、CO 、BF 、CHCOOH等。下列
2 2 2 3 3
说法正确的是( )
A.HO 分子中的O为sp2杂化 B.CO 分子中C原子为sp1杂化
2 2 2
C.BF 分子中的B原子为sp3杂化 D.CHCOOH分子中C原子均为sp2杂化
3 3
【答案】B
【解析】A项,HO 分子中氧原子形成2个σ键,含有2对孤电子对,采取sp3杂化,错误;B项,
2 2
CO 分子中C原子形成2个σ键,没有孤电子对,采取sp1杂化,正确;C项,BF 分子中的B原子的最外
2 3
层电子数为3,形成3个σ键,没有孤电子对,采取sp2杂化,错误;D项,CHCOOH分子中有2个碳原
3
子,其中甲基上的碳原子形成4个σ键,没有孤电子对,采取sp3杂化,错误。
9.了解有机物分子中化学键特征以及成键方式是研究有机物性质的基础。下列关于有机物分子成键
方式的描述不正确的是( )
A.烷烃分子中碳原子均采取sp3杂化成键
B.炔烃分子中的碳碳三键由1个σ键、2个π键组成
资料整理【淘宝店铺:向阳百分百】C.苯分子中所有碳原子均采取sp2杂化成键,苯环中存在6个碳原子共有的大π键
D.甲苯分子中所有碳原子均采取sp2杂化成键
【答案】D
【解析】烷烃分子中碳原子均采取sp3杂化成键,由甲烷得到的甲基上的碳原子也采取sp3杂化,A正
确、D错误;三键一定是由1个σ键、2个π键组成的,B正确;苯环上的碳原子都采取sp2杂化,C正确。
10.NF 是微电子工业中一种优良的等离子蚀刻气体,可通过电解熔融氟化氢铵(NH HF )制得。下列
3 4 2
有关说法错误的是( )
A.NF 的空间构型为平面三角形
3
B.相关元素电负性由大到小的顺序为F>N>H
C.NF 和NH HF 中N原子的杂化方式均为sp3
3 4 2
D.NH HF 晶体中微粒间的作用有离子键、共价键、配位键、氢键
4 2
【答案】A
【解析】A项,NF 分子中N的周围形成3个σ键,孤电子对数= ,故其价层电子对为4,
3
故其的空间构型为三角锥形,A项错误;B项,同一周期从左往右元素的电负性依次增大,同一主族从上
往下依次减小,故相关元素电负性由大到小的顺序为,B项正确;C项,NF 分子中N的周围形成3个σ键,
3
孤电子对数= ,故其价层电子对为4,NH HF 中NH +周围有4个σ键,孤电子对数=
4 2 4
,故其价层电子对为4,NF 和NH HF 中N原子的杂化方式均为sp3,C项正确;D项,
3 4 2
NH HF 晶体中NH +与HF -微粒内存在共价键和配位键,微粒间存在离子键,且HF -与HF -微粒间存在氢
4 2 4 2 2 2
键,D项正确;故选A。
11.催化剂作用下,SO 与Cl 反应生成SO Cl;对SO 水溶液的光谱分析可以检测到HSO -、SO2-和
2 2 2 2 2 3 2 3
痕量的SO 2-,三氧化硫在液态时有单分子SO 和三聚的(SO )(结构如下图所示)两种形式,在高温时能将
3 3 3 3
HBr氧化为Br 。关于说法正确的是( )
2
A.SO 、SO 都是非极性分子
2 3
B.SO Cl 为正四面体结构
2 2
C.SO 、SO 2-中S原子都是sp2杂化
3 3
资料整理【淘宝店铺:向阳百分百】D.1 mol (SO ) 分子中含有12 mol σ键
3 3
【答案】D
【解析】A项,SO 分子中正负电荷重心不重合,因此属于极性分子,而SO 分子中正负电荷重心重
2 3
合,因此该分子属于非极性分子,A错误;B项,SO Cl 分子中与中心S原子形成共价键的O、Cl原子半
2 2
径不同,因此该分子呈四面体结构,但不是正四面体结构,B错误;C项,SO 分子中的中心S原子价层电
3
子对数为3+ =3,则S原子是sp2杂化;SO 2-中S原子价层电子对数是3+ =4,因此S原子杂
3
化类型是sp3杂化,C错误;D项,根据(SO ) 分子结构可知:在1个(SO ) 分子中含有12个σ键,则在1
3 3 3 3
mol (SO ) 分子中含有12 mol σ键,D正确;故选D。
3 3
12.(2023·浙江省衢州市期末)SO 及其三聚体环状结构如图所示。下列说法不正确的是( )
3
A.SO 与CO2-、NO -互为等电子体,空间结构都为平面三角形
3 3 3
B.SO 为非极性分子,中心原子杂化类型sp3
3
C.三聚体环状结构中S与O形成的共价键的键长有a、b两类
D.该三聚体环状结构中含有12个σ键
【答案】B
【解析】A项,具有相同价电子数和相同原子数的分子或离子是等电子体,则SO 与CO2-、NO -互为
3 3 3
等电子体,等电子体具有相同的结构特征,它们的中心原子孤电子对数=0、价层电子对数=3+0=3,故为
sp2杂化、空间结构都为平面三角形,A正确;B项,结合选项A可知SO 中心原子杂化类型sp2,B不正确;
3
C项,由图知:三聚体环状结构中S与O形成的共价键的键长有a、b两类,C正确;D项,该三聚体环状
结构中每个S原子形成4个σ键,则分子内含有12个σ键,D正确;故选B。
13.氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反
应为N(g)+3H(g) 2NH (g)ΔH=-92.4kJ·mol-1。实验室用加热NH Cl和Ca(OH) 固体混合物的方法制取
2 2 3 4 2
少量氨气;侯氏制碱法用氨气、二氧化碳,与饱和食盐水制备纯碱碳酸钠。下列有关NH 、NF 、NH +、
3 3 4
NO -、NO -等含氮粒子的说法正确的是( )
2 3
A.NH 中N-H键角比NH +中N-H键角大
3 4
B.NH 极易溶于水,主要原因是NH 分子间能形成氢键
3 3
C.NH 的水溶液能导电,但一水合氨不能完全电离,因此NH 属于弱电解质
3 3
资料整理【淘宝店铺:向阳百分百】D.NH 、NF 的空间构型都是三角锥型,NO -、NO -中的N都是sp2杂化
3 3 2 3
【答案】D
【解析】A项,分子中中心原子上的孤电子对数越多,键角越小,故NH 中N-H键角比NH +中N-H
3 4
键角小,故A错误;B项,NH 极易溶于水,主要原因是NH 分子与水分子间能形成氢键,故B错误;C
3 3
项,NH 自身不能电离,NH 是非电解质,故C错误;D项,NH 、NF 均为sp3杂化,一个孤电子对,故
3 3 3 3
为三角锥形,NO 的价层电子对数为2+ =3,NO -的价层电子对数为3+ =3,故N原子
3
都是sp2杂化,故D正确;故选D。
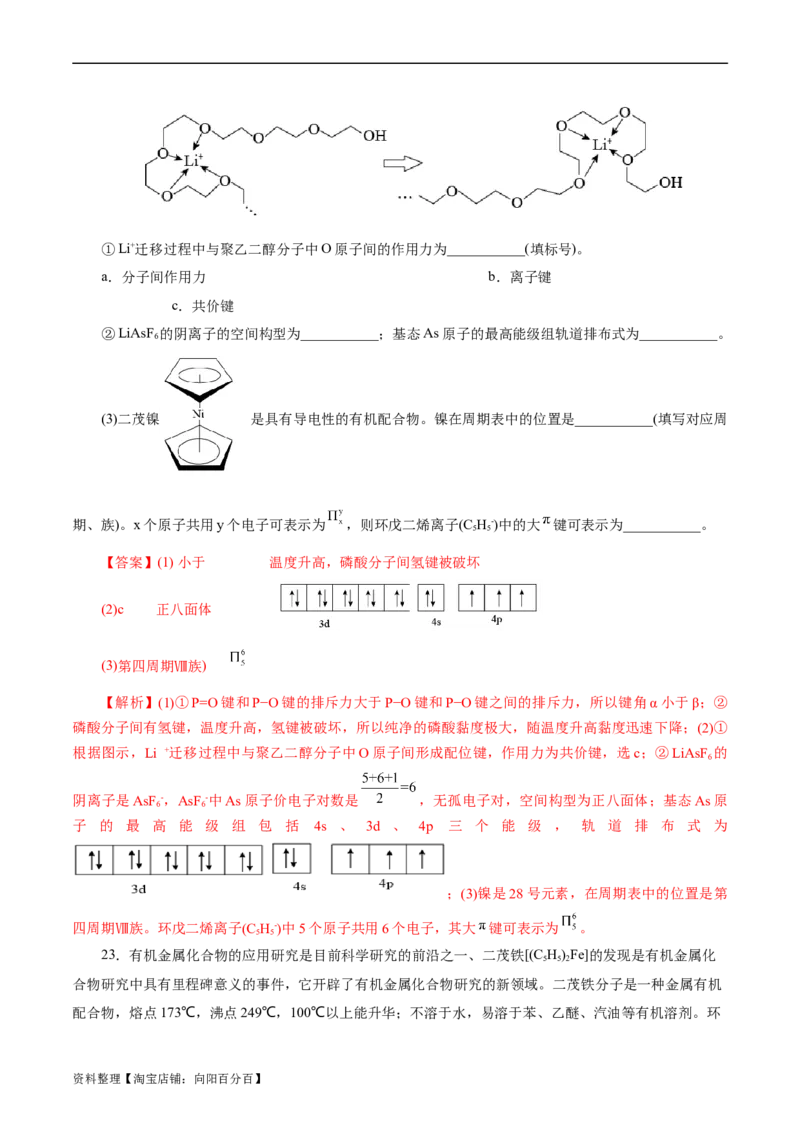
14.铜有Cu(Ⅰ)和Cu(Ⅱ)两种离子,铜的离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热
点。铜的离子可与多种配体形成配位化合物,有一种配离子结构如图。下列有关说法中错误的是( )
A.该配离子中所含基态铜离子的价层电子排布图为
B.该离子的配体中,N原子采用了sp2和sp3两种杂化方式
C.该配离子中铜的配位数和所含配位键的数目均为4
D.从核外电子排布角度分析,稳定性:Cu(Ⅰ)<Cu(Ⅱ)
【答案】D
【解析】A项,该配离子中铜离子为+1价,所以价层电子排布图为 ,A正确;B项,
该离子的配体中,N原子采用了sp2和sp3两种杂化方式,B正确;C项,由图可知铜离子配位数和每个离
子所含配位键数均为4,C正确;D项,由于Cu(Ⅰ)的3d轨道全充满,所以更稳定,故D错误。故选D。
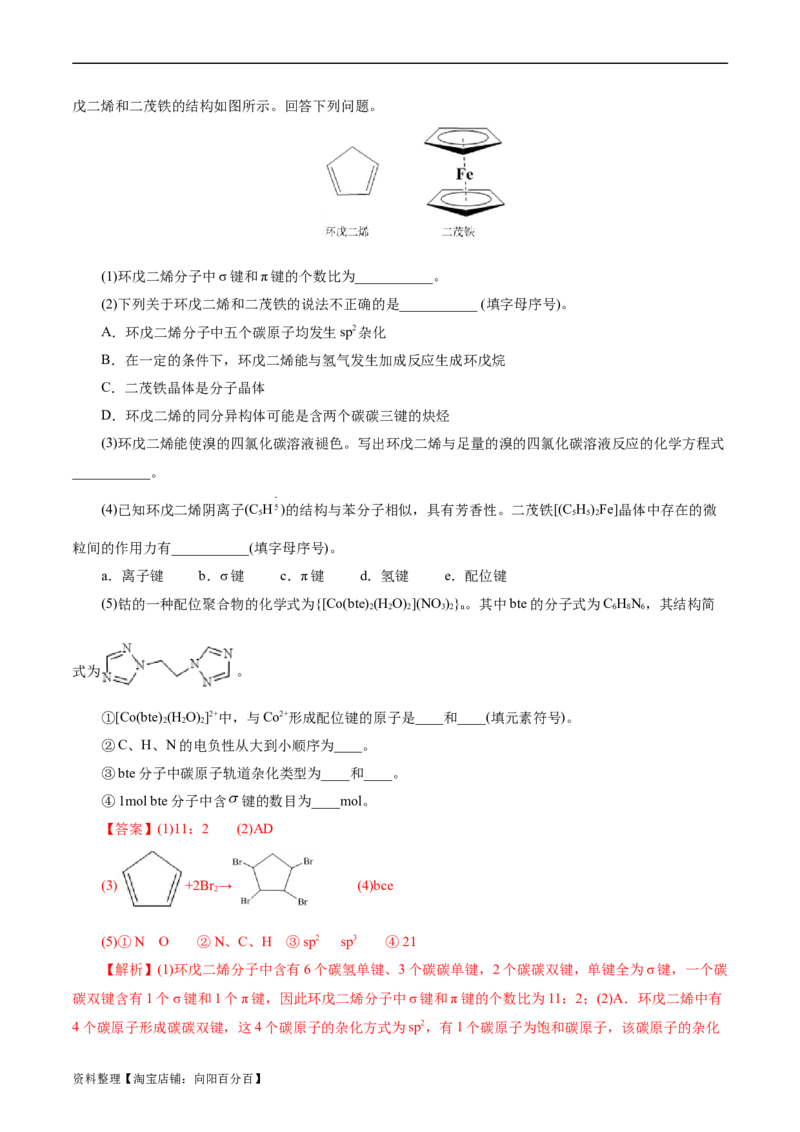
15.某种硫化橡胶的部分结构如图所示。下列说法错误的是( )
资料整理【淘宝店铺:向阳百分百】A.图中元素位于s区和p区的种数之比为1:2
B.基态硫原子和碳原子最高能级电子云轮廓图均为哑铃形
C.图中的硫原子和碳原子共有两种杂化方式
D.图示结构中含有σ键、π键和氢键等作用力
【答案】D
【解析】A项,位于s区的元素有H元素,位于p区的元素有C、S元素,则图中元素位于s区和p区
的种数之比为1:2,A正确;B项,p能级的电子电子云轮廓图为哑铃形,s能级的电子电子云轮廓图为球
形,基态S原子最高能级为3p能级、基态C原子最高能级为2p能级,所以电子云轮廓图都是哑铃形,B
正确;C项,连接双键的碳原子采用sp2杂化,价层电子对数是4的碳原子、硫原子采用sp3杂化,所以
C、S原子共有两种杂化方式,C正确;D项,图中不存在氢键,存在σ键、π键,D错误;故选D。
16.已知运送卫星的火箭所需燃料除液态HO 外,还有另一种液态氮氢化合物。已知该化合物中氢元
2 2
素的质量分数为12.5%,相对分子质量为32,结构分析发现该化合物分子中只有单键。
(1)该氮氢化合物的电子式为 ,其中N原子采取 杂化,该分子是 (填“极
性”或“非极性”)分子。
(2)若该物质与液态HO 反应,产生两种无毒又不污染环境的物质,在该反应的反应物和生成物中既
2 2
含有极性键又含有非极性键的是 (填化学式,下同),只含有非极性键的是 ,只含
有极性键的是 。
(3)已知NH 分子中的N原子有一对孤电子对,能发生反应:NH+HCl=NH Cl。试写出将上述液态氮氢
3 3 4
化合物加入足量盐酸中时,发生反应的化学方程式: 。
H H
【答案】(1)H··········H sp3 极性 (2)N H 和HO N HO
N N 2 4 2 2 2 2
·· ··
(3)N H+2HCl= N HCl
2 4 2 6 2
【解析】(1)由该物质的相对分子质量和氢元素的质量分数可知其分子式为NH,分子中的键全部是单
2 4
键,它的结构可看作是NH 分子中的一个H原子被—NH 取代后所得,故N原子的杂化方式与NH 分子中
3 2 3
的N原子杂化方式相同,是sp3杂化,该分子为极性分子。(2)N H 与HO 反应后得到N 和HO,两种反
2 4 2 2 2 2
应物中都含有极性键和非极性键,在生成物HO中只含有极性键,N 中只含有非极性键。(3)因为在NH
2 2 2 4
分子的每个N原子上各有一对孤电子对,故一分子NH 能与两分子HCl反应。
2 4
17.硅及其化合物在生产生活中有广泛应用。根据所学知识,回答下列问题:
资料整理【淘宝店铺:向阳百分百】(1)三甲基卤硅烷【(CH)SiX,X为Cl、Br、I】是重要的化工原料。
3 3
①氯元素基态原子的价电子排布式为___;按照核外电子排布对元素周期表分区,溴元素位于___区;
基态硅原子中有____种运动状态不同的电子。
②Br、I的第一电离能的大小关系:I(Br)____I (I)(填“大于”“小于”或“等于”)。
1 1
③常温下,(CH)SiI中Si—I键比(CH)SiCl中Si—Cl键易断裂的原因是____。
3 3 3 3
(2)(CH )SiCl可作为下列有机合成反应的催化剂。
3 3
①1个有机物A分子中采取sp2杂化的碳原子有____个。
②有机物B的沸点低于对羟基苯甲醛( )的沸点,其原因是____。
③CHCN中σ键与π键的个数比为____。
3
【答案】(1) 3s23p5 p 14 大于 I原子半径比Cl的原子半径大,导致Si-I键键能较小,
较易断裂;而Si-Cl键键能较大,较不易断裂
(2) 7 邻羟基苯甲醛主要形成分子内氢键,而对羟基苯甲醛只能形成分子间氢键,所以后者的熔点
高于前者 5:2
【解析】(1)①Cl原子核外有17个电子,核外电子排布式为[Ne] 3s23p5,价电子为3s23p5;溴原子的价
电子为4s24p5,属于p区;硅原子核外有14个电子,每个电子的运动状态各不相同,即有14种运动状态不
同的电子;②同主族自上而下第一电离能减小,所以I(Br)大于I(I);③I原子半径比Cl的原子半径大,导
1 1
致Si-I键键能较小,较易断裂;而Si-Cl键键能较大,较不易断裂;(2)①苯环上的碳原子以及碳氧双键中
的碳原子为sp2杂化,共有7个;②B为邻羟基苯甲醛,羟基与醛基距离较近,主要形成分子内氢键,而
对羟基苯甲醛只能形成分子间氢键,分子间氢键可以增大熔点,所以后者的熔点高于前者;③单键均为σ
键,碳氮三键中有一个σ键、两个π键,所以σ键与π键的个数比为5:2。
【能力提升】
18.离子液体是在室温或接近室温时呈液态的盐类物质,应用广泛。1-乙基-3-甲基咪唑四氟硼酸盐离
子液体结构如图所示,下列相关叙述错误的是( )
A.该离子液体中C、N杂化方式均有sp2和sp3两种
B.阴离子呈正四面体形,存在共价键和配位键
C.阳离子中σ键数目是π键数目的10倍
资料整理【淘宝店铺:向阳百分百】D.该离子液体与水能够形成氢键
【答案】C
【解析】A项,该离子液体中根据C原子接的化学键有1个双键判断应采用的是sp2杂化,还有碳原子
接的是四个单键,判断采用的是sp3杂化。N原子接的有1个双键判断是sp2杂化,另一个N原子接的都是
单键判断是sp3,故A正确;B项,阴离子BF-中的B原子采用sp3杂化,根据VSEPR模型判断空间构型是
4
正四面体。根据杂化理论判断B原子中有空轨道,F-有孤对电子,故还含有配位键,故B正确;C项,根
据单键是σ键,双键是π键判断该物质中含有σ键是19个,π键2,σ键数目不是π键数目的10倍。故C
错误;D项,该物质中含有电负性大的N和F原子故能与水中的氢原子形成氢键,故D正确。
19.[Zn(CN) ]2-在水溶液中可与HCHO发生反应生成[Zn(HO) ]2+和HOCH CN,下列说法错误的是(
4 2 4 2
)
A.Zn2+基态核外电子排布式为[Ar]3d10
B.1mol HCHO分子中含有σ键的数目为1.806×1024
C.HOCH CN分子中碳原子轨道的杂化类型是sp3
2
D.[Zn(CN) ]2-中Zn2+与CN-的C原子形成配位键,结构可表示为
4
【答案】C
【解析】A项,Zn原子序数为30,位于ⅡB族,所以,Zn2+基态核外电子排布式为[Ar]3d10,A正确;
B项,1分子HCHO含2个C-H键和1个C=O键,共有3个σ键,所以,1molHCHO分子中含有σ键的物
质的量为3mol,数目为1.806×1024,B正确;C项,HOCH CN分子中与羟基相连的C为sp3杂化,-CN(-
2
C≡N)中的C为sp杂化,C错误;D项,[Zn(CN) ]2-中Zn2+与CN-的C原子形成配位键,Zn为sp3杂化,配
4
位原子形成正四面体,所以,[Zn(CN) ]2-结构可表示为 ,D正确;故选C。
4
20.氮是一种典型的非金属元素,其单质及化合物在生活和生产中具有广泛的用途。回答下列问题:
(1)磷元素与氮元素同主族,基态磷原子有________个未成对电子,白磷的分子式为P ,其结构如图甲
4
所示。科学家目前合成了 N 分子,N 分子中氮原子的杂化轨道类型是________,N—N—N 键角为
4 4
________;N 分解后能产生N 并释放出大量能量,推测其用途可为________。
4 2
资料整理【淘宝店铺:向阳百分百】(2)NH 与Zn2+可形成[Zn(NH )]2+,其部分结构如图乙所示。
3 3 6
①NH 的空间构型为________。
3
②[Zn(NH )]2+中存在的化学键类型有________;NH 分子中H—N—H键角为107°,判断[Zn(NH )]2+
3 6 3 3 6
离子中H—N—H键角________(填“>”“<”或“=”)107°。
③肼(N H)可视为NH 分子中的一个氢原子被—NH 取代形成的另一种氮的氢化物。与NH 互为等电
2 4 3 2 2 4
子体的分子有________(写出一种即可)。
【答案】(1)3 sp3 60° 用于制造火箭推进剂或炸药(其他合理答案也可)
(2)①三角锥形 ②配位键、共价键 > ③CHOH(或CHSH等)
3 3
【解析】(1)磷原子的价电子排布式为3s23p3,基态原子有3个未成对电子;N 分子与P 分子的结构相
4 4
似,为正四面体形,N 分子中每个氮原子形成3个σ键、含有1对孤电子对,杂化轨道数目为4,氮原子
4
采取sp3杂化;正四面体中的每个面为正三角形,则 N—N—N键角为60°;N 分解后能产生N 并释放出大
4 2
量能量,可以用于制造火箭推进剂或炸药。(2)①NH 中氮原子形成3个σ键,有1对未成键的孤电子对,
3
杂化轨道数为4,采取sp3杂化,分子空间构型是三角锥形。②[Zn(NH )]2+中存在的化学键类型有配位键、
3 6
共价键,受配位键的影响,[Zn(NH )]2+中H—N—H键角大于107°。③等电子体是指原子总数相同、价电
3 6
子总数相同的分子或离子。与NH 互为等电子体的分子有CHOH、CHSH等。
2 4 3 3
21.黄铜矿(主要成分为CuFeS)是生产铜、铁和硫酸的原料。回答下列问题:
2
(1)基态Cu原子的价电子排布式为________。
(2)从原子结构角度分析,第一电离能 I(Fe)与 I(Cu)的关系是:I(Fe)________(填“>”“<”或
1 1 1
“=”)I(Cu)。
1
(3)血红素是吡咯(C HN)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构
4 5
如下图:
①已知吡咯中的各个原子均在同一平面内,则吡咯分子中N原子的杂化类型为________。
②1 mol吡咯分子中所含的σ键总数为________个。分子中的大π键可用Π表示,其中m代表参与形
成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为________。
③C、N、O三种元素的简单氢化物中,沸点由低到高的顺序为________(填化学式)。
④血液中的O 是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的 Fe2+与O 是通过
2 2
________键相结合的。
资料整理【淘宝店铺:向阳百分百】(4)黄铜矿冶炼铜时产生的SO 可经过SO →SO →HSO 途径形成酸雨。SO 的空间构型为________。
2 2 3 2 4 2
HSO 的酸性强于HSO 的原因是________________________________。
2 4 2 3
【答案】(1)3d104s1 (2)>
(3)①sp2 ②10N Π ③CHI(Cu)。(3)①已知吡咯中的氮原子及与其相连的原子均在同一平面内且为平面
1 1
三角形,则吡咯分子中N原子的杂化类型为sp2。②根据分子结构可知1 mol吡咯分子中有8 mol单键、2
mol 双键,所以所含的σ键总数为10N ;吡咯环分子中形成大π键的原子数为5个;氮原子中未参与成键
A
的电子为1对,碳碳原子间除了形成σ键外,还有4个碳分别提供1个电子形成π键,共有电子数为6,所
以吡咯环中的大π键应表示为Π。③CH 分子间无氢键,沸点最低,而NH 、HO分子间均含氢键,由于
4 3 2
氧原子的电负性大于氮原子,所以HO分子间氢键较强,水的沸点最高;因此,三种氢化物的沸点由低到
2
高的顺序为CH