文档内容
考点 42 分子结构与性质
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
2023山东卷16(2)题,12分;2022海南卷11题,4分;2022全国乙卷
共价键及键参数
35(2)题,15分;2021河北卷17(3)(4)(5)(6)题,15分;
2023湖北卷9题,3分;2023浙江1月选考17(1)题,3分;2023北京
卷15(3)题,10分;2022湖北卷11题,3分;2022辽宁卷8题,3分;
分子的空间结构 2022河北卷17(3)题,15分;2022湖南卷18(3)题,15分;2022广东卷
20(2)(4)(5)题,14分;2021全国乙卷35(3)题,15分;2021全国甲卷
35(1)(2)(3)题,15分;2021海南卷19(4)题,14分;
2023山东卷3题,2分;2023北京卷10题,3分;2023浙江1月选考
12题,3分;2023浙江6月选考17(2)题,10分;2023湖南卷4题,3
分;2023湖北卷11题,3分;2023全国乙卷35(2)题,15分; 2022湖
微粒间作用力 北卷10题,3分;2022山东卷5题,2分; 2022全国甲卷35(3)题,15
分;2022海南卷19(3)题,14分;2022福建卷14题,10分;2022山东
卷16题,12分;2021湖北卷9题,3分;2021海南卷10题,4分;
2021山东卷19题,12分;2021湖南卷18(2)题,15分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,本知识点在全国卷中为选考题考查内容,近年来已有较多省市已列入高考必
考题,重点考查从不同层次认识分子的构型,并对共价键进行分类,能运用价层电子对互斥模型和杂化轨
道理论等,解释分子的立体结构及性质,揭示现象的本质与规律。一般必考点有:σ键或π键数目的判断;
等电子体;杂化类型在近几年也必考,此外还有分子构型、配合物等内容。
【备考策略】
1.了解共价键的形成、极性、类型(σ键和π键),了解配位键的含义。
2.能用键能、键长、键角等说明简单分子的某些性质。
3.了解杂化轨道理论及简单的杂化轨道类型(sp、sp2、sp3)。
4.能用价层电子对互斥理论或者杂化轨道理论推测简单分子或离子的立体构型。
5.了解范德华力的含义及对物质性质的影响。
6.了解氢键的含义,能列举存在氢键的物质,并能解释氢键对物质性质的影响。
【命题预测】
预测2024年继续重点考查共价键的不同类型,特别是σ键和π键的判断,考查分子的空间构型以及分
资料整理【淘宝店铺:向阳百分百】子的杂化类型,特别是杂化类型的判断是高考重点,复习时加以关注;能根据实物模型力来培养空间想象
力。
考法 1 共价键及键参数
1.本质:在原子之间形成共用电子对(电子云的重叠)。
2.特征:具有饱和性和方向性。
3.分类
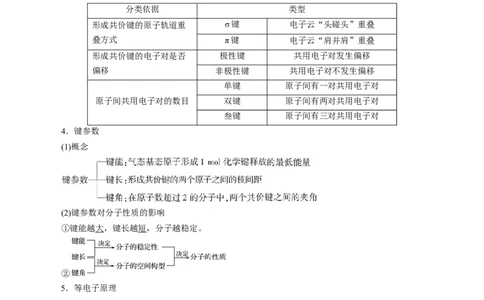
分类依据 类型
形成共价键的原子轨道重 σ键 电子云“头碰头”重叠
叠方式 π键 电子云“肩并肩”重叠
形成共价键的电子对是否 极性键 共用电子对发生偏移
偏移 非极性键 共用电子对不发生偏移
单键 原子间有一对共用电子对
原子间共用电子对的数目 双键 原子间有两对共用电子对
叁键 原子间有三对共用电子对
4.键参数
(1)概念
(2)键参数对分子性质的影响
①键能越大,键长越短,分子越稳定。
②
5.等电子原理
(1)等电子体:原子总数相同、价电子总数相同的粒子互称为等电子体。如:N 和CO、O 与SO 是等
2 3 2
电子体,但N 与C H 不是等电子体。
2 2 2
(2)等电子原理:等电子体具有相似的化学键特征,它们的许多性质相近,此原理称为等电子原理,例
如CO和N 的熔、沸点、溶解性等都非常相近。
2
分类依据 类型
资料整理【淘宝店铺:向阳百分百】σ键 电子云“头碰头”重叠
形成共价键的原子轨道重
叠方式
π键 电子云“肩并肩”重叠
极性键 共用电子对发生偏移
形成共价键的电子对是否
偏移
非极性键 共用电子对不发生偏移
单键 原子间有一对共用电子对
原子间共用电子对的数目 双键 原子间有两对共用电子对
叁键 原子间有三对共用电子对
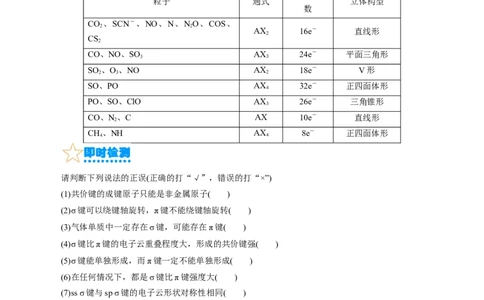
2.常见等电子体
价电子总
粒子 通式 立体构型
数
CO 、SCN-、NO、N、NO、COS、
2 2
AX 16e- 直线形
2
CS
2
CO、NO、SO AX 24e- 平面三角形
3 3
SO 、O、NO AX 18e- V形
2 3 2
SO、PO AX 32e- 正四面体形
4
PO、SO、ClO AX 26e- 三角锥形
3
CO、N、C AX 10e- 直线形
2
CH、NH AX 8e- 正四面体形
4 4
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)共价键的成键原子只能是非金属原子( )
(2)σ键可以绕键轴旋转,π键不能绕键轴旋转( )
(3)气体单质中一定存在σ键,可能存在π键( )
(4)σ键比π键的电子云重叠程度大,形成的共价键强( )
(5)σ键能单独形成,而π键一定不能单独形成( )
(6)在任何情况下,都是σ键比π键强度大( )
(7)ss σ键与sp σ键的电子云形状对称性相同( )
(8)碳碳叁键和碳碳双键的键能分别是碳碳单键键能的3倍和2倍( )
(9)键长等于成键两原子的半径之和( )
(10)σ键可以绕键轴旋转,π键不能绕键轴旋转( )
(11)气体单质中一定存在σ键,可能存在π键( )
(12)σ键比π键的电子云重叠程度大,形成的共价键强(√)
答案:(1)× (2)√ (3)× (4)√ (5)√ (6)× (7)√ (8)× (9)× (10)√ (11)× (12)√
资料整理【淘宝店铺:向阳百分百】例1 (2023·陕西省宝鸡市期中)下列关于σ键和π键的说法中,不正确的是( )
A.N 分子中的π键为p-pπ键,π键不能绕键轴旋转
2
B.HCl分子中的σ键为s-sσ键
C.乙烯分子中σ键与π键的个数比为5:1
D.p轨道和p轨道之间既能形成π键,又能形成σ键
【答案】B
【解析】A项,氮气的结构式为N≡N,分子中含有三键含有1个σ键和2个π键,π键为p-p π键,π
键不能绕键轴旋转,A正确;B项,H只有1s电子,Cl的3p轨道上的电子与H的1s轨道电子以“头碰
头”方式重叠构建s-pσ键,B错误;C项,乙烯分子中含有一个碳碳双键,故π键的个数为1,σ键为5,
σ键与π键的个数比为5:1,C正确;D项,p和p轨道头对头能形成σ键、肩并肩能形成π键,所以p和
p轨道既能形成σ键又能形成π键,D正确;故选B。
例2 (2023·河北省石家庄市期末)下列有关共价键的说法错误的是( )
A.HO 中只有σ键没有π键
2 2
B.所有σ键的强度都比π键的大
C.卤化氢中H-F键的键能最大
D.键长和键角的数值可通过晶体的X射线衍射实验获得
【答案】B
【解析】A项,HO 分子中只有单键,则只有σ键没有π键,A正确;B项,σ键的强度不一定比π键
2 2
的大,如氮气分子中σ键的强度都比π键的小,B错误;C项,H-F的键长是卤化氢中最短的,则H-F的键
能是卤化氢中最大的,C正确;D项,通过晶体X射线衍射实验可以测定分子结构中的键长和键角的数值,
键角是描述分子立体结构的重要参数,D正确;故选B。
对点1 2023·甘肃省武威市期中)下列说法中正确的是( )
A.π键比σ键重叠程度大,形成的共价键稳定
B.两个原子之间形成共价键时,最多有一个σ键
C.气体单质中,一定有σ键,可能有π键
D.CO 分子中有一个σ键,二个π键
2
【答案】B
【解析】A项,σ键是头碰头的重叠,π键是肩并肩的重叠,一般σ键比π键重叠程度大,σ键比π键
稳定,A 错误;B项,两个原子间形成单键时,只能形成1个σ键,两个原子之间形成双键时,含有一个
σ键和一个π键,两个原子之间形成三键时,含有一个σ键和2个π键,B正确;C项,单原子分子中没有
共价键,如稀有气体分子中不存在共价键,C错误;D项,CO 分子中含有两个碳氧双键,即有2个σ键,
2
2个π键,D错误;故选B。
资料整理【淘宝店铺:向阳百分百】对点2 (2023·四川省成都·市联考)下列关于共价键的说法正确的是( )
A.HO和HO 分子内的共价键均是s-pσ键
2 2 2
B.N 分子内的共价键电子云形状均是镜面对称
2
C.H、Cl、HCl分子内的σ键均无方向性
2 2
D.共价化合物一定含σ键,可能含π键
【答案】D
【解析】A项,HO 分子内的共价键还有p-p σ键,故A错误;B项,N 分子内的共价键包括σ键和π
2 2 2
键,所以其电子云形状既有镜面对称也有轴对称,故B错误;C项,Cl、HCl分子内的σ键均有方向性,
2
故C错误;D项,共价化合物一定含σ键,可能含π键,比如氢气只有含σ键,而氧气、氮气含有σ键,
也含有π键,故D正确。故选D。
考法 2 分子的空间构型
1.价层电子对互斥理论
(1)理论要点
①价层电子对在空间上彼此相距最远时,排斥力最小,体系的能量最低。
②孤电子对的排斥力较大,孤电子对越多,排斥力越强,键角越小。
(2)用价层电子对互斥理论推测分子的空间构型的关键是判断分子中的中心原子上的价层电子对数。
其中:a是中心原子的价电子数(阳离子要减去电荷数、阴离子要加上电荷数),b是与中心原子结合的
原子最多能接受的电子数,x是与中心原子结合的原子数。
(3)示例分析
电子对数 σ键电子对数 孤电子对数 电子对空间构型 分子空间构型 实例
2 2 0 直线形 直线形 CO
2
3 0 平面三角形 BF
3
3 三角形
2 1 V形 SO
2
4 0 正四面体形 CH
4
4 3 1 四面体形 三角锥形 NH
3
2 2 V形 HO
2
2.杂化轨道理论
(1)理论要点
当原子成键时,原子的价电子轨道相互混杂,形成与原轨道数相等且能量相同的杂化轨道。杂化轨道
数不同,轨道间的夹角不同,形成分子的空间结构不同。
(2)杂化轨道与分子空间构型的关系
杂化类型 杂化轨道数目 杂化轨道间夹角 空间构型 实例
资料整理【淘宝店铺:向阳百分百】sp1 2 180° 直线形 BeCl
2
sp2 3 120° 平面三角形 BF
3
sp3 4 109.5° 四面体形 CH
4
3.“五方法”判断分子中心原子的杂化类型
(1)根据杂化轨道的空间构型判断。
①若杂化轨道在空间的分布为正四面体形或三角锥形,则分子的中心原子发生sp3杂化。
②若杂化轨道在空间的分布呈平面三角形,则分子的中心原子发生sp2杂化。
③若杂化轨道在空间的分布呈直线形,则分子的中心原子发生sp1杂化。
(2)根据杂化轨道之间的夹角判断
若杂化轨道之间的夹角为109.5°,则分子的中心原子发生sp3杂化;若杂化轨道之间的夹角为120°,
则分子的中心原子发生sp2杂化;若杂化轨道之间的夹角为180°,则分子的中心原子发生sp1杂化。
(3)根据等电子原理进行判断
如CO 是直形线分子,CNS-、N与CO 互为等电子体,所以分子构型均为直线形,中心原子均采用
2 2
sp1杂化。
(4)根据中心原子的价电子对数判断
如中心原子的价电子对数为4,是sp3杂化,为3是sp2杂化,为2是sp1杂化。
(5)根据分子或离子中有无π键及π键数目判断
如没有π键为sp3杂化,含1个π键为sp2杂化,含2个π键为sp1杂化。
4.配位键
(1)孤电子对
分子或离子中没有跟其他原子共用的电子对称孤电子对。
(2)配位键
①配位键的形成:成键原子一方提供孤电子对,另一方提供空轨道形成共价键。
②配位键的表示:常用“→”来表示配位键,箭头指向接受孤电子对的原子,如 NH 可表示为
,在NH中,虽然有一个N—H键形成过程与其他3个N—H键形成过程不同,但是一旦形
成之后,4个共价键就完全相同。
(3)配合物
①组成。如[Cu(NH )]SO
3 4 4
②形成条件。
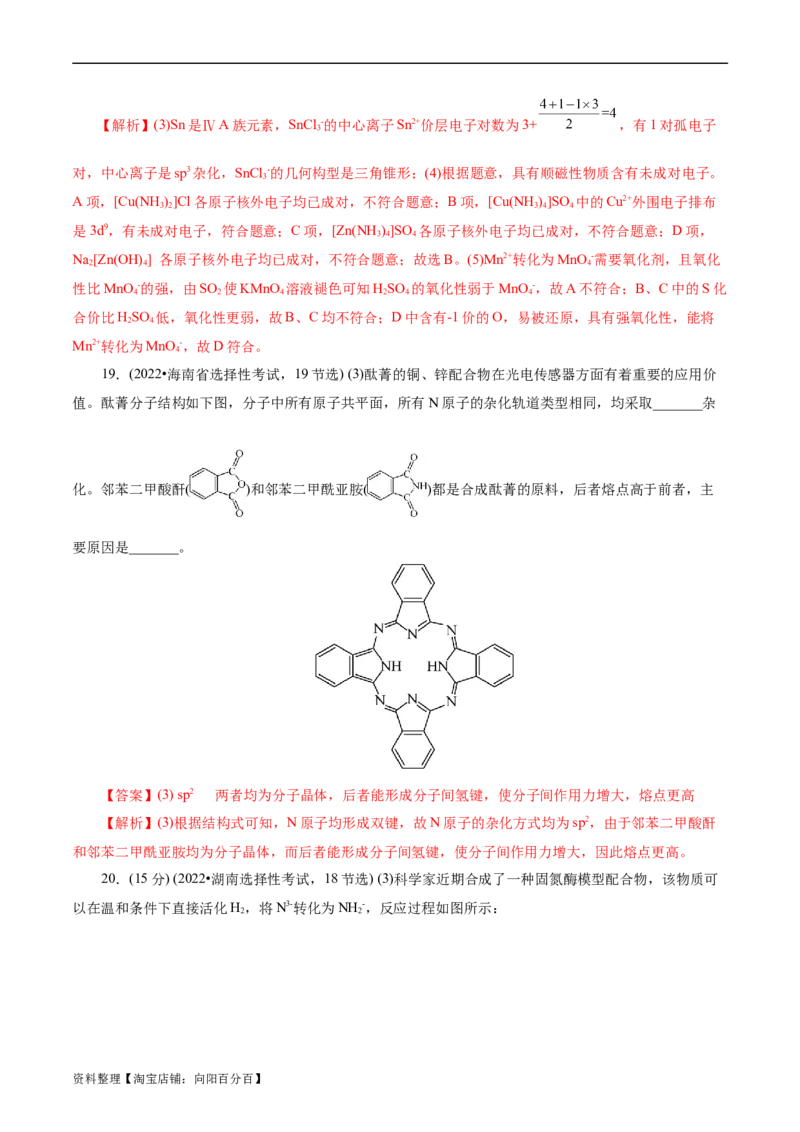
资料整理【淘宝店铺:向阳百分百】1.三原子分子空间结构
化学式 电子式 结构式 键角 空间结构 空间结构名称
CO O==C==O 180° 直线形
2
HO 105° V形
2
2.四原子分子空间结构
化学式 电子式 结构式 键角 空间结构 空间结构名称
CHO 约120° 平面三角形
2
NH 107° 三角锥形
3
3.五原子分子空间结构
化学式 电子式 结构式 键角 空间结构 空间结构名称
CH 109°28′ 正四面体形
4
CCl 109°28′ 正四面体形
4
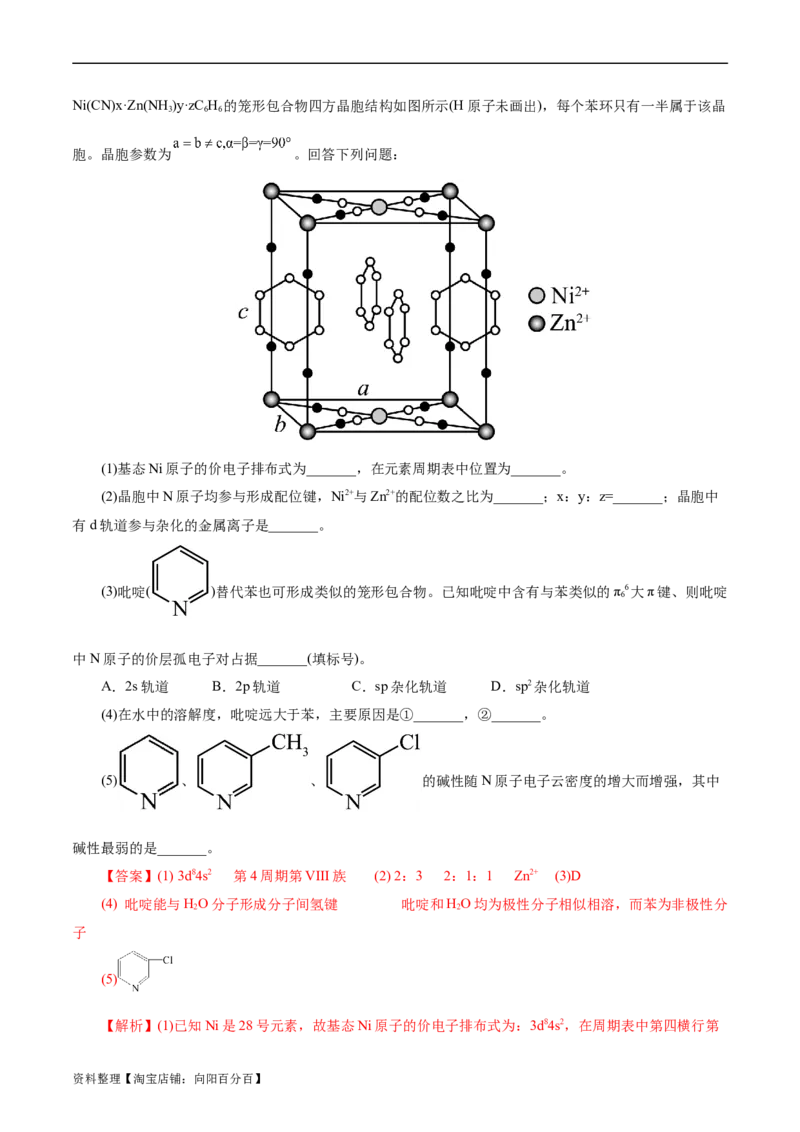
4.其他多原子分子的空间结构
资料整理【淘宝店铺:向阳百分百】请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对( )
(2)分子中中心原子若通过sp3杂化轨道成键,则该分子一定为正四面体结构( )
(3)NH 分子为三角锥形,N原子发生sp2杂化( )
3
(4)只要分子构型为平面三角形,中心原子均为sp2杂化( )
(5)中心原子是sp1杂化的,其分子构型不一定为直线形( )
(6)价层电子对互斥理论中,π键电子对数不计入中心原子的价层电子对数( )
(7)PCl 分子是三角锥形,这是因为P原子是以sp2杂化的结果( )
3
(8)sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道( )
(9)凡中心原子采取sp3杂化的分子,其VSEPR模型都是四面体( )
(10)AB 型的分子空间构型必为平面三角形( )
3
(11)分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构( )
(12)杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对( )
(13)NH 和CH 两个分子中中心原子N和C都是通过sp3杂化轨道成键( )
3 4
(14)杂化轨道理论与VSEPR模型分析分子的空间构型结果常常相互矛盾( )
(15)配位键也是一种静电作用( )
(16)形成配位键的电子对由成键双方原子提供( )
答案:(1)√ (2)× (3)× (4)√ (5)× (6)√ (7)× (8)× (9)√ (10)× (11)√ (12)√ (13)√ (14)×
(15)√ (16)×
例1 (2023•湖北省选择性考试,9)价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确
的是
A.CH 和HO的VSEPR模型均为四面体 B.SO 2-和CO2-的空间构型均为平面三角形
4 2 3 3
C.CF 和SF 均为非极性分子 D.XeF 和XeO 的键角相等
4 4 2 2
【答案】A
【解析】A项,甲烷分子的中心原子的价层电子对为4,水分子的中心原子价层电子对也为4,所以他
们的VSEPR模型都是四面体,A正确;B项,SO 2-的孤电子对为1,CO2-的孤电子对为0,所以SO 2-的空
3 3 3
间构型为三角锥形,CO2-的空间构型为平面三角形,B错误,C项,CH 为正四面体结构,为非极性分子,
3 4
SF 中心原子有孤电子对,为极性分子,C错误;D项,XeF 和XeO 分子中,孤电子对不相等,孤电子对
4 2 2
越多,排斥力越大,所以键角不等,D错误;故选A。
例2 有几种阴离子的信息如下:
阴离子 ClO - ClO - M ClO-
4 3
资料整理【淘宝店铺:向阳百分百】中心元素化合价 +5 +3 +1
中心原子杂化类型 sp3 sp3
下列推断不正确的是( )
A.ClO -和CO2-的价电子总数相同 B.M的化学式为ClO -
3 3 2
C.ClO -、ClO-中氯原子的杂化类型都为sp3 D.M的空间结构为V形
3
【答案】A
【解析】A项,ClO -和CO2-的价电子总数分别为7+3×6+1=26、4+3×6+2=24,不相同,A项错误;
3 3
B项,M中Cl元素的化合价是+3价,杂化轨道类型是sp3,因此M的化学式为ClO -,B项正确;C项,
2
ClO -中价层电子对数是 =4,ClO-中价层电子对数是 =4,因此氯原子的杂
3
化类型都为sp3,C项正确;D项,M中价层电子对数是 =4,含有2对孤对电子,所以空
间结构为V形,D项正确;故选A。
对点1 下列中心原子的杂化轨道类型和分子几何构型不正确的是( )
A.PCl 中P原子sp3杂化,为三角锥形 B.BCl 中B原子sp2杂化,为平面三角形
3 3
C.CS 中C原子sp杂化,为直线形 D.HS分子中,S为sp杂化,为直线形
2 2
【答案】D
【解析】PCl 分子中P原子形成3个σ键,孤对电子数为-3=1,为sp3杂化,三角锥形,A正确;
3
BCl 分子中B原子形成3个σ键,孤对电子数为-3=0,为sp2杂化,平面三角形,B正确;CS 分子中C
3 2
原子形成2个σ键,孤对电子数为-2=0,为sp杂化,直线形,C正确;HS分子中,S原子形成2个σ键,
2
孤对电子数为-2=2,为sp3杂化,V形,D错误。
对点2 根据杂化轨道理论和价层电子对互斥模型,判断下列分子或离子的空间结构正确的是( )
选项 分子或离子 中心原子杂化方式 价层电子对互斥模型 分子或离子的空间结构
A SO sp 直线形 直线形
2
B HCHO sp2 平面三角形 三角锥形
C NF sp2 四面体形 平面三角形
3
D
NH+
sp3 正四面体形 正四面体形
4
【答案】B
资料整理【淘宝店铺:向阳百分百】【解析】SO 分子中心原子杂化方式为sp2,价层电子对互斥模型为平面三角形,含有一对孤电子对,
2
分子的空间结构为V形,A错误;HCHO分子中心原子杂化方式为sp2,价层电子对互斥模型为平面三角
形,没有孤电子对,分子的空间结构为平面三角形,B错误;NF 分子中心原子杂化方式为sp3,价层电子
3
对互斥模型为四面体形,含有一对孤电子对,分子的空间结构为三角锥形,C错误;NH+
的中心原子杂化
4
方式为sp3,价层电子对互斥模型为正四面体形,没有孤电子对,离子的空间结构为正四面体形,D正确。
故选B。
考法 3 分子间作用力
1.分子间作用力
(1)概念:物质分子之间普遍存在的相互作用力,称为分子间作用力。
(2)分类:分子间作用力最常见的是范德华力和氢键。
(3)强弱:范德华力<氢键<化学键。
(4)范德华力
范德华力主要影响物质的熔点、沸点、硬度等物理性质。范德华力越强,物质的熔点、沸点越高,硬
度越大。一般来说,组成和结构相似的物质,随着相对分子质量的增加,范德华力逐渐增大。
(5)氢键
①形成:已经与电负性很强的原子形成共价键的氢原子(该氢原子几乎为裸露的质子)与另一个分子中
电负性很强的原子之间的作用力,称为氢键。
②表示方法:A—H…B
③特征:具有一定的方向性和饱和性。
④分类:氢键包括分子内氢键和分子间氢键两种。
⑤分子间氢键对物质性质的影响
主要表现为使物质的熔、沸点升高,对电离和溶解度等产生影响。
2.分子的性质
(1)分子的极性
类型 非极性分子 极性分子
正电中心和负电中心重合的 正电中心和负电中心不重合的
形成原因
分子 分子
存在的共价键 非极性键或极性键 非极性键或极性键
分子内原子排列 对称 不对称
(2)分子的溶解性
①“相似相溶”的规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。若溶剂
和溶质分子之间可以形成氢键,则溶质的溶解度增大。
②随着溶质分子中憎水基个数的增多,溶质在水中的溶解度减小。如甲醇、乙醇和水以任意比互溶,
而戊醇在水中的溶解度明显减小。
(3)分子的手性
资料整理【淘宝店铺:向阳百分百】①手性异构:具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为镜像,在三维空
间里不能重叠的现象。
②手性分子:具有手性异构体的分子。
③手性碳原子:在有机物分子中,连有四个不同基团或原子的碳原子。含有手性碳原子的分子是手性
分子,如 。
(4)无机含氧酸分子的酸性
无机含氧酸的通式可写成(HO) RO ,如果成酸元素R相同,则n值越大,R的正电性越高,使R—O
m n
—H中O的电子向R偏移,在水分子的作用下越易电离出H+,酸性越强,如酸性:HClO<HClO<HClO
2 3
<HClO。
4
1.范德华力、氢键、共价键的比较
范德华力 氢键 共价键
已经与电负性很大的原子
分子间普遍存在的一种相互作 (N、O、F)形成共价键的氢原 原子间通过共用电子对形
概念
用力,但不是化学键 子与另一个电负性很大的原 成的化学键
子(N、O、F)之间的作用力
存在范 氢原子与F、N、O原子(分子
分子或原子(稀有气体)之间 相邻原子间
围 内、分子间)
特征 无方向性、无饱和性 有方向性、有饱和性 有方向性、有饱和性
强度比
共价键>氢键>范德华力
较
①随着分子极性和相对分子质
影响强 量的增大而增大; 对于 A—H…B,A、B 原子 成键原子半径越小、键长
度 ②组成和结构相似的物质,相 的电负性越大,B原子的半径 越短,键能越大,共价键
的因素 对分子质量越大,范德华力越 越小,氢键键能越大 越稳定
大
①影响物质的熔、沸点、溶解 分子间氢键的存在,使物质 ①影响分子的稳定性,共
对物质
度等物理性质; 的熔、沸点升高,在水中的 价键键能越大,分子稳定
性
②组成和结构相似的物质,随 溶解度增大;分子内氢键会 性越强;
质的影
相对分子质量的增大,物质的 使物质的熔、沸点降低,在 ②影响原子晶体的熔、沸
响
熔、沸点升高 水中溶解度减小 点,硬度
2.配合物
配合物的组成 [中心离子(配体)][外界]
n
资料整理【淘宝店铺:向阳百分百】典型配合物 Cu(NH )SO Fe(SCN) Ag(NH)OH
3 4 4 3 3 2
中心离子 Cu2+ Fe3+ Ag+
中心离子结构特点 一般是金属离子,特别是过渡金属离子,必须有空轨道
配体 NH SCN- NH
3 3
配体结构特点 分子或离子,必须含有孤对电子(如NH 、HO、CO、Cl-、SCN-等)
3 2
配位数(n) 4 3 2
外界 SO 2- 无 OH-
4
颜色 深蓝色 血红色 无色
配离子所含化学键 配体通过配位键与中心离子结合
配合物所含化学键 配位键、离子键;配体或外界中可能还含有共价键
配合物的常见性质 属于离子化合物,多数能溶解、能电离,多数有颜色
是过渡金属和一氧化碳配位形成的配合物,如四羰基镍[Ni(CO) ]。在许多有机
金属羰基配合物 4
化合物的合成反应中,金属羰基配合物常常作为这些反应的催化剂
二茂铁的结构为一个铁原子处在两个平行的环戊二烯的环之间。在固体状态
下,两个茂环相互错开成全错位构型,温度升高时则绕垂直轴相对转动。二茂
二茂铁 铁的化学性质稳定,类似芳香族化合物
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)范德华力与化学键的区别是作用力的强弱不同( )
(2)任何分子间在任意情况下都会产生范德华力( )
(3)分子间作用力是分子间相互作用力的总称,包括氢键与范德华力( )
(4)范德华力的实质也是一种电性作用,所以范德华力是一种特殊的化学键( )
(5)范德华力非常微弱,故破坏范德华力不需要消耗能量( )
(6)氢键是一种特殊的化学键,它广泛存在于自然界中( )
(7)范德华力与物质的性质没有必然的联系( )
(8)范德华力能够影响物质的化学性质和物理性质( )
(9)范德华力仅是影响物质部分物理性质的一种因素( )
(10)范德华力是决定由分子构成的物质的熔点、沸点高低的唯一因素( )
(11)范德华力与氢键可同时存在于分子之间( )
(12)可燃冰(CH·8H O)中甲烷分子与水分子间形成了氢键( )
4 2
(13)乙醇分子和水分子间只存在范德华力( )
(14)氢键具有方向性和饱和性( )
(15)氢键的存在,使水凝结为冰时密度减小,体积增大( )
(16)H O 分子间存在氢键( )
2 2
(17)卤素单质、卤素氢化物、卤素碳化物(即CX)的熔、沸点均随着相对分子质量的增大而增大( )
4
(18)氢键的存在一定能使物质的熔、沸点升高( )
(19)H O比HS稳定是因为水分子间存在氢键( )
2 2
资料整理【淘宝店铺:向阳百分百】(20)分子间氢键的形成除使物质的熔点、沸点升高外,对物质的溶解、电离等也都有影响( )
答案:(1)√ (2)× (3)× (4)× (5)× (6)× (7)× (8)× (9)√ (10)× (11)√ (12)× (13) (14)√
(15)√ (16)√ (17)× (18)× (19)× (20)√
例1 (2023•湖南卷,4)下列有关物质结构和性质的说法错误的是( )
A.含有手性碳原子的分子叫做手性分子
B.邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点
C.酰胺在酸或碱存在并加热的条件下可发生水解反应
D.冠醚(18-冠-6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子
【答案】A
【解析】A项,有手性异构体的分子被称为手性分子,当分子中存在两个或两个以上的手性碳原子时,
会出现内消旋体,这种含有内消旋体的分子不是手性分子,A错误;B项,邻羟基苯甲醛中含有分子内氢
键,分子内氢键可以降低物质的熔沸点,因此邻羟基苯甲醛的熔沸点低于对羟基苯甲醛的熔沸点,B正确;
C项,酰胺在酸性条件下反应生成羧基和氨基,在碱性条件下反应生成羧酸盐和氨气,二者均为水解反应,
C正确;D项,超分子是由两种或两种以上的分子通过分子间作用力形成的分子聚集体,冠醚(18-冠-6)的
空穴大小为260~320pm,可以适配K+(276pm)、Rb+(304pm),冠醚与离子之间以配位的形式结合,D正确;
故选A。
例2 (2023•湖北省选择性考试,11)物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
( )
选项 性质差异 结构因素
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B 熔点:AlF (1040℃)远高于AlCl (178℃升华) 晶体类型
3 3
C 酸性:CFCOOH(pKa=0.23)远强于CHCOOH(pKa=4.76) 羟基极性
3 3
D 溶解度(20℃):NaCO(29g)大于NaHCO (8g) 阴离子电荷
2 3 3
【答案】D
【解析】A项,正戊烷和新戊烷形成的晶体都是分子晶体,由于新戊烷支链多,对称性好,分子间作
用力小,所以沸点较低,故A正确;B项,AlF 为离子化合物,形成的晶体为离子晶体,熔点较高,AlCl
3 3
为共价化合物,形成的晶体为分子晶体,熔点较低,则 AlF 熔点远高于AlCl ,故B正确;C项,由于电
3 3
负性F>H,C-F键极性大于C-H键,使得羧基上的羟基极性增强,氢原子更容易电离,酸性增强,故C正
确;D项,碳酸氢钠在水中的溶解度比碳酸钠小的原因是碳酸氢钠晶体中 HCO -间存在氢键,与晶格能大
3
小无关,即与阴离子电荷无关,故D错误;故选D。
资料整理【淘宝店铺:向阳百分百】对点1 下列对分子及其性质的解释中,不正确的是( )
A.液态氟化氢分子间存在氢键,所以氟化氢的沸点比氯化氢高
B.CH、CO、BF 都是含有极性键的非极性分子
4 2 3
C.[Cu(NH )]2+ 中含有离子键、极性键、配位键
3 4
D.因为非羟基氧原子数目逐渐减少,所以酸性HClO>H SO >H PO
4 2 4 3 4
【答案】C
【解析】A项,液态氟化氢中存在氢键,所以氟化氢的沸点比氯化氢高,A项正确;B项,CH、
4
CO、BF 都是含有极性键的非极性分子,B项正确;C项,[Cu(NH )]2+中含有极性键、配位键,C项错误;
2 3 3 4
D项,非羟基氧原子数目越多酸性越强,而在HClO 中有3个非羟基氧原子,HSO 中有2个非羟基氧原子,
4 2 4
HPO 中有1个非羟基氧原子,所以酸性强弱的顺序为:HClO>H SO >H PO ,D项正确;故选C。
3 4 4 2 4 3 4
对点2 关于CS、SO 、NH 三种物质的说法中正确的是( )
2 2 3
A.CS 在水中的溶解度很小,是由于其属于极性分子
2
B.SO 和NH 均易溶于水,原因之一是它们都是极性分子
2 3
C.CS 为非极性分子,所以在三种物质中熔沸点最低
2
D.NH 在水中溶解度很大只是由于NH 分子有极性
3 3
【答案】B
【解析】根据“相似相溶”原理,水是极性分子,CS 是非极性分子,SO 和NH 都是极性分子,故A
2 2 3
项错误、B项正确;由于CS 常温下是液体,SO 和NH 常温下是气体,故C项错误;NH 在水中溶解度很
2 2 3 3
大,除了由于NH 分子有极性外,还因为NH 分子和HO分子之间可以形成氢键,故D项错误。故选B。
3 3 2
1.(2023•山东卷,3)下列分子属于极性分子的是( )
A.CS B.NF C.SO D.SiF
2 3 3 4
【答案】B
【解析】A项,CS 中C上的孤电子对数为 ×(4-2×2)=0,σ键电子对数为2,价层电子对数为2,CS
2 2
的空间构型为直线形,分子中正负电中心重合,CS 属于非极性分子,A项不符合题意;B项,NF 中N上
2 3
的孤电子对数为 ×(5-3×1)=1,σ键电子对数为3,价层电子对数为4,NF 的空间构型为三角锥形,分子
3
中正负电中心不重合,NF 属于极性分子,B项符合题意;C项,SO 中S上的孤电子对数为 ×(6-
3 3
3×2)=0,σ键电子对数为3,价层电子对数为3,SO 的空间构型为平面正三角形,分子中正负电中心重合,
3
资料整理【淘宝店铺:向阳百分百】SO 属于非极性分子,C项不符合题意;D项,SiF 中Si上的孤电子对数为 ×(4-4×1)=0,σ键电子对数为
3 4
4,价层电子对数为4,SiF 的空间构型为正四面体形,分子中正负电中心重合,SiF 属于非极性分子,D
4 4
项不符合题意;故选B。
2.(2023•北京卷,10)下列事实不能通过比较氟元素和氯元素的电负性进行解释的是( )
A. 键的键能小于Cl-Cl键的键能
B.三氟乙酸的K 大于三氯乙酸的K
a a
C.氟化氢分子的极性强于氯化氢分子的极性
D.气态氟化氢中存在(HF) ,而气态氯化氢中是 分子
2
【答案】A
【解析】A项,F原子半径小,电子云密度大,两个原子间的斥力较强,F-F键不稳定,因此F-F键的
键能小于Cl-Cl键的键能,与电负性无关,A符合题意;B项,氟的电负性大于氯的电负性。F-C键的极性
大于Cl-C键的极性,使FC—的极性大于ClC—的极性,导致三氟乙酸的羧基中的羟基极性更大,更容易
3 3
电离出氢离子,酸性更强,B不符合题意;C项,氟的电负性大于氯的电负性,F-H键的极性大于Cl-H键
的极性,导致HF分子极性强于HCl,C不符合题意;D项,氟的电负性大于氯的电负性,与氟原子相连的
氢原子可以与另外的氟原子形成分子间氢键,因此气态氟化氢中存在(HF) ,D不符合题意;故选A。
2
3.(2023•浙江省1月选考,12)共价化合物Al Cl 中所有原子均满足8电子稳定结构,一定条件下可发
2 6
生反应: ,下列说法不正确的是( )
A.Al Cl 的结构式为 B.Al Cl 为非极性分子
2 6 2 6
C.该反应中NH 的配位能力大于氯 D.Al Br 比Al Cl 更难与 发生反应
3 2 6 2 6
【答案】D
【解析】A项,由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分子的结构式为
,故A正确;B项,由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分
子的结构式为 ,则双聚氯化铝分子为结构对称的非极性分子,故B正确;C项,由
反应方程式可知,氨分子更易与具有空轨道的铝原子形成配位键,配位能力大于氯原子,故C正确;D项,
资料整理【淘宝店铺:向阳百分百】溴元素的电负性小于氯元素,原子的原子半径大于氯原子,则铝溴键弱于铝氯键,所以双聚溴化铝的铝溴
键更易断裂,比双聚氯化铝更易与氨气反应,故D错误;故选D。
4.(2022•海南省选择性考试,11)已知CHCOOH+Cl ClCH COOH+HCl,ClCH COOH的酸性
3 2 2 2
比CHCOOH强。下列有关说法正确的是( )
3
A.HCl的电子式为 B.Cl-Cl键的键长比I-I键短
C.CHCOOH分子中只有σ键 D.ClCH COOH的酸性比ICHCOOH强
3 2 2
【答案】BD
【解析】A项,HCl为共价化合物,H原子和Cl原子间形成共用电子对,其电子式为 ,A错
误;B项,原子半径Cl<I,故键长:Cl—Cl<I—I,B正确;C项,CHCOOH分子中,羧基的碳氧双键中
3
含有π键,C错误;D项,电负性Cl>I,-Cl能使-COOH上的H原子具有更大的活动性,因此
ClCH COOH的酸性比ICHCOOH强,D正确;故选BD。
2 2
5.(2022•湖北省选择性考试,11)磷酰三叠氮是一种高能分子,结构简式为O=P(N )。下列关于该分
3 3
子的说法正确的是( )
A.为非极性分子 B.立体构型为正四面体形
C.加热条件下会分解并放出N D.分解产物 的电子式为
2
【答案】C
【解析】A项,磷酰三叠氮分子不是对称结构,分子中的正负电荷重心是不重合的,是极性分子,A
项错误;B项,磷酰三叠氮分子含有三个P-N键及一个P=O双键,则立体构型为四面体构型,B项错误;
C项,磷酰三叠氮是一种高能分子,加热条件下会分解并放出N,C项正确;D项,NPO为共价化合物,
2
则电子式为 ,D项错误;故选C。
6.(2022•湖北省选择性考试,10)Be2+和Al3+的电荷与半径之比相近,导致两元素性质相似。下列说法
错误的是( )
A.Be2+与Al3+都能在水中与氨形成配合物
B.BeCl 和AlCl 的熔点都比MgCl 的低
2 3 2
C.Be(OH) 和Al(OH) 均可表现出弱酸性
2 3
D.Be和Al的氢化物都不能在酸中稳定存在
【答案】A
资料整理【淘宝店铺:向阳百分百】【解析】A项,Al3+半径小,不能容纳6个氮原子和它配位,则不能在水中与氨形成配合物,A项错误;
B项,BeCl 和AlCl 属于分子晶体,而MgCl 属于离子晶体,则BeCl 和AlCl 的熔点都比MgCl 的低,B
2 3 2 2 3 2
项正确;C项,Be(OH) 和Al(OH) 均为两性氢氧化物,则均可表现出弱酸性,C项正确;D项,Be和Al
2 3
的氢化物与酸反应,生成对应的盐和氢气,则都不能在酸中稳定存在,D项正确;故选A。
7.(2022•辽宁省选择性考试,8)理论化学模拟得到一种N +离子,结构如图。下列关于该离子的说法
13
错误的是( )
A.所有原子均满足8电子结构 B.N原子的杂化方式有2种
C.空间结构为四面体形 D.常温下不稳定
【答案】B
【解析】A项,由N +的结构式可知,所有N原子均满足8电子稳定结构,A正确;B项,中心N原
13
子为sp3杂化,与中心N原子直接相连的N原子为sp2杂化,与端位N原子直接相连的N原子为sp杂化,
端位N原子为sp2杂化,则N原子的杂化方式有3种,B错误;C项,中心N原子为sp3杂化,则其空间结
构为四面体形,C正确;D项,N +中含叠氨结构( ),常温下不稳定,D正确;故选B。
13
8.(2022•山东卷,5)AlN、GaN属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
键、 键。下列说法错误的是( )
A. 的熔点高于 B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取sp3杂化 D.晶体中所有原子的配位数均相同
【答案】A
【解析】根据元素周期表,Al和Ga均为第ⅢA元素,N属于第ⅤA元素,结合题意AlN、GaN的成
键结构与金刚石相似,则其为共价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似,
AlN、GaN晶体中,N原子与其相邻的原子形成3个普通共价键和1个配位键。A项,因为AlN、GaN为
结构相似的共价晶体,由于Al原子的半径小于Ga,N—Al的键长小于N—Ga的,则N—Al的键能较大,
键能越大则其对应的共价晶体的熔点越高,故GaN的熔点低于AlN,A说错误;B项,不同种元素的原子
之间形成的共价键为极性键,故两种晶体中所有化学键均为极性键,B说法正确;C项,金刚石中每个C
原子形成4个共价键(即C原子的价层电子对数为4),C原子无孤电子对,故C原子均采取sp3杂化;由于
AlN、GaN与金刚石互为等电子体,则其晶体中所有原子均采取sp3杂化,C说法正确;D项,金刚石中每
资料整理【淘宝店铺:向阳百分百】个C原子与其周围4个C原子形成共价键,即C原子的配位数是4,由于AlN、GaN与金刚石互为等电子
体,则其晶体中所有原子的配位数也均为4,D说法正确。故选A。
9.(2021•湖北选择性考试,9)下列有关N、P及其化合物的说法错误的是( )
A.N的电负性比P的大,可推断NCl 分子的极性比PCl 的大
3 3
B.N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高
C.NH 的成键电子对间排斥力较大,可推断NH 的键角比PH 的大
3 3 3
D.HNO 的分子间作用力较小,可推断HNO 的熔点比HPO 的低
3 3 3 4
【答案】A
【解析】Cl、P的电负性差值大于Cl、N的电负性差值,三氯化氮、三氯化磷的空间结构都是三角锥
形,故三氯化氮的分子极性小于三氯化磷,A项错误;分子的稳定性与键能、键数目有关,N与N的π键
比P与P的强,可推断N≡N的稳定性比P≡P的高,B项正确;
NH 、PH 分子空间结构都是三角锥形,N、P原子价层孤电子对数都为1,杂化类型都是sp3,但是N
3 3
原子半径小于P,N的电负性大于P,NH 分子中成键电子对之间排斥力大于PH ,故NH 键角大于PH ,
3 3 3 3
C项正确;晶体熔点高低由构成晶体的微粒之间作用力大小决定,它们都是分子晶体,硝酸的相对分子质
量小于磷酸,HNO 分子间作用力小于HPO ,磷酸的熔点高于硝酸,D项正确。
3 3 4
10.(2021•海南选择性考试,10)关于NH 性质的解释合理的是( )
3
选
性质 解释
项
A 比PH 容易液化 NH 分子间的范德华力更大
3 3
B 熔点高于PH N-H键的键能比P-H大
3
C 能与Ag以配位键结合 NH 中氮原子有孤电子对
3
D 氨水中存在NH + NH ·H O是离子化合物
4 3 2
【答案】C
【解析】A项,NH 和PH 都属于同一主族是氢化物,分子晶体的沸点与其相对分子质量成正比,但
3 3
氨气中含有氢键, PH 不含氢键,氢键的存在导致氨气的沸点升高,故A错误;B项,NH 熔点高于
3 3
PH ,是因为氨气中含有氢键,氢键的存在导致氨气的熔点升高,不是N-H键的键能比P-H大,故B错误;
3
C项,NH 中氮原子有孤电子对,使Ag+和NH 以配位键结合形成[Ag(NH)]+,故C正确;D项,NH ·H O
3 3 3 2 3 2
是共价化合物,是弱碱,在水溶液中部分电离出NH +和OH-,故D错误;故选C。
4
11.(2023•全国乙卷,35节选) (2)已知一些物质的熔点数据如下表:
物质 熔点/℃
NaCl 800.7
资料整理【淘宝店铺:向阳百分百】SiCl
4
GeCl
4
SnCl
4
Na与Si均为第三周期元素,NaCl熔点明显高于SiCl ,原因是_______。分析同族元素的氯化物
4
SiCl 、GeCl 、SnCl 熔点变化趋势及其原因_______。SiCl 的空间结构为_______,其中Si的轨道杂化形式
4 4 4 4
为_______。
【答案】(2) 钠的电负性小于硅,氯化钠为离子晶体,而SiCl 为分子晶体 随着同族元素的电子
4
层数的增多,其熔点依次升高,其原因是:SiCl 、GeCl 、SnCl 均形成分子晶体,分子晶体的熔点由分子
4 4 4
间作用力决定,分子间作用力越大则其熔点越高;随着其相对分子质量增大,其分子间作用力依次增大
正四面体 sp3
【解析】(2)Na与Si均为第三周期元素,NaCl熔点明显高于SiCl ,原因是:钠的电负性小于硅,氯化
4
钠为离子晶体,其熔点较高;而SiCl 为分子晶体,其熔点较低。由表中的数据可知,SiCl 、GeCl 、SnCl
4 4 4 4
熔点变化趋势为:随着同族元素的电子层数的增多,其熔点依次升高,其原因是:SiCl 、GeCl 、SnCl 均
4 4 4
形成分子晶体,分子晶体的熔点由分子间作用力决定,分子间作用力越大则其熔点越高;随着其相对分子
质量增大,其分子间作用力依次增大。SiCl 的空间结构为正四面体,其中Si的价层电子对数为4,因此Si
4
的轨道杂化形式为sp3。
12.(2023•浙江省1月选考,17节选) (10分)(1) Si(NH ) 分子的空间结构(以Si为中心)名称为________,
2 4
分子中氮原子的杂化轨道类型是_______。Si(NH ) 受热分解生成Si N 和NH ,其受热不稳定的原因是
2 4 3 4 3
________。
【答案】(1)四面体 sp3
Si周围的NH 基团体积较大,受热时斥力较强[Si(NH ) 中Si-N键键能相对较小];产物中气态分子数
2 2 4
显著增多(熵增)
【解析】(1)Si(NH ) 分子可视为SiH 分子中的4个氢原子被—NH (氨基)取代形成的,所以Si(NH ) 分
2 4 4 2 2 4
子中Si原子轨道的杂化类型是sp3,分子的空间结构(以Si为中心)名称为四面体;氨基(-NH )氮原子形成3
2
个σ键,含有1对孤对电子,N原子杂化轨道数目为4,N原子轨道的杂化类型是sp3;Si周围的NH 基团
2
体积较大,受热时斥力较强 Si(NH ) 中Si-N键能相对较小];产物中气态分子数显著增多(熵增),故
2 4
Si(NH ) 受热不稳定,容易分解生成Si N 和NH 。
2 4 3 4 3
13.(2023•山东卷,16节选) (2) Cl O中心原子为Cl,Cl O中心原子为 ,二者均为 形结构,但
2 2
ClO 中存在大 键 。ClO 中Cl原子的轨道杂化方式_____;为O-Cl-O键角_____Cl-O-Cl键角(填“>”
2 2
“ <”或“=”)。比较ClO 与Cl O中Cl-O键的键长并说明原因_____。
2 2
【答案】(2) sp2 > ClO 分子中Cl-O键的键长小于Cl O中Cl-O键的键长,其原因是:ClO
2 2 2
资料整理【淘宝店铺:向阳百分百】分子中既存在σ键,又存在大π键,原子轨道重叠的程度较大,因此其中Cl-O键的键长较小,而Cl O只
2
存在普通的σ键
【解析】(2)ClO 中心原子为Cl,Cl O中心原子为O,二者均为V形结构,但ClO 中存在大π键( )。
2 2 2
由ClO 中存在 可以推断,其中Cl原子只能提供1对电子,有一个O原子提供1个电子,另一个O原子
2
提供1对电子,这5个电子处于互相平行的p轨道中形成大π键,Cl提供孤电子对与其中一个O形成配位
键,与另一个O形成的是普通的共价键(σ键,这个O只提供了一个电子参与形成大π键), Cl的价层电子
对数为3,则 原子的轨道杂化方式为sp2;Cl O中心原子为O,根据价层电子对的计算公式可知
2
,因此,O的杂化方式为sp3;根据价层电子对互斥理论可知,n =4时,价电子对的几何构
型为正四面体,n =3时,价电子对的几何构型平面正三角形,sp2杂化的键角一定大于sp3的,因此,虽然
ClO 和Cl O均为V形结构,但O-Cl-O键角大于Cl-O-Cl键角,孤电子对对成键电子对的排斥作用也改变不
2 2
了这个结论。ClO 分子中Cl-O键的键长小于Cl O中Cl-O键的键长,其原因是:ClO 分子中既存在σ键,
2 2 2
又存在大π键,原子轨道重叠的程度较大,因此其中Cl-O键的键长较小,而Cl O只存在普通的σ键。
2
14.(10分)(2023•北京卷,15节选) (3) S O2-的空间结构是 。
2 3
(4)同位素示踪实验可证实SO2-中两个 原子的化学环境不同,实验过程为
2 3
。过程ⅱ中,SO2-断裂的只有硫硫键,若过程ⅰ所用试剂是Na32SO
2 3 2 3
和35S,过程ⅱ含硫产物是 。
【答案】(3)四面体形
(4) Na 32SO 和Ag35S
2 4 2
【解析】(3)SO 2-的中心原子S的价层电子对数为4,无孤电子对,空间构型为四面体形,SO2-可看作
4 2 3
是SO 2-中1个O原子被S原子取代,则SO2-的空间构型为四面体形;(4)过程Ⅱ中SO2-断裂的只有硫硫键,
4 2 3 2 3
根据反应机理可知,整个过程中SO 2-最终转化为SO 2-,S最终转化为AgS;若过程ⅰ所用的试剂为
3 4 2
Na32SO 和35S,过程Ⅱ的含硫产物是Na32SO 和35S。
2 3 2 4
15.(2023•浙江省6月选考,17节选)氮的化合物种类繁多,应用广泛。
(2)与碳氢化合物类似,N、H两元素之间也可以形成氮烷、氮烯。
①下列说法不正确的是___________。
A.能量最低的激发态N原子的电子排布式:1s22s12p33s1
资料整理【淘宝店铺:向阳百分百】B.化学键中离子键成分的百分数:CaN>MgN
3 2 3 2
C.最简单的氮烯分子式:NH
2 2
D.氮烷中N原子的杂化方式都是sp3
②氮和氢形成的无环氨多烯,设分子中氮原子数为n,双键数为m,其分子式通式为______。
③给出H+的能力:NH _______[ CuNH ]2+ (填“>”或“<”),理由是___________。
3 3
【答案】(2)① A ②NH ( ,m为正整数) ③< ④[CuNH ]2+形成配位键后,由于
n n+2−2m 3
Cu对电子的吸引,使得电子云向铜偏移,进一步使氮氢键的极性变大,故其更易断裂
【答案】(3) ①CaCN ②6
2
【解析】(2)①A项,能量最低的激发态N原子应该是2p能级上一个电子跃迁到3s能级,其电子排布
式:1s22s22p23s1,故A错误;B项,钙的金属性比镁的金属性强,则化学键中离子键成分的百分数:CaN
3 2
>MgN ,故B正确;C项,氮有三个价键,最简单的氮烯即含一个氮氮双键,另一个价键与氢结合,则
3 2
其分子式:NH ,故C正确;D项,氮烷中N原子有一对孤对电子,有三个价键,则氮原子的杂化方式都
2 2
是sp3,故D正确;故选A。②氮和氢形成的无环氨多烯,一个氮的氮烷为NH ,两个氮的氮烷为NH ,
3 2 4
三个氮的氮烷为NH ,四个氮的氮烷为NH ,设分子中氮原子数为n,其氮烷分子式通式为NH ,根据
3 5 4 6 n n+2
又一个氮氮双键,则少2个氢原子,因此当双键数为m,其分子式通式为NH ( ,m为正整数);
n n+2−2m
③[CuNH ]2+形成配位键后,由于Cu对电子的吸引,使得电子云向铜偏移,进一步使氮氢键的极性变大,
3
故其更易断裂,因此给出H+的能力:NH <[CuNH ]2+。
3 3
16.(15分) (2022•全国甲卷,35节选) (3)固态氟化氢中存在(HF)n形式,画出(HF) 的链状结构_______。
3
(4) CF =CF 和ETFE分子中C的杂化轨道类型分别为_______和_______;聚四氟乙烯的化学稳定性高
2 2
于聚乙烯,从化学键的角度解释原因_______。
【答案】(3)
(4) sp2 sp3 C-F键的键能大于聚乙烯中C-H的键能,键能越大,化学性质越稳定
【解析】(3)固体HF中存在氢键,则(HF) 的链状结构为 ;(4)CF =CF 中C原子
3 2 2
存在3对共用电子对,其C原子的杂化方式为sp2杂化,但其共聚物ETFE中C原子存在4对共用电子对,
其C原子为sp3杂化;由于F元素的电负性较大,因此在与C原子的结合过程中形成的C-F键的键能大于
聚乙烯中C-H的键能,键能的强弱决定物质的化学性质,键能越大,化学性质越稳定,因此聚四氟乙烯的
资料整理【淘宝店铺:向阳百分百】化学稳定性高于聚乙烯。
17.(15分) (2022•全国乙卷,35节选) (2)①一氯乙烯(C HCl)分子中,C的一个_______杂化轨道与Cl
2 3
的3p 轨道形成C-Cl_______键,并且Cl的3p 轨道与C的2p 轨道形成3中心4电子的大π键 。
x x x
②一氯乙烷(C HCl)、一氯乙烯(C HCl)、一氯乙炔(C HCl)分子中,C-Cl键长的顺序是_______,理由:
2 5 2 3 2
(ⅰ)C的杂化轨道中s成分越多,形成的 键越强:(ⅱ)_______。
【答案】(2) sp2 σ 一氯乙烷>一氯乙烯>一氯乙炔 Cl参与形成的大π键越多,形成的C-
Cl键的键长越短
【解析】(2)①一氯乙烯的结构式为 ,碳为双键碳,采取sp2杂化,因此C的一个
sp2杂化轨道与Cl的3p 轨道形成C-Clσ键。②C的杂化轨道中s成分越多,形成的C-Cl键越强,C-Cl键
x
的键长越短,一氯乙烷中碳采取sp3杂化,一氯乙烯中碳采取sp2杂化,一氯乙炔中碳采取sp杂化,sp杂化
时p成分少,sp3杂化时p成分多,因此三种物质中C-Cl键键长顺序为:一氯乙烷>一氯乙烯>一氯乙炔,
同时Cl参与形成的大π键越多,形成的C-Cl键的键长越短,一氯乙烯中Cl的3p 轨道与C的2p 轨道形成
x x
3中心4电子的大π键( ),一氯乙炔中Cl的3p 轨道与C的2p 轨道形成2套3中心4电子的大π键(
x x
),因此三种物质中C-Cl键键长顺序为:一氯乙烷>一氯乙烯>一氯乙炔。
18.(2022•河北省选择性考试,17节选) (3) SnCl -的几何构型为_______,其中心离子杂化方式为
3
_______。
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属
于顺磁性物质的是_______(填标号)。
A.[Cu(NH )]Cl B.[Cu(NH )]SO C.[ Zn(NH)]SO D.Na[Zn(OH) ]
3 2 3 4 4 3 4 4 2 4
(5)如图是硫的四种含氧酸根的结构:
A B C D
根据组成和结构推断,能在酸性溶液中将Mn2+转化为MnO -的是_______(填标号)。理由是_______。
4
【答案】(3) 三角锥形 sp3杂化
(4)B
(5) D D中含有-1价的O,易被还原,具有强氧化性,能将Mn2+转化为MnO -
4
资料整理【淘宝店铺:向阳百分百】【解析】(3)Sn是ⅣA族元素,SnCl -的中心离子Sn2+价层电子对数为3+ ,有1对孤电子
3
对,中心离子是sp3杂化,SnCl -的几何构型是三角锥形;(4)根据题意,具有顺磁性物质含有未成对电子。
3
A项,[Cu(NH )]Cl各原子核外电子均已成对,不符合题意;B项,[Cu(NH )]SO 中的Cu2+外围电子排布
3 2 3 4 4
是3d9,有未成对电子,符合题意;C项,[Zn(NH )]SO 各原子核外电子均已成对,不符合题意;D项,
3 4 4
Na[Zn(OH) ] 各原子核外电子均已成对,不符合题意;故选B。(5)Mn2+转化为MnO -需要氧化剂,且氧化
2 4 4
性比MnO -的强,由SO 使KMnO 溶液褪色可知HSO 的氧化性弱于MnO -,故A不符合;B、C中的S化
4 2 4 2 4 4
合价比HSO 低,氧化性更弱,故B、C均不符合;D中含有-1价的O,易被还原,具有强氧化性,能将
2 4
Mn2+转化为MnO -,故D符合。
4
19.(2022•海南省选择性考试,19节选) (3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价
值。酞菁分子结构如下图,分子中所有原子共平面,所有N原子的杂化轨道类型相同,均采取_______杂
化。邻苯二甲酸酐( )和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前者,主
要原因是_______。
【答案】(3) sp2 两者均为分子晶体,后者能形成分子间氢键,使分子间作用力增大,熔点更高
【解析】(3)根据结构式可知,N原子均形成双键,故N原子的杂化方式均为sp2,由于邻苯二甲酸酐
和邻苯二甲酰亚胺均为分子晶体,而后者能形成分子间氢键,使分子间作用力增大,因此熔点更高。
20.(15分) (2022•湖南选择性考试,18节选) (3)科学家近期合成了一种固氮酶模型配合物,该物质可
以在温和条件下直接活化H,将N3-转化为NH -,反应过程如图所示:
2 2
资料整理【淘宝店铺:向阳百分百】①产物中N原子的杂化轨道类型为_______;
②与NH -互为等电子体的一种分子为_______(填化学式)。
2
【答案】(3) sp3杂化 HO
2
【解析】(3)①由结构简式可知,产物中氮原子的价层电子对数为4,原子的杂化方式为sp3杂化;②水
分子和氨基阴离子的原子个数都为3、价电子数都为8,互为等电子体。
21.(2022•广东选择性考试,20节选) (2)HSe的沸点低于HO,其原因是_______。
2 2
(3)关于I~III三种反应物,下列说法正确的有_______。
A.I中仅有 键
B.I中的Se-Se键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有sp与sp2
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______。
(5)硒的两种含氧酸的酸性强弱为HSeO_______ H SeO(填“>”或“<”)。研究发现,给小鼠喂食适量
2 4 2 3
硒酸钠(Na SeO)可减轻重金属铊引起的中毒。SeO2-的立体构型为_______。
2 4 4
【答案】(2)两者都是分子晶体,由于水存在分子间氢键,沸点高
(3)BDE
(4)O、Se
(5)> 正四面体形
【解析】(2) H Se的沸点低于HO,其原因是两者都是分子晶体,由于水存在分子间氢键,沸点高;
2 2
(3)A项,I中有 键,还有大π键,故A错误;B项,Se−Se是同种元素,因此I中的Se−Se键为非极性共
价键,故B正确;C项,烃都是难溶于水,因此II难溶于水,故B错误;D项,II中苯环上的碳原子和碳
碳双键上的碳原子杂化类型为sp2,碳碳三键上的碳原子杂化类型为sp,故D正确;E.根据同周期从左到
右电负性逐渐增大,同主族从上到下电负性逐渐减小,因此I~III含有的元素中,O电负性最大,故E正确;
故选BDE。(4)根据题中信息IV中O、Se都有孤对电子,碳、氢、硫都没有孤对电子;(5)根据非羟基氧越
多,酸性越强,因此硒的两种含氧酸的酸性强弱为HSeO>HSeO。SeO2-中Se价层电子对数为
2 4 2 3 4
,其立体构型为正四面体形。
资料整理【淘宝店铺:向阳百分百】22.(2022•福建卷,14节选)(10分)1962年首个稀有气体化合物XePtF 问世,目前已知的稀有气体化
6
合物中,含氙( Xe)的最多,氪 ( Kr)次之,氩( Ar)化合物极少。[BrOF ][ AsF ]·xKrF 是[BrOF ]+、[ AsF ]-
54 36 18 2 2 2 2 2
与KrF 分子形成的加合物,其晶胞如下图所示。
2
回答下列问题:
(1)基态As原子的价电子排布式为_______。
(2) Ar、Kr、Xe原子的活泼性依序增强,原因是_______。
(3)晶体熔点:KrF _______ XeF (填“>”“<”或“=”),判断依据是_______。
2 2
(4) [BrOF ]+的中心原子Br的杂化轨道类型为_______。
2
(5) [BrOF ][ AsF]·xKrF 加合物中x=_______,晶体中的微粒间作用力有_____(填标号)。
2 2 2
a.氢键 b.离子键 c.极性共价键 d.非极性共价键
【答案】(1) 4s24p3
(2)同族元素,从上而下原子半径逐渐增大,原子核对外层电子的有效吸引逐渐减弱,失电子能力逐渐
增强
(3) < 二者为同构型的分子晶体,XeF 相对分子质量大,范德华力大,熔点高
2
(4) sp3
(5) 2 bc
【解析】(1)As位于元素周期表中第四周期VA族,原子序数为33,由构造原理写出其价电子排布式为
4s24p3。(2)同族元素,从上而下原子半径逐渐增大,原子核对外层电子的有效吸引逐渐减弱,失电子能力
逐渐增强,故Ar、Kr、Xe原子的活泼性依序增强。(3)KrF 和XeF 是同构型的分子晶体,XeF 相对分子质
2 2 2
量大,范德华力大,熔点高,晶体熔点:KrF < XeF 。(4)[BrOF ]+的中心原子Br的价层电子对数为:3+
2 2 2
=4,杂化轨道类型为sp3。(5)由晶胞结构可知,其中含有8个KrF 、4个[BrOF ]+、4个
2 2
[ AsF ]-,则[BrOF ][ AsF ]·xKrF 加合物中x=2,晶体中的微粒间作用力有离子键、极性共价键,故选bc。
2 2 2 2
23.(2022•山东卷,16)(12分)研究笼形包合物结构和性质具有重要意义。化学式为
资料整理【淘宝店铺:向阳百分百】Ni(CN)x·Zn(NH )y·zC H 的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶
3 6 6
胞。晶胞参数为 。回答下列问题:
(1)基态Ni原子的价电子排布式为_______,在元素周期表中位置为_______。
(2)晶胞中N原子均参与形成配位键,Ni2+与Zn2+的配位数之比为_______;x:y:z=_______;晶胞中
有d轨道参与杂化的金属离子是_______。
(3)吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的π 6大π键、则吡啶
6
中N原子的价层孤电子对占据_______(填标号)。
A.2s轨道 B.2p轨道 C.sp杂化轨道 D.sp2杂化轨道
(4)在水中的溶解度,吡啶远大于苯,主要原因是①_______,②_______。
(5) 、 、 的碱性随N原子电子云密度的增大而增强,其中
碱性最弱的是_______。
【答案】(1) 3d84s2 第4周期第VIII族 (2) 2:3 2:1:1 Zn2+ (3)D
(4) 吡啶能与HO分子形成分子间氢键 吡啶和HO均为极性分子相似相溶,而苯为非极性分
2 2
子
(5)
【解析】(1)已知Ni是28号元素,故基态Ni原子的价电子排布式为:3d84s2,在周期表中第四横行第
资料整理【淘宝店铺:向阳百分百】10纵列即位于第4周期第VIII族;(2)由题干晶胞示意图可知,一个晶胞中含有Ni2+个数为: =1,
Zn2+个数为: =1,含有CN-为: =4,NH 个数为: =2,苯环个数为: =2,则该晶胞的
3
化学式为:Ni(CN) ·Zn(NH )·2C H,且晶胞中每个N原子均参与形成配位键,Ni2+周围形成的配位键数目
4 3 2 6 6
为:4,Zn2+周围形成的配位键数目为:6,则Ni2+与Zn2+的配位数之比,4:6=2:3;x:y:z=4:2:2=2:
1:1;由以上分析可知,Ni2+的配位数为4,则Ni2+采用sp3杂化,而Zn2+的配位数为6,Zn2+采用sp3d2杂化,
即晶胞中有d轨道参与杂化的金属离子是Zn2+;(3)吡啶( )替代苯也可形成类似的笼形包合物。已知
吡啶中含有与苯类似的π 6大π键,则说明吡啶中N原子也是采用sp2杂化,杂化轨道只用于形成σ键和存
6
在孤电子对,则吡啶中N原子的价层孤电子对占据sp2杂化轨道,故选D;(4)已知苯分子为非极性分子,
HO分子为极性分子,且吡啶中N原子上含有孤电子对能与HO分子形成分子间氢键,从而导致在水中的
2 2
溶解度,吡啶远大于苯;(5)已知-CH 为推电子基团,-Cl是吸电子基团,则导致N原子电子云密度大小顺
3
序为: > > ,结合题干信息可知,其中碱性最弱的为: 。
24.(2021•全国乙卷,35节选) (3) [Cr(NH )(H O) Cl]2+中配体分子NH 、HO以及分子PH 的空间结
3 3 2 2 3 2 3
构和相应的键角如图所示。
PH 中P的杂化类型是_______。NH 的沸点比PH 的_______,原因是_______,HO的键角小于NH
3 3 3 2 3
的,分析原因_______。
【答案】(3)sp3 高 NH 存在分子间氢键 NH 含有一对孤对电子,而HO含有两对孤对电子,
3 3 2
HO中的孤对电子对成键电子对的排斥作用较大
2
【解析】(3) PH 的价层电子对为3+1=4,故PH 中P的杂化类型是sp3; N原子电负性较强,NH 分子
3 3 3
之间存在分子间氢键,因此NH 的沸点比PH 的高;HO的键角小于NH 的,原因是:NH 含有一对孤对
3 3 2 3 3
资料整理【淘宝店铺:向阳百分百】电子,而HO含有两对孤对电子,HO中的孤对电子对成键电子对的排斥作用较大。
2 2
25.(2021•广东选择性考试,19节选)(4)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法
正确的有________。
A.在I中S原子采取sp3杂化 B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180° D.在Ⅲ中存在离子键与共价键
E. 在Ⅳ中硫氧键的键能均相等
(5)汞解毒剂的水溶性好,有利于体内 重金属元素汞的解毒。化合物I与化合物Ⅲ相比,水溶性较好的
是________。
【答案】(4)D (5)化合物III
【解析】(4)A项, 中S原子的价层电子对数=2+ =4,因此S原子采取sp3杂化,故A
正确;B项, 中含有的元素为H、C、O、S、Hg,同周期元素从左至右元素的电负性逐渐增大,
同主族元素从上至下元素的电负性逐渐减小,因此5种元素中电负性最大的为O元素,故B错误;C项,
中C原子成键均为单键,因此C原子采取sp3杂化,所以C-C-C键角接近109º28’,故C错误;
D项, 中存在C-H、C-C、C-S、S=O、S-O、S-H共价键和 与Na+之间的离子键,故D正确;
故选BD。(5) 中羟基能与水分子之间形成分子间氢键, 为易溶于水的钠盐,溶于水后电
资料整理【淘宝店铺:向阳百分百】离出的 中O原子均能与水分子之间形成氢键,相同物质的量两种物质溶于水后, 形成的氢
键更多,因此化合物III更易溶于水。
26.(2021•全国甲卷,35节选)我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为
“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。
回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排式为________;单晶硅的晶体类
型为_________。SiCl 是生产高纯硅的前驱体,其中Si采取的杂化类型为_______。SiCl 可发生水解反应,
4 4
机理如下:
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、
③sp3d2,中间体SiCl (H O)中Si采取的杂化类型为________(填标号)。
4 2
(2)CO 分子中存在_______个 键和______个 键。
2
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CHSH,7.6℃)之间,其原因是________。
3
【答案】(1)3s23p2 原子晶体(共价晶体) sp3 ②
(2) 2 2
(3)甲硫醇不能形成分子间氢键,而水和甲醇均能,且水比甲醇的氢键多
【解析】(1)基态Si原子的核外电子排布式为1s22s22p63s23p2,因此Si的价电子层的电子排式为
3s23p2;晶体硅中Si原子与Si原子之间通过共价键相互结合,整块晶体是一个三维的共价键网状结构,因
此晶体硅为原子晶体;SiCl 中Si原子价层电子对数为4+ =4,因此Si原子采取sp3杂化;由图可知,
4
SiCl (H O)中Si原子的δ键数为5,说明Si原子的杂化轨道数为5,由此可知Si原子的杂化类型为sp3d;
4 2
(2)CO 的结构式为O=C=O,1个双键中含有1个δ键和1个π键,因此1个CO 分子中含有2个δ键和2个
2 2
π键;(3)甲醇分子之间和水分子之间都存在氢键,因此沸点高于不含分子间氢键的甲硫醇,甲醇分子之间
氢键的总强度低于水分子之间氢键的总强度,因此甲醇的沸点介于水和甲硫醇之间。
27.(2021•海南选择性考试,19节选) (14分) (4)CO 2-中碳原子的杂化轨道类型是___________,写出
3
一种与具有相同空间结构的-1价无机酸根离子的化学式___________。
(5) CH Mn(CO) 可看作是HMn(CO) 中的氢原子被甲基取代的产物。CHMn(CO) 与I 反应可用于制备
3 5 5 3 5 2
CHI,反应前后锰的配位数不变,CHMn(CO) 与I 反应的化学方程式为___________。
3 3 5 2
资料整理【淘宝店铺:向阳百分百】【答案】(4)sp2 NO -
3
(5)CH Mn(CO) +I →CHI+ MnI(CO)
3 5 2 3 5
【解析】(4)①根据价层电子对互斥理论,CO2-中心原子C连接3个O原子,所以δ键为3,孤电子对
3
数 (阴离子计算孤电子对数时,所带负电荷绝对值要与中心原子价电子数相加),所
以CO2-中C原子价层电子对数为3,孤电子对数为0,故其离子结构为平面三角形;再根据价层电子对数
3
与杂化轨道对应关系,可知CO2-中C原子的杂化轨道类型是sp2,故本问第一空应填“sp2”;②按题目要求,
3
阴离子中心原子价层电子对数应为3,孤电子对数为0,带电荷量为-1,无机酸根一般是含氧酸阴离子,所
以代入孤电子对公式可解得其中心原子价电子数为5,所以本问第二空应填“NO -”;(5)根据题目描述,
3
CHMn(CO) 与I 交换原子(或原子团),形成新物质,故本问应填“CHMn(CO) +I →CHI+ MnI(CO) ”。
3 5 2 3 5 2 3 5
28.(2021•湖南选择性考试,18节选) (2)硅和卤素单质反应可以得到SiX。
4
SX 的熔沸点
4
SiF SiCl SiBr SiI
4 4 4 4
熔点/K 183.0 203.2 278.6 393.7
沸点/K 187.2 330.8 427.2 560.7
①0℃时,SiF 、SiCl 、SiBr 、SiI 呈液态的是 (填化学式),沸点依次升高的原
4 4 4 4
因是 ,气态SiX 分子的空间构型是 ;
4
②SiCl 与N﹣甲基咪唑( )反应可以得到M2+,其结构如图所示:
4
N﹣甲基咪唑分子中碳原子的杂化轨道类型为 ,H、C、N的电负性由大到小的
顺序为 ,1个M2+中含有 个σ键;
【答案】(2)①SiCl SiX 都是结构相似的分子晶体,相对分子质量依次增大,分子间作用力依次增
4 4
大 正四面体形 ② sp2、sp3 N>C>H 54
【解析】(2)①0℃为273K,呈液态的物质是:熔点<273K<沸点;根据表中数据知,SiF 的熔沸点都
4
比273K低,而SiBr 和SiI 的熔沸点都比273K高,只有SiCl 的熔点低于273K,沸点高于273K;根据表
4 4 4
中数据知,其熔沸点依次升高,这4种物质熔沸点都较低,说明为分子晶体,且都不含有氢键,结构相似
的分子晶体熔沸点与分子间作用力成正比,其相对分子质量依次增大,分子间作用力逐渐增强,所以其熔
资料整理【淘宝店铺:向阳百分百】1
沸点依次升高;根据价层电子对互斥理论,SiX 分子的中心原子的价层电子对数个数为4+ (4﹣4×1)=4,
4 2
则分子空间构型为正四面体构型;②甲基的C原子形成4个σ键,无孤电子对,C原子价层电子对个数是
4,为sp3杂化;环上C原子形成3个σ键,无孤电子对,价层电子对个数是3,为sp2杂化;元素非金属性
越强,其电负性越大,元素的非金属性大小:N>C>H,则电负性大小顺序为N>C>H;共价单键为σ键、
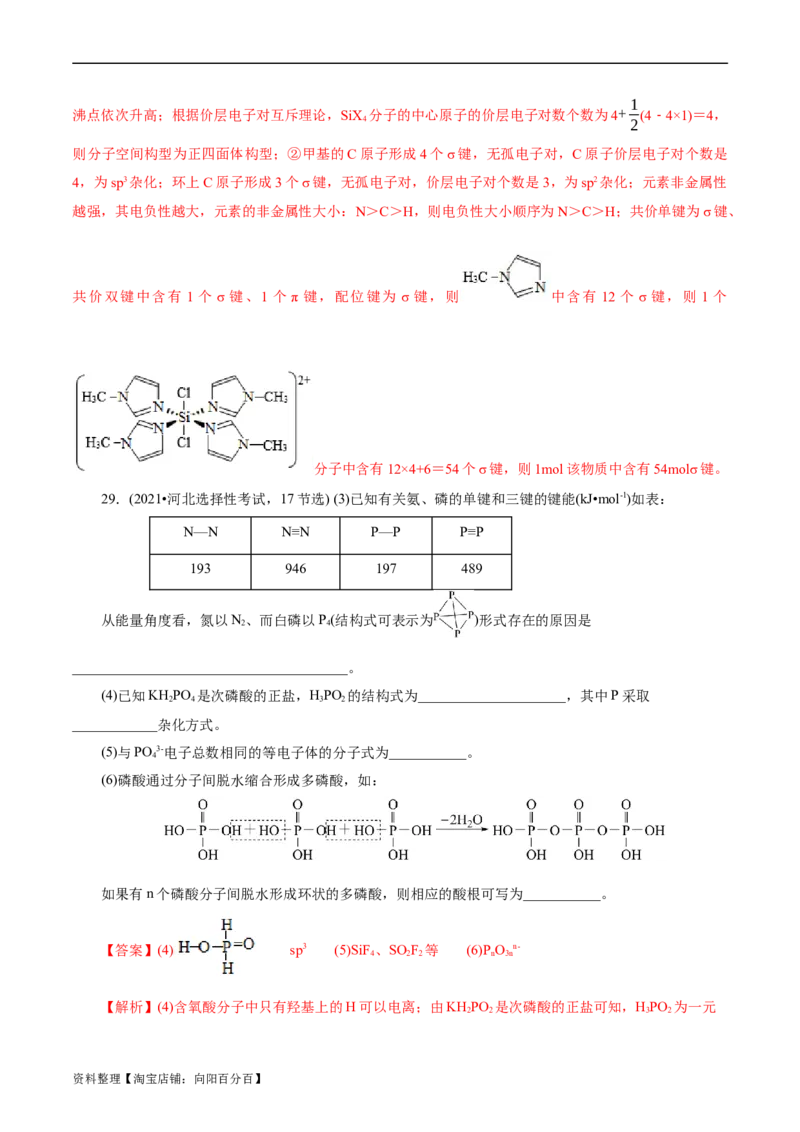
共价双键中含有 1 个 σ 键、1 个 π 键,配位键为 σ 键,则 中含有 12 个 σ 键,则 1 个
分子中含有12×4+6=54个σ键,则1mol该物质中含有54molσ键。
29.(2021•河北选择性考试,17节选) (3)已知有关氨、磷的单键和三键的键能(kJ•mol-1)如表:
N—N N≡N P—P P≡P
193 946 197 489
从能量角度看,氮以N、而白磷以P(结构式可表示为 )形式存在的原因是
2 4
_______________________________________。
(4)已知KH PO 是次磷酸的正盐,HPO 的结构式为_____________________,其中P采取
2 4 3 2
____________杂化方式。
(5)与PO 3-电子总数相同的等电子体的分子式为___________。
4
(6)磷酸通过分子间脱水缩合形成多磷酸,如:
如果有n个磷酸分子间脱水形成环状的多磷酸,则相应的酸根可写为___________。
【答案】(4) sp3 (5)SiF 、SO F 等 (6)P O n-
4 2 2 n 3n
【解析】(4)含氧酸分子中只有羟基上的H可以电离;由KH PO 是次磷酸的正盐可知,HPO 为一元
2 2 3 2
资料整理【淘宝店铺:向阳百分百】酸,其分子中只有一个羟基,另外2个H与P成键,还有一个O与P形成双键,故其结构式为
,其中P共形成4个σ键、没有孤电子对,故其价层电子对数为4,其采取sp3杂化。(5)等电
子体之间的原子总数和价电子总数都相同,根据前加后减、前减后加、总数不变的原则,可以找到与PO 3-
4
电子总数相同的等电子体分子为SiF、SO F 等。(6)由题中信息可知,n个磷酸分子间脱去(n-1)个水分子形
4 2 2
成链状的多磷酸,因此,如果有n个磷酸分子间脱水形成环状的多磷酸,则可脱去n个水分子得到
(HPO ),其失去H+后得到相应的酸根,故该酸根可写为PO n-。
3 n n 3n
资料整理【淘宝店铺:向阳百分百】