文档内容
考点 8 微粒间相互作用力
本考点考查化学键的本质是原子间的静电作用,着重分析分子间作用力和氢键对物质性质的影响,对
于结构和组成相似的物质,随着相对分子质量的增加,范德华力增强,范德华力越强,物质的熔点和沸点
越高;氢键属于一种较强的分子间作用力,分子间氢键使物质的熔、沸点升高,溶解性增大。
预测2023年化学键高考考查力度不是很大,注意有关概念辨析、化学键类型与存在的判断,能多角度、
动态的分析化学键,分析比较化学用语;分子间作用力对物质物理性质的影响;通过氢键解释一些有关的
反常物理性质。以实现宏观辨识与微观探析学科核心素养的提升。
一、化学键
二、分子间作用力
三、氢键
四、化学用语
化学键
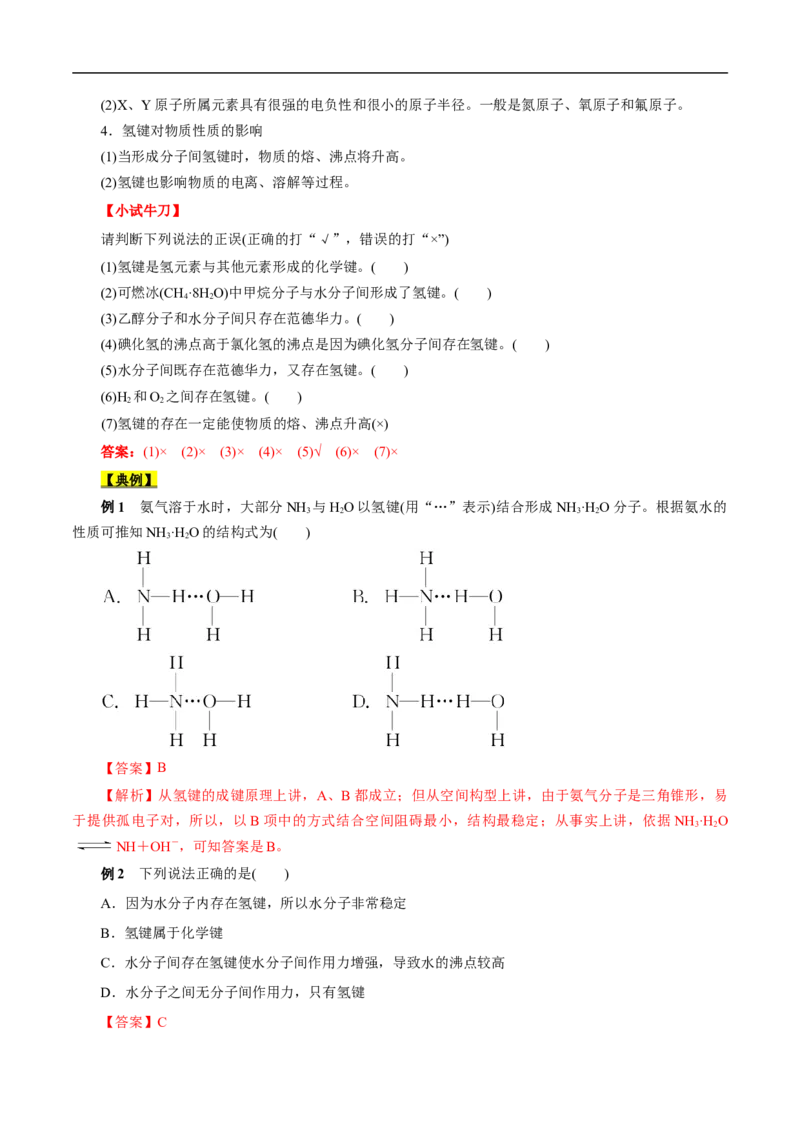
1.化学键
(1)化学键的定义及分类
(2)化学反应的本质:反应物的旧化学键断裂与生成物的新化学键形成。
2.共价键与离子键的比较
键型 共价键 离子键
原子间通过共用电子对形成的强烈 使带相反电荷的阴、阳离子结合的相
定义
的相互作用 互作用
成键微粒 原子 阴、阳离子成键原因 原子有形成稳定结构的趋势 原子有形成稳定结构的趋势
成键方式 共用电子对 阴、阳离子间的静电作用
一般为活泼金属元素(通常指ⅠA
成键元素 一般为非金属元素 族、ⅡA族元素)与活泼非金属元素
(通常指ⅥA族、ⅦA族元素)
3.共价键的分类
共价键类型 形成原子种类 电子对偏向情况
非极性共价键 同种元素原子 无偏向
极性共价键 不同种元素的原子 偏向吸引电子能力强的一方
4.化学键与物质类别
(1)只含有共价键的物质
①同种非金属元素构成的单质,如I、N、P、金刚石、晶体硅等。
2 2 4
②不同种非金属元素构成的共价化合物,如HCl、NH 、SiO、CS 等。
3 2 2
(2)只含有离子键的物质
活泼非金属元素与活泼金属元素形成的化合物,如NaS、CsCl、KO、NaH等。
2 2
(3)既含有离子键又含有共价键的物质
如NaO、NH Cl、NaOH、NaSO 等。
2 2 4 2 4
(4)无化学键的物质
稀有气体,如氩气、氦气等。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1) 只含共价键的物质一定是共价化合物( )
(2)由非金属元素组成的化合物不一定是共价化合物( )
(3)非极性键只存在于双原子单质分子里( )
(4)不同元素组成的多原子分子里的化学键一定是极性键( )
(5)化学键是相邻离子或原子间的一种强作用力,既包括静电吸引力,又包括静电排斥力( )
(6)所有物质中都存在化学键( )
(7)由活泼金属元素与活泼非金属元素形成的化学键都是离子键( )
(8)原子最外层只有一个电子的元素原子跟卤素原子结合时,所形成的化学键一定是离子键(×)
(9)非金属元素的两个原子之间一定形成共价键,但多个原子间也可能形成离子键( )
(10)离子化合物中可能含有共价键,共价化合物中一定不含离子键( )
(11)NaOH和NaO 中均含共价键和离子键( )
2 2
(12)将NaH溶于水,得到的水溶液能导电说明NaH是离子化合物( )
(13)形成离子键的阴、阳离子间只存在静电吸引力( )
(14)全部由非金属元素形成的化合物一定是共价化合物( )(15)某些金属与非金属原子间能形成共价键( )
(16)分子中只有共价键的化合物一定是共价化合物( )
(17)在水溶液中能导电的化合物一定是离子化合物( )
(18)离子化合物在任何状态下都能导电( )
答案:(1)× (2) √ (3)× (4)× (5) √ (6)× (7)× (8)× (9) √ (10)√ (11)√ (12)× (13)× (14)×
(15)√ (16)× (17) (18)×
【典例】
例1 (2019•上海卷)下列反应只需要破坏共价键的是( )
A.晶体硅熔化 B.碘升华 C.熔融 Al O D.NaCl 溶于水
2 3
【答案】A
【解析】A项,晶体硅为原子晶体,Si 原子之间只以共价键连接,因此熔化只需要破坏共价键,A 正
确;B项,碘为分子晶体,升华克服分子间作用力,B 错误;C项,Al O 为离子晶体,熔融破坏离子键,
2 3
C 错误;D项,NaCl 为离子晶体,溶于水电离成钠离子和氯离子,破坏离子键,D 错误。
例2 (2022•浙江1月选考)下列含有共价键的盐是( )
A.CaCl B.HSO C.Ba(OH) D.NaCO
2 2 4 2 2 3
【答案】D
【解析】A项,CaCl 由Ca2+和Cl-构成,只含有离子键不含有共价键,A不符合题意;B项,HSO 由
2 2 4
分子构成,只含有共价键不含有离子键,B不符合题意;C项,Ba(OH) 由Ba2+和OH-构成,属于碱,不属
2
于盐,C不符合题意;D项,NaCO 有Na+和CO2-构成,含有离子键,CO2-内部C与O原子之间还含有共
2 3 3 3
价键,D符合题意;故选D。
【对点提升】
对点1 下列关于化学键的叙述中,正确的是( )
A.共价化合物中可能含离子键,离子化合物中只含离子键
B.离子化合物中可能含共价键,共价化合物中不含离子键
C.构成单质分子的微粒一定含有共价键
D.在氧化钠中,只存在氧离子和钠离子的静电吸引作用
【答案】B
【解析】离子化合物是阴、阳离子通过离子键结合而成的,因此,离子化合物中一定含有离子键;除
离子键外,离子化合物中还可能含共价键,如NaOH是由Na+和OH-结合而成的离子化合物,而OH-中含
O—H共价键;在共价化合物中各原子均通过共用电子对相结合,不存在离子键,故B正确,A错误。稀
有气体分子中不存在化学键,C错误。在离子化合物中除阴、阳离子电荷之间的静电吸引作用外,还存在
电子与电子、原子核与原子核之间的排斥作用,D错误。
对点2 下列各组中每种物质都既有离子键又有共价键的一组是( )
A.NaOH HSO (NH )SO B.MgO NaSO HNO
2 4 4 2 4 2 4 3C.NaO KOH NaPO D.HCl Al O MgCl
2 2 3 4 2 3 2
【答案】C
【解析】HSO 中只含共价键,A错误;MgO中只含离子键,HNO 中只含共价键,B错误;各物质均
2 4 3
只含一种化学键,分别是共价键、离子键和离子键,D错误。
【巧学妙记】
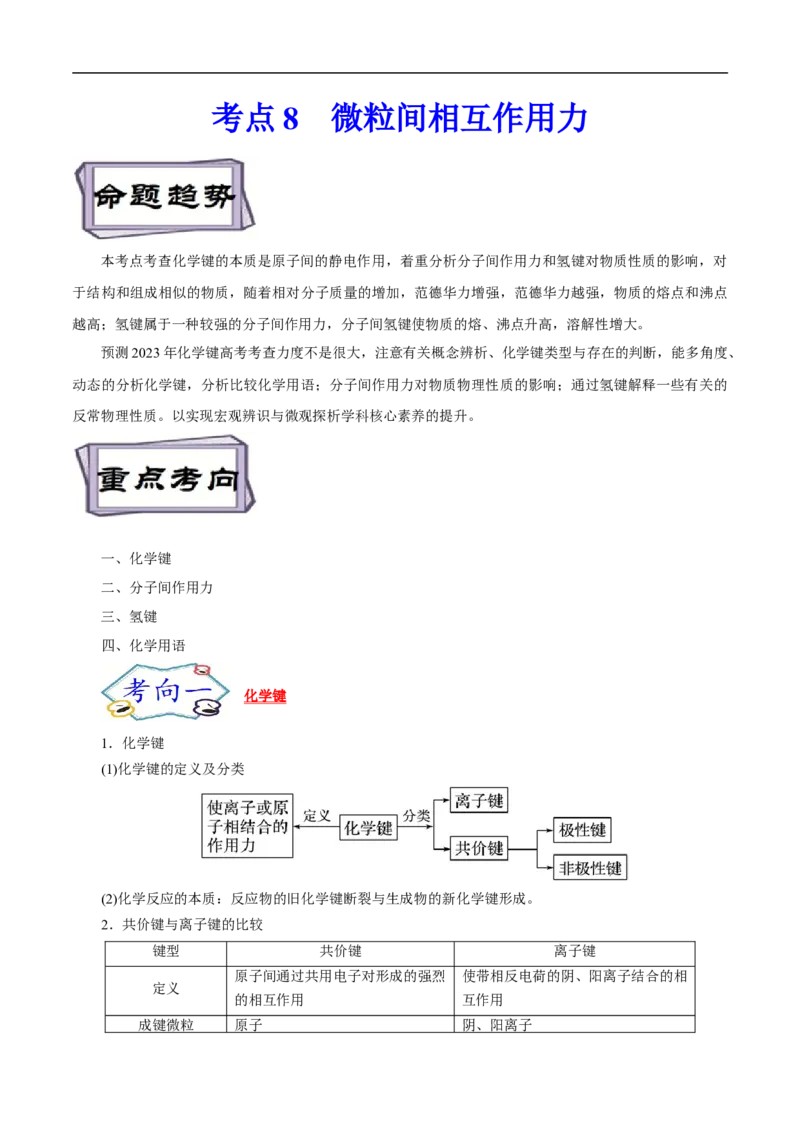
1.化学键与化合物的关系
2.判断离子化合物和共价化合物的三种方法
分子间作用力
1.分子间作用力的概念:分子间存在着将分子聚集在一起的作用力,这种作用力称为分子间作用力,
亦可称为范德华力。
2.分子间作用力的特征:
(1)分子间作用力比化学键弱得多。
(2)存在于分子之间,且分子充分接近时才有相互间的作用力,如固体和液体物质中。
(3)分子间作用力主要影响有分子构成物质的熔沸点、溶解性等物理性质,而化学键主要影响物质的化
学性质。如水从液态转化为气态只需要克服分子间作用力,而水分解需要破坏化学键。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)范德华力存在于任何物质中( )
(2)范德华力比化学键弱得多( )(3)CH 、C H、C H 的熔点、沸点依次升高( )
4 2 6 3 8
(4)HF、HCl、HBr、HI的稳定性依次减弱,是因为分子间作用力依次减弱( )
(5)卤素单质、卤素氢化物、卤素碳化物(即CX)的熔、沸点均随着相对分子质量的增大而增大(×)
4
(6)加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏( )
(7)CO 溶于水和干冰升华都只有分子间作用力改变( )
2
(8)石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏( )
答案:(1)× (2)√ (3)√ (4)× (5)× (6)√ (7)× (8)√
【典例】
例1 共价键、离子键和分子间作用力是构成物质的微粒间的不同作用方式,下列物质中,存在分子
间作用力和共价键的是( )
A.干冰 B.氯化钠 C.氢氧化钠 D.金刚石
【答案】A
【解析】干冰是由分子构成的物质,分子间存在着分子间作用力,分子内存在共价键。氯化钠的离子
化合物,只存在离子键。氢氧化钠是离子化合物,它不仅存在离子键,其“OH—”中还存在共价键。金刚
石是由原子构成的物质,只存在共价键。
例2 下列叙述与范德华力无关的是( )
A.气体物质在加压或降温时能凝结或凝固
B.干冰易于升华
C.氟、氯、溴、碘单质的熔点、沸点依次升高
D.氯化钠的熔点较高
【答案】D
【解析】一般来说,由分子构成的物质,其物理性质通常与范德华力的大小密切相关。A、B、C三个
选项中涉及的物质都是由分子构成,故其表现的物理性质与范德华力的大小有关系。只有D选项中的NaCl
是离子化合物,不存在分子,故其物理性质与范德华力无关。
【对点提升】
对点1 下列物质的性质可用范德华力的大小来解释的是( )
A.HF、HCl、HBr、HI的热稳定性依次减弱
B.F、Cl、Br 、I 的熔、沸点依次升高
2 2 2 2
C. 、H—O—H、C H—OH中—OH上氢原子的活泼性依次减弱
2 5
D.CH—O—CH 、C HOH的沸点依次升高
3 3 2 5
【答案】B
【解析】HF、HCl、HBr、HI的热稳定性依次减弱是由于H—X键键能依次减小。F 、Cl 、Br 、I 的
2 2 2 2相对分子质量依次增大,分子间的范德华力也依次增大,所以其熔、沸点也依次增大。 、H
—O—H、C H—OH中—OH上氢原子的活泼性依次减弱,与O—H键的极性有关。CH—O—CH 的沸点
2 5 3 3
比C HOH的低是由于C HOH分子间形成氢键而增大了分子间作用力。
2 5 2 5
对点2 下列关于范德华力的叙述中,正确的是( )
A.范德华力的实质也是一种电性作用,所以范德华力是一种特殊化学键
B.范德华力与化学键的区别是作用力的强弱不同
C.任何分子间在任意情况下都会产生范德华力
D.范德华力非常微弱,故破坏范德华力不需要消耗能量
【答案】B
【解析】范德华力是分子与分子之间的一种相互作用,其实质与化学键类似,也是一种电性作用,但
两者的区别是作用力的强弱不同。化学键必须是强烈的相互作用(120~800 kJ/mol),范德华力只有几到几
十千焦每摩尔,故范德华力不是化学键;虽然范德华力非常微弱,但破坏它时也要消耗能量;范德华力普
遍地存在于分子之间,但也必须满足一定的距离要求,若分子间的距离足够大,分子之间也难产生相互作
用。
【巧学妙记】
化学键与分子间的作用力比较:
微粒间作用力 组成微粒 存在 作用力 影响范围
阴、阳离
离子键 离子化合物 强 离子化合物的化学性质
子
化 学
键 共价化合物、离
单质、化合物的化学性
共价键 子化合物、非金 强
原子 属单质 质
分子间作 熔沸点、溶解度等物理
分子 分子间 弱
分 子 用力 性质
间 作
用力 熔沸点、溶解度等物理
氢键 分子 分子间 弱
性质
氢键
1.氢键的概念
当氢原子与电负性大的原子X以共价键结合时,H原子与另一个电负性大的原子Y之间的静电相互作
用和一定程度的轨道重叠作用。
2.氢键的表示形式
(1)通常用X—H…Y表示氢键,其中X—H表示氢原子和X原子以共价键相结合。
(2)氢键的键长是指X和Y间的距离,键能是指X—H…Y分解为 X—H和Y所需要的能量。
3.氢键形成的条件
(1)氢原子位于X原子和Y原子之间。(2)X、Y原子所属元素具有很强的电负性和很小的原子半径。一般是氮原子、氧原子和氟原子。
4.氢键对物质性质的影响
(1)当形成分子间氢键时,物质的熔、沸点将升高。
(2)氢键也影响物质的电离、溶解等过程。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)氢键是氢元素与其他元素形成的化学键。( )
(2)可燃冰(CH·8H O)中甲烷分子与水分子间形成了氢键。( )
4 2
(3)乙醇分子和水分子间只存在范德华力。( )
(4)碘化氢的沸点高于氯化氢的沸点是因为碘化氢分子间存在氢键。( )
(5)水分子间既存在范德华力,又存在氢键。( )
(6)H 和O 之间存在氢键。( )
2 2
(7)氢键的存在一定能使物质的熔、沸点升高(×)
答案:(1)× (2)× (3)× (4)× (5)√ (6)× (7)×
【典例】
例1 氨气溶于水时,大部分NH 与HO以氢键(用“…”表示)结合形成NH ·H O分子。根据氨水的
3 2 3 2
性质可推知NH ·H O的结构式为( )
3 2
【答案】B
【解析】从氢键的成键原理上讲,A、B都成立;但从空间构型上讲,由于氨气分子是三角锥形,易
于提供孤电子对,所以,以B项中的方式结合空间阻碍最小,结构最稳定;从事实上讲,依据NH ·H O
3 2
NH+OH-,可知答案是B。
例2 下列说法正确的是( )
A.因为水分子内存在氢键,所以水分子非常稳定
B.氢键属于化学键
C.水分子间存在氢键使水分子间作用力增强,导致水的沸点较高
D.水分子之间无分子间作用力,只有氢键
【答案】C【解析】水分子之间存在分子间作用力,也存在氢键,由于氢键的存在,使得水的沸点较高,化学键
是分子内相邻原子或离子之间强烈的相互作用,由于HO中氢氧共价键较强,故水分子较稳定,氢键不属
2
于化学键。
【对点提升】
对点1 下列事实与氢键无关的是( )
A.液态氟化氢中有三聚氟化氢(HF) 分子存在
3
B.冰的密度比液态水的密度小
C.乙醇能与水以任意比混溶而甲醚(CH—O—CH )难溶于水
3 3
D.NH 比PH 稳定
3 3
【答案】D
【解析】氢键是已经与电负性很强的原子形成共价键的氢原子与另一个分子中电负性很强的原子之间
的作用力,它只影响物质的物理性质,故只有D与氢键无关。
对点2 固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。下列叙述错误的是( )
A.冰表面第一层中,HCl以分子形式存在
B.冰表面第二层中,H+浓度为5×10−3 mol·L−1(设冰的密度为0.9 g·cm−3)
C.冰表面第三层中,冰的氢键网格结构保持不变
D.冰表面各层之间,均存在可逆反应HCl H++Cl−
【答案】D
【解析】A项,图可知,冰的表面第一层主要为氯化氢的吸附,氯化氢以分子形式存在,故 A正确;
B项,题给数据可知,冰的表面第二层中氯离子和水的个数比为10—4:1,第二层中溶解的氯化氢分子应少
于第一层吸附的氯化氢分子数,与水的质量相比,可忽略其中溶解的氯化氢的质量。设水的物质的量为
1mol,则所得溶液质量为18g/mol×1mol=18g,则溶液的体积为 ×10—3L/ml=2.0×10—2L,由第二层
氯离子和水个数比可知,溶液中氢离子物质的量等于氯离子物质的量,为 10—4mol,则氢离子浓度为=5×10—3mol/L,故B正确;C项,图可知,第三层主要是冰,与氯化氢的吸附和溶解无关,冰的氢
键网络结构保持不变,故C正确;D项,图可知,只有第二层存在氯化氢的电离平衡HCl H++Cl—,
而第一层和第三层均不存在,故D错误。故选D。
【巧学妙记】
范德华力 氢键 共价键
已经与电负性很强的原子
物质分子之间普遍存在的一 形成共价键的氢原子与另 原子间通过共用电子
概念
种作用力 一个电负性很强的原子之 对所形成的相互作用
间的静电作用
极性共价键
分类 分子内氢键、分子间氢键
非极性共价键
特征 无方向性和饱和性 有方向性和饱和性 有方向性和饱和性
强度 共价键>氢键>范德华力
①随分子极性的增大而增大 成键原子半径和共用
影响强 对于X—H…Y,X、Y的
度 ②组成和结构相似的物质, 电负性越大,Y原子的半 电子对数目。键长越
相对分子质量越大,分子间 短,键能越大,共价
的因素 作用力越大 径越小,作用越强 键越稳定
①影响物质的熔点、沸点、
溶解度等物理性质 分子间氢键的存在,使物
对物质
质的熔、沸点升高,在水 ①影响分子的稳定性
性 ②组成和结构相似的物质,
中的溶解度增大,如熔、
随相对分子质量的增大,物 ②共价键键能越大,
质的影 质的熔、沸点升高。如 沸点:H 2 O>H 2 S, 分子稳定性越强
响 F 2 HCl,NH 3 >PH 3
CFH O>NH
3 2 2 3B.氢键只能存在于分子间,不能存在于分子内
C.没有氢键,就没有生命
D.相同量的水在气态、液态和固态时均有氢键,且氢键的数目依次增多
【答案】C
【解析】NH 、HO、HF在常温下只有HO是液体,所以水的沸点最高。氢键既可以存在于分子间,
3 2 2
又可以存在于分子内。水在气态时,分子间距过大,水分子间没有氢键。
49.关于氢键,下列说法正确的是( )
A.每一个水分子内含有两个氢键
B.冰、水中都存在氢键
C.分子间形成的氢键使物质的熔点和沸点降低
D.HO是一种非常稳定的化合物,这是由于氢键所致
2
【答案】B
【解析】A项,氢键是一种特殊的分子间作用力,只存在于水分子之间,水分子内没有氢键,故A错
误;B项,冰和水分子中都存在氢键,故B正确;C项,水只能形成分子间氢键,分子间形成的氢键使物
质的熔点和沸点升高,故C错误;D项,氢键不是化学键,HO是一种非常稳定的化合物,说明了氧的非
2
金属性很强,与水分子之间的氢键无关,故D错误;故选B。
50.下列说法不正确的是( )
A.HCl、HBr、HI的熔、沸点依次升高与分子间作用力大小有关
B.标准状况下,N 个HF分子约为22.4L
A
C.I 易溶于CCl 可以用相似相溶原理解释
2 4
D.NH 分子间存在氢键,故氨气易液化
3
【答案】B
【解析】A项,HCl、HBr、HI均为分子晶体,结构相似,相对分子质量依次增加,分子间作用力依
次增加,熔、沸点依次升高,A正确;B项,标况下HF不是气体,无法计算体积,B错误;C项,I 和
2
CCl 均为非极性分子,非极性分子易溶于非极性溶剂,可以用相似相溶原理解释,C正确;D项,N原子
4
电负性较大,所以NH 分子间存在氢键,沸点较低,易液化,D正确;故选B。
3
51.下列说法正确的是( )
A.干冰气化克服范德华力和共价键
B.HO的热稳定性比HS强,是由于HO分子间形成氢键
2 2 2
C.2NaO+4HCl=4NaCl+2H O+O↑,该反应既有离子健、极性健和非极性键的断裂又有其形成
2 2 2 2
D.KCl、HCl、KOH的水溶液都能导电,所以它们都属于离子化合物【答案】C
【解析】A项,干冰气化只需要克服范德华力,不需要克服共价键,故A错误;B项,HO的热稳定
2
性比HS强,是由于氧元素的非金属性强于硫元素,与HO分子间形成氢键无关,故B错误;C项,过氧
2 2
化钠和氯化钠为离子化合物,氯化氢和水为共价化合物,氧气为非金属单质,则过氧化钠与氯化氢反应时,
既有离子健、极性健和非极性键的断裂又有离子健、极性健和非极性键的形成,故C正确;D项,氯化氢
是共价化合物,故D错误;故选C。
52.下列说法正确的是( )
A.范德华力普遍存在于分子之间,如液态水中因范德华力的存在使水分子发生缔合
B.HSO 为强电解质,硫酸晶体是能导电的
2 4
C.冰中1个HO可通过氢键与4个水分子相连,所以冰中HO分子与氢键的比值为1:4
2 2
D.因为水分子间氢键,液态水结成冰时体积会变大
【答案】D
【解析】A项,液态水中因分子间氢键的存在使水分子发生缔合,A不正确;B项,虽然HSO 为强
2 4
电解质,但是硫酸晶体是分子晶体,其不能导电,B不正确;C项,冰中1个HO可通过氢键与4个水分
2
子相连,两个水分子间只能形成一个氢键,所以冰中HO分子与氢键的比值为1:2,C不正确;D项,氢
2
键有饱和性和方向性,所以液态水结成冰时水分子之间的空隙变大,故其体积会变大,D正确;故选D。
53.如表为元素周期表的一部分,请回答有关问题:
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
1 ①
2 ② ③ ④
3 ⑤ ⑥ ⑦ ⑧
4 ⑨ ⑩
(1)已知第四周期有18种元素,其中元素⑩的一种核素,中子数为45,用原子符号表示该核素为
_______。
(2)由元素①和④形成的10电子分子的结构式为_______。
(3)用电子式表示元素⑤和⑦的原子形成的化合物(该化合物含有三个原子核)的形成过程_______。
(4)由元素④和⑤构成的淡黄色固体,该化合物所含的化学键类型为_______,元素④和⑦的简单氢化
物沸点较高的是_______(填化学式),理由是:_______。元素⑧和⑩的最高价氧化物对应的水化物酸性较强的是(填化学式)_______。
(5)元素⑦、⑧、⑨的离子半径由大到小的顺序是_______(用离子符号表示);元素⑨的最高价氧化物的
水化物与元素⑥的最高价氧化物反应的离子方程式为_______。
(6)已知NH •H O的电离方程式为NH •H O NH ++OH-,试判断NH 溶于水后形成的NH •H O的
3 2 3 2 4 3 3 2
合理结构_______(填字母代号)。
【答案】(1) Br (2)H—O—H
(3)
(4)离子键、非极性共价键 HO 水分子间存在氢键 HClO
2 4
(5)r(S2-)>r(Cl-)>r(K+) Al O+2OH-=2AlO -+H O (6)b
2 3 2 2
【解析】(1)元素⑩为Br,质子数为35,中子数为45,则质量数为35+45=80,用原子符号表示该核素
为 Br。(2)元素①为H,④为O,形成的10电子分子为HO,结构式为H—O—H。(3)元素⑤为Na,⑦为
2
S,形成的含有三个原子核的化合物为NaS,用电子式表示其形成过程为:
2
。(4)元素④为O,⑤为Na,两者构成的淡黄色固体为
NaO,该化合物是离子化合物,含有离子键,阴离子过氧根离子里还含有非极性共价键;元素④为O,⑦
2 2
为S,由于水分子间存在氢键,所以HO的沸点较高。元素⑧为Cl,⑩为Br,元素的非金属性越强,最高
2
价氧化物对应的水化物的酸性越强,Cl和Br是同族元素,Cl的非金属性强于Br,则Cl的最高价氧化物对
应的水化物HClO 酸性较强。(5)元素⑦、⑧、⑨的离子分别为S2-、Cl-、K+,电子层结构相同,质子数越
4
多,半径越小,所以这三种离子半径由大到小的顺序是r(S2-)>r(Cl-)>r(K+);元素⑨为K,最高价氧化物的
水化物为KOH,元素⑥为Al,最高价氧化物为Al O,两者反应的离子方程式为Al O+2OH-=2AlO -
2 3 2 3 2
+H O。(6)NH •H O的电离方程式为NH •H O NH ++OH-,当NH 溶于水后,和水分子间形成氢键,
2 3 2 3 2 4 3
要形成NH +,则需要用NH 的N和水分子中的H形成氢键,则形成的NH •H O的合理结构是b。
4 3 3 21.(2022·广东省普通高中学业水合格性考试模拟)下列物质中属于含有共价键的离子化合物的是( )
A.NaCl B.KOH C.CO D.HSO
2 2 4
【答案】B
【解析】A项,NaCl中只有离子键,A不符合题意;B项,KOH中K+与OH-之间为离子键,O和H
之间为共价键,属于含有共价键的离子化合物,B符合题意;C项,CO 只有共价键,C不符合题意;D项,
2
HSO 只有共价键,D不符合题意;故选B。
2 4
2.(2022·海南省普通高中学业水平合格性考试)下列物质中,含有非极性共价键的是( )
A.NaOH B.Cl C.KCl D.HCl
2
【答案】B
【解析】离子键是指阴阳离子之间的静电作用,共价键是指非金属原子之间通过共用电子对形成的强
烈相互作用,同种非金属原子之间形成非极性共价键,不同同种非金属原子之间形成极性共价键。A项,
NaOH含有离子键和极性共价键,A不合题意;B项,Cl 只含非极性共价键,B符合题意;C项,KCl只
2
含离子键,C不合题意;D项,HCl只含极性共价键,D不合题意;故选B。
3.(2022·海南省普通高中学业水平合格性考试)下列变化过程中没有破坏化学键的是( )
A.H 在Cl 中燃烧 B.干冰升华
2 2
C.通电分解HO D.NH HCO 受热分解
2 4 3
【答案】B
【解析】A项,H 在Cl 中燃烧生成氯化氢,是化学变化,有破坏化学键,A错误;B.干冰升华是物
2 2
理变化,没有破坏化学键,B正确;C项,通电分解HO生成氢气和氧气,是化学变化,有破坏化学键,
2
C错误;D项,NH HCO 受热分解生成氨气、水、二氧化碳那,是化学变化,有破坏化学键,D错误;故
4 3
选B。
4.(2022·浙江省高三选考三模)下列叙述不正确的是( )
A.带相反电荷的离子之间的强烈相互作用称为离子键
B.两种非金属元素形成的化合物中不可能含有离子键
C.金属元素与非金属元素化合时,不一定形成离子键
D.某主族元素原子最外层只有一个电子,它与卤素原子结合时形成的化学键可能是共价键
【答案】B
【解析】A项,离子键的定义就是带相反电荷的离子之间的强烈相互作用,包括静电引力和斥力;B项,比如NH H,存在离子键,B项错误;C项,比如AlCl 、FeCl 易升华,属于分子,形成的是共价键,
4 3 3
C项正确;D项,若该元素为H,则HX(X 为卤素),则含有共价键,D正确;故选B。
5.(2022·天津市高三九校联盟二模)下列说法中正确的是( )
A.氢键仅存在于分子间
B.SO 和SiO 晶体类型相同
2 2
C. 的沸点比CO低主要是由于范德华力不同
D.CO 溶于水和干冰升华都只有范德华力改变
2
【答案】C
【解析】A项,有的物质(如邻羟基苯甲酸)分子内存在氢键,因此氢键不仅存在于分子间,有的也存
在于分子内,故A错误;B项,SO 是由分子构成的晶体,SiO 是由原子构成的空间网状结构的晶体,前
2 2
者属于分子晶体,后者属于共价晶体,二者晶体类型不同,故B错误;C项,N 与CO 都属于分子晶体,
2
则N 的沸点比CO低主要是由于范德华力不同,故C正确;D项,CO 溶于水可与水反应生成碳酸,除了
2 2
范德华力改变,共价键也发生了改变,干冰升华仅有范德华力改变,故D错误;故选C。
6.(2022·湖南省五市十校教研教改共同体高三第二次大联考)下列关于化学用语的表述错误的是
A. 的电子式: B.中子数为143的 原子:
C.氨分子的结构式: D.氯原子的结构示意图:
【答案】A
【解析】A项,由于B原子最外层只有3个电子,故在BF 中只能形成3对共用电子对,电子式为
3
,故A错误;B项,U的质子数为92,质量数=质子数+中子数=92+143=235,其原子可以表示为:
,故B正确;C项,氨分子中氮和氢共有电子对,含有3个N-H键,其结构式为 ,故C正确;D项,氯原子为17号元素,核外电子排布为2、8、7,,结构示意图为: ,故D正确;
故选A。
7.(2022·河北省石家庄市高三教学质量检测)牙膏内含有多种化学成分,下列有关化学用语的说法错
误的是( )
A.保湿剂甘油(丙三醇)的球棍模型为
B.缓冲剂 的电子式为
C.摩擦剂方解石粉在水中的电离方程式为CaCO Ca2++CO2-
3 3
D.防蛀剂 微溶于水,其溶解平衡表达式为ZnF(s) Zn2+(aq)+2F-(aq)
2
【答案】C
【解析】A项,丙三醇的结构简式为 ,球棍模型为 ,故A正确;B项,氢氧
化钠是含有共价键的离子化合物,电子式为 ,故B正确;C项,摩擦剂方解石粉的主要成
分是碳酸钙,溶于水的碳酸钙在溶液中完全电离,电离方程式为CaCO= Ca2++CO2-,故C错误;D项,氟
3 3
化锌微溶于水,在溶液中存在如下溶解平衡ZnF(s) Zn2+(aq)+2F-(aq),故D正确;故选C。
2
8.(2022·湖北省新高考联考协作体高三联考)下列表示错误的是( )
A.乙烯的结构简式:CH=CH B. 的结构式: O=C=O
2 2
C.丙烯的空间充填模型为: D.氯离子的结构示意图:
【答案】C
【解析】A项,乙烯的官能团为碳碳双键,结构简式中必须标出官能团,乙烯正确的结构简式为:
CH=CH ,故A正确;B项,二氧化碳是共价化合物,中心C原子与O原子之间以双键结合,其结构式为
2 2O=C=O,故B正确;C项, 为丙烷的球棍模型,故C错误;D项,氯离子的核电荷数
为17,最外层为8个电子,氯离子正确的电子式为: ,故D正确;故选C。
9.(2022·辽宁省高三联考)下列化学用语正确的是( )
A.过氧化钙的电子式:
B.基态铬原子的价层电子排布式: 3d44s2
C.2-丁烯的结构简式:CHCHCHCH
3 3
D.硫离子的结构示意图:
【答案】A
【解析】A项,过氧化钙是离子化合物,由过氧根离子和钙离子构成,其电子式为 ,
A项正确;B项,由洪特规则知,基态铬原子的价层电子排布式应为3d54s1,B项错误;C项,碳碳双键应
该表示出来,2-丁烯的结构简式:CHCH=CHCH ,C项错误;D项,S2-的质子数是16而不是18,D项错
3 3
误;故选A。
10.(2022·江西省景德镇市一模)下列化学用语描述正确的是
A.CCl 的球棍模型: B. 的名称:3—乙基—1,3—丁二烯
4
C.氦—3的符号: 3He D.次氯酸的结构式:H—Cl—O
2
【答案】C
【解析】A项,球棍模型中用球代表原子,用棍代表化学键,所以CCl 的球棍模型是: ,故
4A错误;B项, 为键线式结构,表示主链含有4个碳原子的二烯烃,根据二烯烃的命名原则,其
名称应为:2—乙基—1,3—丁二烯,故B错误;C项,氦—3表示质量数为3的氦原子,其符号为:
3He,故C正确;D项,次氯酸分子中存在H-O和O-Cl键,其结构式为:H—O—Cl,故D错误;故选
2
C。
11.(2022·江苏省海安市高三联考)金属钠与四氯化碳在高温下可发生反应:4Na+CCl
4
4NaCl+C。下列有关化学用语表示正确的是( )
A.Na+的结构示意图: B.CCl 的电子式:
4
C.NaCl的电离方程式:NaCl Na++Cl- D.中子数为8的碳原子: 14C
6
【答案】D
【解析】A项,已知Na是11号元素,故质子数为11,则Na+的结构示意图: ,A错误;B
项,CCl 为共价化合物,Cl原子周围有8电子稳定结构,故CCl 的电子式为: ,B错误;C项,
4 4
NaCl是强电解质,故NaCl的电离方程式:NaCl=Na++Cl-,C错误;D项,根据质量数等于质子数加中子
数,故中子数为8的碳原子可表示为:14C,D正确;故选D。
6
12.(2022·天津市静海区四校高三联考)下列化学用语或图示表达不正确的是( )
A.HClO的结构式为:H-O-Cl B.CO 的电子式:
2
C.溴乙烷的分子模型: D.Na+的结构示意图:
【答案】B
【解析】A项,HClO中O原子分别与H原子和Cl原子形成共价键,故其结构式为H-O-Cl,故A正
确;B项,二氧化碳中C原子和氧原子之间以双键结合,其电子式为 ,故B错误;C项,溴乙烷的结构简式为CHCHBr,其中Br原子半径大于C和H原子半径,其分子模型为 ,故C正确;D
3 2
项,钠离子的核内有11个质子,核外有10个电子,结构示意图为 ,故D正确;故选B。
13.(2022·湖北省重点校高三联考)已知反应:2F+2NaOH=OF (二氟化氧)+2NaF+H O,下列有关的化
2 2 2
学用语描述正确的是( )
A.OF 为极性分子 B.核内有12个中子的Na:
2
C.F-的核外电子排布式: D.HO分子的球棍模型:
2
【答案】A
【解析】A项,OF 的结构式为 ,类似水分子,分子中正、负电荷的重心不能重合,因此该
2
分子为极性分子,A正确;B项,核内有12个中子的Na原子的质量数为11+12=23,该原子应表示为 ,
B错误;C项,F-的质子数为9,核外电子数为10,用离子结构示意图表示为: ,C错误;D项,
氧原子的半径比氢原子的半径大,且HO分子的空间结构为V形,而不是直线形,HO分子的球棍模型为:
2 2
,D错误;故选A。
14.(2022·上海市闵行区高三期末质量调研)有关化学用语正确的是( )
A.氯化氢的比例模型: B.37Cl—的结构示意图:C.乙烯分子的球棍模型: D.甲基的电子式:
【答案】C
【解析】A项,氯化氢分子是直线形分子,氯原子比氢原子大,氯化氢的比例模型为 ,故A
错误;B项,氯离子核电荷数为17,核外电子数为18,有3个电子层,最外层电子数为8,离子的结构示
意图为 ,故B错误;C项,乙烯分子的结构简式为CH=CH ,分子的球棍模型为 ,故
2 2
C正确;D项,甲基的结构简式为—CH,电子式为 ,故D正确;故选C。
3
15.(2022·湖北省腾云联盟高三联考)下列化学用语正确的是( )
A.乙烯的结构式:C H B.异戊烷的系统名称为2-甲基丁烷
2 4
C.乙酸的比例模型: D.次氯酸的电子式:
【答案】B
【解析】A项,乙烯分子中存在存在碳碳双键,乙烯正确的结构式为 ,A错误;B项,
异戊烷是含有一个甲基的5个碳的烷烃,其系统名称为2-甲基丁烷,B正确;C项, 为乙
酸的球棍模型,C错误;D项,氯原子最外层有7个电子,氧原子最外层有6个电子,在次氯酸中,氯原
子与氧原子形成1对共用电子对,氢原子与氧原子形成1对共用电子对,都达稳定结构,电子式为
,D错误;故选B。16.(2022·河南省名校联盟高三毕业班阶段联考)已知:HOCH CHOH (乙二醇)
2 2
(草酸)。下列叙述正确的是( )
A.乙二醇的比例模型为
B. 、 为同种核素
C. 在水溶液中的电离方程式为HC O=2H++C O2-
2 2 4 2 4
D.乙二醇生成草酸的反应是氧化反应
【答案】D
【解析】A项,乙二醇的球棍模型为 , A项错误;B项, 、 为不同元素,只是质量数
相等,但不是同种核素,B项错误;C项,草酸是二元弱酸,其电离分步进行,且为可逆反应,电离方程
式为:HC O H++HC O-、HC O- H++C O2-,C项错误;D项,乙二醇生成草酸,其中碳的化
2 2 4 2 4 2 4 2 4
合价,由-1价变为0价,发生氧化反应,D项正确;故选D。
17.(2022·山西省吕粱市名校金科大联考)下列化学用语表述正确的是( )
A.NaS在水溶液中水解的离子方程式为
2
B.中子数为146,质子数为92的铀(U)原子:
C. 的名称为 乙基丁烷
D.CaO 的电子式为
2
【答案】B
【解析】A项,NaS的水溶液中,S2-的水解是分步进行的,其水解的离子方程式为S2-+H O HS-
2 2
+OH-,HS-+H O HS+OH-,故A错误;B项,中子数为146,质子数为92的铀原子的质量数为
2 2A=Z+N=92+146=238,即 ,故B正确;C项,由 的结构简式可知,选最长碳链
作主链,离取代基最近的编号,即 ,其名称为3-甲基戊烷,故C错误;D项,
由CaO 可知,该结构中钙离子与过氧根通过离子键形成的离子化合物,其电子式为 ,故
2
D错误;故选B。
18.(2022·安徽省百校联盟高三联考)下列相关化学用语表示正确的是( )
A.具有3个中子的锂原子:
B.聚乙丙烯的结构简式:
C.三氯化氮的电子式:
D.乙酸的比例模型:
【答案】B
【解析】A项,中子数为3的锂原子的质量数为6,可表示为 ,A项错误;
B项,聚乙丙烯的结构简式可表示为 或
,B项正确;C项,三氯化氮的电子式为 ,C项错误;D
项,图示为乙酸的球棍模型,D项错误;故选B。19.(2022·湖南省三湘名校联盟高三第二次大联考)下列化学用语表述正确的是( )
A.NaS在水溶液中水解的离子方程式为S2-+2H O=HS↑+2OH-
2 2 2
B.中子数为146,质子数为92的铀(U)原子: U
C. 的名称为2—乙基丁烷
D.CaO 的电子式为
2
【答案】B
【解析】A项,S2-的水解是分步进行的,故NaS在水溶液中水解的离子方程式为S2-+H O HS-
2 2
+OH-,A错误;B项,中子数为146,质子数为92的铀原子的质量数为238,即 ,B正确;C项,
的正确命名为3-甲基戊烷,C错误;D项,CaO 正确的电子式为
2
,D错误。故选B。
20.(2022·江苏省如皋中学三模)降低汽油中的含硫量有利于环境的保护,一种利用Ni/ZnO脱除汽油
中含硫有机物中硫元素,并进行Ni/ZnO的再生转化过程如下图所示:
下列说法正确的是( )
A.转化①中既有极性键也有非极性键的断裂
B.转化①中消耗的 和H 的物质的量之比为1∶2
2
C.转化②中消耗的O 和生成的SO 的物质的量之比为3∶2
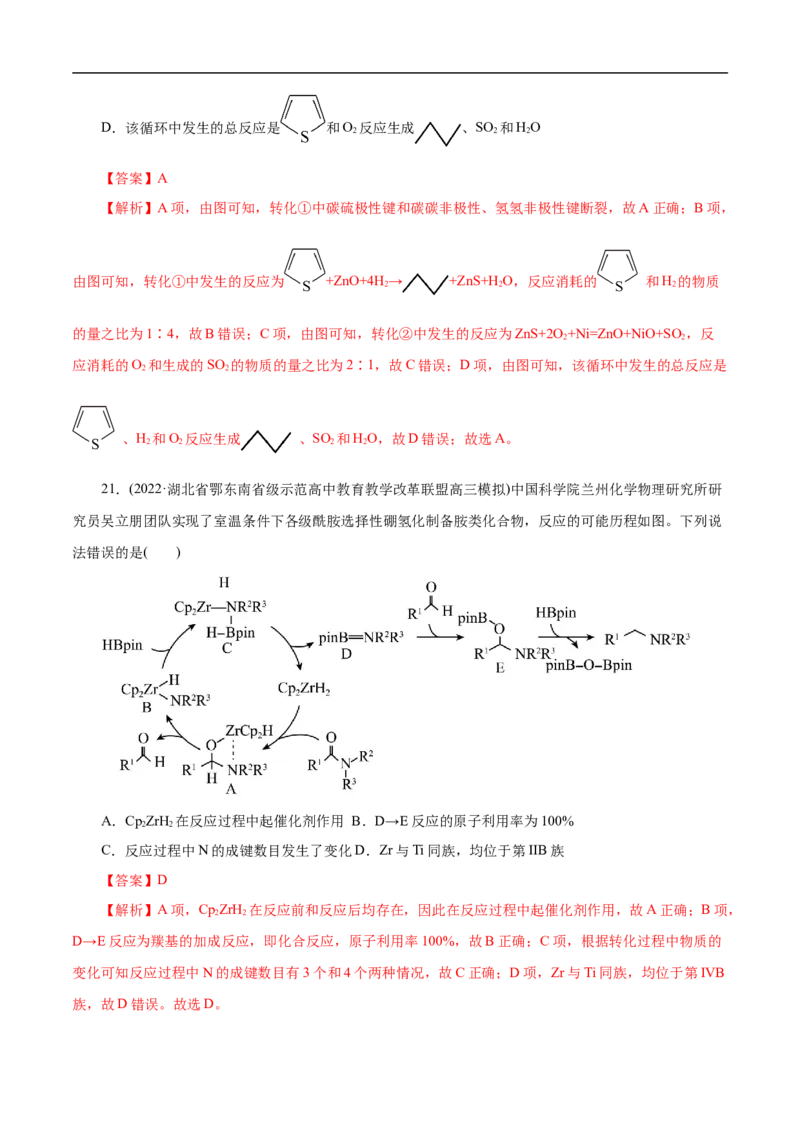
2 2D.该循环中发生的总反应是 和O 反应生成 、SO 和HO
2 2 2
【答案】A
【解析】A项,由图可知,转化①中碳硫极性键和碳碳非极性、氢氢非极性键断裂,故A正确;B项,
由图可知,转化①中发生的反应为 +ZnO+4H → +ZnS+H O,反应消耗的 和H 的物质
2 2 2
的量之比为1∶4,故B错误;C项,由图可知,转化②中发生的反应为ZnS+2O +Ni=ZnO+NiO+SO ,反
2 2
应消耗的O 和生成的SO 的物质的量之比为2∶1,故C错误;D项,由图可知,该循环中发生的总反应是
2 2
、H 和O 反应生成 、SO 和HO,故D错误;故选A。
2 2 2 2
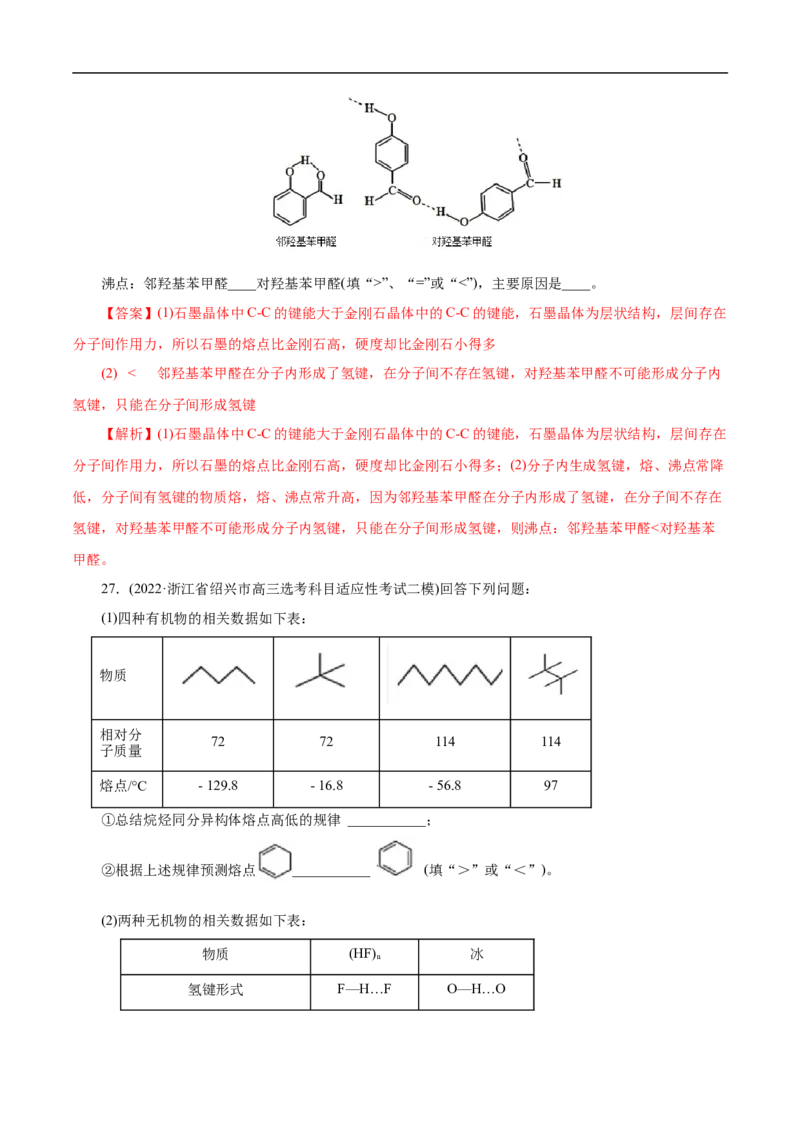
21.(2022·湖北省鄂东南省级示范高中教育教学改革联盟高三模拟)中国科学院兰州化学物理研究所研
究员吴立朋团队实现了室温条件下各级酰胺选择性硼氢化制备胺类化合物,反应的可能历程如图。下列说
法错误的是( )
A.Cp ZrH 在反应过程中起催化剂作用 B.D→E反应的原子利用率为100%
2 2
C.反应过程中N的成键数目发生了变化D.Zr与Ti同族,均位于第IIB族
【答案】D
【解析】A项,Cp ZrH 在反应前和反应后均存在,因此在反应过程中起催化剂作用,故A正确;B项,
2 2
D→E反应为羰基的加成反应,即化合反应,原子利用率100%,故B正确;C项,根据转化过程中物质的
变化可知反应过程中N的成键数目有3个和4个两种情况,故C正确;D项,Zr与Ti同族,均位于第IVB
族,故D错误。故选D。22.(2022·山东·模拟预测)近年,在钯(Pd)催化下进行的偶联反应成为研究热点,其一种反应机理如图
所示,下列说法错误的是( )
已知:R 、R 表示烃基,X表示卤原子,Y表示羟基。
1 2
A.转化过程中涉及氧化还原反应
B.转化过程中未发生非极性键的断裂和形成
C.R —Pd(II) —OC(CH ) 是中间体
2 3 3
D.转化过程中存在反应:R —Pd(II)—X+NaOC(CH )→NaX+R —Pd(II)—OC(CH )
2 3 3 2 3 3
【答案】B
【解析】A项,由图可知,转化过程中Pd元素的化合价发生改变,涉及氧化还原反应,故A正确;B
项,烃基R 与R 的成键过程中形成碳碳非极性键,共B错误;C项,由图中转化关系知,R −Pd(Ⅱ)
1 2 2
−OC(CH ) 是中间体之一,故C正确;D项,转化过程中存在反应:R −Pd(Ⅱ)
3 3 2
−X+NaOC(CH )→NaX+R −Pd(Ⅱ)−OC(CH ),故D正确;故选B。
3 3 2 3 3
23.(2022·湖南省永州市第一中学高三期中)氮气电化学还原反应利用氮气和水来合成氨气,可以直接
将可再生能源产生的电能转化为易于储存和运输的氨气,并保证二氧化碳的零排放,为解决当前严峻的能
源和环境问题提供了新的思路。其在金表面催化反应的工作原理如图所示。下列说法错误的是( )A.利用金作催化剂可降低反应的活化能,提高单位时间内反应的转化率
B.该过程中有非极性共价键和极性共价键的形成
C.升温将有利于反应气体的吸附
D.1molN H 中含5mol共价键
2 4
【答案】C
【解析】A项,利用金作催化剂可降低反应的活化能,加快反应速率,即提高单位时间内反应的转化
率,A正确;B项,该过程中有非极性键N-N键和极性键N-H键生成,B正确;C项,温度高分子动能大,
难于被吸附,故升温不利于反应气体的吸附,C错误;D项,如图所示:1molN H 中含5mol共价键,D正
2 4
确;故选C。
24.(2022·浙江省宁波市高三下学期模拟考试二模)回答下列问题:
(1)立方氮化硼(BN)是一种超硬材料,硬度仅次于金刚石;砷化镓(GaAs)是一种重要半导体材料,具有
空间网状结构,比较立方氮化硼和砷化镓熔点的高低并说明理由:
________________________________________。
(2)四种有机物的沸点数据如表:
物质 CHOH C H CH(CH)OH CH(CH)CH
3 2 6 3 2 9 3 2 9 3
相对分子质量 32 30 158 156
沸点/℃ 64.5 -88.6 228 196
CHOH和C H 沸点相差较大,CH(CH)OH和CH(CH)CH 沸点相差较小,原因是
3 2 6 3 2 9 3 2 9 3
____________________________________________。
【答案】(1)立方氮化硼熔点高。两种晶体均为原子晶体,N和B原子半径更小(或键长更短),键能更
大,熔点更高(2)甲醇分子间可形成氢键,比乙烷分子间作用力强得多,所以沸点相差较大;CH(CH)OH由于烃基
3 2 9
较大,氢键作用被削弱,分子间以分子间作用力为主,所以与分子量接近的CH(CH)CH 沸点相差较小
3 2 9 3
【解析】(1)GaAs和BN均为原子晶体,且由于N和B原子半径更小(或键长更短),键能更大,熔点更
高;(2)CH OH和C H 沸点相差较大是因为甲醇分子间可形成氢键,比乙烷分子间作用力强得多,但是
3 2 6
CH(CH)OH由于烃基较大,氢键作用被削弱,分子间以分子间作用力为主,所以与分子量接近的
3 2 9
CH(CH)CH 沸点相差较小。
3 2 9 3
25.(2022·浙江省台州市高三下学期4月教学质量评估二模)回答下列问题:
(1)已知C H 和NH 均含有18个电子的分子,判断在水中的溶解性大小并说明理由_______。
2 6 2 4
(2)四种晶体的熔点数据如下表:
物质 ZnF ZnCl ZnBr ZnI
2 2 2 2
熔点/℃ 872 283 394 446
ZnF 和ZnCl 熔点相差较大,后三者熔点相差较小,原因是_______。
2 2
【答案】(1)溶解性:NH 大于C H,理由是NH 与HO分子之间能形成氢键,从而增大溶解;而乙
2 4 2 6 2 4 2
烷不能与HO分子之间能形成氢键,溶解性较小
2
(2) ZnF 是离子晶体,ZnCl、ZnBr 、ZnI 是分子晶体,离子键的作用大于分子间作用力,故ZnF 的熔
2 2 2 2 2
点较大,而后三者熔点较低且相差较小
【解析】(1) N H 分子与HO分子之间能形成氢键,而乙烷不能和水分子形成氢键,导致肼在水中的
2 4 2
溶解性大于乙醇;(2)氟元素最活泼的非金属元素,ZnF 是离子晶体;而ZnCl、ZnBr 、ZnI 是分子晶体,
2 2 2 2
离子键的作用大于分子间作用力,故ZnF 的熔点较大,而后三者熔点较低且相差较小。
2
26.(2022·浙江省湖州、丽水、衢州三地市教学质量检测)回答下列问题:
(1)金刚石和石墨的部分物理性质数据如表:
物质 金刚石 石墨
熔点/℃ 3550 3652
硬度 10 1.5
石墨的熔点比金刚石高,硬度却比金刚石小得多,原因是____。
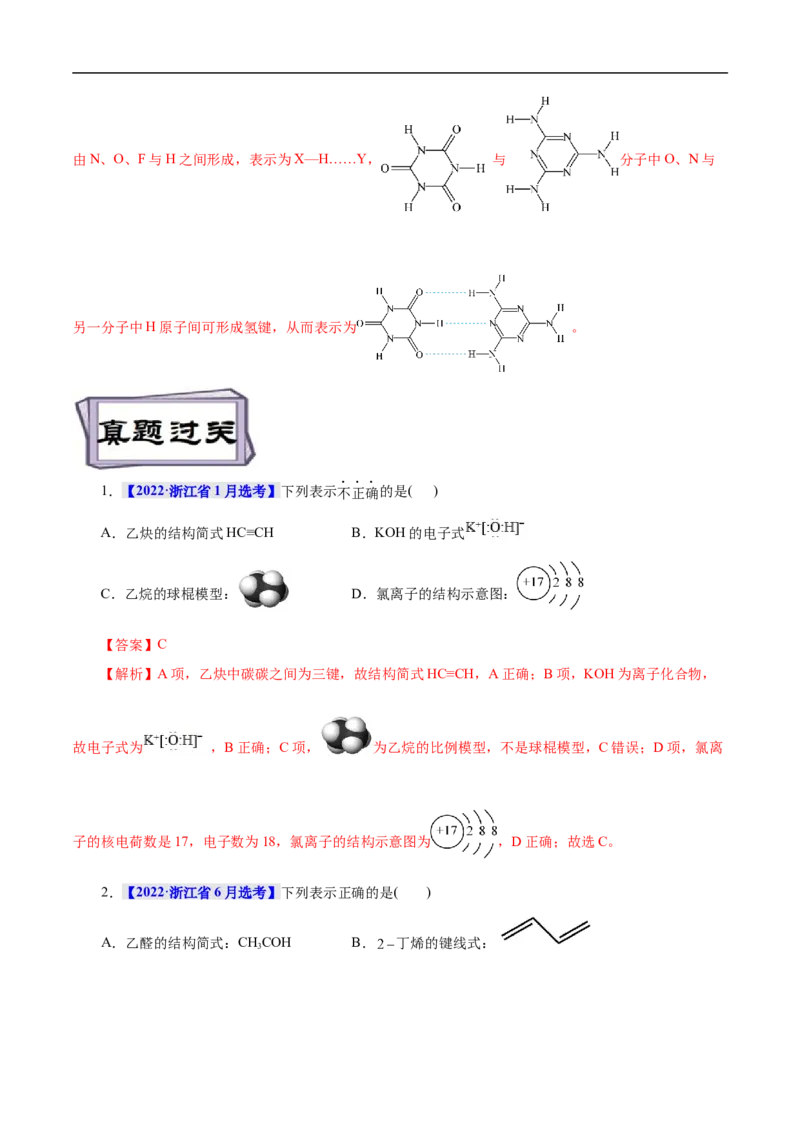
(2)互为同分异构体的两种有机物形成氢键如图所示:沸点:邻羟基苯甲醛____对羟基苯甲醛(填“>”、“=”或“<”),主要原因是____。
【答案】(1)石墨晶体中C-C的键能大于金刚石晶体中的C-C的键能,石墨晶体为层状结构,层间存在
分子间作用力,所以石墨的熔点比金刚石高,硬度却比金刚石小得多
(2) < 邻羟基苯甲醛在分子内形成了氢键,在分子间不存在氢键,对羟基苯甲醛不可能形成分子内
氢键,只能在分子间形成氢键
【解析】(1)石墨晶体中C-C的键能大于金刚石晶体中的C-C的键能,石墨晶体为层状结构,层间存在
分子间作用力,所以石墨的熔点比金刚石高,硬度却比金刚石小得多;(2)分子内生成氢键,熔、沸点常降
低,分子间有氢键的物质熔,熔、沸点常升高,因为邻羟基苯甲醛在分子内形成了氢键,在分子间不存在
氢键,对羟基苯甲醛不可能形成分子内氢键,只能在分子间形成氢键,则沸点:邻羟基苯甲醛<对羟基苯
甲醛。
27.(2022·浙江省绍兴市高三选考科目适应性考试二模)回答下列问题:
(1)四种有机物的相关数据如下表:
物质
相对分
72 72 114 114
子质量
熔点/°C - 129.8 - 16.8 - 56.8 97
①总结烷烃同分异构体熔点高低的规律 ___________;
②根据上述规律预测熔点 ___________ (填“>”或“<”)。
(2)两种无机物的相关数据如下表:
物质 (HF) 冰
n
氢键形式 F—H…F O—H…O氢键键能/kJ·mol-1 28 19
沸点/°C 20 100
(HF) 中氢键键能大于冰,但(HF) 沸点却低于冰,原因是 ___________。
n n
【答案】(1) 分子对称性越高,熔点越高 小于
(2)冰中氢键数目比(HF) 中多
n
【解析】(1)①根据题中表格数据,同分异构体分子对称性越高,熔点越高;② 的对称性比
差,分子对称性越高,熔点越高,所以熔点: 小于 ;(2)1molHF只能形成1mol氢键,
1molH O能形成2mol氢键,由于冰中氢键数目比(HF) 中多,所以 (HF) 沸点低于冰。
2 n n
28.(2022·浙江省浙南名校高三联考)填空。
(1)已知两种有机物的相关数据如下表:
物质 CHCHF CHCHNH
3 2 3 2 2
相对分子质量 48 45
沸点/℃ -37.7 16.6
化合物CHCHNH 的沸点高于CHCHF的原因是___________。
3 2 2 3 2
(2)已知C HNH NO 的熔点只有12℃,而NH NO 的熔点170℃,NH NO 熔点高于C HNH NO 的原
2 5 3 3 4 3 4 3 2 5 3 3
因是___________。
【答案】(1)两者均为分子晶体,CHCHNH 可以形成分子间氢键使分子间作用力增大,而CHCHF
3 2 2 3 2
不能
(2)两者熔化时需克服的均为离子键,由于C HNH +的半径大于NH +,离子键弱于NH NO ,故熔点低
2 5 3 4 4 3
【解析】(1)对于分子晶体,熔沸点的高低从分子间作用力来解释,分子间的作用力包含范德华力和氢
键,分子间氢键的存在会使分子间作用力增大,沸点升高,CHCHNH 可以形成分子间氢键使分子间作用
3 2 2
力增大,而CHCHF不能,所以CHCHNH 沸点高。故答案为:两者均为分子晶体,CHCHNH 可以形
3 2 3 2 2 3 2 2
成分子间氢键使分子间作用力增大,而CHCHF不能;(2) C HNH NO 和NH NO 为离子化合物,熔点结
3 2 2 5 3 3 4 3
合离子键强弱判断,阴阳离子所带电荷数相同时,可以通过离子半径大小来比较离子键强弱,C HNH NO
2 5 3 3
中C HNH +的半径大于NH +,离子键弱于NH NO ,故熔点低。
2 5 3 4 4 3
29.(2022·浙江省镇海中学高三选考模拟)卤化钠(NaX)和四卤化钛(TiX)的熔点如图所示。
4(1)TiX 熔点变化趋势的原因_______。
4
(2)多重氢键在生命体、分子自组装和响应型功能材料领域都有重要应用。三聚氰酸和三聚氰胺(1∶1)
可以通过多重氢键自组装构成二维片状结构,被形象地称为“分子饼”。请用虚线在下图中直接画出两个
分子间存在的氢键_______。
【答案】(1)TiF 离子晶体,离子键强于分子间作用力;TiCl 、TiBr 、TiI 分子晶体,随相对分子质量
4 4 4 4
增加,分子间作用力增加,熔点升高
(2)
【解析】(1)若TiX 都为离子晶体,则X从F到I,晶格能依次减小,熔点依次降低;若TiX 都为分子
4 4
晶体,则随相对分子质量的不断增大,分子间作用力不断增大,熔点不断升高。分析图象,可确定TiF 为
4
离子晶体,TiCl 、TiBr 、TiI 为分子晶体。TiX 熔点变化趋势的原因:TiF 离子晶体,离子键强于分子间
4 4 4 4 4
作用力;TiCl 、TiBr 、TiI 分子晶体,随相对分子质量增加,分子间作用力增加,熔点升高;(2)氢键通常
4 4 4由N、O、F与H之间形成,表示为X—H……Y, 与 分子中O、N与
另一分子中H原子间可形成氢键,从而表示为 。
1.【2022·浙江省1月选考】下列表示不正确的是( )
A.乙炔的结构简式HC≡CH B.KOH的电子式
C.乙烷的球棍模型: D.氯离子的结构示意图:
【答案】C
【解析】A项,乙炔中碳碳之间为三键,故结构简式HC≡CH,A正确;B项,KOH为离子化合物,
故电子式为 ,B正确;C项, 为乙烷的比例模型,不是球棍模型,C错误;D项,氯离
子的核电荷数是17,电子数为18,氯离子的结构示意图为 ,D正确;故选C。
2.【2022·浙江省6月选考】下列表示正确的是( )
A.乙醛的结构简式:CHCOH B. 丁烯的键线式:
3C.S2-的结构示意图: D.过氧化钠的电子式:
【答案】D
【解析】A项,乙醛含醛基,其结构简式为:CHCHO,A错误;B项,2-丁烯的结构简式为
3
CHCH=CHCH ,键线式为: ,B错误;C项,硫的原子序数为16,硫原子最外层有6个电
3 3
子,得2个电子形成硫离子,硫离子的结构示意图为: ,C错误;D项,过氧化钠为离子化合物,
含离子键和氧氧非极性共价键,其电子式为: ,D正确;故选D。
3.【2021•浙江6月选考】下列表示不正确的是( )
A.乙炔的实验式C H B.乙醛的结构简式CHCHO
2 2 3
C.2,3-二甲基丁烷的键线式 D.乙烷的球棍模型
【答案】A
【解析】A项,乙炔的分子式为C H,实验式为CH,故A错误;B项,乙醛的分子式为C HO,结
2 2 2 4
构简式为CHCHO,故B正确;C项,2,3—二甲基丁烷的结构简式为(CH)CHCH(CH ),键线式为
3 3 2 3 2
,故C正确;D项,乙烷的结构简式为CH CH,球棍模型为 ,故D正确;故选A。
3 3
4.【2021•浙江1月选考】下列表示正确的是( )
A.甲醛的电子式 B.乙烯的球棍模型
C.2-甲基戊烷的键线式 D.甲酸乙酯的结构简式CHCOOCH
3 3
【答案】B
【解析】A项,O原子最外层有6个电子,故甲醛的电子式为 ,A错误;B项,乙烯中碳原子之间以双键形式存在,乙烯的球棍模型为 ,B正确;C项,2-甲基戊烷的键线式为 ,
C错误;D.甲酸乙酯甲酸和乙醇酯化得到,故甲酸乙酯的结构简式为HCOOCH ,D错误;故选B。
3
5.【2020•浙江1月选考】有共价键的离子化合物是( )
A.NaO B.HSO C.CHCl D.SiC
2 2 2 4 2 2
【答案】A
【解析】A项,NaO 中钠离子与过氧根之间为离子键,故为离子化合物,过氧根中氧原子之间为共
2 2
价价,故A正确;B项,硫酸为只含共价键的共价化合物,故B错误;C项,二氯甲烷为只含共价键的共
价化合物,故C错误;D项,碳化硅为只含共价键的共价化合物,故D错误;故选A。
6.【2020•浙江7月选考】下列表示不正确的是( )
A.乙烯的结构式: B.甲酸甲酯的结构简式:C HO
2 4 2
C. 甲基丁烷的键线式: D.甲基的电子式:
【答案】B
【解析】A项,结构式是每一对共用电子对用一个短横来表示,乙烯分子中每个碳原子和每个氢原子
形成一对共用电子对,碳原子和碳原子形成两对共用电子对,故A正确;B项,结构简式中需要体现出特
殊结构和官能团,甲酸甲酯中要体现出酯基,其结构简式为HCOOCH ,故B错误;C项,键线式中每个
3
端点为一个C原子,省略C—H键,故C正确;D项,甲基中碳原子和三个氢原子形成3对共用电子对,
还剩一个成单电子,故D正确;故选B。
7.【2020•江苏卷】反应8NH +3Cl=6NHCl+N 可用于氯气管道的检漏。下列表示相关微粒的化学用
3 2 4 2
语正确的是( )
A.中子数为9的氮原子: B.N 分子的电子式:
2
C.Cl 分子的结构式:Cl—Cl D.Cl-的结构示意图:
2
【答案】C
【解析】A项,N原子的质子数为7,中子数为9的氮原子的质量数为7+9=16,该氮原子表示为 ,A错误;B项,N 分子中两个N原子间形成3对共用电子对,N 分子的电子式为 ,B错误;C
2 2
项,Cl 分子中两个Cl原子间形成1对共用电子对,Cl 分子的结构式为Cl—Cl,C正确;D项,Cl-的核电
2 2
荷数为17,核外有18个电子,Cl-的结构示意图为 ,D错误;故选C。
8.【2020•浙江1月选考】下列表示不正确的是( )
A.羟基的电子式: B.乙烯的结构简式:CHCH
2 2
C.氯原子的结构示意图: D.NH 分子的球棍模型:
3
【答案】B
【解析】A项,羟基中氧原子还有一个未成对的单电子,电子式为 ,故A正确;B项,乙烯的官
能团为碳碳双键,结构简式为CH=CH ,故B错误;C项,氯原子的核外有3个电子层,最外层有7个电
2 2
子,原子的结构示意图为 ,故C正确;D项,氨气为三角锥形的极性分子,球棍模型为 ,
故D正确;故选B。
9.【2020•浙江1月选考】下列说法不正确的是( )
A.16O和18O互为同位素
8 8
B.金刚石和石墨互为同素异形体
C. 和 互为同系物
D.CHCOOCH CH 和CHCHCHCOOH互为同分异构体
3 2 3 3 2 2
【答案】C
【解析】A项,16O和18O的质子数相同,中子数不同,互为同位素,故A正确;B项,金刚石和石
8 8
墨是碳元素形成的不同种单质,互为同素异形体,故B正确;C项,同系物必须是结构相似,相差一个或若干个CH 原子团的同类物质, 属于酚类, 属于芳香醇,不是同类物质,不互为
2
同系物,故C错误;D项,CHCOOCH CH 和CHCHCHCOOH的分子式都为C HO,结构不同,互为
3 2 3 3 2 2 4 8 2
同分异构体,故D正确;故选C。
10.【2019•上海卷】下列选项不正确的是( )
A.含有共价键的化合物是共价化合物 B.含有极性键的分子可能是非极性分子
C.有电子转移的反应是氧化还原反应 D.水溶液中能完全电离的电解质是强电解质
【答案】A
【解析】A.含有共价键的化合物也可能是离子化合物,如 NaOH,A 错误;B.含有极性键的分子可
能是非极性分子,如 CH4,B 正确;C.有电子转移的反应一定是氧化还原反应,C 正确;D.水溶液中
能完全电离的电解质是强电解质,D 正确;故选 A。
11.【2019•上海卷】关于离子化合物 NH5,下列说法正确的是( )
A.N 为-5 价 B.阴阳离子个数比是 1:1
C.阴离子为 8 电子稳定结构 D.阳离子的电子数为 11
【答案】B
-
【解析】A.离子化合物由 NH +和 H 构成,N 的化合价为-3,A 错误;B.阴阳离子个数比为 1:
4
1,B 正确;C.阴离子为 H-,最外层 2 个电子,不满足 8 电子稳定结构,C 错误;D.阳离子为
NH4+,电子数为 10,D 错误。故故选 B
12.【2019•浙江4月选考】下列说法不正确的是
A.纯碱和烧碱熔化时克服的化学键类型相同
B.加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏
C.CO 溶于水和干冰升华都只有分子间作用力改变
2
D.石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏
【答案】C
【解析】A项,烧碱和纯碱均属于离子化合物,熔化时须克服离子键,A项正确;B项,加热蒸发氯
化钾水溶液,液态水变为气态水,水分子之间的分子间作用力被破坏,B项正确;C项,CO 溶于水发生
2
反应:CO+H O HCO ,这里有化学键的断裂和生成,C项错误;D项,石墨属于层状结构晶体,每层石
2 2 2 3
墨原子间为共价⇌键,层与层之间为分子间作用力,金刚石只含有共价键,因而石墨转化为金刚石既有共价
键的断裂和生成,也有分子间作用力的破坏,D项正确。故选C。
13.【2018•江苏卷】用化学用语表示 NH + HCl=NHCl中的相关微粒,其中正确的是( )
3 4A. 中子数为8 的氮原子: B. HCl 的电子式:
C. NH 的结构式: D. Cl−的结构示意图:
3
【答案】C
【解析】A项,中子数为8的氮原子的质量数为15,表示为 ,A项错误;B项,HCl中只含共价键,
HCl的电子式为 ,B项错误;C项,NH 中含3个N-H键,NH 的结构式为 ,C项正确;D
3 3
项,Cl-最外层有8个电子,Cl-的结构示意图为 ,D项错误。
14.【2017•江苏卷】下列有关化学用语表示正确的是 ( )
A.质量数为31的磷原子: B.氟原子的结构示意图:
C.CaCl 的电子式: D.明矾的化学式:Al (SO )
2 2 4 3
【答案】A
【解析】A.P的质子数是15,A正确;B.F原子的电子数为9,B错误;C.离子化合物中阴、阳离
子间隔排列,其电子式中离子分开写、不能合并,C错误;D.明矾是十二水合硫酸铝钾,D错误。
15.【2016•江苏卷】下列有关化学用语表示正确的是( )
A.中子数为10的氧原子: B.Mg2+的结构示意图:
C.硫化钠的电子式: D.甲酸甲酯的结构简式:C HO
2 4 2
【答案】B
【解析】A项,在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数。因为质子数和
中子数之和是质量数,因此中子数为10的氧原子可表示为 ,A错误;B项,Mg2+的质子数是12,核外电子数是10,则镁离子的结构示意图为可表示为 ;B正确;C项,硫化钠为离子化合物,含有离子
键,电子式为 ,C错误;D项,甲酸甲酯的结构简式为HCOOCH ,D错误。答案选B。
3
16.【2022·浙江省1月选考】回答下列问题:
(1)两种有机物的相关数据如表:
物质 HCON(CH ) HCONH
3 2 2
相对分子质量 73 45
沸点/℃ 153 220
HCON(CH ) 的相对分子质量比HCONH 的大,但其沸点反而比HCONH 的低,主要原因是
3 2 2 2
____________________________________。
(2)四种晶体的熔点数据如表:
物质 CF SiF BF AlF
4 4 3 3
熔点/℃ -183 -90 -127 >1000
CF 和SiF 熔点相差较小,BF 和AlF 熔点相差较大,原因是________________。
4 4 3 3
【答案】(1)HCON(CH ) 分子间只有一般的分子间作用力,HCONH 分子间存在氢键,破坏一般的分
3 2 2
子间作用力更容易,所以沸点低。
(2)CF 和SiF 都是分子晶体,结构相似,分子间作用力相差较小,所以熔点相差较小;BF 通过分子间
4 4 3
作用力形成分子晶体,AlF 通过离子键形成离子晶体,破坏离子键需要能量多得多,所以熔点相差较大。
3
【解析】(1)HCON(CH ) 分子间只有一般的分子间作用力,HCONH 分子间存在氢键,破坏一般的分
3 2 2
子间作用力更容易,所以沸点低;(2)CF 和SiF 都是分子晶体,结构相似,分子间作用力相差较小,所以
4 4
熔点相差较小;BF 通过分子间作用力形成分子晶体,AlF 通过离子键形成离子晶体,破坏离子键需要能
3 3
量多得多,所以熔点相差较大。
17.【2022·浙江省6月选考】回答下列问题:
(1)乙醇的挥发性比水的强,原因是_______。
(2)金属氢化物是应用广泛的还原剂。KH的还原性比NaH的强,原因是_______。
【答案】(1)乙醇分子间形成氢键的数量比水分子间形成氢键的数量少,分子间作用力小
(2)Na+半径小于K+,Na+与H—的离子键作用强,H—更难失电子,还原性更弱
【解析】(1)乙醇和水均可形成分子晶体,且其均可形成分子间氢键,但是,水分子中的2个H均可参与形成氢键,而乙醇分子中只有羟基上的1个H可以参与形成氢键,故水分子间形成氢键的数量较多,水
分子间的作用力较大,水的沸点较高而乙醇的沸点较低。因此,乙醇的挥发性比水的强的原因是:乙醇分
子间形成氢键的数量比水分子间形成氢键的数量少,分子间作用力小。(2)KH和NaH均可形成离子晶体,
Na+半径小于K+,故NaH的晶格能较大,Na+与H—的离子键作用较强,其中的H—更难失电子、还原性更
弱,因此,KH的还原性比NaH的强的原因是:Na+半径小于K+,Na+与H—的离子键作用强,H—更难失电
子,还原性更弱。
18.【2021•浙江6月选考】(1)已知3种原子晶体的熔点数据如下表:
金刚石 碳化硅 晶体硅
熔点/℃ >3550 2600 1415
金刚石熔点比晶体硅熔点高的原因是_______。
(2)提纯含有少量氯化钠的甘氨酸样品:将样品溶于水,调节溶液的pH使甘氨酸结晶析出,可实现甘
氨酸的提纯。其理由是_______。
【答案】(1)原子半径C<Si(或键长C-C<Si-Si),键能C-C>Si-Si
(2)当调节溶液pH至甘氨酸主要以两性离子的形态存在时(即等电点,此时两性离子间相互吸引力最
大),溶解度最小
【解析】(1)原子半径的大小决定键长大小,键长越短键能越大,此时物质的熔、沸点越高,在C和Si
组成的物质中原子半径C<Si(或键长C-C<Si-Si),键能C-C>Si-Si,故金刚石的熔点高于晶体硅的熔点;
(2) 当调节溶液pH至甘氨酸主要以两性离子的形态存在时(即等电点,此时两性离子间相互吸引力最大),
溶解度最小,此时析出的固体为甘氨酸,可以实现甘氨酸的提纯。
19.【2021•浙江1月选考】(1)用质谱仪检测气态乙酸时,谱图中出现质荷比(相对分子质量)为120的
峰,原因是______。
(2)金属镓(Ga)位于元素周期表中第4周期IIIA族,其卤化物的熔点如下表:
GaF GaCl GaBr
3 3 3
熔点/℃ > 1000 77. 75 122. 3
GaF 熔点比GaCl 熔点高很多的原因是______。
3 3
【答案】(1)两个乙酸分子通过氢键形成二聚体( )
(2)GaF 是离子晶体,GaCl 是分子晶体;离子键强于分子间作用力
3 3
【解析】(1)质谱检测乙酸时,出现质荷比为120的峰,说明可能为两分子的乙酸结合在一起,由于乙酸分子中存在可以形成氢键的O原子,故这种结合为以氢键形式结合的二聚体( ),故
答案为:两个乙酸分子通过氢键形成二聚体( );(2)F的非金属性比Cl强,比较GaF 和
3
GaCl 的熔点可知,GaF 为离子晶体,GaCl 为分子晶体,离子晶体中主要的作用为离子键,分子晶体中主
3 3 3
要的作用为分子间作用力,离子键强于分子间作用力,故GaF 的熔点高于GaCl ,故答案为:GaF 是离子
3 3 3
晶体,GaCl 是分子晶体;离子键强于分子间作用力。
3
20.【2018•新课标Ⅱ卷】如图为S 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要
8
原因为______________________________________________。
【答案】S 相对分子质量大,分子间范德华力强
8
21.【2018•新课标Ⅲ卷】ZnF 为离子化合物,ZnF 不溶于有机溶剂而ZnCl、ZnBr 、ZnI 能够溶于乙
2 2 2 2 2
醇 、 乙 醚 等 有 机 溶 剂 , 原 因 是
_____________________________________________________________________。
【答案】ZnCl、ZnBr 、ZnI 的化学键以共价键为主、极性较小
2 2 2
22.【2017•新课标Ⅱ卷,35】我国科学家最近成功合成了世界上首个五氮阴离子盐
(N )(H O) (NH )Cl(用R代表)。
5 6 3 3 4 4
图中虚线代表氢键,其表示式为(NH)N—H…Cl、________、________。
【答案】(H O+)O—H…N(N) (NH)N—H……N(N)
3
23.【2017•新课标Ⅲ卷】CO +3H===CH OH+HO反应所涉及的4种物质中,沸点从高到低的顺序
2 2 3 2
为________,原因是__________________________________________。
【答案】HO>CHOH>CO >H HO与CHOH均为极性分子,HO中氢键比甲醇多;CO 与H 均为
2 3 2 2 2 3 2 2 2
非极性分子,CO 相对分子质量较大,范德华力较大
2