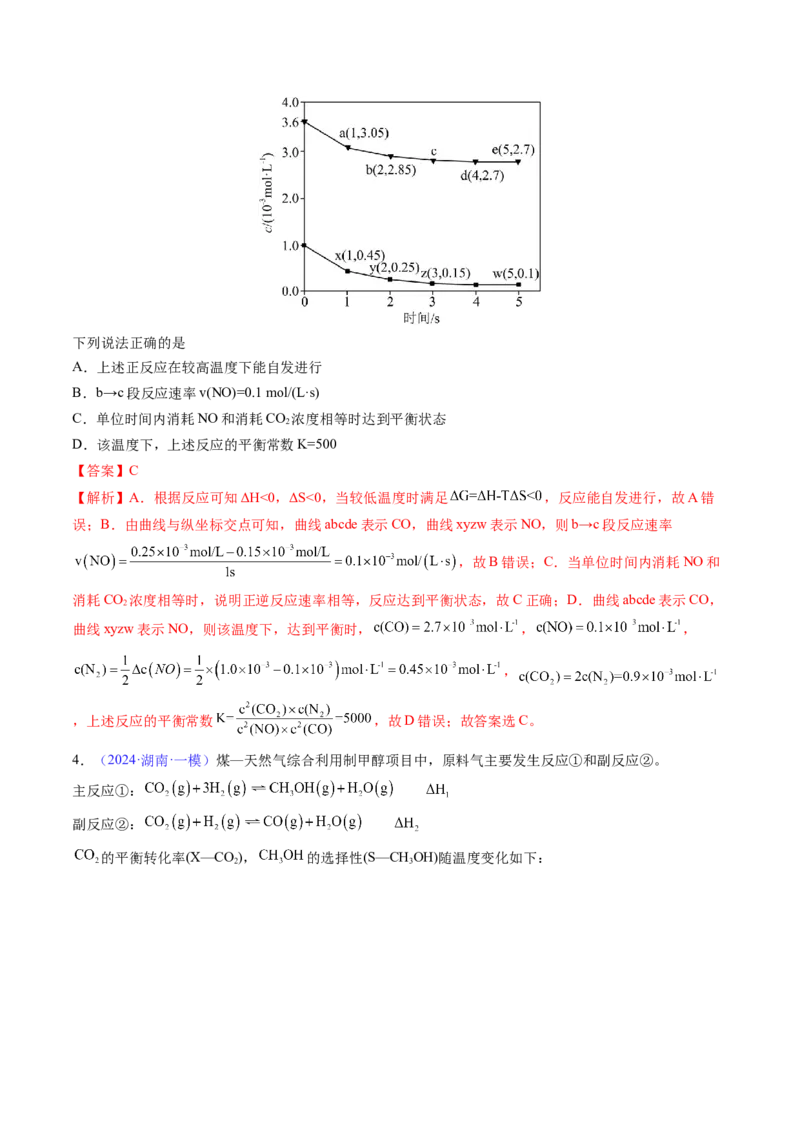
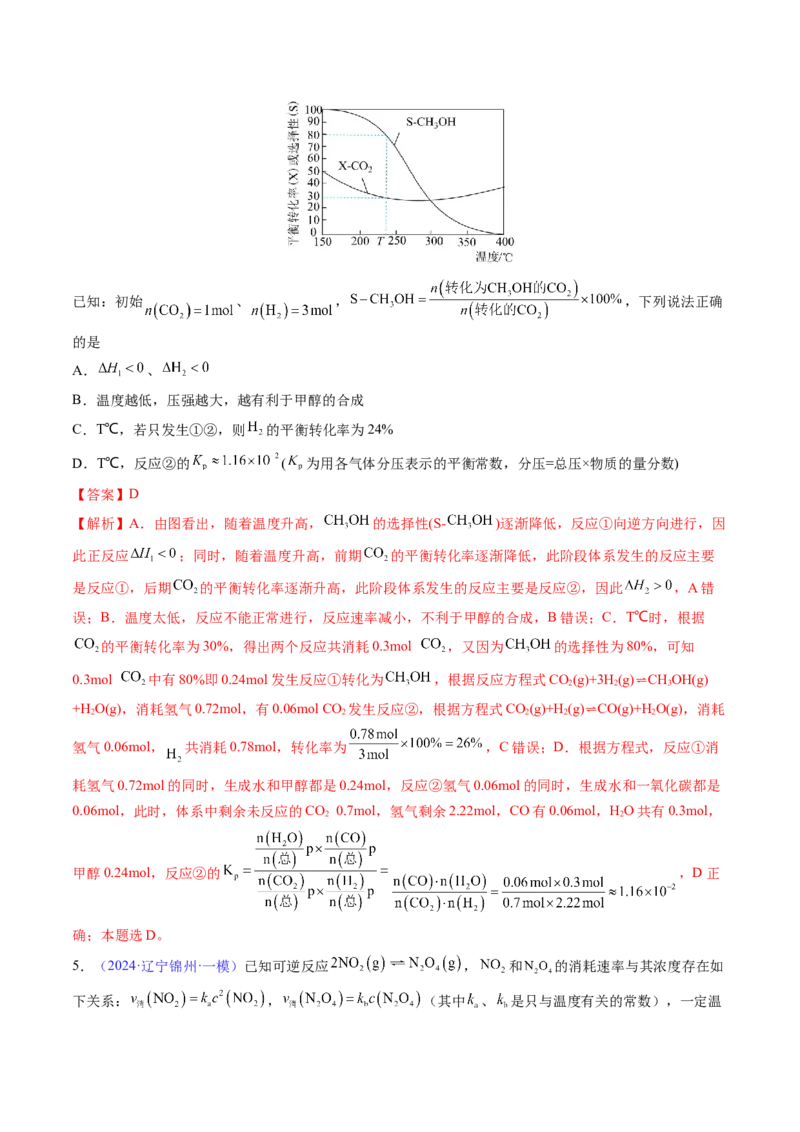
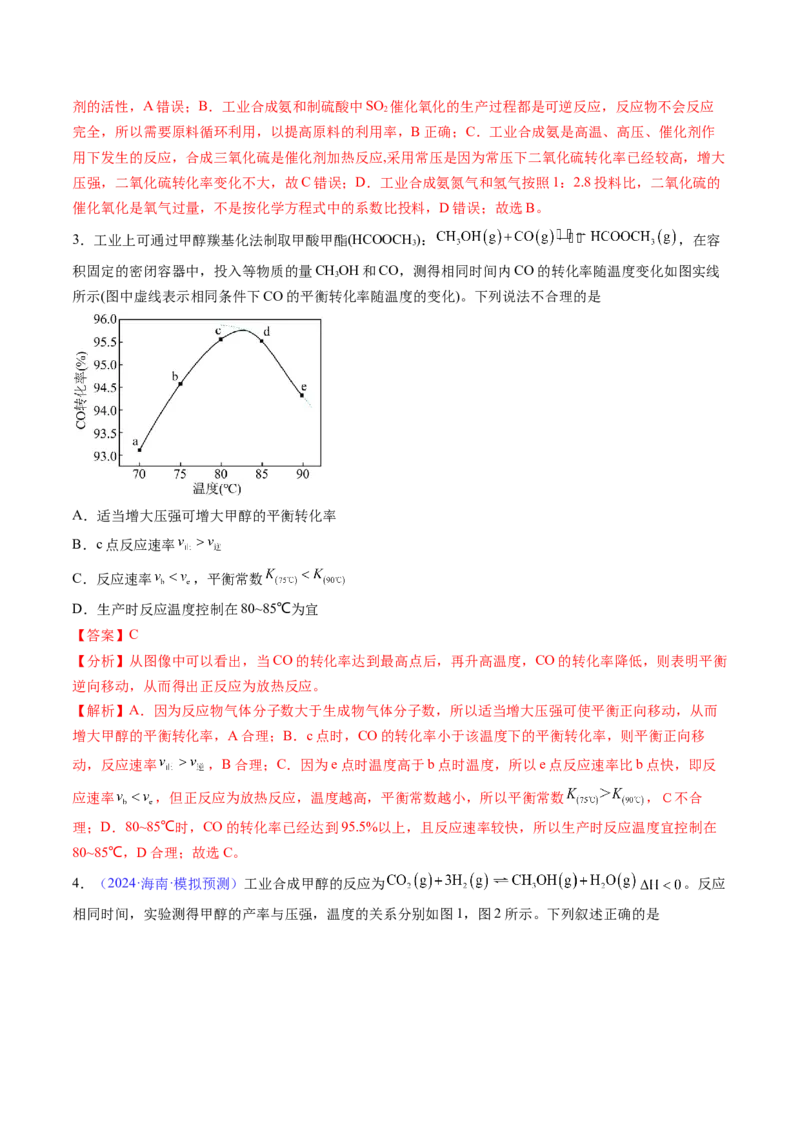
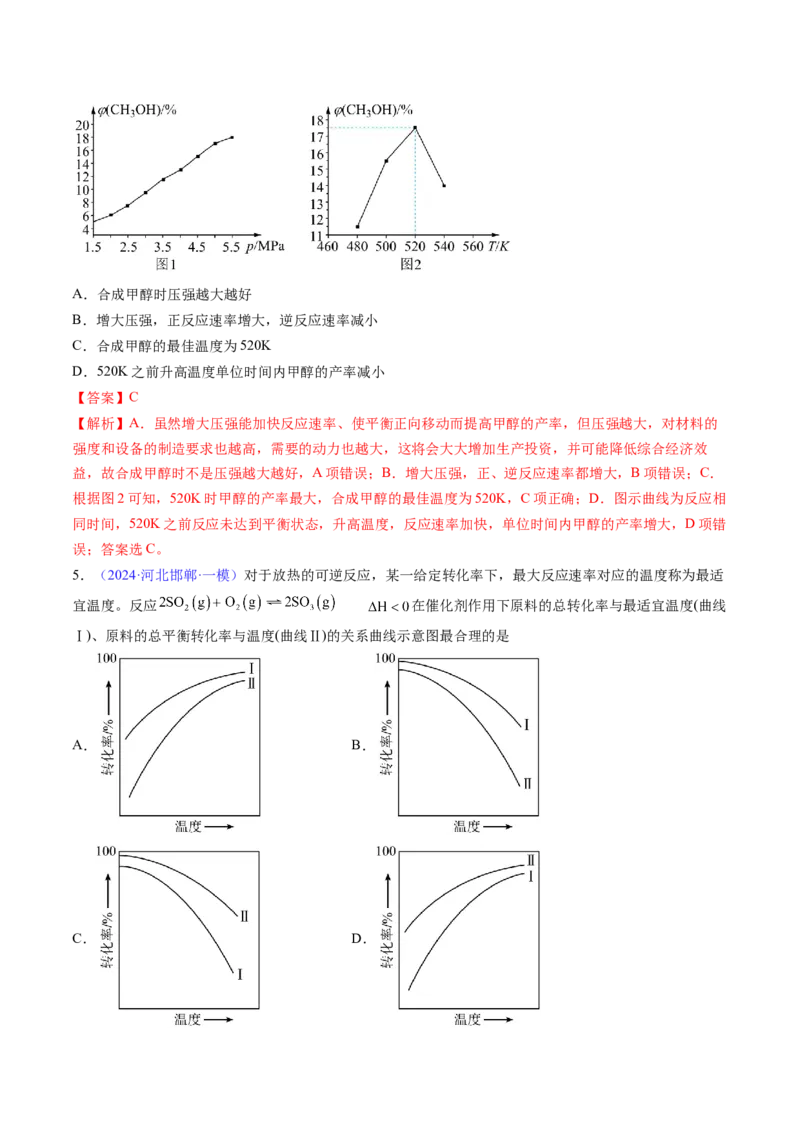
文档内容
通关 08 化学反应速率及化学平衡
目录
【高考预测】预测考向,总结常考点及应对的策略
【技法必备】提供方法技巧,解决问题策略
【误区点拨】点拨常见的易错点
【抢分通关】分析命题热点,把握解题技巧,精选名校模拟题
概率预测 ☆ ☆ ☆ ☆ ☆
题型预测 选择题、主观题☆ ☆ ☆ ☆ ☆
考向预测 化学反应速率与化学平衡的综合分析及应用
以科技前沿或化学史话或生产环保为试题情景,考查速率、平衡有关的计算、图像图表。在考查方式上更
加偏向与模块的融合,不再单一考查这章节的内容,体现了知识的衔接性。侧重考查学生的理解与辨析能
力;从图像中提取有效信息的能力;结合反应原理进行分析判断、迁移应用的能力;化学定量计算能力。
预测2024年高考在这一专题的考点还是化学反应机理、碰撞理论、催化剂、反应速率、平衡常数转化率、
多重平衡的选择性,考查信息获取与加工能力、读图能力、计算能力、概念理解与迁移能力、理论分析与
文字表述能力。考查变化观念与平衡思想、证据推理与模型认知、宏观辨识与微观探析的学科素养。
技法1 热化学方程式的书写及反应热计算技巧
首先根据要求书写目标热化学方程式的反应物、生成物并配平,其次在反应物和生成物的后面括号内注明
其状态,再次将目标热化学方程式与已有的热化学方程式比对(主要是反应物和生成物的位置、化学计量
数),最后根据盖斯定律进行适当运算得出目标热化学方程式的反应热ΔH,空一格写在热化学方程式右边
即可。
技法2 解答化学平衡移动问题的步骤
1.正确分析反应特点:包括反应物、生成物的状态、气体体积变化、反应的热效应。
2.明确外界反应条件:恒温恒容、恒温恒压、反应温度是否变化、反应物配料比是否变化。
3.结合图像或K与Q的关系、平衡移动原理等,判断平衡移动的方向或结果。
(4)结合题意,运用“三段式”,分析计算、确定各物理量的变化。
技法3 化学平衡图像题解题技巧
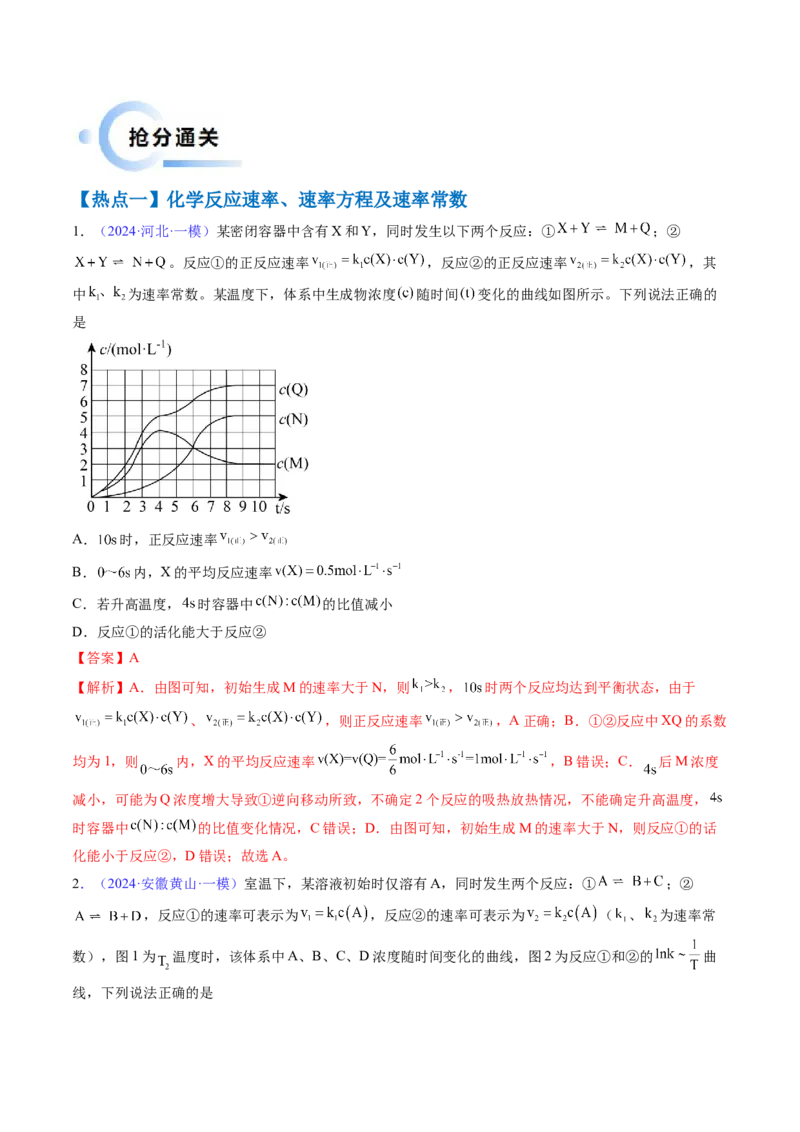
(1)“定一议二”原则
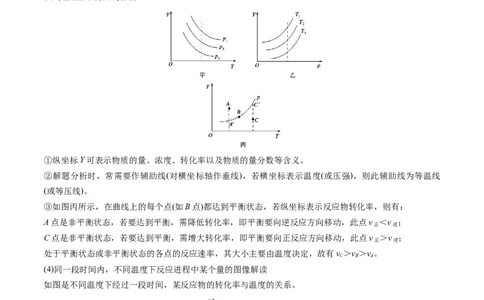
在化学平衡图像中,了解纵轴、横轴和曲线所表示的三个量的意义。在确定横轴所表示的量后,讨论纵轴与曲线的关系,或在确定纵轴所表示的量后,讨论横轴与曲线的关系。
比如:反应2A(g)+B(g)
2C(g)达到化学平衡时,A的平衡转化率与压强和温度的关系如图1所示[A
的平衡转化率(α),横轴为反应温度(T)]。
图1
定压看温度变化,升高温度曲线走势降低,说明A的转化率降低,平衡向逆反应方向移动,正反应是放热
反应。
定温看压强变化,因为此反应是反应后气体体积减小的反应,压强增大,平衡向正反应方向移动,A的转
化率增大,故p>p。
2 1
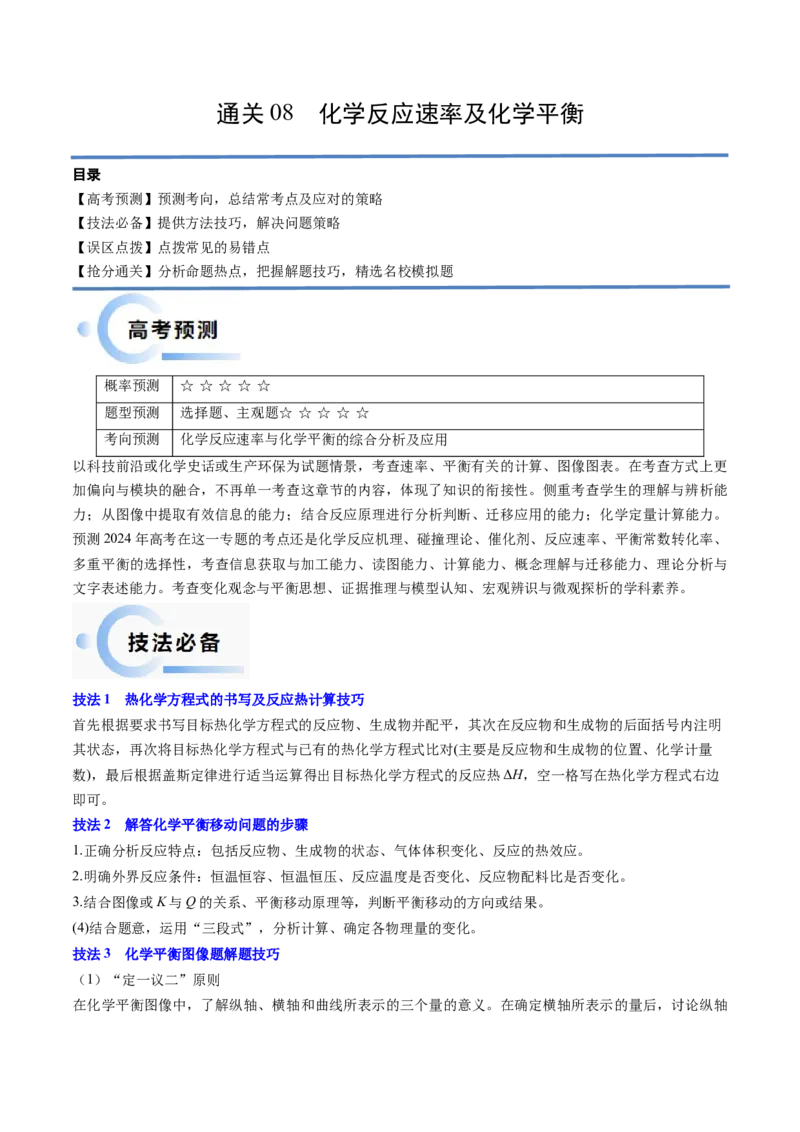
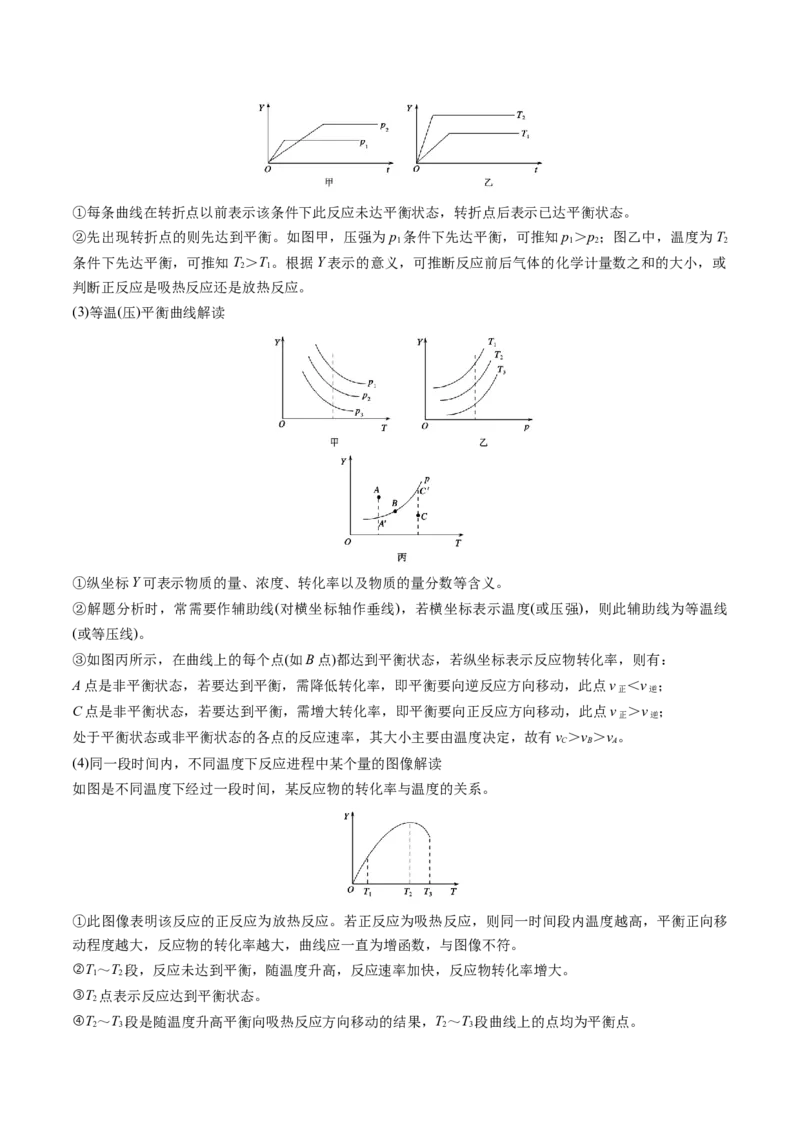
(2)“先拐先平数值大”原则
对于同一化学反应在化学平衡图像中,先出现拐点的反应先达到平衡状态,先出现拐点的曲线表示的温度
较高(如图2所示,α表示反应物的转化率)或压强较大[如图3所示,φ(A)表示反应物A的体积分
数]。
图2 图3
图2:T>T,正反应放热。
2 1
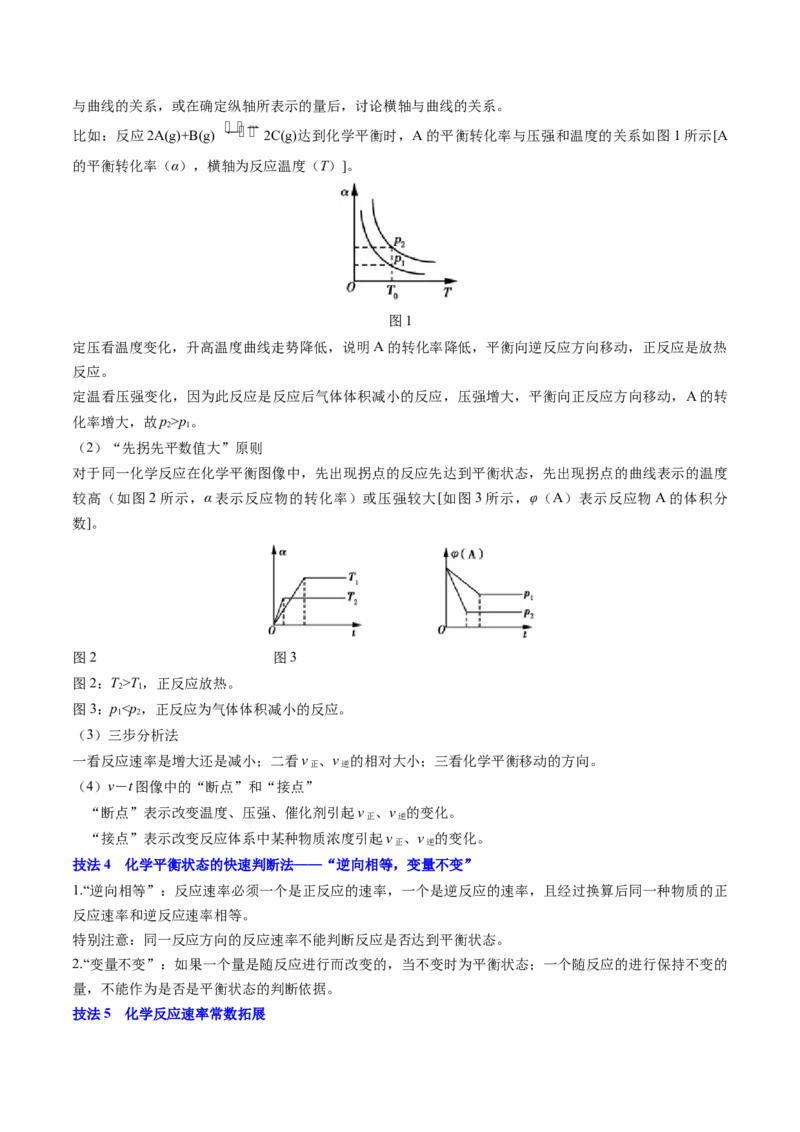
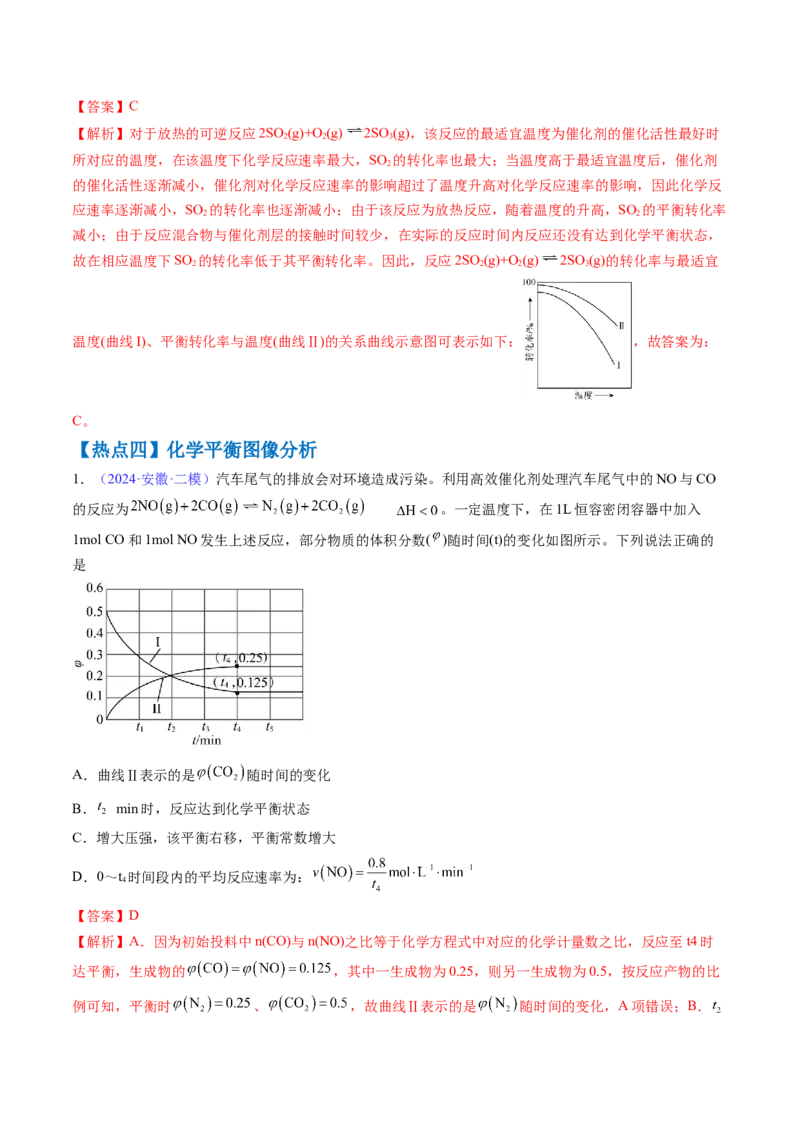
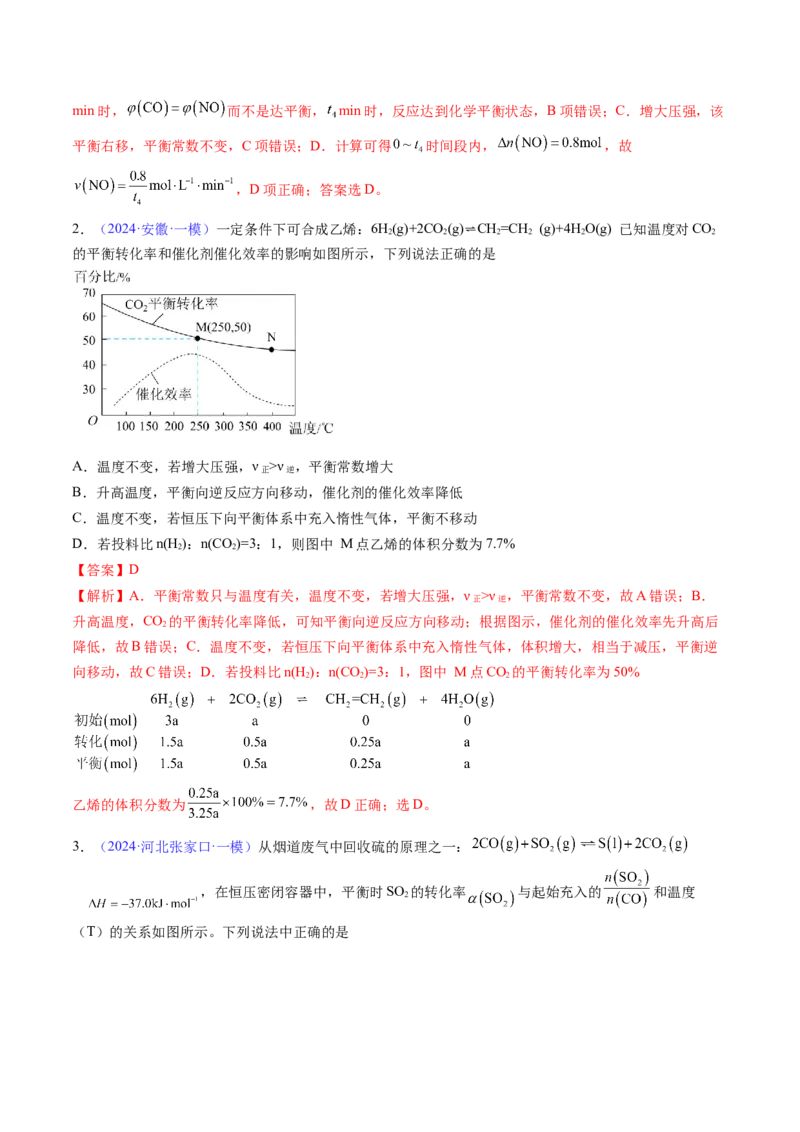
图3:pν ,平衡常数增大
正 逆
B.升高温度,平衡向逆反应方向移动,催化剂的催化效率降低
C.温度不变,若恒压下向平衡体系中充入惰性气体,平衡不移动
D.若投料比n(H ):n(CO)=3:1,则图中 M点乙烯的体积分数为7.7%
2 2
【答案】D
【解析】A.平衡常数只与温度有关,温度不变,若增大压强,ν >ν ,平衡常数不变,故A错误;B.
正 逆
升高温度,CO 的平衡转化率降低,可知平衡向逆反应方向移动;根据图示,催化剂的催化效率先升高后
2
降低,故B错误;C.温度不变,若恒压下向平衡体系中充入惰性气体,体积增大,相当于减压,平衡逆
向移动,故C错误;D.若投料比n(H ):n(CO)=3:1,图中 M点CO 的平衡转化率为50%
2 2 2
乙烯的体积分数为 ,故D正确;选D。
3.(2024·河北张家口·一模)从烟道废气中回收硫的原理之一:
,在恒压密闭容器中,平衡时SO 的转化率 与起始充入的 和温度
2
(T)的关系如图所示。下列说法中正确的是A.正反应的活化能
B.CO的转化率 :M>N
C.正反应速率 :M>Q
D.该反应的化学平衡常数表达式:
【答案】B
【分析】由题干图示信息可知,当 相同时,该反应正反应是一个放热反应,则升高温度,平衡逆
向移动,则SO 的平衡转化率减小,可知T<T,据此分析解题。
2 1 2
【解析】A.根据 =-37kJ/mol,则 由于不知道Ea 的数值,故无法确定正
逆
反应的活化能的大小,A错误;B.由题可知,N点到M点,温度降低平衡正向移动,CO的转化率增大,
N点到M点 增大,CO的转化率增大,故M、N点的转化率 :M>N,B正确;C.已知M
点对应的温度T<Q点对应的温度T,温度越高反应速率越快,故正反应速率 :M<Q,C错误;
1 2
D.已知S为液体,故该反应的化学平衡常数表达式: ,D错误;故答案为:B。
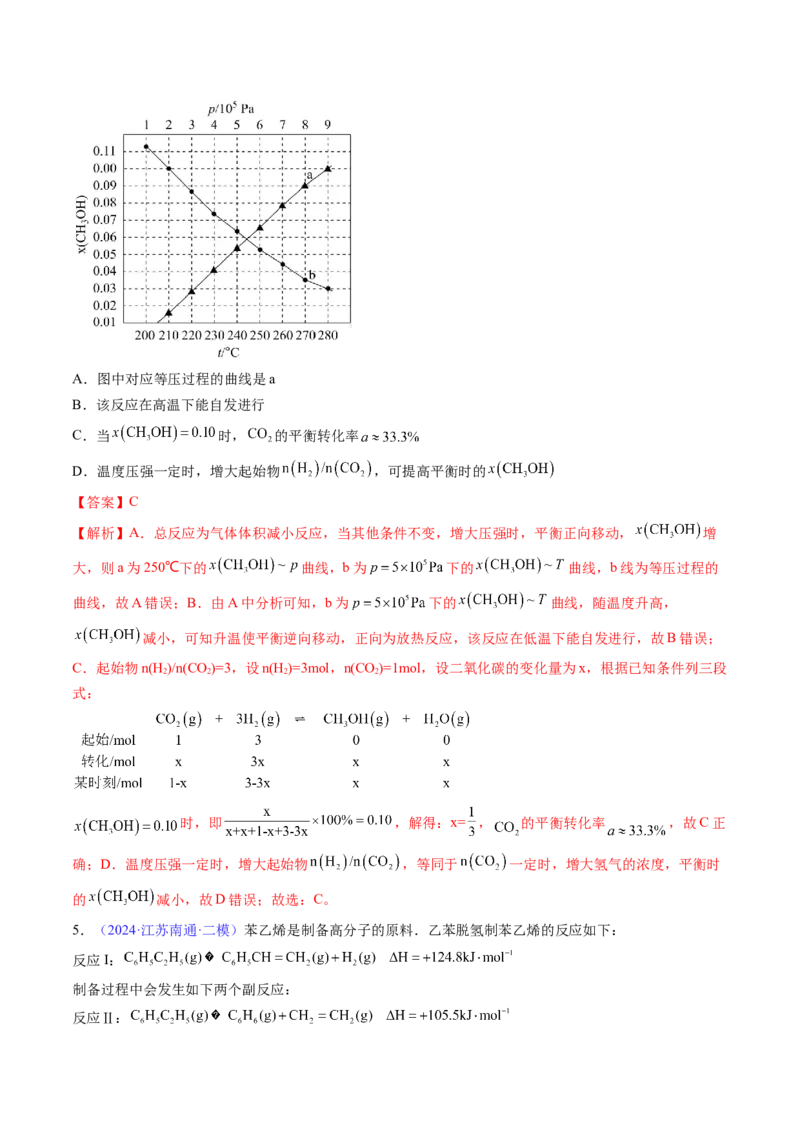
4.(2024·湖南长沙·一模)二氧化碳催化加氢制甲醇,有利于减少温室气体一氧化碳。其原理为
。在起始物n(H )/n(CO)=3时,在不同条件下达到平衡,设体系
2 2
中甲醇的物质的量分数为 ,在T=250℃下的 、在 下的
曲线如图所示。下列说法正确的是A.图中对应等压过程的曲线是a
B.该反应在高温下能自发进行
C.当 时, 的平衡转化率
D.温度压强一定时,增大起始物 ,可提高平衡时的
【答案】C
【解析】A.总反应为气体体积减小反应,当其他条件不变,增大压强时,平衡正向移动, 增
大,则a为250℃下的 曲线,b为 下的 曲线,b线为等压过程的
曲线,故A错误;B.由A中分析可知,b为 下的 曲线,随温度升高,
减小,可知升温使平衡逆向移动,正向为放热反应,该反应在低温下能自发进行,故B错误;
C.起始物n(H )/n(CO)=3,设n(H )=3mol,n(CO)=1mol,设二氧化碳的变化量为x,根据已知条件列三段
2 2 2 2
式:
时,即 ,解得:x= , 的平衡转化率 ,故C正
确;D.温度压强一定时,增大起始物 ,等同于 一定时,增大氢气的浓度,平衡时
的 减小,故D错误;故选:C。
5.(2024·江苏南通·二模)苯乙烯是制备高分子的原料.乙苯脱氢制苯乙烯的反应如下:
反应I:
制备过程中会发生如下两个副反应:
反应Ⅱ:反应Ⅲ:
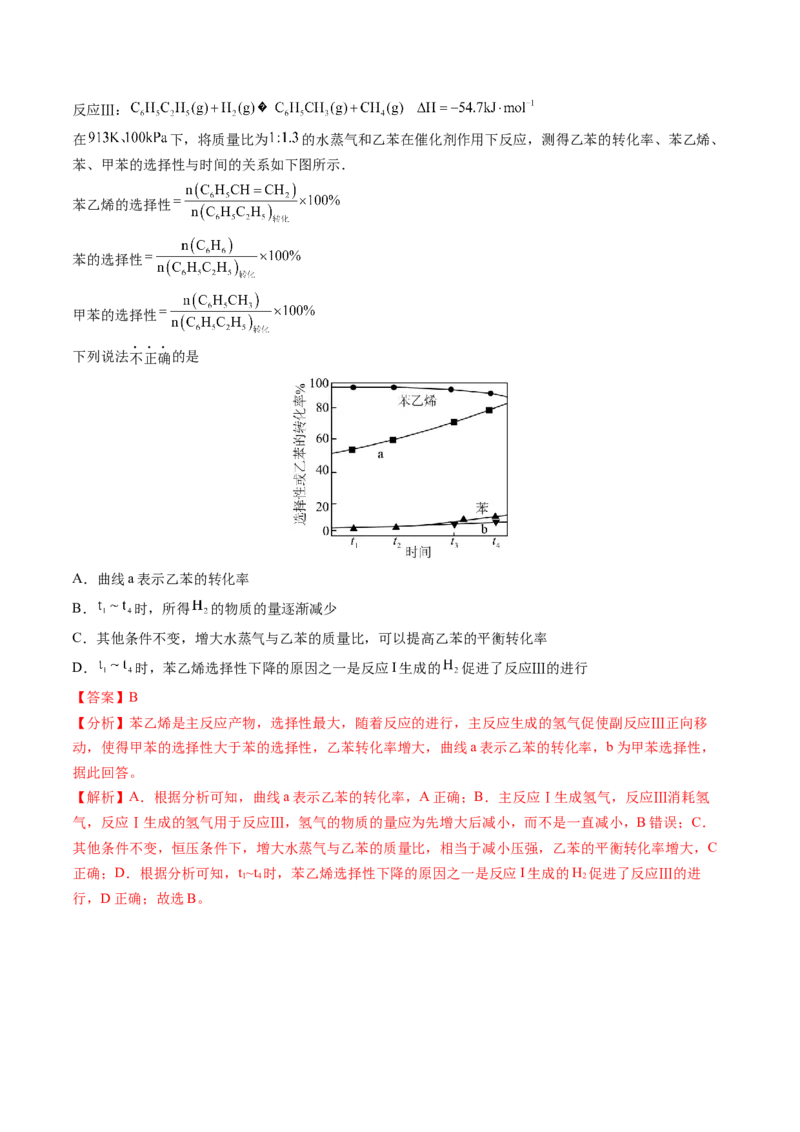
在 下,将质量比为 的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率、苯乙烯、
苯、甲苯的选择性与时间的关系如下图所示.
苯乙烯的选择性
苯的选择性
甲苯的选择性
下列说法不正确的是
A.曲线a表示乙苯的转化率
B. 时,所得 的物质的量逐渐减少
C.其他条件不变,增大水蒸气与乙苯的质量比,可以提高乙苯的平衡转化率
D. 时,苯乙烯选择性下降的原因之一是反应I生成的 促进了反应Ⅲ的进行
【答案】B
【分析】苯乙烯是主反应产物,选择性最大,随着反应的进行,主反应生成的氢气促使副反应Ⅲ正向移
动,使得甲苯的选择性大于苯的选择性,乙苯转化率增大,曲线a表示乙苯的转化率,b为甲苯选择性,
据此回答。
【解析】A.根据分析可知,曲线a表示乙苯的转化率,A正确;B.主反应Ⅰ生成氢气,反应Ⅲ消耗氢
气,反应Ⅰ生成的氢气用于反应Ⅲ,氢气的物质的量应为先增大后减小,而不是一直减小,B错误;C.
其他条件不变,恒压条件下,增大水蒸气与乙苯的质量比,相当于减小压强,乙苯的平衡转化率增大,C
正确;D.根据分析可知,t~t 时,苯乙烯选择性下降的原因之一是反应I生成的H 促进了反应Ⅲ的进
1 4 2
行,D正确;故选B。