文档内容
通关 09 电化学原理及应用
目录
【高考预测】预测考向,总结常考点及应对的策略
【技法必备】提供方法技巧,解决问题策略
【误区点拨】点拨常见的易错点
【抢分通关】分析命题热点,把握解题技巧,精选名校模拟题
概率预测 ☆ ☆ ☆ ☆ ☆
题型预测 选择题☆ ☆ ☆ ☆ ☆
考向预测 原电池、新型化学电源、电解池、金属腐蚀的综合分析及应用
不论是全国卷还是各自主命题省份的试卷,对电化学考查的概率为 100%,这主要源于电化学在中学化学
中的重要地位,在生活、生产中有着广泛而重要的应用,并且能很好地考查考生宏观辨识与微观探折、变
化观念与平衡思想以及证据推理与摸型认知等多重学科素养,根据对近年来考题的分析,电化学命题往往
以可充电电池的工作原理及电解原理的应用为背景,考查电极反应式的书写、离子移动方向、金属的电化
学腐蚀及防护等知识。或将原电池、电解原理与物质的制备、金属的提纯、金属的防护结合起来考查,考
查的角度主要有电极反应方程式的书写或正误判断、离子移动的方向、电极产物种类的判断与量的计算
等;同时也对信息提取、应用能力进行考查。预计在今后的高考中电化学考点还有“变热”的趋势,题目
也会更加新颖。备考时要侧重原电池与电解池工作原理中基础考点的复习和电极反应式书写技巧的掌握。
技法1 电化学的解题流程
第一步:读题
逐字逐句读,挖掘关键字,排除无效信息,找到对解题有价值的信息,并作标记。
第一步:确定装置类型
放电为原电池,充电为电解池。
第二步:判断电极名称
放电时的正极为充电时间阳极,放电时的负极为充电时的阴极。
第三步:写出电极反应
放电时的正极反应颠倒过来为充电时的阳极反应;放电时的负极反应颠倒过来为充电时的阴极反应。
第四步:分析离子移动
由生成一极向消耗一极移动;区域pH变化:OH-生成区,H+消耗区,pH增大;OH-消耗区,H+生成区,pH
减小。技法2 判断电极
(1)通过反应类型判断
①失去电子的电极为负极,发生氧化反应;
②得到电子的电极为正极,发生还原反应。
(2)通过电子定向移动方向和电流方向判断
①电子流出的电极为负极,电子经外电路流入正极;
②电流流出的电极为正极,电流经外电路流入负极。
(3)根据离子移动方向判断
阴离子向负极移动,阳离子向正极移动。
(4)根据电极现象判断
一般不断溶解、质量减轻的电极为负极;有固体析出、质量增加或不变或有气体产生的电极为正极。
技法3 书写电极反应式
1.直接书写
2.间接书写
第一步,写出电池总反应式。
第二步,写出电极的正极反应式。
第三步,负极反应式=总反应式-正极反应式。
技法4 充、放电时电解质溶液中离子移动方向的判断
分析电池工作过程中电解质溶液的变化时,要结合电池总反应进行分析。
1.首先应分清电池是放电还是充电。
2.再判断出正、负极或阴、阳极。
放电:阳离子→正极,阴离子→负极;
充电:阳离子→阴极,阴离子→阳极;
总之:阳离子→发生还原反应的电极;阴离子→发生氧化反应的电极。
技法5 燃料电池电极反应式的书写
第一步:写出电池总反应式。
燃料电池的总反应与燃料燃烧的反应一致,若产物能和电解质反应,则总反应为加合后的反应。如甲烷燃
料电池(电解质溶液为NaOH溶液)的反应如下:
CH+2O===CO +2HO①
4 2 2 2
CO+2NaOH===Na CO+HO②
2 2 3 2①+②可得甲烷燃料电池的总反应式:CH+2O+2NaOH===Na CO+3HO。
4 2 2 3 2
第二步:写出电池的正极反应式。
根据燃料电池的特点,一般在正极上发生还原反应的物质都是O ,因电解质溶液不同,故其电极反应也会
2
有所不同:
燃料电池电解质 正极反应式
酸性电解质 O+4H++4e-===2H O
2 2
碱性电解质 O+2HO+4e-===4OH-
2 2
固体电解质(高温下能传导O2-) O+4e-===2O2-
2
熔融碳酸盐(如熔融KCO) O+2CO+4e-===2CO
2 3 2 2
第三步:电池的总反应式-电池的正极反应式=电池的负极反应式。
技法6 金属腐蚀快慢的判断方法
(1)对同一电解质溶液来说,腐蚀速率的快慢:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有
防护措施的腐蚀。
(2)对同一金属来说,在不同溶液中腐蚀速率的快慢:强电解质溶液中>弱电解质溶液中>非电解质溶液中。
(3)活动性不同的两种金属,活动性差别越大,腐蚀速率越快。
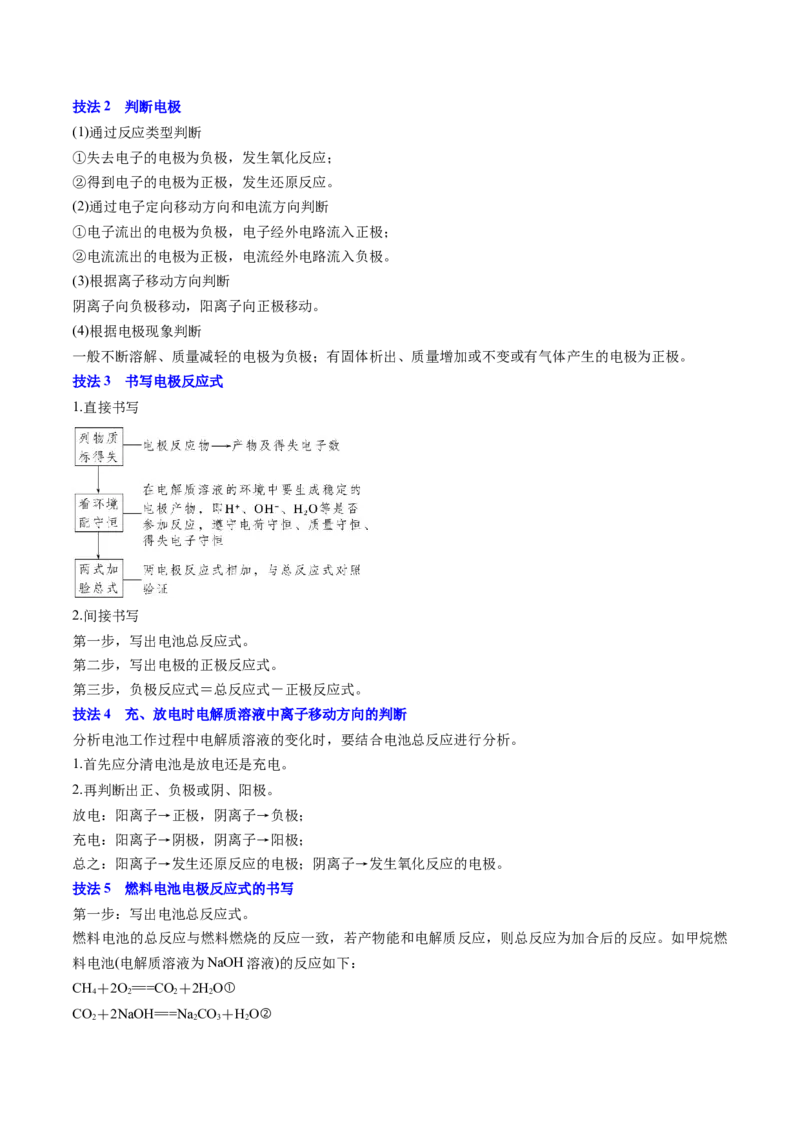
(4)对同一种电解质溶液来说,电解质浓度越大,金属腐蚀越快。技法7 电解池电极反应式的书写步骤
微提醒:通常电极反应可以根据阳极材料和电解质溶液的性质进行判断,但在高考题中往往需要结合题给
信息进行判断。
技法8 有关离子交换膜的类型及其应用
(1)阳离子交换膜(只允许阳离子和水分子通过,阻止阴离子和气体通过)
以锌铜原电池为例,中间用阳离子交换膜隔开
①负极反应式:Zn-2e-=Zn2+
②正极反应式:Cu2++2e-=Cu
③Zn2+通过阳离子交换膜进入正极区
④阳离子→透过阳离子交换膜→原电池正极(或电解池的阴极)
(2)阴离子交换膜(只允许阴离子和水分子通过,阻止阳离子和气体通过)以Pt为电极电解淀粉KI溶液,中间用阴离子交换膜隔开
①阴极反应式:2HO+2e-=H ↑+2OH-
2 2
②阳极反应式:2I-_2e-=I
2
③阴极产生的OH-移向阳极与阳极产物反应:3I+6OH-=IO -+5I-
2 3
+3HO
2
④阴离子→透过阴离子交换膜→电解池阳极(或原电池的负极)
(3)质子交换膜(只允许H+和水分子通过)
在微生物作用下电解有机废水(含CHCOOH),可获得清洁能源H
3 2
①阴极反应式:2H++2e-=H ↑
2
②阳极反应式:CHCOOH-8e-+2HO=2CO↑+8H+
3 2 2
③阳极产生的H+通过质子交换膜移向阴极
④H+→透过质子交换膜→原电池正极(或电解池的阴极)
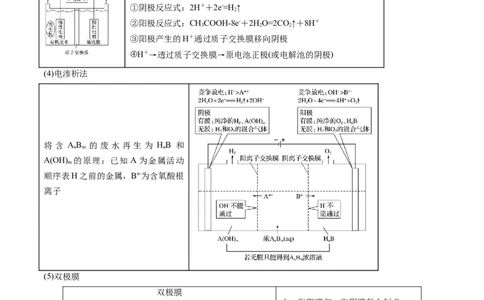
(4)电渗析法
将 含 AB 的 废 水 再 生 为 HB 和
n m n
A(OH) 的原理:已知A为金属活动
m
顺序表H之前的金属,Bn-为含氧酸根
离子
(5)双极膜
双极膜
由一张阳膜和一张阴膜复合制成。
该膜特点是在直流电的作用下,
阴、阳膜复合层间的HO解离成H+
2
和OH-并通过阳膜和阴膜分别向两
极区移动,作为H+和OH-的离子源
(6)解题流程
第一步,分清隔膜类型。即交换膜属于阳离子交换膜、阴离子交换膜或质子交换膜中的哪一种,判断允许
哪种离子通过隔膜。第二步,写出电极反应,判断交换膜两侧离子变化,推断电荷变化,根据电荷平衡判断离子迁移方向。
第三步,分析隔膜作用。在产品制备中,隔膜作用主要是提高产品纯度,避免产物之间发生反应,或避免
产物因发生反应而造成危险。
技法9 电化学综合计算的三种常用方法
(1)根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
(2)根据电子守恒计算
①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电子数
相等。
②用于混合溶液中电解的分阶段计算。
(3)根据关系式计算
根据得失电子守恒定律建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
一、关于原电池的认识误区
1.原电池的电极类型不仅跟电极材料有关,还与电解质溶液的性质有关。如镁—铝电极在稀硫酸中构成原
电池,镁为负极,铝为正极,但若以氢氧化钠为电解质溶液,则铝为负极,镁为正极。
2.原电池闭合回路的形成有多种方式,可以是导线连接两个电极,也可以是两电极相接触。
3.无论在原电池还是在电解池中,电子均不能通过电解质溶液。
4.通电时,溶液中的溶质粒子分别向两级移动,或不移动(溶质粒子为分子,不带电);而胶体中的分散
质粒子向某一极移动。
5.燃料电池负极上燃料放电生成CO2,要考虑溶液酸碱性,若为碱性,则CO2+2OH-=CO3 2-+H2O。
6.对蓄电池而言,其正、负极在充电时应分别和外接电源的正、负极相连。即正极接正极,负极接负极。
7.原电池电解质溶液中,阴离子向电池负极移动,阳离子向电池正极移动;电解池中阴离子向电池阳极移动,阳
离子向电池阴极移动,与导线中电子的定向移动共同组成了一个完整的闭合回路。。
8.原电池和电解池的外电路:电子定向移动形成电流;内电路:离子定向移动形成电流。
9.在船身装上锌块利用的是牺牲阳极的阴极保护法(专业名词),即使是原电池但也是这种说法。
10.原电池才考虑是析氢腐蚀还是吸氧腐蚀。
11.废电池中对环境形成污染的主要物质是多种重金属。
二、电解过程中易出现的认识误区
1.金属活动性顺序中银以前的金属(含银)作电极时,由于金属本身可以参与阳极反应,称为金属电极或活
性电极(如Zn、Fe、Cu、Ag等);金属活动性顺序中银以后的金属或非金属作电极时,称为惰性电极,主
要有铂(Pt)、石墨等。
2.电解时,在外电路中有电子通过,而在溶液中是靠离子移动导电,即电子不通过电解质溶液。
3.书写电解池的电极反应式时,可以用实际放电的离子表示,但书写电解池的总反应时,弱电解质要写成分子式。如用惰性电极电解食盐水时,阴极反应式为2H++2e-===H ↑(或2HO+2e-===H ↑+2OH-);
2 2 2
总反应离子方程式为2Cl-+2HO=====2OH-+H↑+Cl↑。
2 2 2
4.电解水溶液时,应注意放电顺序,位于H+、OH-之后的离子一般不参与放电。
5.Fe3+在阴极上放电时生成Fe2+而不是得到单质Fe。
6.判断电解产物、书写电极反应式以及分析电解质溶液的变化时首先要注意阳极是活性材料还是惰性材
料。
7.书写电解化学方程式时,应看清是电解电解质的水溶液还是熔融电解质。Al3+、Mg2+、Na+、Ca2+、K
+只有在熔融状态下才放电。
8.电解Hg (NO ) 溶液时,阴极上电极方程式可表示为:Hg 2++2e-=2Hg。
2 3 2 2
三、电解时溶液pH的变化规律
①若电解时阴极上产生H,阳极上无O 产生,电解后溶液pH增大;
2 2
②若阴极上无H 产生,阳极上产生O,则电解后溶液pH减小;
2 2
③若阴极上有H 产生,阳极上有O 产生,且VH=2VO,则有“酸更酸,碱更碱,中性就不变”,即:
2 2 2 2
a.如果原溶液是酸溶液,则pH变小;
b.如果原溶液为碱溶液,则pH变大;
c.如果原溶液为中性溶液,则电解后pH不变。
四、电解质溶液的复原措施
电解后的溶液恢复到原状态,出什么加什么(即一般加入阴极产物与阳极产物的化合物)。如用惰性电极电
解盐酸(足量)一段时间后,若使溶液复原,应通入HCl气体而不能加入盐酸。
【热点一】考查原电池工作原理的分析判断
1.(2024·贵州·二模)2023年诺贝尔化学奖授予了三位科学家,以表彰他们为“发现和合成量子点”作出
的贡献。一种含有新型量子点(简写为 )的复合光催化剂利用太阳能高效制氢的原理如图所示。
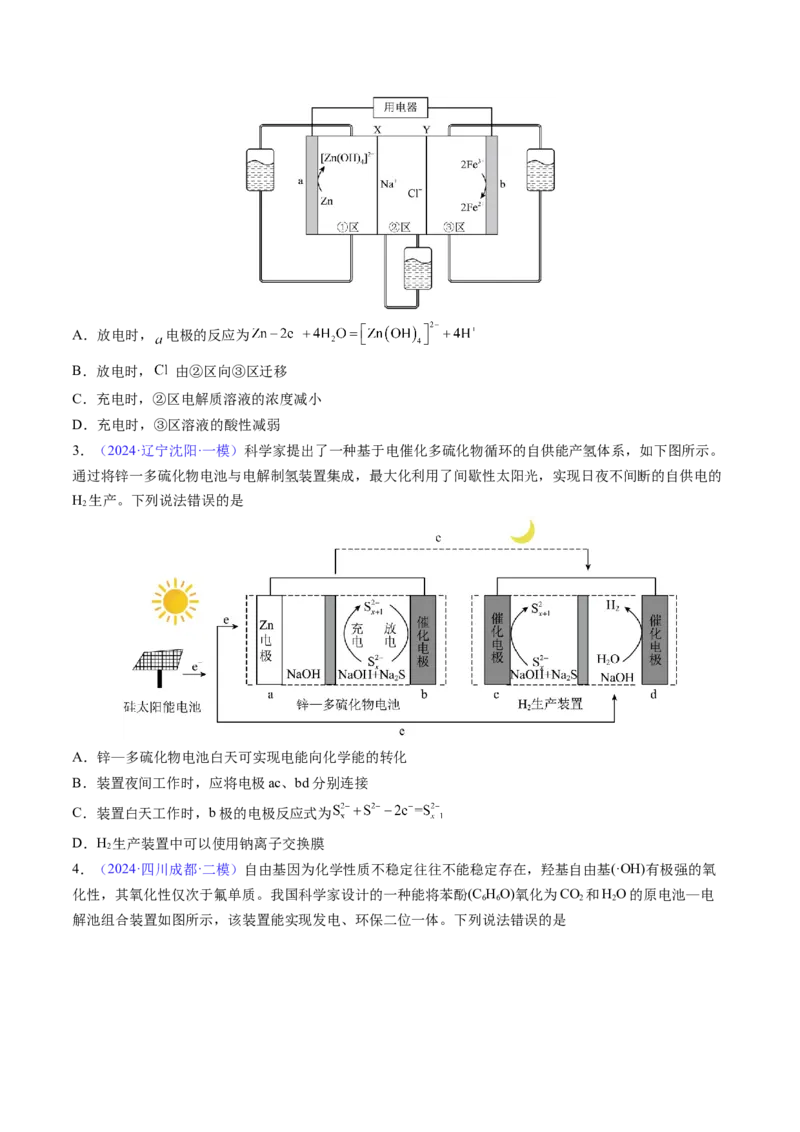
下列说法正确的是A.电子由电极b沿导线流向电极a
B.电极a的电极反应式为:S2-+3H O-6e-= +6H+
2
C.标准状况下,当电路转移2mol电子时电极 生成11.2L
D.电池的总反应方程式为:S2-+3H O +3H ↑
2 2
2.(2024·海南省直辖县级单位·模拟预测)铝空气燃料电池具有能量密度大、质量轻、无污染、可靠性
高、寿命长、使用安全等优点,图1是一种中性(盐水)铝空气燃料电池装置图,其空气电极结构如图2所
示。
已知:空气电极转化过程为 (过氧氢根离子) ,下列说法正确的是
A.铝为电池负极,Al发生还原反应
B.空气电极生成 的电极反应:
C.放电时电子转移方向:铝→电解质溶液→空气电极
D.多孔催化层和多孔防水透气层可增大反应速率
3.(2024·广东·二模)一种基于原电池原理的氧气传感器可用于测定样气中氧气的含量,其装置如图所
示。下列说法正确的是
A.铅电极为正极
B.银电极上发生的反应为
C.电子由铅电极经过KOH溶液流向银电极
D.工作过程中,传感器的质量不变
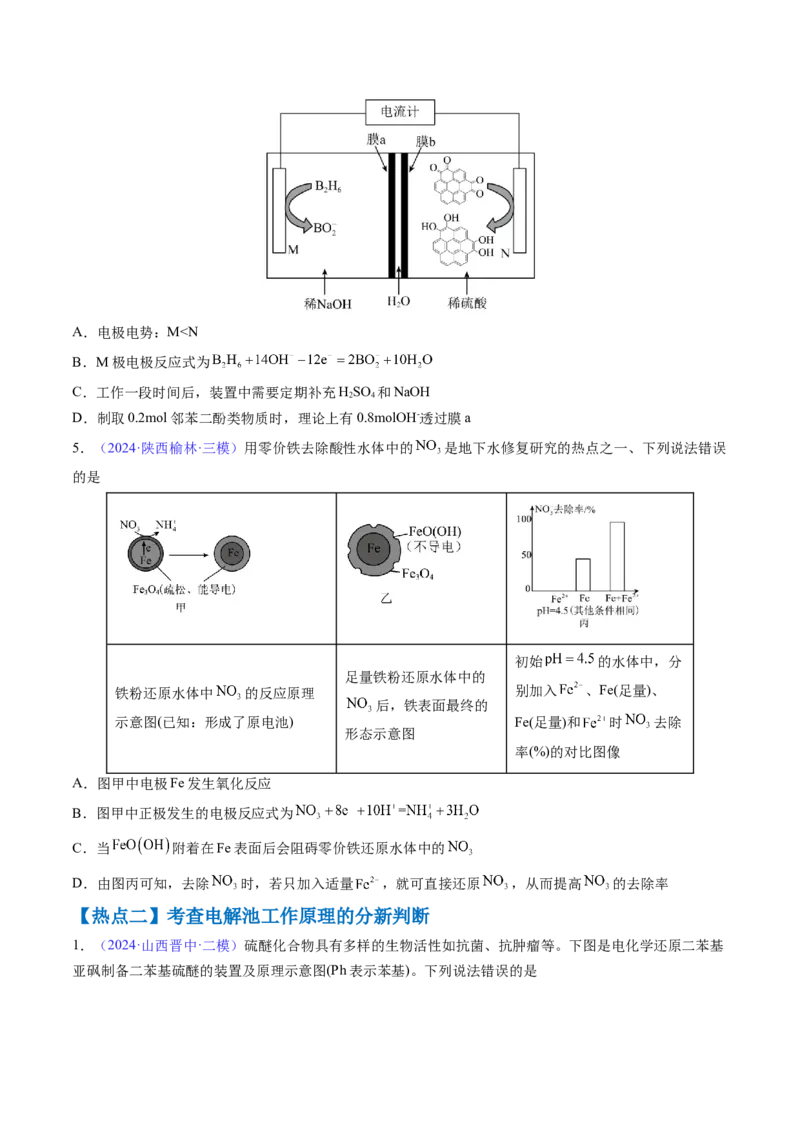
4.(2024·山东济南·一模)我国科学家发现,利用如下装置可以将邻苯二醌类物质转化为邻苯二酚类物
质,已知双极膜(膜a、膜b)中间层中的HO可解离为H+和OH-。下列说法错误的是
2A.电极电势:M