文档内容
反应机理的图象分析与应用
目 录
1
2
考点一 反应历程中的能量变化图像 2
【真题研析·规律探寻】 2
解题技巧
三步突破能量变化能垒图 5
【核心提炼·考向探究】 5
1.题在书外,理在书中——选编教材中的经典图示 5
2.变形考查——源于教材高于教材 6
3.不断创新——真情境考查真应用 6
【题型特训·命题预测】 7
题型一 相对能量变化图 7
题型二 能垒图 13
题型三 过渡态能量变化图 18
考点二 催化剂的催化反应机理分析 22
【真题研析·规律探寻】 22
解题技巧 26
1. 催化反应机理的分析思维模型 26
2.催化反应机理题的解题思路 26
【核心提炼·考向探究】 27
1.催化剂具有的三大特征 27
2.催化剂与化学反应 27
资料整理【淘宝店铺:向阳百分百】3.催化剂与中间产物 27
4.探究催化剂的催化机理 28
易错题型 29
认识催化剂的四大误区 29
【题型归纳·命题预测】 30
题型一 无机反应机理图分析 30
题型二 有机反应机理图分析 39
考点要求 考题统计 考情分析
2023•浙江省1月选考 【命题规律】
14题,3分;2022•湖 化学反应机理试题以图示的形式来描述某一化学变化所经由
反应历程中的能
南选择性考试12题,4 的全部反应,就是把一个复杂反应分解成若干个反应,然后
量变化图像
按照一定规律组合起来,从而达到阐述复杂反应的内在联系
分;2021•湖南选择性
的目的。近几年这类题型是高考热点,呈现方式每年都有变
考试14题,4分
化,意对解题模型进行掌握。
2023•广东卷15题,3
【命题预测】
分;2023•全国新课标
反应机理在近几年高考题中频繁出现,预计在 2023年高考
卷12题,6分;2023•
催化剂的催化反 中,会以选择和在化学反应原理中图像进行呈现,考查学生
浙江省6月选考14
应机理分析 知识运用与推理能力。反应机理真实情境进行分析,思维转
题,3分;2022湖南卷
化大,考查考生的迁移运用能力和创新思维,具有一定的难
9题,3分;2022山东
度。
卷10题,2分
资料整理【淘宝店铺:向阳百分百】考点一 反应历程中的能量变化图像
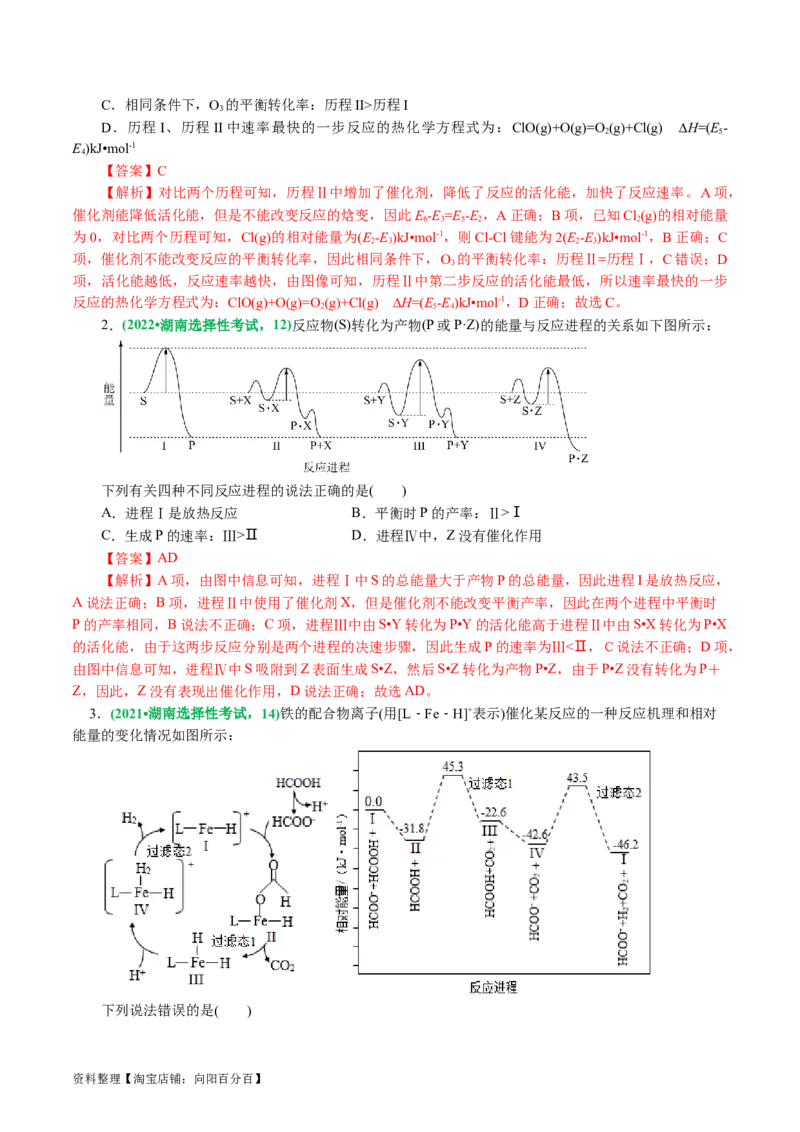
1.(2023•浙江省1月选考,14)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下
[已知O(g)和Cl(g)的相对能量为0],下列说法不正确的是 ( )
2 2
A.E-E=E-E
6 3 5 2
B.可计算Cl-Cl键能为2(E-E)kJ•mol-1
2 3
资料整理【淘宝店铺:向阳百分百】C.相同条件下,O 的平衡转化率:历程II>历程I
3
D.历程I、历程II中速率最快的一步反应的热化学方程式为:ClO(g)+O(g)=O (g)+Cl(g) ∆H=(E-
2 5
E)kJ•mol-1
4
【答案】C
【解析】对比两个历程可知,历程Ⅱ中增加了催化剂,降低了反应的活化能,加快了反应速率。A项,
催化剂能降低活化能,但是不能改变反应的焓变,因此E-E=E-E,A正确;B项,已知Cl(g)的相对能量
6 3 5 2 2
为0,对比两个历程可知,Cl(g)的相对能量为(E-E)kJ•mol-1,则Cl-Cl键能为2(E-E)kJ•mol-1,B正确;C
2 3 2 3
项,催化剂不能改变反应的平衡转化率,因此相同条件下,O 的平衡转化率:历程Ⅱ=历程Ⅰ,C错误;D
3
项,活化能越低,反应速率越快,由图像可知,历程Ⅱ中第二步反应的活化能最低,所以速率最快的一步
反应的热化学方程式为:ClO(g)+O(g)=O (g)+Cl(g) ∆H=(E-E)kJ•mol-1,D正确;故选C。
2 5 4
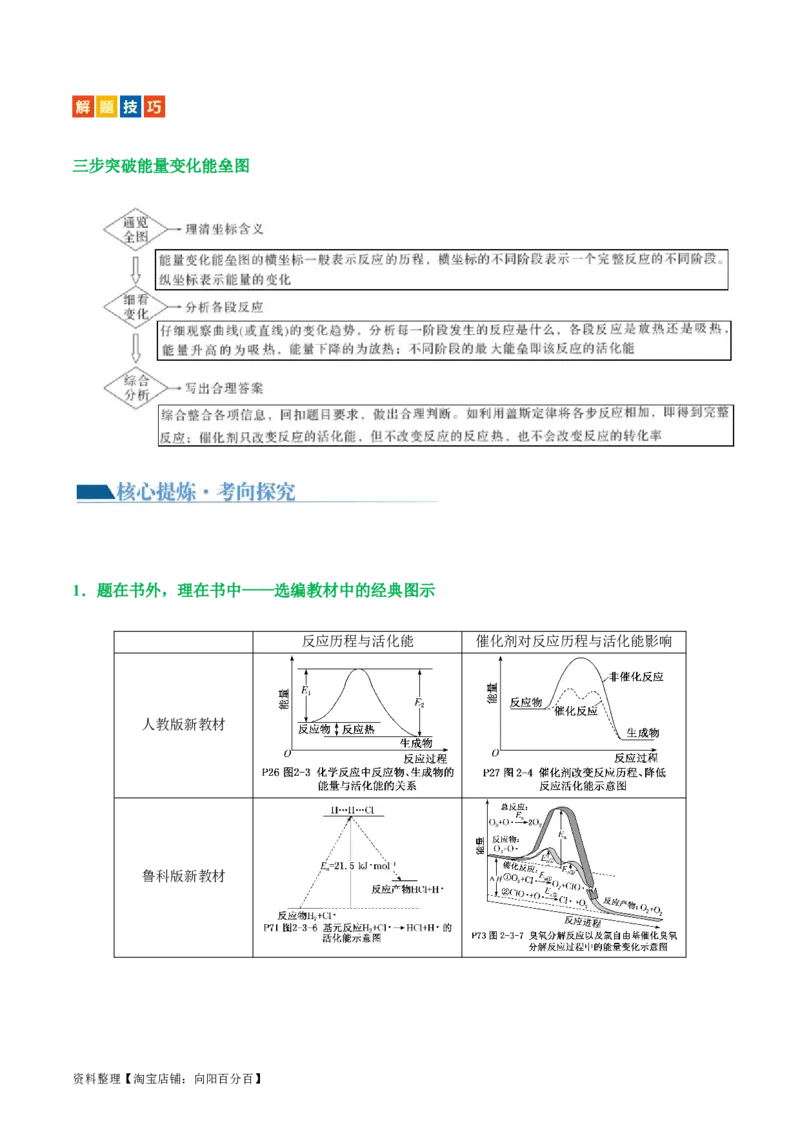
2.(2022•湖南选择性考试,12)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
下列有关四种不同反应进程的说法正确的是( )
A.进程Ⅰ是放热反应 B.平衡时P的产率:Ⅱ>Ⅰ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
【答案】AD
【解析】A项,由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,
A说法正确;B项,进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时
P的产率相同,B说法不正确;C项,进程Ⅲ中由S•Y转化为P•Y的活化能高于进程Ⅱ中由S•X转化为P•X
的活化能,由于这两步反应分别是两个进程的决速步骤,因此生成P的速率为Ⅲ<Ⅱ,C说法不正确;D项,
由图中信息可知,进程Ⅳ中S吸附到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有转化为P+
Z,因此,Z没有表现出催化作用,D说法正确;故选AD。
3.(2021•湖南选择性考试,14)铁的配合物离子(用[L﹣Fe﹣H]+表示)催化某反应的一种反应机理和相对
能量的变化情况如图所示:
下列说法错误的是( )
资料整理【淘宝店铺:向阳百分百】A.该过程的总反应为HCOOH CO↑+H ↑ B.H+浓度过大或者过小,均导致反应速率降低
2 2
C.该催化循环中Fe元素的化合价发生了变化 D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
【答案】D
【解析】反应历程 HCOOH→HCOO﹣+H+,[L﹣Fe﹣H]++HCOO﹣→ , →CO+
2
, +H+→ , →Ⅰ[L﹣Fe﹣H]++H ↑。A项,合并HCOOH→HCOO﹣
2
+H+ , [L﹣Fe﹣H]++HCOO﹣→ , → CO+ , +H+→ ,
2
→Ⅰ[L﹣Fe﹣H]++H ,得总方程式,该过程的总反应为HCOOH CO↑+H ↑,故A正确;
2 2 2
B项,H+浓度过大HCOO﹣浓度减小,[L﹣Fe﹣H]++HCOO﹣→ 反应慢,H+浓度过小 +H+→
反应慢,H+浓度过大或者过小,均导致反应速率降低,故B正确;C项, →CO+
2
,碳的化合价升高,铁的化合价降低,故C正确;D项,决定化学反应速率的步骤是最慢的一步,
活化能越高,反应越慢,从反应机理图中可知,Ⅳ→Ⅰ的活化能最大,该过程的总反应速率由Ⅳ→Ⅰ步骤
决定,故D错误;故选D。
资料整理【淘宝店铺:向阳百分百】三步突破能量变化能垒图
1.题在书外,理在书中——选编教材中的经典图示
反应历程与活化能 催化剂对反应历程与活化能影响
人教版新教材
鲁科版新教材
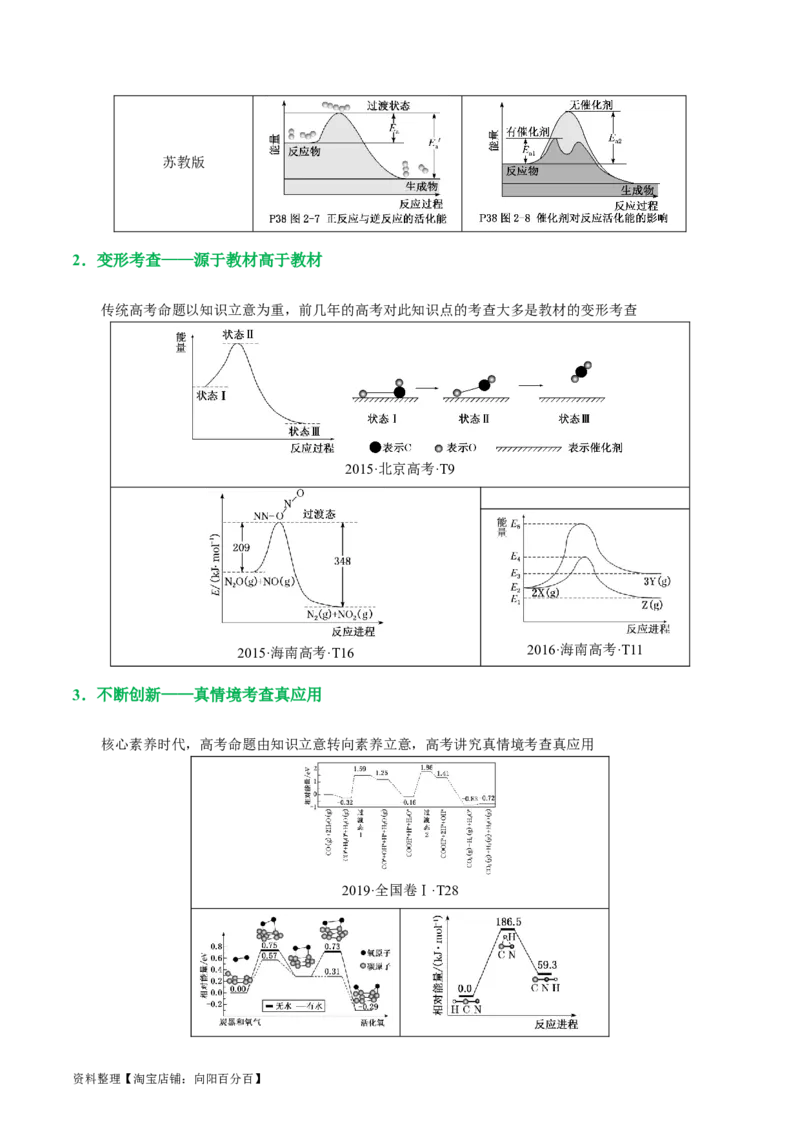
资料整理【淘宝店铺:向阳百分百】苏教版
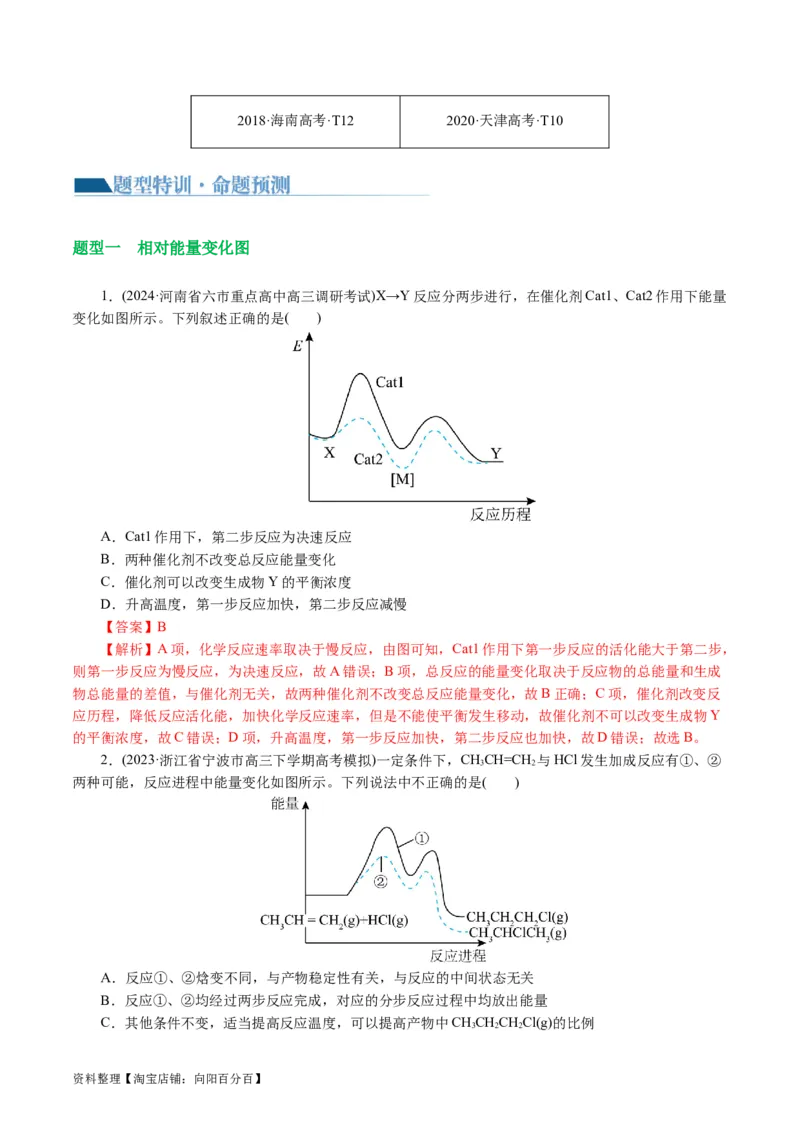
2.变形考查——源于教材高于教材
传统高考命题以知识立意为重,前几年的高考对此知识点的考查大多是教材的变形考查
2015·北京高考·T9
2015·海南高考·T16 2016·海南高考·T11
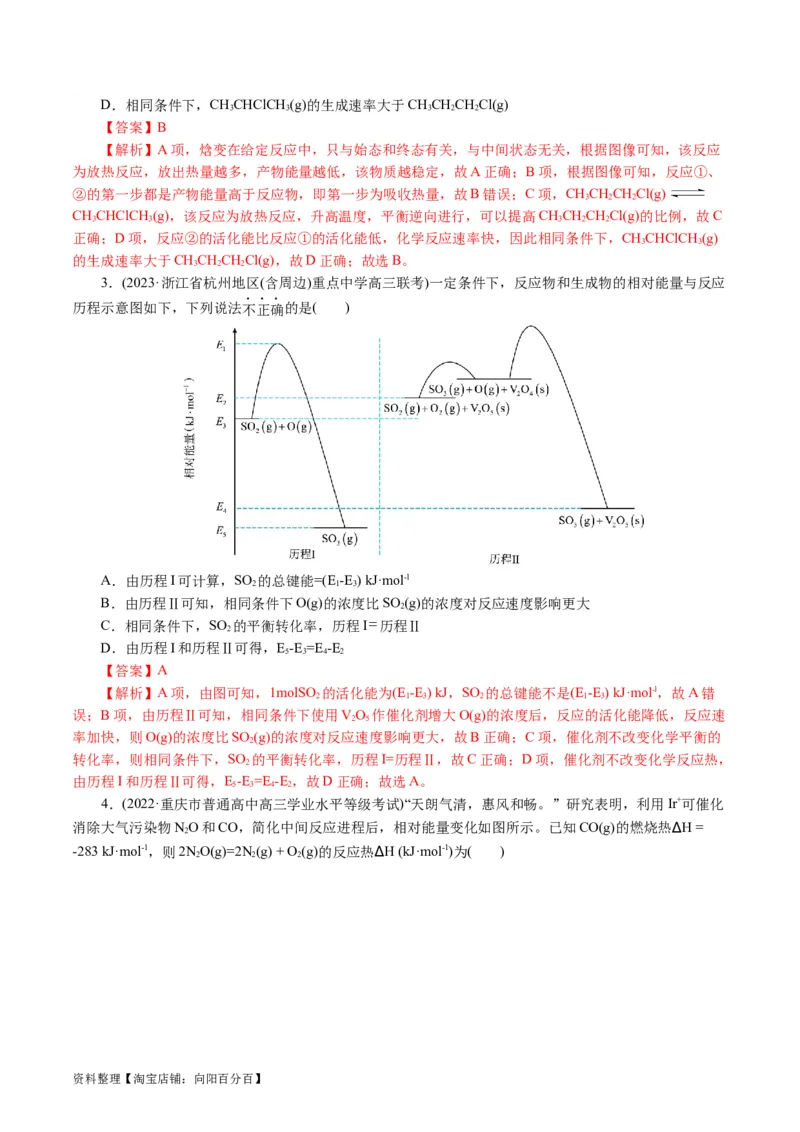
3.不断创新——真情境考查真应用
核心素养时代,高考命题由知识立意转向素养立意,高考讲究真情境考查真应用
2019·全国卷Ⅰ·T28
资料整理【淘宝店铺:向阳百分百】2018·海南高考·T12 2020·天津高考·T10
题型一 相对能量变化图
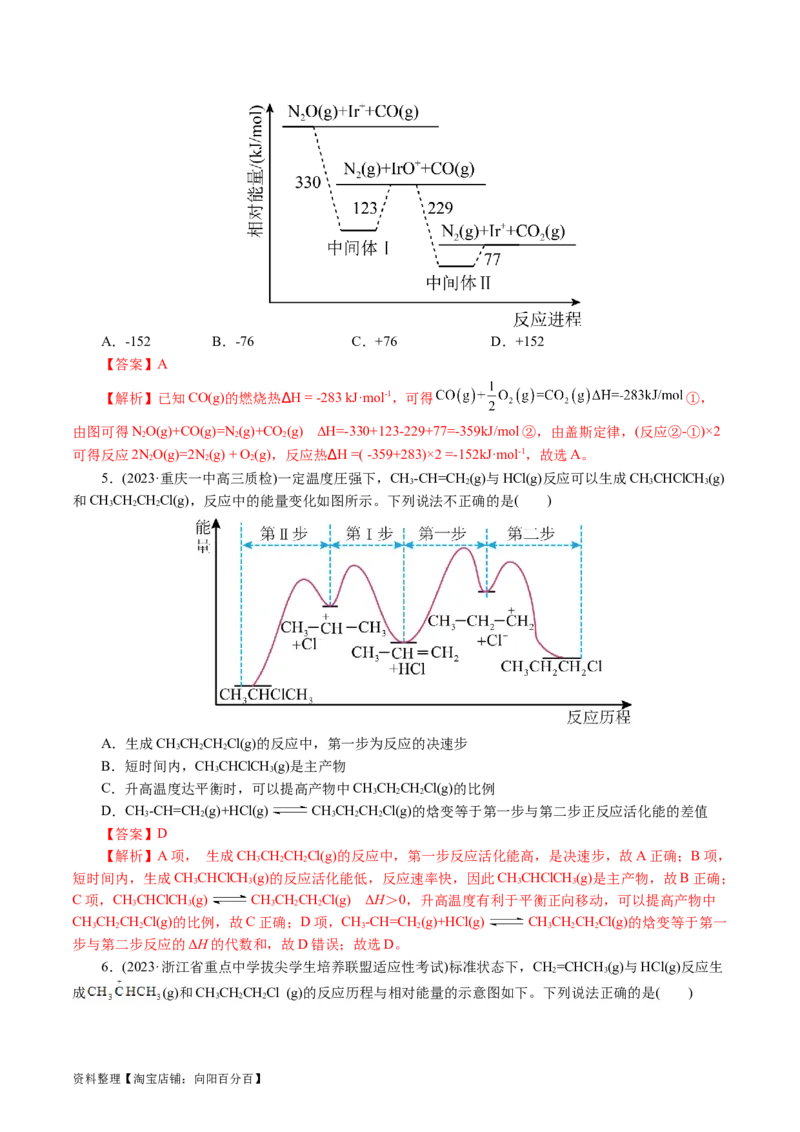
1.(2024·河南省六市重点高中高三调研考试)X→Y反应分两步进行,在催化剂Cat1、Cat2作用下能量
变化如图所示。下列叙述正确的是( )
A.Cat1作用下,第二步反应为决速反应
B.两种催化剂不改变总反应能量变化
C.催化剂可以改变生成物Y的平衡浓度
D.升高温度,第一步反应加快,第二步反应减慢
【答案】B
【解析】A项,化学反应速率取决于慢反应,由图可知,Cat1作用下第一步反应的活化能大于第二步,
则第一步反应为慢反应,为决速反应,故A错误;B项,总反应的能量变化取决于反应物的总能量和生成
物总能量的差值,与催化剂无关,故两种催化剂不改变总反应能量变化,故B正确;C项,催化剂改变反
应历程,降低反应活化能,加快化学反应速率,但是不能使平衡发生移动,故催化剂不可以改变生成物Y
的平衡浓度,故C错误;D项,升高温度,第一步反应加快,第二步反应也加快,故D错误;故选B。
2.(2023·浙江省宁波市高三下学期高考模拟)一定条件下,CHCH=CH 与HCl发生加成反应有①、②
3 2
两种可能,反应进程中能量变化如图所示。下列说法中不正确的是( )
A.反应①、②焓变不同,与产物稳定性有关,与反应的中间状态无关
B.反应①、②均经过两步反应完成,对应的分步反应过程中均放出能量
C.其他条件不变,适当提高反应温度,可以提高产物中CHCHCHCl(g)的比例
3 2 2
资料整理【淘宝店铺:向阳百分百】D.相同条件下,CHCHClCH (g)的生成速率大于CHCHCHCl(g)
3 3 3 2 2
【答案】B
【解析】A项,焓变在给定反应中,只与始态和终态有关,与中间状态无关,根据图像可知,该反应
为放热反应,放出热量越多,产物能量越低,该物质越稳定,故A正确;B项,根据图像可知,反应①、
②的第一步都是产物能量高于反应物,即第一步为吸收热量,故B错误;C项,CHCHCHCl(g)
3 2 2
CHCHClCH (g),该反应为放热反应,升高温度,平衡逆向进行,可以提高CHCHCHCl(g)的比例,故C
3 3 3 2 2
正确;D项,反应②的活化能比反应①的活化能低,化学反应速率快,因此相同条件下,CHCHClCH (g)
3 3
的生成速率大于CHCHCHCl(g),故D正确;故选B。
3 2 2
3.(2023·浙江省杭州地区(含周边)重点中学高三联考)一定条件下,反应物和生成物的相对能量与反应
历程示意图如下,下列说法不正确的是( )
A.由历程I可计算,SO 的总键能=(E-E ) kJ·mol-l
2 1 3
B.由历程Ⅱ可知,相同条件下O(g)的浓度比SO (g)的浓度对反应速度影响更大
2
C.相同条件下,SO 的平衡转化率,历程I 历程Ⅱ
2
D.由历程I和历程Ⅱ可得,E-E =E-E
5 3 4 2
【答案】A
【解析】A项,由图可知,1molSO 的活化能为(E -E ) kJ,SO 的总键能不是(E -E ) kJ·mol-l,故A错
2 1 3 2 1 3
误;B项,由历程Ⅱ可知,相同条件下使用VO 作催化剂增大O(g)的浓度后,反应的活化能降低,反应速
2 5
率加快,则O(g)的浓度比SO (g)的浓度对反应速度影响更大,故B正确;C项,催化剂不改变化学平衡的
2
转化率,则相同条件下,SO 的平衡转化率,历程I=历程Ⅱ,故C正确;D项,催化剂不改变化学反应热,
2
由历程I和历程Ⅱ可得,E-E =E-E ,故D正确;故选A。
5 3 4 2
4.(2022·重庆市普通高中高三学业水平等级考试)“天朗气清,惠风和畅。”研究表明,利用Ir+可催化
消除大气污染物NO和CO,简化中间反应进程后,相对能量变化如图所示。已知CO(g)的燃烧热∆H =
2
-283 kJ·mol-1,则2NO(g)=2N (g) + O(g)的反应热∆H (kJ·mol-1)为( )
2 2 2
资料整理【淘宝店铺:向阳百分百】A.-152 B.-76 C.+76 D.+152
【答案】A
【解析】已知CO(g)的燃烧热∆H = -283 kJ·mol-1,可得 ①,
由图可得NO(g)+CO(g)=N (g)+CO (g) ∆H=-330+123-229+77=-359kJ/mol②,由盖斯定律,(反应②-①)×2
2 2 2
可得反应2NO(g)=2N (g) + O(g),反应热∆H =( -359+283)×2 =-152kJ·mol-1,故选A。
2 2 2
5.(2023·重庆一中高三质检)一定温度圧强下,CH-CH=CH(g)与HCl(g)反应可以生成CHCHClCH (g)
3 2 3 3
和CHCHCHCl(g),反应中的能量变化如图所示。下列说法不正确的是( )
3 2 2
A.生成CHCHCHCl(g)的反应中,第一步为反应的决速步
3 2 2
B.短时间内,CHCHClCH (g)是主产物
3 3
C.升高温度达平衡时,可以提高产物中CHCHCHCl(g)的比例
3 2 2
D.CH-CH=CH(g)+HCl(g) CHCHCHCl(g)的焓变等于第一步与第二步正反应活化能的差值
3 2 3 2 2
【答案】D
【解析】A项, 生成CHCHCHCl(g)的反应中,第一步反应活化能高,是决速步,故A正确;B项,
3 2 2
短时间内,生成CHCHClCH (g)的反应活化能低,反应速率快,因此CHCHClCH (g)是主产物,故B正确;
3 3 3 3
C项,CHCHClCH (g) CHCHCHCl(g) ΔH>0,升高温度有利于平衡正向移动,可以提高产物中
3 3 3 2 2
CHCHCHCl(g)的比例,故C正确;D项,CH-CH=CH(g)+HCl(g) CHCHCHCl(g)的焓变等于第一
3 2 2 3 2 3 2 2
步与第二步反应的ΔH的代数和,故D错误;故选D。
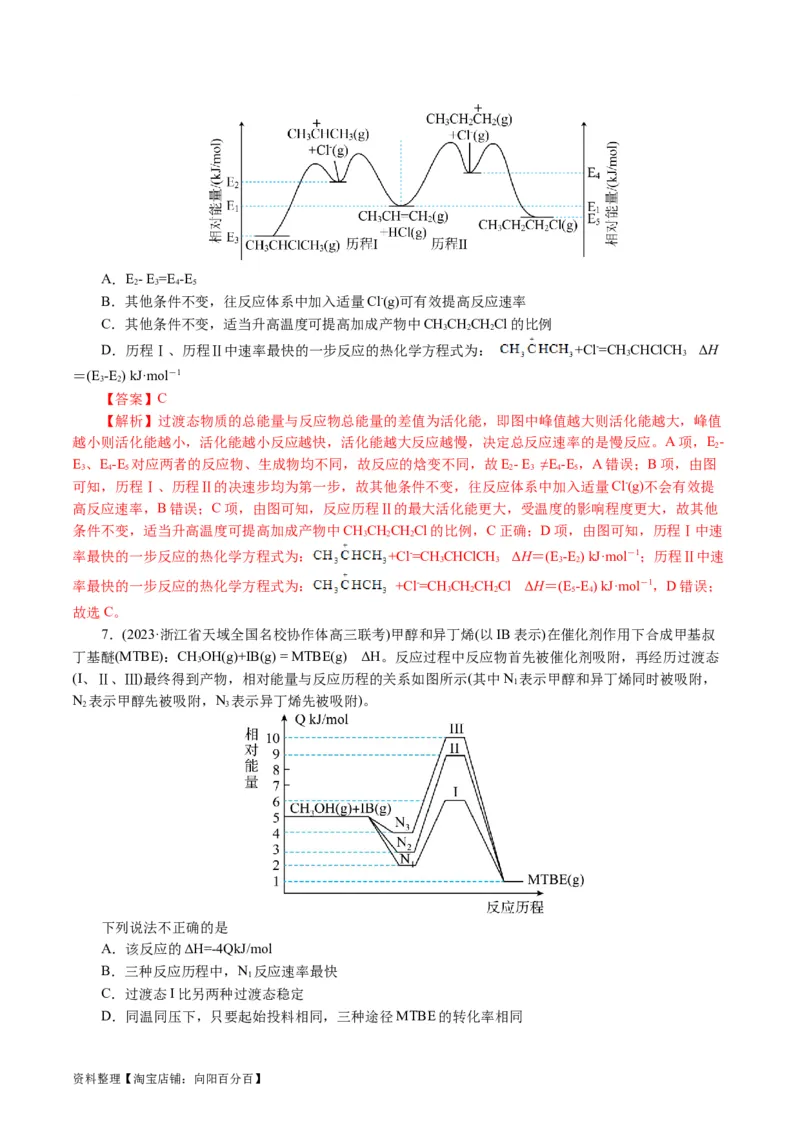
6.(2023·浙江省重点中学拔尖学生培养联盟适应性考试)标准状态下,CH=CHCH(g)与HCl(g)反应生
2 3
成 (g)和CHCHCHCl (g)的反应历程与相对能量的示意图如下。下列说法正确的是( )
3 2 2
资料整理【淘宝店铺:向阳百分百】A.E- E =E-E
2 3 4 5
B.其他条件不变,往反应体系中加入适量Cl-(g)可有效提高反应速率
C.其他条件不变,适当升高温度可提高加成产物中CHCHCHCl的比例
3 2 2
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为: +Cl-=CH CHClCH ΔH
3 3
=(E -E ) kJ·mol-1
3 2
【答案】C
【解析】过渡态物质的总能量与反应物总能量的差值为活化能,即图中峰值越大则活化能越大,峰值
越小则活化能越小,活化能越小反应越快,活化能越大反应越慢,决定总反应速率的是慢反应。A项,E-
2
E、E-E 对应两者的反应物、生成物均不同,故反应的焓变不同,故E- E ≠E-E ,A错误;B项,由图
3 4 5 2 3 4 5
可知,历程Ⅰ、历程Ⅱ的决速步均为第一步,故其他条件不变,往反应体系中加入适量Cl-(g)不会有效提
高反应速率,B错误;C项,由图可知,反应历程Ⅱ的最大活化能更大,受温度的影响程度更大,故其他
条件不变,适当升高温度可提高加成产物中CHCHCHCl的比例,C正确;D项,由图可知,历程Ⅰ中速
3 2 2
率最快的一步反应的热化学方程式为: +Cl-=CH CHClCH ΔH=(E -E ) kJ·mol-1;历程Ⅱ中速
3 3 3 2
率最快的一步反应的热化学方程式为: +Cl-=CH CHCHCl ΔH=(E -E ) kJ·mol-1,D错误;
3 2 2 5 4
故选C。
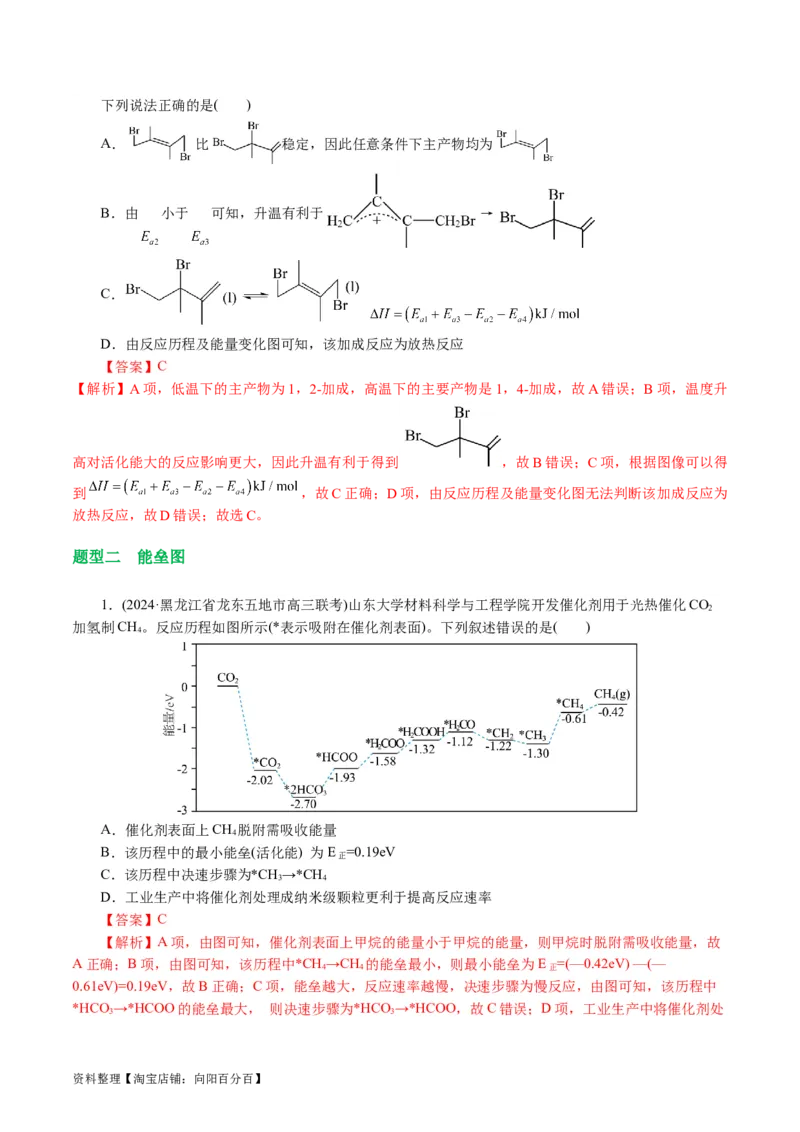
7.(2023·浙江省天域全国名校协作体高三联考)甲醇和异丁烯(以IB表示)在催化剂作用下合成甲基叔
丁基醚(MTBE):CHOH(g)+IB(g) = MTBE(g) ΔH。反应过程中反应物首先被催化剂吸附,再经历过渡态
3
(I、Ⅱ、Ⅲ)最终得到产物,相对能量与反应历程的关系如图所示(其中N 表示甲醇和异丁烯同时被吸附,
1
N 表示甲醇先被吸附,N 表示异丁烯先被吸附)。
2 3
下列说法不正确的是
A.该反应的ΔH=-4QkJ/mol
B.三种反应历程中,N 反应速率最快
1
C.过渡态I比另两种过渡态稳定
D.同温同压下,只要起始投料相同,三种途径MTBE的转化率相同
资料整理【淘宝店铺:向阳百分百】【答案】D
【解析】A项,该反应的焓变△H为生成物的总能量减去反应物的总能量,则△H=(1-5)QkJ/
mol=-4QkJ/mol, 该反应的热化学方程式为该条件下反应的热化学方程式为:CH OH(g)+IB(g) = MTBE(g)
3
ΔH=-4QkJ/mol,A正确;B项,N、N、 N 三种反应历程的活化能分别为(6-2)QkJ/mol=4 QkJ/mol、(9-
1 2 3
3)QkJ/mol=6QkJ/mol、(10-4)QkJ/mol=6QkJ/mol,则N 反应速率最快,B正确;C项,过渡态I的能量最低,
1
能量越低越稳定,故过渡态I比另两种过渡态稳定,C正确;D项,N、N、N 三种反应历程的活化能不
1 2 3
相等,则同温同压下,只有起始投料相同,相同时间三种途径MTBE的转化率不相同,D错误;故选D。
8.(2023·浙江省精诚联盟高三三模)XH和O 反应生成X或XO的能量-历程变化如图。在恒温恒容的
2
密闭容器中加入一定量的XH和O,t min时测得c(XO)<c(X),下列有关说法不正确的是( )
2 1
A.t min时容器内的压强比初始状态更大
1
B.
C.只改变反应温度,t min时可能出现c(X)<c(XO)
1
D.相同条件下,在t min (t >t)时测定,可能出现c(X)<c(XO)
2 2 1
【答案】D
【解析】由图可知XH和O 反应生成X或XO都是放热反应,相对而言生成XO的活化能更低,反应
2
速率更快,时间上要出现c(X)<c(XO)时间上要比t min 更短。A项,据图可知生成1molXO气体物质的
1
量减小生成1mol,生成1molX气体物质的量增加2mol,因为t min时测得c(XO)<c(X),所以t min时气
1 1
体总的物质的量是增大的,因此t min时容器内的压强比初始状态更大,A正确;B项,由图可知,B正
1
确;C项,XH和O 反应生成X或XO都是放热反应,相对而言生成XO的活化能更低,反应速率更快,
2
只改变反应温度,t min时可能出现c(X)<c(XO),C正确;D项,根据题干信息t min时测得c(XO)<
1 1
c(X),说明XO是动力学产物,时间上要出现c(X)<c(XO)时间上要比t min 更短,D错误;故选D。
1
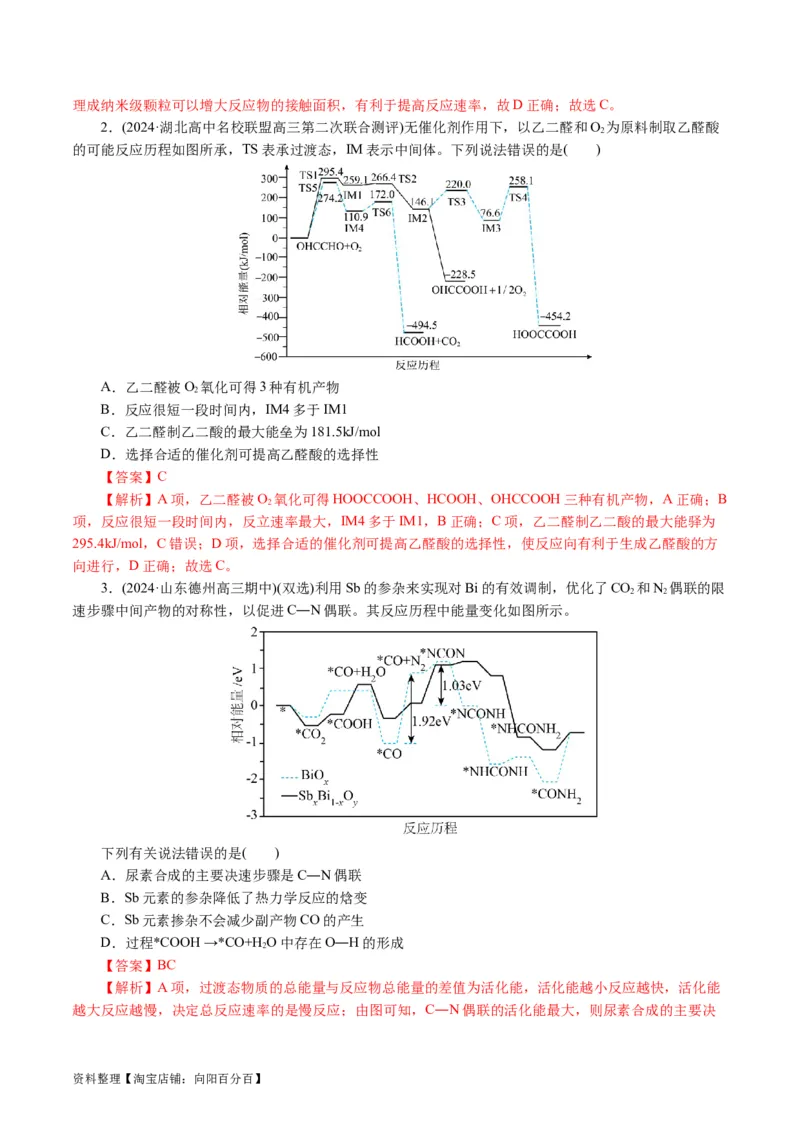
9.(2023·浙江省稽阳联谊学校高三联考)一定条件下,2,3-二甲基-1,3-丁二烯与溴单质发生液相加
成反应(1,2-加成和1,4-加成同时存在),已知体系中两种产物可通过中间产物 互相
转化,反应历程及能量变化如图所示:
资料整理【淘宝店铺:向阳百分百】下列说法正确的是( )
A. 比 稳定,因此任意条件下主产物均为
B.由 小于 可知,升温有利于 →
C.
D.由反应历程及能量变化图可知,该加成反应为放热反应
【答案】C
【解析】A项,低温下的主产物为1,2-加成,高温下的主要产物是1,4-加成,故A错误;B项,温度升
高对活化能大的反应影响更大,因此升温有利于得到 ,故B错误;C项,根据图像可以得
到 ,故C正确;D项,由反应历程及能量变化图无法判断该加成反应为
放热反应,故D错误;故选C。
题型二 能垒图
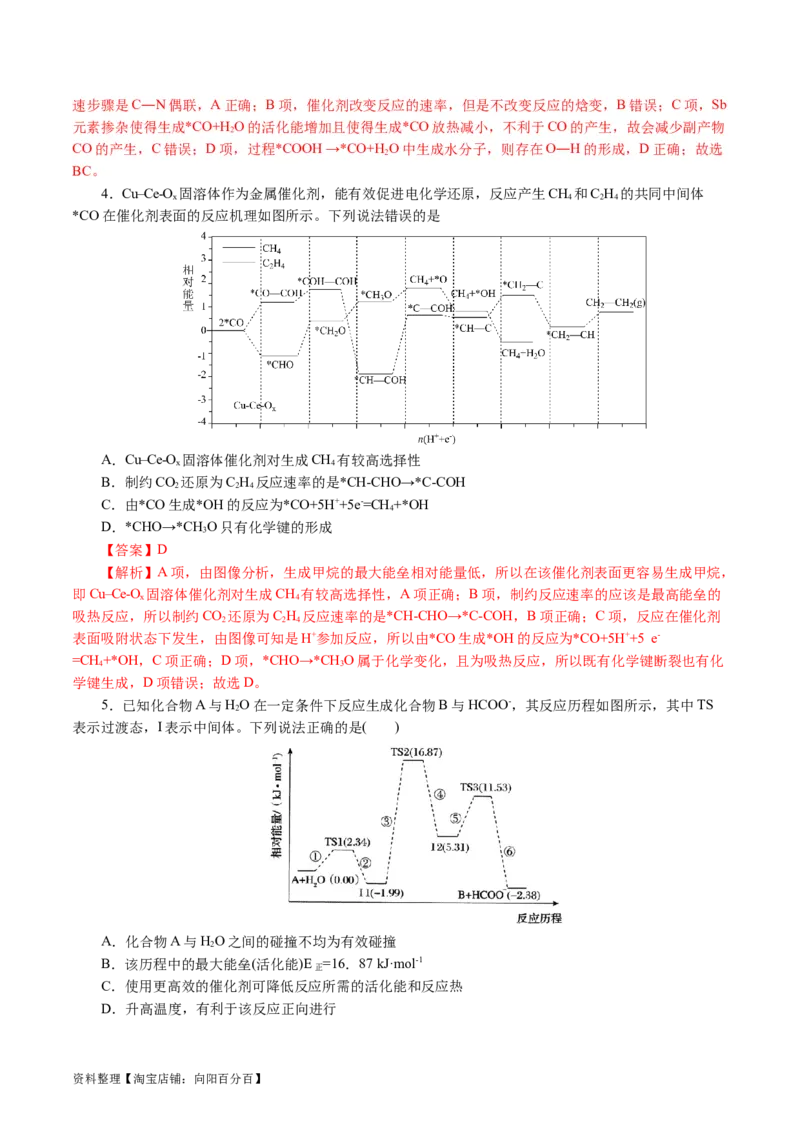
1.(2024·黑龙江省龙东五地市高三联考)山东大学材料科学与工程学院开发催化剂用于光热催化CO
2
加氢制CH。反应历程如图所示(*表示吸附在催化剂表面)。下列叙述错误的是( )
4
A.催化剂表面上CH 脱附需吸收能量
4
B.该历程中的最小能垒(活化能) 为E =0.19eV
正
C.该历程中决速步骤为*CH→*CH
3 4
D.工业生产中将催化剂处理成纳米级颗粒更利于提高反应速率
【答案】C
【解析】A项,由图可知,催化剂表面上甲烷的能量小于甲烷的能量,则甲烷时脱附需吸收能量,故
A正确;B项,由图可知,该历程中*CH→CH 的能垒最小,则最小能垒为E =(—0.42eV) —(—
4 4 正
0.61eV)=0.19eV,故B正确;C项,能垒越大,反应速率越慢,决速步骤为慢反应,由图可知,该历程中
*HCO →*HCOO的能垒最大, 则决速步骤为*HCO →*HCOO,故C错误;D项,工业生产中将催化剂处
3 3
资料整理【淘宝店铺:向阳百分百】理成纳米级颗粒可以增大反应物的接触面积,有利于提高反应速率,故D正确;故选C。
2.(2024·湖北高中名校联盟高三第二次联合测评)无催化剂作用下,以乙二醛和O 为原料制取乙醛酸
2
的可能反应历程如图所承,TS表承过渡态,IM表示中间体。下列说法错误的是( )
A.乙二醛被O 氧化可得3种有机产物
2
B.反应很短一段时间内,IM4多于IM1
C.乙二醛制乙二酸的最大能垒为181.5kJ/mol
D.选择合适的催化剂可提高乙醛酸的选择性
【答案】C
【解析】A项,乙二醛被O 氧化可得HOOCCOOH、HCOOH、OHCCOOH三种有机产物,A正确;B
2
项,反应很短一段时间内,反立速率最大,IM4多于IM1,B正确;C项,乙二醛制乙二酸的最大能驿为
295.4kJ/mol,C错误;D项,选择合适的催化剂可提高乙醛酸的选择性,使反应向有利于生成乙醛酸的方
向进行,D正确;故选C。
3.(2024·山东德州高三期中)(双选)利用Sb的参杂来实现对Bi的有效调制,优化了CO 和N 偶联的限
2 2
速步骤中间产物的对称性,以促进C―N偶联。其反应历程中能量变化如图所示。
下列有关说法错误的是( )
A.尿素合成的主要决速步骤是C―N偶联
B.Sb元素的参杂降低了热力学反应的焓变
C.Sb元素掺杂不会减少副产物CO的产生
D.过程*COOH →*CO+H O中存在O―H的形成
2
【答案】BC
【解析】A项,过渡态物质的总能量与反应物总能量的差值为活化能,活化能越小反应越快,活化能
越大反应越慢,决定总反应速率的是慢反应;由图可知,C―N偶联的活化能最大,则尿素合成的主要决
资料整理【淘宝店铺:向阳百分百】速步骤是C―N偶联,A正确;B项,催化剂改变反应的速率,但是不改变反应的焓变,B错误;C项,Sb
元素掺杂使得生成*CO+HO的活化能增加且使得生成*CO放热减小,不利于CO的产生,故会减少副产物
2
CO的产生,C错误;D项,过程*COOH →*CO+H O中生成水分子,则存在O―H的形成,D正确;故选
2
BC。
4.Cu–Ce-O 固溶体作为金属催化剂,能有效促进电化学还原,反应产生CH 和C H 的共同中间体
x 4 2 4
*CO在催化剂表面的反应机理如图所示。下列说法错误的是
A.Cu–Ce-O 固溶体催化剂对生成CH 有较高选择性
x 4
B.制约CO 还原为C H 反应速率的是*CH-CHO→*C-COH
2 2 4
C.由*CO生成*OH的反应为*CO+5H++5e-=CH +*OH
4
D.*CHO→*CH O只有化学键的形成
3
【答案】D
【解析】A项,由图像分析,生成甲烷的最大能垒相对能量低,所以在该催化剂表面更容易生成甲烷,
即Cu–Ce-O 固溶体催化剂对生成CH 有较高选择性,A项正确;B项,制约反应速率的应该是最高能垒的
x 4
吸热反应,所以制约CO 还原为C H 反应速率的是*CH-CHO→*C-COH,B项正确;C项,反应在催化剂
2 2 4
表面吸附状态下发生,由图像可知是H+参加反应,所以由*CO生成*OH的反应为*CO+5H++5 e-
=CH +*OH,C项正确;D项,*CHO→*CH O属于化学变化,且为吸热反应,所以既有化学键断裂也有化
4 3
学键生成,D项错误;故选D。
5.已知化合物A与HO在一定条件下反应生成化合物B与HCOO-,其反应历程如图所示,其中TS
2
表示过渡态,I表示中间体。下列说法正确的是( )
A.化合物A与HO之间的碰撞不均为有效碰撞
2
B.该历程中的最大能垒(活化能)E =16.87 kJ·mol-1
正
C.使用更高效的催化剂可降低反应所需的活化能和反应热
D.升高温度,有利于该反应正向进行
资料整理【淘宝店铺:向阳百分百】【答案】A
【解析】A项,根据有效碰撞理论可知,化合物A与HO之间的碰撞不均为有效碰撞,A正确;B项,
2
该历程中的最大能垒(活化能) E =16.87kJ/mol−(−1.99kJ/mol)=18.86kJ/mol,B错误;C项,使用更高
正
效的催化剂可降低反应所需的活化能,但催化剂不改变反应热,C错误;D项,由图知,化合物A与HO
2
在一定条件下反应生成化合物B与HCOO-为放热反应,升高温度,不利于该反应正向进行,D错误;故选
A。
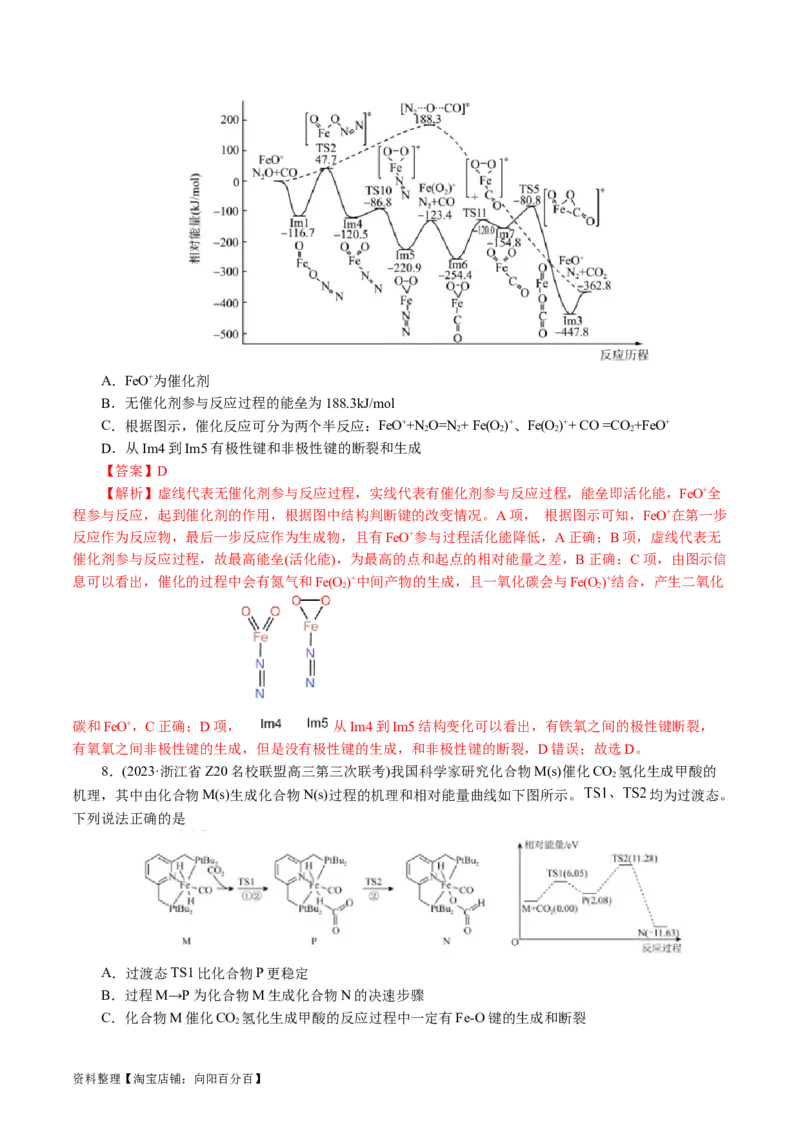
6.NO有毒,是一种大气污染物,科学家利用一种催化剂使NO在其表面分解,反应历程如图所示
(TS表示反应中的过渡态)。下列有关说法中正确的是( )。
A.NO分解的反应为吸热反应
B.3→4反应为分解反应的决速步骤
C.五种中间产物中TS5最稳定
D.催化剂能够使该反应的活化能降低,反应热减小
【答案】C
【解析】由图像可知,反应物的总能量高于生成物的总能量,NO分解的反应为放热反应,A项错误;
根据图示计算可得,历程中“5→TS4→6”的活化能最大,活化能越大,反应速率越慢,反应历程中慢反应
决定整个反应的速率,B项错误;由图像可知,中间产物TS5的能量最低,最稳定,C项正确;使用高效
催化剂,可以改变反应物的活化能,但不能影响反应热,反应热由反应物的总能量和生成物的总能量决定,
D项错误。
7.(2023·河北省部分学校高三联考)笑气(N O)是工业废气,近年发现它有很强的温室效应,在催化剂
2
下,CO还原NO是有效的去除方法,反应为CO+ N O =N +CO ,其反应历程如图。下列说法错误的是(
2 2 2 2
)
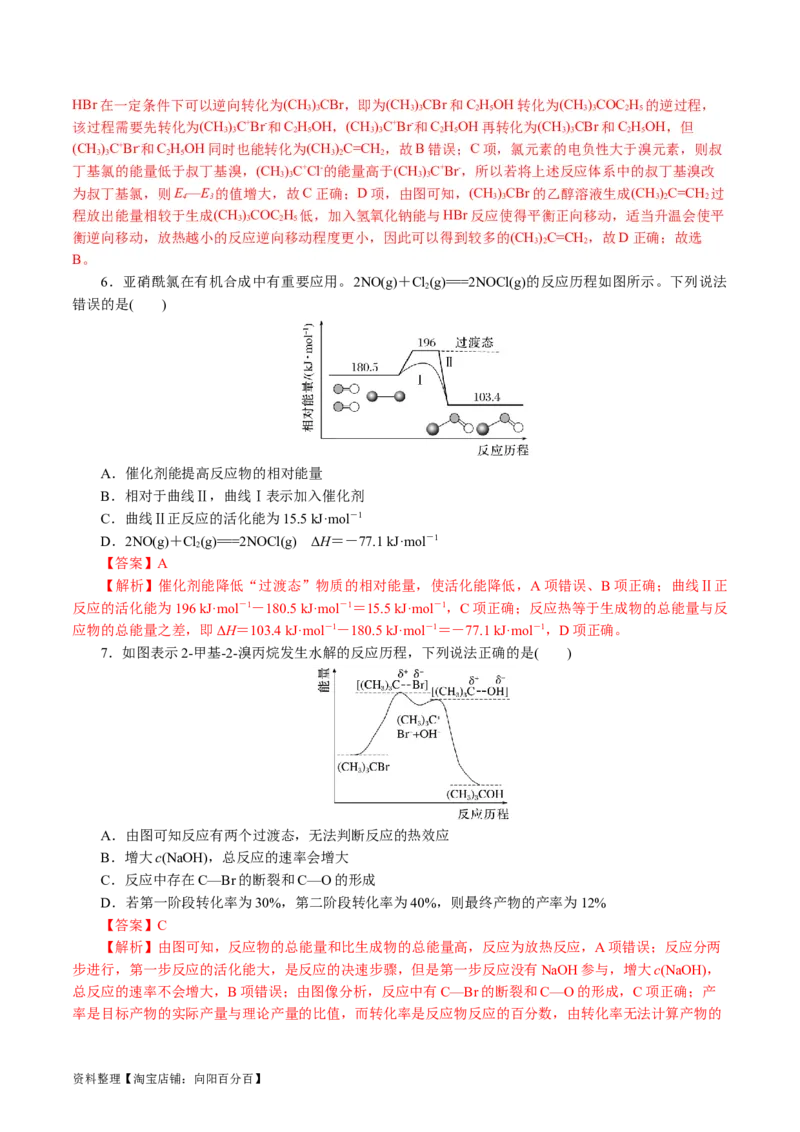
资料整理【淘宝店铺:向阳百分百】A.FeO+为催化剂
B.无催化剂参与反应过程的能垒为188.3kJ/mol
C.根据图示,催化反应可分为两个半反应:FeO++N O=N+ Fe(O )+、Fe(O )++ CO =CO +FeO+
2 2 2 2 2
D.从Im4到Im5有极性键和非极性键的断裂和生成
【答案】D
【解析】虚线代表无催化剂参与反应过程,实线代表有催化剂参与反应过程,能垒即活化能,FeO+全
程参与反应,起到催化剂的作用,根据图中结构判断键的改变情况。A项, 根据图示可知,FeO+在第一步
反应作为反应物,最后一步反应作为生成物,且有FeO+参与过程活化能降低,A正确;B项,虚线代表无
催化剂参与反应过程,故最高能垒(活化能),为最高的点和起点的相对能量之差,B正确;C项,由图示信
息可以看出,催化的过程中会有氮气和Fe(O )+中间产物的生成,且一氧化碳会与Fe(O )+结合,产生二氧化
2 2
碳和FeO+,C正确;D项, 从Im4到Im5结构变化可以看出,有铁氧之间的极性键断裂,
有氧氧之间非极性键的生成,但是没有极性键的生成,和非极性键的断裂,D错误;故选D。
8.(2023·浙江省Z20名校联盟高三第三次联考)我国科学家研究化合物M(s)催化CO 氢化生成甲酸的
2
机理,其中由化合物M(s)生成化合物N(s)过程的机理和相对能量曲线如下图所示。 均为过渡态。
下列说法正确的是
A.过渡态TS1比化合物Р更稳定
B.过程M→P为化合物M生成化合物N的决速步骤
C.化合物M催化CO 氢化生成甲酸的反应过程中一定有Fe-O键的生成和断裂
2
资料整理【淘宝店铺:向阳百分百】D.由M(s)生成N(s)的热化学方程式:M(s)+CO (g)=N(s)ΔH=-0.51kJmol-1
2
【答案】C
⋅
【解析】A项,由图可知,过渡态TS1比P能量高,则P更稳定,A错误;B项,由图可知,过程
P→TS2为两步反应中活化能较大的反应,为慢反应,即为化合物M生成化合物N的决速步骤,B错误;
C项,化合物M为催化剂,反应前后结构不会改变,比较M、N的结构可知,当Fe-O键的断裂重新连接
氢原子生成M,所以一定有Fe-O键的生成和断裂,C正确;D项,图示为一个二氧化碳分子反应过程,能
量变化为-11.63eV,所以当有1mol二氧化碳反应能量变化为-11.63eV×1.6×10-19J/
eV×6.02×1023=1.12×106J=1120kJ,则该过程的热化学方程式为:M(s)+CO (g)=N(s)ΔH=-1120kJ mol-1,D错
2
误;故选C。
⋅
题型三 过渡态能量变化图
1.(2024·河南省部分名校高三阶段性测试)电喷雾电离等方法得到的M+( 、 、 等)与O 反应
3
可得MO+,MO+与CH 反应过程中体系的能量随反应进程的变化如图所示。下列有关说法正确的是( )
4
A.CH 的二氯代物有两种 B.过渡态1比过渡态2稳定
4
C.步骤I、II均涉及极性键形成 D.CH 与MO+生成CHOH、M+的反应为吸热反应
4 3
【答案】C
【解析】A项,甲烷是空间正四面体结构,四个氢原子完全等效,其二氯代物只有一种,故A错误;
B项,能量越低,物质状态越稳定,过渡态1比过渡态2能量高,则过渡态2更稳定,故B错误;C项,
步骤I涉及形成O-H极性键,步骤II涉及C-O极性键的形成,故C正确;D项,根据反应历程能量变化
图所示CH 与MO+生成CHOH、M+的反应为放热反应,故D错误;故选C。
4 3
2.(2024·重庆沙坪坝高三期中)电喷雾电离等方法得到的M+(Fe+、Co+或Ni+等)匀O 反应可得MO+在一
3
定条件下,MO++CH =M++CH OH,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变
4 3
慢。MO+与CH 或CT 体系的能量随反应进程的变化如图所示,下列说法错误的是( )
4 4
资料整理【淘宝店铺:向阳百分百】A.该反应是放热反应
B.步骤Ⅰ和步骤Ⅱ中氢原子的成键方式均发生了变化
C.MO+与CT 反应的能量变化为曲线c
4
D.相同情况下,MO+与CHT 反应,氚代甲醇CT OH的产量大于CHT OT
3 3 2
【答案】B
【解析】A项,根据图示可知:反应物的总能量比生成物的总能量高,因此发生反应会放出热量,因
此该反应是放热反应,A正确;B项,根据图示可知:在步骤Ⅰ中C-H键变为H-O的形成;在步骤Ⅱ中涉
及O-M键的断裂和C-O键的形成,可见只有步骤Ⅰ中氢原子的成键方式发生了变化,B错误;C项,直接
参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,即反应的活化能变大,所以MO+与
CT 反应的能量变化应为图中曲线c,C正确;D项,根据题中信息可知,MO+与CH 反应时,直接参与化
4 4
学键变化的元素被替换为更重的同位素时,反应速率会变慢,则在相同情况下,产物的量会更少些,因此
MO+与CHT 反应,氚代甲醇CT OH的产量大于CHT OT,D正确;故选B。
3 3 2
3.(2024·江西赣州高三能力诊断性测试)某溴丁烷与乙醇反应的能量转化如图(“ ”表示过渡态)。下列
说法错误的是( )
A.总反应为取代反应
B.该反应过程中C原子杂化方式有变化
C.反应过程中(CH)C+是中间产物
3 3
D.决定该过程正反应快慢的步骤与逆反应快慢的步骤互为可逆反应
【答案】D
【解析】A项,该反应的总反应为(CH)CBr+C HOH (CH)COC H+HBr,属于取代反应,
3 3 2 5 3 3 2 5
A正确;B项,该反应过程中,(CH)CBr、C HOH中C原子发生sp3杂化,(CH)C+中C原子发生sp3和
3 3 2 5 3 3
sp2杂化,杂化方式有变化,B正确;C项,反应过程中共出现两种含碳中间产物,(CH)C+是其中一种中
3 3
间产物,C正确;D项,正、逆反应的决速步骤由活化能最大、反应速率最慢的反应决定,决定该过程正
反应快慢的步骤是第一步,决定逆反应快慢的步骤为第二步,二者不互为可逆反应,D错误;故选D。
4.(2023·浙江省北斗星盟高三联考)下面是丙烷(用 表示)的氯化和溴化反应时的相对能量变化图(已
知 )及产率关系。有关说法不正确的是( )
资料整理【淘宝店铺:向阳百分百】A.1molRH(g)完全生成1molRCl(g)放热1.6×10-19(a-b) J
B. 比 稳定
C.以丙烷、卤素、氢氧化钠溶液为原料制备2-丙醇,Br 优于Cl
2 2
D.溴代和氯代第一步都是决速反应
【答案】A
【解析】A项,由图可知,1个RH(g)分子转化成RCl(g)放热1.6×10-19(a-b) J,则1molRH(g)完全生成
1molRCl(g)放热N ×1.6×10-19(a-b) J,故A错误;B项,由图可知, 的能量比 低,则 比 稳定,
A
故B正确;C项,由题目信息可知,丙烷和Br 发生取代反应时相比和Cl 发生取代反应更加容易生成
2 2
CHCH(X)CH,CHCH(X)CH 在NaOH水溶液中发生水解反应可以得到2-丙醇,则以丙烷、卤素、氢氧化
2 3 2 3
钠溶液为原料制备2-丙醇,Br 优于Cl,故C正确;D项,由图可知,溴代和氯代第一步反应活化能大于
2 2
第二步,说明第一步反应速率小于第二步,则溴代和氯代第一步都是决速反应,故D正确;故选A。
5.(2023·浙江省临海、新昌两地高三适应性考试5月模考)叔丁基溴在乙醇中反应的能量变化如图所
示:
反应1:(CH)CBr→(CH)C=CH +HBr
3 3 3 2 2
反应2:C HOH+(CH )CBr→(CH)COC H+HBr
2 5 3 3 3 3 2 5
下列说法不正确的是( )
A.过渡态能量:①>②>③
B.(CH)COC H 可以逆向转化为(CH)CBr,但不会转化为(CH)C=CH
3 3 2 5 3 3 3 2 2
C.若将上述反应体系中的叔丁基溴改为叔丁基氯,则E—E 的值增大
4 3
D.向(CH)CBr的乙醇溶液中加入NaOH并适当升温,可以得到较多的(CH)C=CH
3 3 3 2 2
【答案】B
【解析】A项,由图可知,过渡态能量的大小顺序为①>②>③,故A正确;B项,(CH)COC H 与
3 3 2 5
资料整理【淘宝店铺:向阳百分百】HBr在一定条件下可以逆向转化为(CH)CBr,即为(CH)CBr和C HOH转化为(CH)COC H 的逆过程,
3 3 3 3 2 5 3 3 2 5
该过程需要先转化为(CH)C+Br-和C HOH,(CH)C+Br-和C HOH再转化为(CH)CBr和C HOH,但
3 3 2 5 3 3 2 5 3 3 2 5
(CH)C+Br-和C HOH同时也能转化为(CH)C=CH ,故B错误;C项,氯元素的电负性大于溴元素,则叔
3 3 2 5 3 2 2
丁基氯的能量低于叔丁基溴,(CH)C+Cl-的能量高于(CH)C+Br-,所以若将上述反应体系中的叔丁基溴改
3 3 3 3
为叔丁基氯,则E—E 的值增大,故C正确;D项,由图可知,(CH)CBr的乙醇溶液生成(CH)C=CH 过
4 3 3 3 3 2 2
程放出能量相较于生成(CH)COC H 低,加入氢氧化钠能与HBr反应使得平衡正向移动,适当升温会使平
3 3 2 5
衡逆向移动,放热越小的反应逆向移动程度更小,因此可以得到较多的(CH)C=CH ,故D正确;故选
3 2 2
B。
6.亚硝酰氯在有机合成中有重要应用。2NO(g)+Cl(g)===2NOCl(g)的反应历程如图所示。下列说法
2
错误的是( )
A.催化剂能提高反应物的相对能量
B.相对于曲线Ⅱ,曲线Ⅰ表示加入催化剂
C.曲线Ⅱ正反应的活化能为15.5 kJ·mol-1
D.2NO(g)+Cl(g)===2NOCl(g) ΔH=-77.1 kJ·mol-1
2
【答案】A
【解析】催化剂能降低“过渡态”物质的相对能量,使活化能降低,A项错误、B项正确;曲线Ⅱ正
反应的活化能为196 kJ·mol-1-180.5 kJ·mol-1=15.5 kJ·mol-1,C项正确;反应热等于生成物的总能量与反
应物的总能量之差,即ΔH=103.4 kJ·mol-1-180.5 kJ·mol-1=-77.1 kJ·mol-1,D项正确。
7.如图表示2-甲基-2-溴丙烷发生水解的反应历程,下列说法正确的是( )
A.由图可知反应有两个过渡态,无法判断反应的热效应
B.增大c(NaOH),总反应的速率会增大
C.反应中存在C—Br的断裂和C—O的形成
D.若第一阶段转化率为30%,第二阶段转化率为40%,则最终产物的产率为12%
【答案】C
【解析】由图可知,反应物的总能量和比生成物的总能量高,反应为放热反应,A项错误;反应分两
步进行,第一步反应的活化能大,是反应的决速步骤,但是第一步反应没有NaOH参与,增大c(NaOH),
总反应的速率不会增大,B项错误;由图像分析,反应中有C—Br的断裂和C—O的形成,C项正确;产
率是目标产物的实际产量与理论产量的比值,而转化率是反应物反应的百分数,由转化率无法计算产物的
资料整理【淘宝店铺:向阳百分百】产率,D项错误。
考点二 催化剂的催化反应机理分析
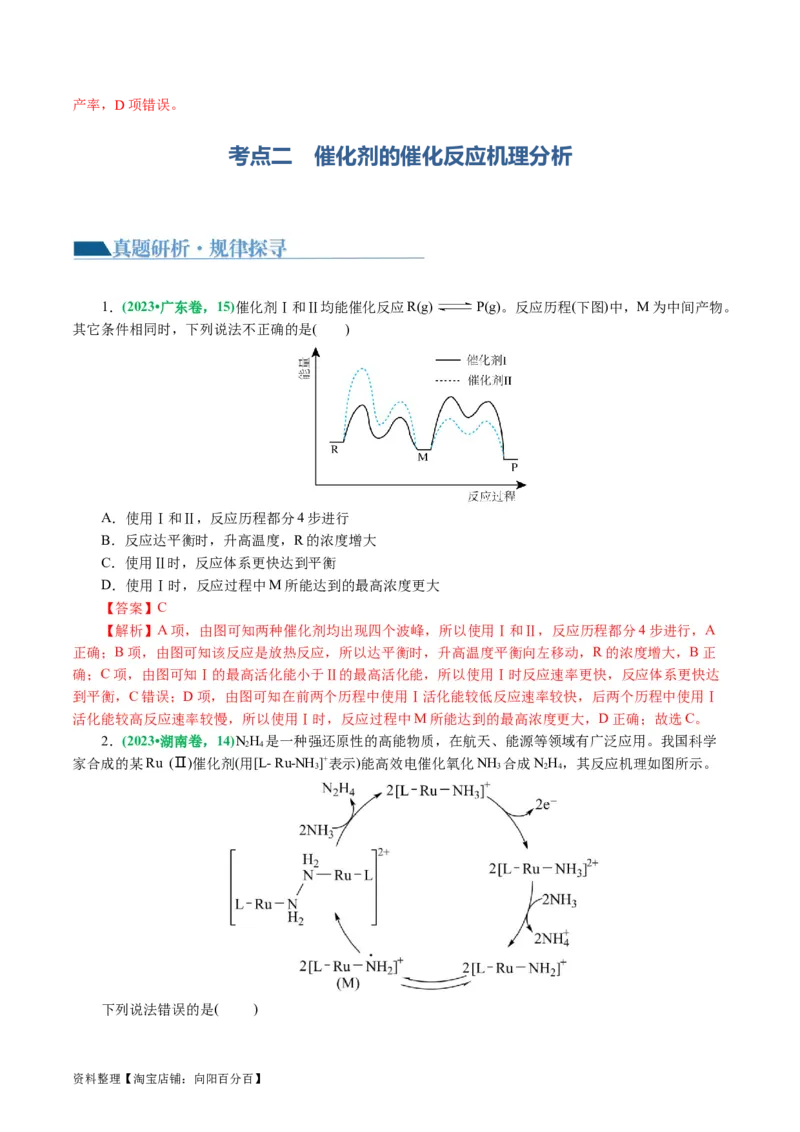
1.(2023•广东卷,15)催化剂Ⅰ和Ⅱ均能催化反应R(g) P(g)。反应历程(下图)中,M为中间产物。
其它条件相同时,下列说法不正确的是( )
A.使用Ⅰ和Ⅱ,反应历程都分4步进行
B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡
D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
【答案】C
【解析】A项,由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,A
正确;B项,由图可知该反应是放热反应,所以达平衡时,升高温度平衡向左移动,R的浓度增大,B正
确;C项,由图可知Ⅰ的最高活化能小于Ⅱ的最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达
到平衡,C错误;D项,由图可知在前两个历程中使用Ⅰ活化能较低反应速率较快,后两个历程中使用Ⅰ
活化能较高反应速率较慢,所以使用Ⅰ时,反应过程中M所能达到的最高浓度更大,D正确;故选C。
2.(2023•湖南卷,14)NH 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学
2 4
家合成的某Ru (Ⅱ)催化剂(用[L- Ru-NH ]+表示)能高效电催化氧化NH 合成NH,其反应机理如图所示。
3 3 2 4
下列说法错误的是( )
资料整理【淘宝店铺:向阳百分百】A.Ru (Ⅱ)被氧化至Ru (Ⅲ)后,配体NH 失去质子能力增强
3
B.M中Ru的化合价为
C.该过程有非极性键的形成
D.该过程的总反应式:4NH -2e- =N H+2NH+
3 2 4 4
【答案】B
【解析】A项,Ru (Ⅱ)被氧化至Ru (Ⅲ)后,[L- Ru-NH ]2+中的Ru带有更多的正电荷,其与N原子成
3
键后,Ru吸引电子的能力比Ru (Ⅱ)强,这种作用使得配体NH 中的N-H键极性变强且更易断裂,因此其
3
失去质子(H+)的能力增强,A正确;B项,Ru (Ⅱ)中Ru的化合价为+2,当其变为Ru (Ⅲ)后,Ru的化合价
变为+3,Ru (Ⅲ)失去2个质子后,N原子产生了1个孤电子对,Ru的化合价不变;M为 ,
当[L- Ru-NH ]+变为M时,N原子的孤电子对拆为2个电子并转移给Ru 1个电子,其中Ru的化合价变为
2
+2,因此,B不正确;C项,该过程M变为[L-Ru-NH -NH - Ru-L]2+时,有N-N键形成,N-N是非极性键,
2 2
C正确;D项,从整个过程来看, 4个NH 失去了2个电子后生成了1个NH 和2个NH +,Ru (Ⅱ)是催
3 2 4 4
化剂,因此,该过程的总反应式为4NH -2e- =N H+2NH+,D正确;故选B。
3 2 4 4
3.(2023•全国新课标卷,12) “肼合成酶”以其中的Fe2+配合物为催化中心,可将NH OH与NH 转化
2 3
为肼(NH NH ),其反应历程如下所示。
2 2
下列说法错误的是( )
A.NH OH、NH 和HO均为极性分子
2 3 2
B.反应涉及 、 键断裂和 键生成
C.催化中心的Fe2+被氧化为Fe3+,后又被还原为Fe2+
D.将NH OH替换为ND OD,反应可得ND ND
2 2 2 2
【答案】D
【解析】A项,NH OH,NH ,HO的电荷分布都不均匀,不对称,为极性分子,A正确;B项,由
2 3 2
反应历程可知,有N-H,N-O键断裂,还有N-H键的生成,B正确;C项,由反应历程可知,反应过
程中,Fe2+先失去电子发生氧化反应生成Fe3+,后面又得到电子生成Fe2+,C正确;D项,由反应历程可知,
反应过程中,生成的NH NH 有两个氢来源于NH ,所以将NH OH替换为ND OD,不可能得到ND ND ,
2 2 3 2 2 2 2
得到ND NH 和HDO,D错误;故选D。
.2 2
4 (2023•浙江省6月选考,14)一定条件下,1-苯基丙炔(Ph—C≡C-CH)可与HCl发生催化加成,反应
3
如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正
资料整理【淘宝店铺:向阳百分百】确的是( )
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物1
【答案】C
【解析】A项,反应I、Ⅲ为放热反应,相同物质的量的反应物,反应I放出的热量小于反应Ⅱ放出的
热量,反应放出的热量越多,其焓变越小,因此反应焓变:反应I>反应Ⅱ,故A正确;B项,短时间里反
应I得到的产物比反应Ⅱ得到的产物多,说明反应I的速率比反应Ⅱ的速率快,速率越快,其活化能越小,
则反应活化能:反应I<反应Ⅱ,故B正确;C项,增加HCl浓度,平衡正向移动,但平衡时产物Ⅱ和产物
I的比例可能降低,故C错误;D项,根据图中信息,选择相对较短的反应时间,及时分离可获得高产率
的产物1,故D正确。故选C。
5.(2022•湖南选择性考试,9)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将
海洋中的NO -转化为N 进入大气层,反应过程如图所示。
2 2
下列说法正确的是( )
A.过程Ⅰ中NO -发生氧化反应
2
B.a和b中转移的e-数目相等
C.过程Ⅱ中参与反应的n(NO):n(NH +)=1:4
4
D.过程Ⅰ→Ⅲ的总反应为NO -+NH+=N ↑+2H O
2 4 2 2
【答案】D
【解析】A项,由图示可知,过程I中NO -转化为NO,氮元素化合价由+3价降低到+2价,NO -作氧
2 2
化剂,被还原,发生还原反应,A错误;B项,由图示可知,过程I为NO -在酶1的作用下转化为NO和
2
HO,依据得失电子守恒、电荷守恒和原子守恒可知,反应的离子方程式为:NO -+2H++e- NO+H O,
2 2 2
生成1molNO,a过程转移1mole-,过程II为NO和NH +在酶2的作用下发生氧化还原反应生成HO和
4 2
NH,依据得失电子守恒、电荷守恒和原子守恒可知,反应的离子方程式为:NO+NH ++2H++3e-
2 4 4
=H O+NH,消耗1molNO,b过程转移3mol e-,转移电子数目不相等,B错误;C项,由图示可知,过程
2 2 4
II发生反应的过程为:NO+NH ++2H++3e- =H O+NH,n(NO):n(NH +)=1:1,C错误;D项,由图示可知,
4 2 2 4 4
过程Ⅰ→Ⅲ的总反应为NO -+NH+=N ↑+2H O,D正确;故选D。
2 4 2 2
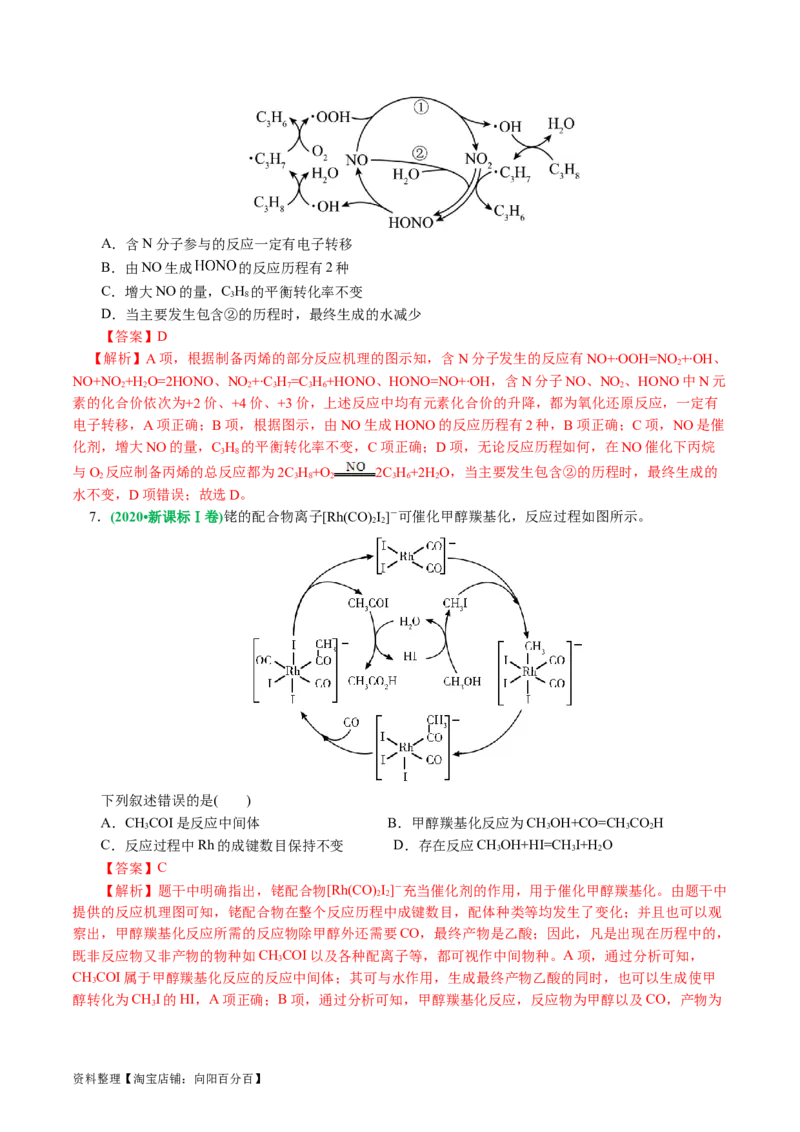
6.(2022•山东卷,10)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错
误的是( )
资料整理【淘宝店铺:向阳百分百】A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量,C H 的平衡转化率不变
3 8
D.当主要发生包含②的历程时,最终生成的水减少
【答案】D
【解析】A项,根据制备丙烯的部分反应机理的图示知,含N分子发生的反应有NO+∙OOH=NO+∙OH、
2
NO+NO +H O=2HONO、NO +∙C H=C H+HONO、HONO=NO+∙OH,含N分子NO、NO 、HONO中N元
2 2 2 3 7 3 6 2
素的化合价依次为+2价、+4价、+3价,上述反应中均有元素化合价的升降,都为氧化还原反应,一定有
电子转移,A项正确;B项,根据图示,由NO生成HONO的反应历程有2种,B项正确;C项,NO是催
化剂,增大NO的量,C H 的平衡转化率不变,C项正确;D项,无论反应历程如何,在NO催化下丙烷
3 8
与O 反应制备丙烯的总反应都为2C H+O 2C H+2H O,当主要发生包含②的历程时,最终生成的
2 3 8 2 3 6 2
水不变,D项错误;故选D。
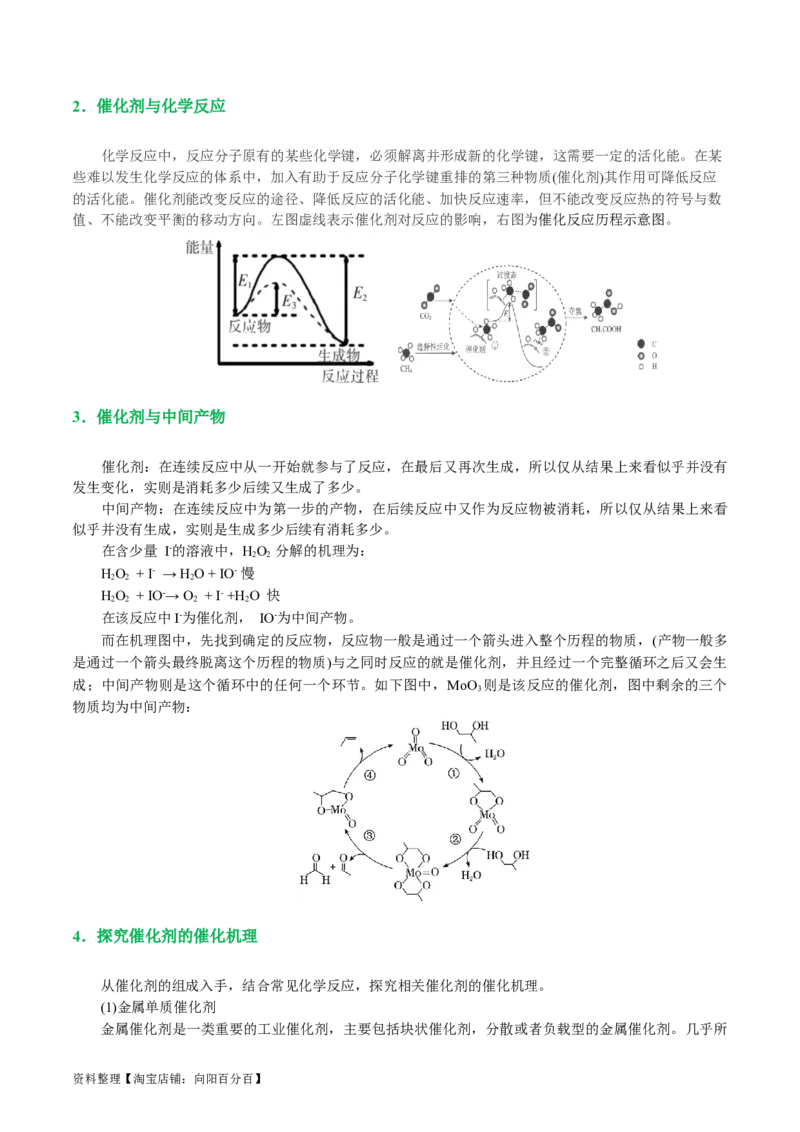
7.(2020•新课标Ⅰ卷)铑的配合物离子[Rh(CO) I]-可催化甲醇羰基化,反应过程如图所示。
2 2
下列叙述错误的是( )
A.CHCOI是反应中间体 B.甲醇羰基化反应为CHOH+CO=CH COH
3 3 3 2
C.反应过程中Rh的成键数目保持不变 D.存在反应CHOH+HI=CH I+H O
3 3 2
【答案】C
【解析】题干中明确指出,铑配合物[Rh(CO) I]-充当催化剂的作用,用于催化甲醇羰基化。由题干中
2 2
提供的反应机理图可知,铑配合物在整个反应历程中成键数目,配体种类等均发生了变化;并且也可以观
察出,甲醇羰基化反应所需的反应物除甲醇外还需要CO,最终产物是乙酸;因此,凡是出现在历程中的,
既非反应物又非产物的物种如CHCOI以及各种配离子等,都可视作中间物种。A项,通过分析可知,
3
CHCOI属于甲醇羰基化反应的反应中间体;其可与水作用,生成最终产物乙酸的同时,也可以生成使甲
3
醇转化为CHI的HI,A项正确;B项,通过分析可知,甲醇羰基化反应,反应物为甲醇以及CO,产物为
3
资料整理【淘宝店铺:向阳百分百】乙酸,方程式可写成:CHOH+CO CHCOOH,B项正确;C项,通过分析可知,铑配合物在
3
整个反应历程中,成键数目,配体种类等均发生了变化,C项不正确;D项,通过分析可知,反应中间体
CHCOI与水作用生成的HI可以使甲醇转化为CHI,方程式可写成:CHOH+ HI→CH I+H O,D项正确;
3 3 3 3 2
故选C。
1.催化反应机理的分析思维模型
第一步:分析反应目的,反应物和目标产物分清
第二步:找出各步反应历程的反应物和生成物
第三步:综合分析所有反应历程,确定总反应的反应物、生成物、中间物质,循环物质等
2.催化反应机理题的解题思路
(1)通览全图,找准一“剂”三“物”
催化剂在机理图中多数是以完整的循环出现的,以催化剂粒子为主题的多个物
一“剂”指催化剂
种一定在机理图中的主线上
反应物 通过一个箭头进入整个历程的物质一般是反应物
三“物”指反应 生成物 通过一个箭头最终脱离整个历程的物质多是产物
物、生成物、中间 通过一个箭头脱离整个历程,但又生成的是中间体,通过两个箭头进
物种(或中间体) 中间体 入整个历程的中间物质也是中间体,中间体有时在反应历程中用“[
]”标出
(2)逐项分析得答案
根据第一步由题给情境信息,找出催化剂、反应物、生成物、中间体,再结合每一选项设计的问题逐
项分析判断,选出正确答案。
1.催化剂具有的三大特征
催化剂是通过降低反应活化能,从而改变了反应的途径,此即催化剂加速化学反应的主要原因所在。
总结起来,催化剂的特征主要表现在这样几个方面:
第一,催化剂可以改变反应速率,但其自身在反应前后的组成、质量和化学性质不变。
第二,催化剂不改变化学平衡。即催化剂既能加快正向反应的速率,也能加快逆向反应的速率,从而
缩短化学反应达到平衡的时间。
第三,催化剂具有特殊的选择性,不同类型的反应,需要选择不同的催化剂。同一种反应物,使用不
同的催化剂,可以得到不同的产物。
资料整理【淘宝店铺:向阳百分百】2.催化剂与化学反应
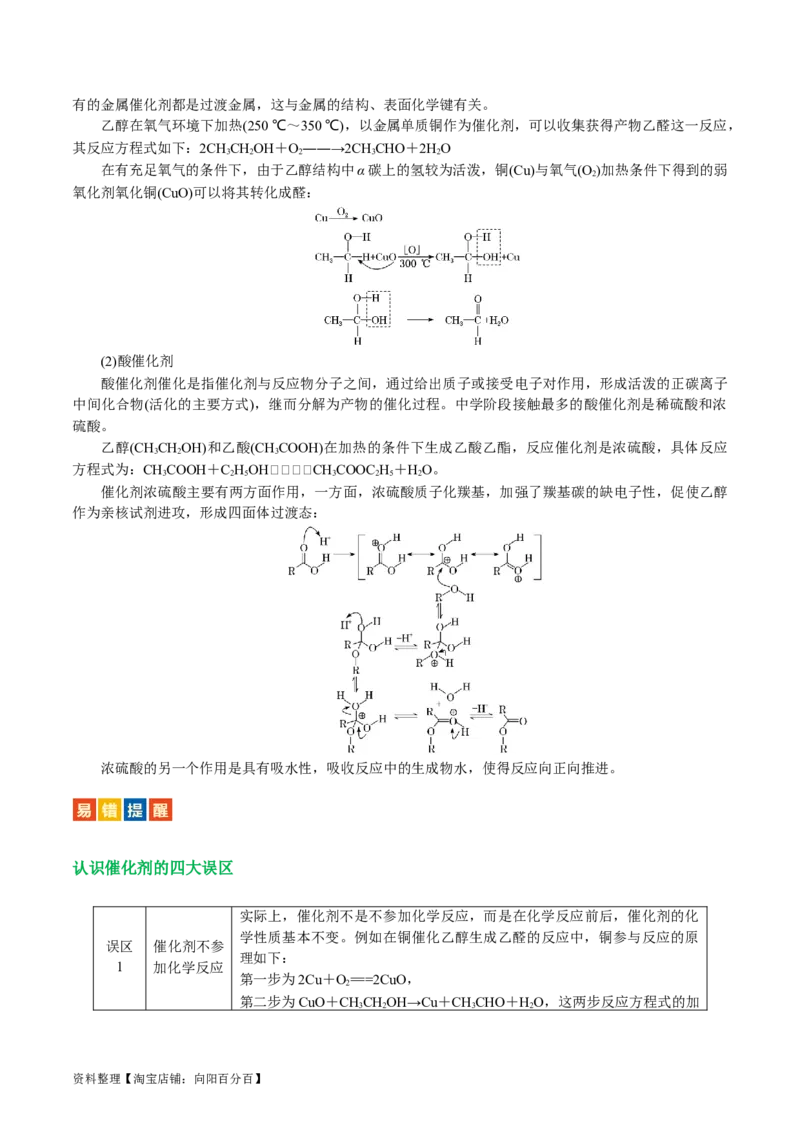
化学反应中,反应分子原有的某些化学键,必须解离并形成新的化学键,这需要一定的活化能。在某
些难以发生化学反应的体系中,加入有助于反应分子化学键重排的第三种物质(催化剂)其作用可降低反应
的活化能。催化剂能改变反应的途径、降低反应的活化能、加快反应速率,但不能改变反应热的符号与数
值、不能改变平衡的移动方向。左图虚线表示催化剂对反应的影响,右图为催化反应历程示意图。
3.催化剂与中间产物
催化剂:在连续反应中从一开始就参与了反应,在最后又再次生成,所以仅从结果上来看似乎并没有
发生变化,实则是消耗多少后续又生成了多少。
中间产物:在连续反应中为第一步的产物,在后续反应中又作为反应物被消耗,所以仅从结果上来看
似乎并没有生成,实则是生成多少后续有消耗多少。
在含少量 I-的溶液中,HO 分解的机理为:
2 2
HO + I- → H O + IO- 慢
2 2 2
HO + IO-→ O + I- +H O 快
2 2 2 2
在该反应中I-为催化剂, IO-为中间产物。
而在机理图中,先找到确定的反应物,反应物一般是通过一个箭头进入整个历程的物质,(产物一般多
是通过一个箭头最终脱离这个历程的物质)与之同时反应的就是催化剂,并且经过一个完整循环之后又会生
成;中间产物则是这个循环中的任何一个环节。如下图中,MoO 则是该反应的催化剂,图中剩余的三个
3
物质均为中间产物:
4.探究催化剂的催化机理
从催化剂的组成入手,结合常见化学反应,探究相关催化剂的催化机理。
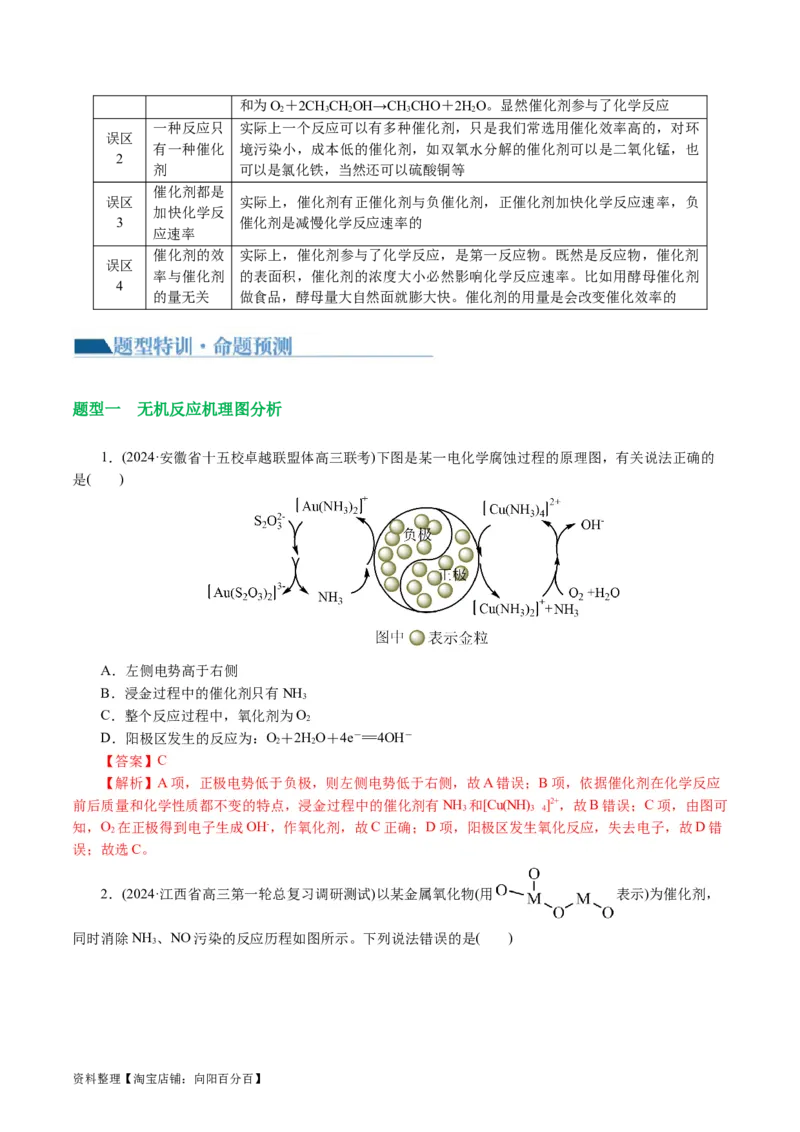
(1)金属单质催化剂
金属催化剂是一类重要的工业催化剂,主要包括块状催化剂,分散或者负载型的金属催化剂。几乎所
资料整理【淘宝店铺:向阳百分百】有的金属催化剂都是过渡金属,这与金属的结构、表面化学键有关。
乙醇在氧气环境下加热(250 ℃~350 ℃),以金属单质铜作为催化剂,可以收集获得产物乙醛这一反应,
其反应方程式如下:2CHCHOH+O――→2CHCHO+2HO
3 2 2 3 2
在有充足氧气的条件下,由于乙醇结构中α碳上的氢较为活泼,铜(Cu)与氧气(O )加热条件下得到的弱
2
氧化剂氧化铜(CuO)可以将其转化成醛:
(2)酸催化剂
酸催化剂催化是指催化剂与反应物分子之间,通过给出质子或接受电子对作用,形成活泼的正碳离子
中间化合物(活化的主要方式),继而分解为产物的催化过程。中学阶段接触最多的酸催化剂是稀硫酸和浓
硫酸。
乙醇(CHCHOH)和乙酸(CHCOOH)在加热的条件下生成乙酸乙酯,反应催化剂是浓硫酸,具体反应
3 2 3
方程式为:CHCOOH+C HOHCHCOOC H+HO。
3 2 5 3 2 5 2
催化剂浓硫酸主要有两方面作用,一方面,浓硫酸质子化羰基,加强了羰基碳的缺电子性,促使乙醇
作为亲核试剂进攻,形成四面体过渡态:
浓硫酸的另一个作用是具有吸水性,吸收反应中的生成物水,使得反应向正向推进。
认识催化剂的四大误区
实际上,催化剂不是不参加化学反应,而是在化学反应前后,催化剂的化
学性质基本不变。例如在铜催化乙醇生成乙醛的反应中,铜参与反应的原
误区 催化剂不参
理如下:
1 加化学反应
第一步为2Cu+O===2CuO,
2
第二步为CuO+CHCHOH→Cu+CHCHO+HO,这两步反应方程式的加
3 2 3 2
资料整理【淘宝店铺:向阳百分百】和为O+2CHCHOH→CH CHO+2HO。显然催化剂参与了化学反应
2 3 2 3 2
一种反应只 实际上一个反应可以有多种催化剂,只是我们常选用催化效率高的,对环
误区
有一种催化 境污染小,成本低的催化剂,如双氧水分解的催化剂可以是二氧化锰,也
2
剂 可以是氯化铁,当然还可以硫酸铜等
催化剂都是
误区 实际上,催化剂有正催化剂与负催化剂,正催化剂加快化学反应速率,负
加快化学反
3 催化剂是减慢化学反应速率的
应速率
催化剂的效 实际上,催化剂参与了化学反应,是第一反应物。既然是反应物,催化剂
误区
率与催化剂 的表面积,催化剂的浓度大小必然影响化学反应速率。比如用酵母催化剂
4
的量无关 做食品,酵母量大自然面就膨大快。催化剂的用量是会改变催化效率的
题型一 无机反应机理图分析
1.(2024·安徽省十五校卓越联盟体高三联考)下图是某一电化学腐蚀过程的原理图,有关说法正确的
是( )
A.左侧电势高于右侧
B.浸金过程中的催化剂只有NH
3
C.整个反应过程中,氧化剂为O
2
D.阳极区发生的反应为:O+2HO+4e-=4OH-
2 2
【答案】C
【解析】A项,正极电势低于负极,则左侧电势低于右侧,故A错误;B项,依据催化剂在化学反应
前后质量和化学性质都不变的特点,浸金过程中的催化剂有NH 和[Cu(NH) ]2+,故B错误;C项,由图可
3 3 4
知,O 在正极得到电子生成OH-,作氧化剂,故C正确;D项,阳极区发生氧化反应,失去电子,故D错
2
误;故选C。
2.(2024·江西省高三第一轮总复习调研测试)以某金属氧化物(用 表示)为催化剂,
同时消除NH 、NO污染的反应历程如图所示。下列说法错误的是( )
3
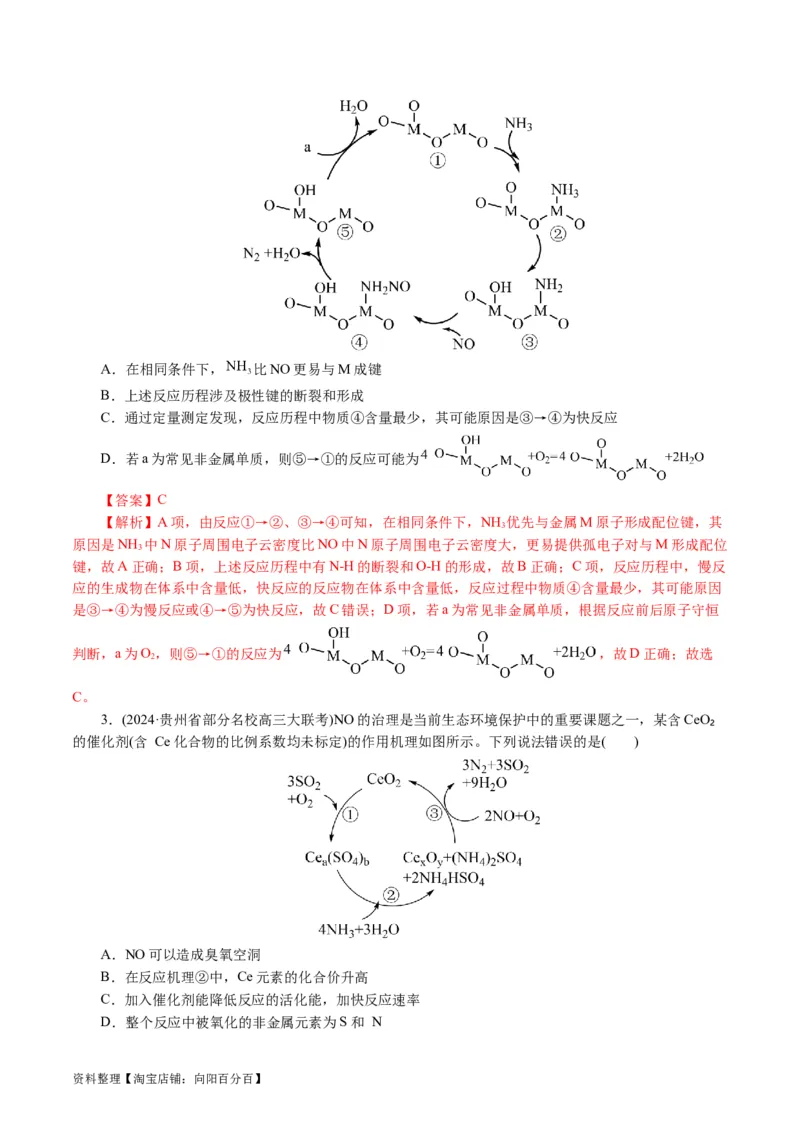
资料整理【淘宝店铺:向阳百分百】A.在相同条件下, 比NO更易与M成键
B.上述反应历程涉及极性键的断裂和形成
C.通过定量测定发现,反应历程中物质④含量最少,其可能原因是③→④为快反应
D.若a为常见非金属单质,则⑤→①的反应可能为
【答案】C
【解析】A项,由反应①→②、③→④可知,在相同条件下,NH 优先与金属M原子形成配位键,其
3
原因是NH 中N原子周围电子云密度比NO中N原子周围电子云密度大,更易提供孤电子对与M形成配位
3
键,故A正确;B项,上述反应历程中有N-H的断裂和O-H的形成,故B正确;C项,反应历程中,慢反
应的生成物在体系中含量低,快反应的反应物在体系中含量低,反应过程中物质④含量最少,其可能原因
是③→④为慢反应或④→⑤为快反应,故C错误;D项,若a为常见非金属单质,根据反应前后原子守恒
判断,a为O,则⑤→①的反应为 ,故D正确;故选
2
C。
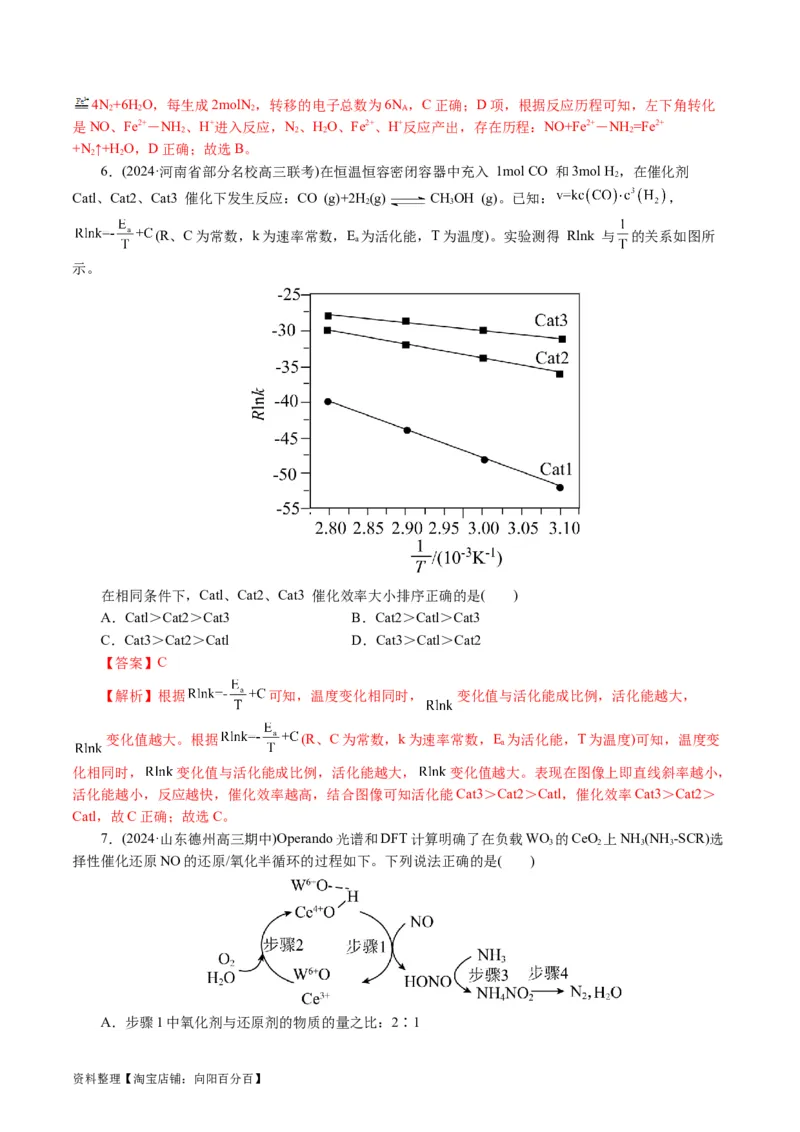
3.(2024·贵州省部分名校高三大联考)NO的治理是当前生态环境保护中的重要课题之一,某含CeO₂
的催化剂(含 Ce化合物的比例系数均未标定)的作用机理如图所示。下列说法错误的是( )
A.NO可以造成臭氧空洞
B.在反应机理②中,Ce元素的化合价升高
C.加入催化剂能降低反应的活化能,加快反应速率
D.整个反应中被氧化的非金属元素为S和 N
资料整理【淘宝店铺:向阳百分百】【答案】B
【解析】A项,NO具有还原性、臭氧具有氧化性,两者可以反应造成臭氧空洞,A正确;B项,在反
应机理②中,硫、氧、氮、氢元素化合价没有改变,则Ce元素的化合价也不会改变,B错误;C项,加入
催化剂能降低反应的活化能,加快反应速率,C正确;D项,由图可知整个反应中化合价升高被氧化的非
金属元素为S和N,D正确;故选B。
4.(2024·江苏徐州高三期中)Na SO- Co O 可作为光催化水生产物质X的高效催化剂,反应部分机理
2 2 8 3 4
如题图所示。下列说法正确的是( )
A.Co元素位于元素周期表IB族
B.在激光作用下,NaSO 发生氧化反应
2 2 8
C.物质X为H
2
D.工业上煅烧CoCO 制备Co O 的反应:CoCO+O 2Co O+6CO
3 3 4 3 2 3 4 2
【答案】D
【解析】根据图示,过程Ⅰ中,SO2-与Co O 反应生成SO 2-和Co3+,过程Ⅱ中Co3+转化为Co4+,过程
2 8 3 4 4
Ⅲ,Co4+与HO生成Co O 与O。A项,Co为27号元素,位于元素周期表第四周期第Ⅷ族,A错误;B项,
2 3 4 2
NaSO 中硫的化合价为+6,Na为+1价,则正价总数为14,所以负价总数为14,含有1个过氧键(-O-
2 2 8
O-),则NaSO 发生还原反应,B错误;C项,Co4+化合价降低发生还原反应生成Co O,3Co4+
2 2 8 3 4
+6H O=Co O+O ↑+12H+,则X为氧气,C错误;D项,煅烧CoCO 制备 Co O,根据原子守恒,
2 3 4 2 3 3 4
CoCO+O 2Co O+6CO ,D正确;故选D。
3 2 3 4 2
5.(2024·四川遂宁高三理综合测试)保护环境工作常常涉及到含氮化合物的治理,某研究发现NH 与
3
NO的反应历程如图所示,下列说法错误的( )
A.该反应历程中形成了非极性键和极性键
B.Fe2+能降低总反应的活化能,提高反应速率
C.每生成2molN ,转移的电子总数为6N
2 A
D.该反应历程中存在:NO+Fe2+-NH =Fe2++N ↑+H O
2 2 2
【答案】B
【解析】A项,该反应的化学方程式为4NH +4NO+O 4N+6H O,因此历程中形成了非极性键N≡N
3 2 2 2
和极性键H-O,A正确;B项,由图可知: Fe3+开始参与反应,最后又重新生成,因此Fe3+在该反应中作为
催化剂,能够降低总反应的活化能,提高反应速率,B错误;C项,该反应的化学方程式为4NH +4NO+O
3 2
资料整理【淘宝店铺:向阳百分百】4N+6H O,每生成2molN ,转移的电子总数为6N ,C正确;D项,根据反应历程可知,左下角转化
2 2 2 A
是NO、Fe2+-NH 、H+进入反应,N、HO、Fe2+、H+反应产出,存在历程:NO+Fe2+-NH =Fe2+
2 2 2 2
+N ↑+H O,D正确;故选B。
2 2
6.(2024·河南省部分名校高三联考)在恒温恒容密闭容器中充入 1mol CO 和3mol H,在催化剂
2
Catl、Cat2、Cat3 催化下发生反应:CO (g)+2H(g) CHOH (g)。已知: ,
2 3
(R、C为常数,k为速率常数,E 为活化能,T为温度)。实验测得 Rlnk 与 的关系如图所
a
示。
在相同条件下,Catl、Cat2、Cat3 催化效率大小排序正确的是( )
A.Catl>Cat2>Cat3 B.Cat2>Catl>Cat3
C.Cat3>Cat2>Catl D.Cat3>Catl>Cat2
【答案】C
【解析】根据 可知,温度变化相同时, 变化值与活化能成比例,活化能越大,
变化值越大。根据 (R、C为常数,k为速率常数,E 为活化能,T为温度)可知,温度变
a
化相同时, 变化值与活化能成比例,活化能越大, 变化值越大。表现在图像上即直线斜率越小,
活化能越小,反应越快,催化效率越高,结合图像可知活化能Cat3>Cat2>Catl,催化效率Cat3>Cat2>
Catl,故C正确;故选C。
7.(2024·山东德州高三期中)Operando光谱和DFT计算明确了在负载WO 的CeO 上NH (NH -SCR)选
3 2 3 3
择性催化还原NO的还原/氧化半循环的过程如下。下列说法正确的是( )
A.步骤1中氧化剂与还原剂的物质的量之比:2∶1
资料整理【淘宝店铺:向阳百分百】B.氧化性强弱顺序: CeO>O>NO
2 2
C.每生成1molN 理论上消耗0.25molO
2 2
D.上述过程的总反应方程式:6NO+ 4NH =5N +6H O
3 2 2
【答案】C
【解析】A项,由题干反应历程图可知,步骤1中反应方程式为: +NO=HONO+Ce3+
+W6+O,故氧化剂与还原剂的物质的量之比:1∶1,A错误;B项,由题干反应历程图步骤2反应可知,
O 为氧化剂,CeO 为氧化产物,故氧化性强弱顺序:O>CeO>NO,B错误;C项,由题干反应历程图
2 2 2 2
可知,上述过程的总反应方程式为:4NO+O +4NH=4N +6H O,故每生成1molN 理论上消耗0.25molO,
2 3 2 2 2 2
C正确;D项,由C项分析可知,上述过程的总反应方程式:4NO+O +4NH=4N +6H O,D错误;故选
2 3 2 2
C。
8.(2022·山东省烟台市、德州市高三一模)H 在石墨烯负载型Pd单原子催化剂(Pd/SVG)上还原NO生成
2
N 和NH 的路径机理及活化能(kJ·mol-1)如图所示。下列说法错误的是( )
2 3
A.H 还原NO生成N 的决速步为反应⑥
2 2
B.Pd/SVG上H 还原NO,更容易生成NH
2 3
C.根据如图数据可计算NO+5H===NH+HO的ΔH
3 2
D.由图可知,相同催化剂条件下反应可能存在多种反应历程
【答案】C
【解析】活化能最大的基元反应为决速步,则H 还原NO生成N 的决速步为反应⑥,A正确;由图知,
2 2
Pd/SVG上H 还原NO,经过①到⑤步即可生成氨气,经过①到⑧步才能生成氮气,而决速步反应⑥的活
2
化能最大,发生最困难,则更容易生成NH ,B正确;根据如图数据可计算NO+5H===NH +HO的正反
3 3 2
应的活化能,不知道逆反应的活化能,故不能计算ΔH,C不正确;由图可知,相同催化剂条件下反应可能
存在多种反应历程,可能得到不同产物,D正确。
9.硼氢化钠(NaBH )可用作还原剂和塑料发泡剂。如图为它在催化剂作用下与水反应制取氢气的微观过
4
程示意图,下列说法不正确的是( )
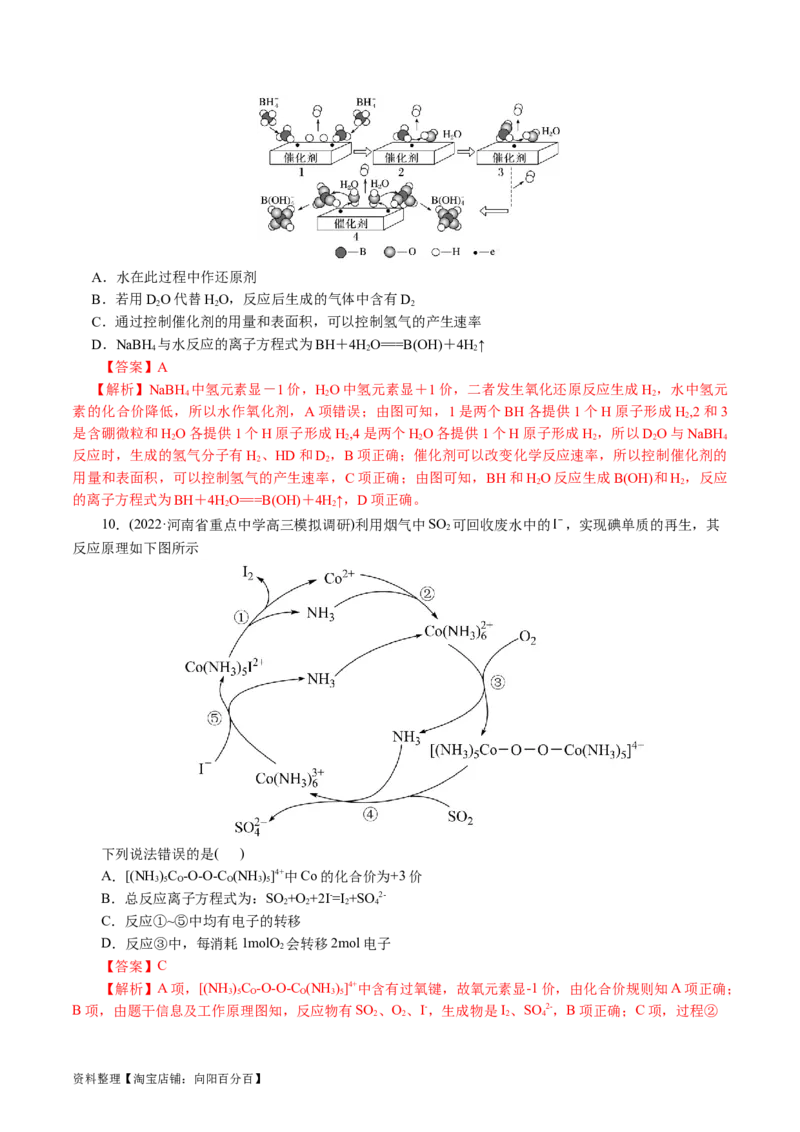
资料整理【淘宝店铺:向阳百分百】A.水在此过程中作还原剂
B.若用DO代替HO,反应后生成的气体中含有D
2 2 2
C.通过控制催化剂的用量和表面积,可以控制氢气的产生速率
D.NaBH 与水反应的离子方程式为BH+4HO===B(OH)+4H↑
4 2 2
【答案】A
【解析】NaBH 中氢元素显-1价,HO中氢元素显+1价,二者发生氧化还原反应生成H ,水中氢元
4 2 2
素的化合价降低,所以水作氧化剂,A项错误;由图可知,1是两个BH各提供1个H原子形成H,2和3
2
是含硼微粒和HO各提供1个H原子形成H,4是两个HO各提供1个H原子形成H ,所以DO与NaBH
2 2 2 2 2 4
反应时,生成的氢气分子有H 、HD和D ,B项正确;催化剂可以改变化学反应速率,所以控制催化剂的
2 2
用量和表面积,可以控制氢气的产生速率,C项正确;由图可知,BH和HO反应生成B(OH)和H ,反应
2 2
的离子方程式为BH+4HO===B(OH)+4H↑,D项正确。
2 2
10.(2022·河南省重点中学高三模拟调研)利用烟气中SO 可回收废水中的 ,实现碘单质的再生,其
2
反应原理如下图所示
下列说法错误的是( )
A.[(NH )C -O-O-C (NH )]4+中Co的化合价为+3价
3 5 O O 3 5
B.总反应离子方程式为:SO +O +2I-=I +SO2-
2 2 2 4
C.反应①~⑤中均有电子的转移
D.反应③中,每消耗1molO 会转移2mol电子
2
【答案】C
【解析】A项,[(NH )C -O-O-C (NH )]4+中含有过氧键,故氧元素显-1价,由化合价规则知A项正确;
3 5 O O 3 5
B项,由题干信息及工作原理图知,反应物有SO 、O、I-,生成物是I、SO 2-,B项正确;C项,过程②
2 2 2 4
资料整理【淘宝店铺:向阳百分百】和⑤中没有电子转移,C项错误;D项,反应③中O 得到电子后转化为过氧键,D项正确。故选C。
2
11.(2022·湖北省武汉腾云联盟高三联考)近期我国科技工作者开发了高效NO 催化净化(脱硝)催化剂,
x
实现NO 减排,其催化原理如图所示(“□”代表氧原子空位)。下列说法错误的是( )
x
A.反应过程中涉及O-H的断裂和生成
B.Ce原子的成键数目发生了改变
C.基态Ti原子价电子排布式为3d24s2
D.催化循环的总反应为4NH +6NO 5N+6H O
3 2 2
【答案】D
【解析】A项,从图中分析,催化剂表面的O与NH 中的H生成O-H键,一个O原子结合两个H生
3
成两个O-H键即以HO的形式脱离催化剂,催化剂表面两个O-H键也可断裂一个O-H生成水的同时留一
2
O在催化剂表面,反应过程中有O-H生成,也有O-H的断裂,A正确;B项,从图中分析,Ce的成键数目
有氧空位和无氧空位不同,是否与N原子成键也影响其成键数目,反应过程中Ce的成键数目发生改变,B
正确;C项,Ti是22号元素,其3d、4s能级上的电子为其价电子,这两个能级上分别含有2个电子,则
该原子价电子排布式为3d24s2,C正确;D项,从图中分析,全过程进入体系的物质有“ ”、两次的
“NH +NO”,出来的物质有“HO”、“N”、“N+ 2H O”,故催化循环的总反应为:4NH +4NO+O
3 2 2 2 2 3 2
4N+6H O,D错误;故选D。
2 2
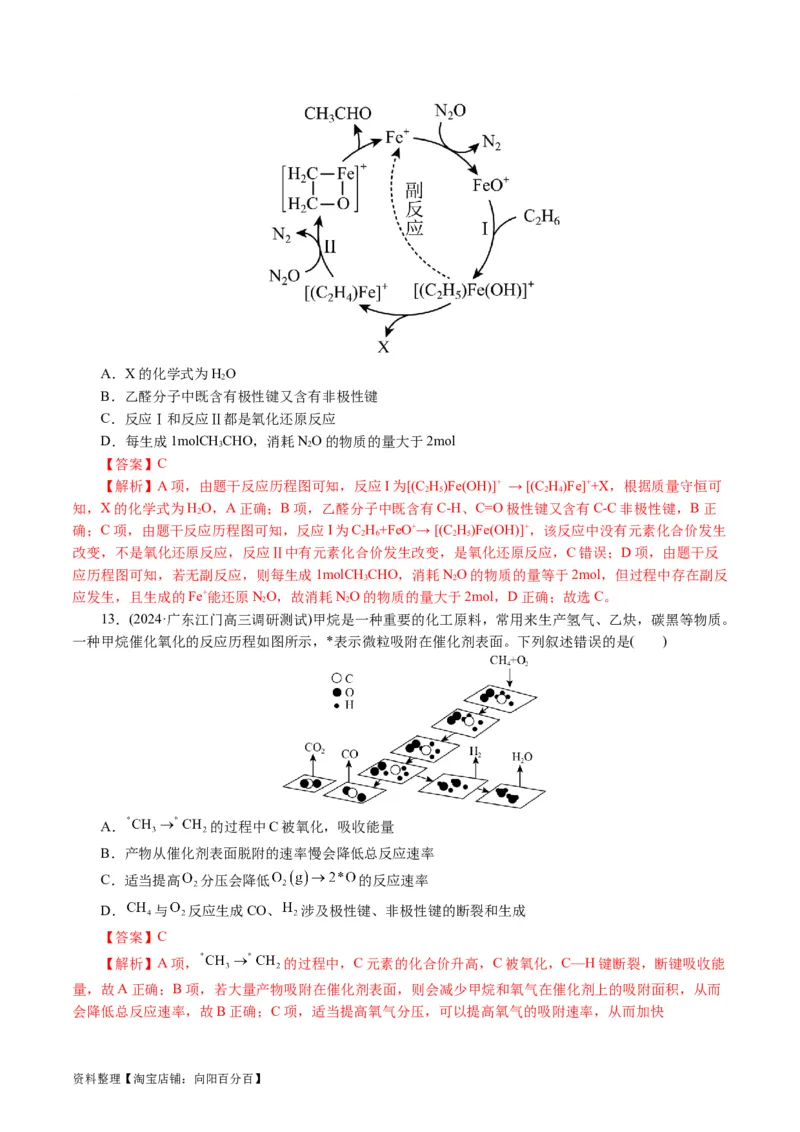
12.(2024·重庆市高三调研测试)乙烷催化氧化为乙酫在合成化学和碳资源利用等方面均有重大意义。
在Fe+催化下乙烷氧化成乙醛的机理如图所示。下列说法不正确的是( )
资料整理【淘宝店铺:向阳百分百】A.X的化学式为HO
2
B.乙醛分子中既含有极性键又含有非极性键
C.反应Ⅰ和反应Ⅱ都是氧化还原反应
D.每生成1molCH CHO,消耗NO的物质的量大于2mol
3 2
【答案】C
【解析】A项,由题干反应历程图可知,反应I为[(C H)Fe(OH)]+ → [(C H)Fe]++X,根据质量守恒可
2 5 2 4
知,X的化学式为HO,A正确;B项,乙醛分子中既含有C-H、C=O极性键又含有C-C非极性键,B正
2
确;C项,由题干反应历程图可知,反应I为C H+FeO+→ [(C H)Fe(OH)]+,该反应中没有元素化合价发生
2 6 2 5
改变,不是氧化还原反应,反应Ⅱ中有元素化合价发生改变,是氧化还原反应,C错误;D项,由题干反
应历程图可知,若无副反应,则每生成1molCH CHO,消耗NO的物质的量等于2mol,但过程中存在副反
3 2
应发生,且生成的Fe+能还原NO,故消耗NO的物质的量大于2mol,D正确;故选C。
2 2
13.(2024·广东江门高三调研测试)甲烷是一种重要的化工原料,常用来生产氢气、乙炔,碳黑等物质。
一种甲烷催化氧化的反应历程如图所示,*表示微粒吸附在催化剂表面。下列叙述错误的是( )
A. 的过程中C被氧化,吸收能量
B.产物从催化剂表面脱附的速率慢会降低总反应速率
C.适当提高 分压会降低 的反应速率
D. 与 反应生成CO、 涉及极性键、非极性键的断裂和生成
【答案】C
【解析】A项, 的过程中,C元素的化合价升高,C被氧化,C—H键断裂,断键吸收能
量,故A正确;B项,若大量产物吸附在催化剂表面,则会减少甲烷和氧气在催化剂上的吸附面积,从而
会降低总反应速率,故B正确;C项,适当提高氧气分压,可以提高氧气的吸附速率,从而加快
资料整理【淘宝店铺:向阳百分百】的反应速率,故C错误;D项,CH 与O 反应生成CO、H 涉及极性键、非极性键的断裂和
4 2 2
生成,故D正确;故选C。
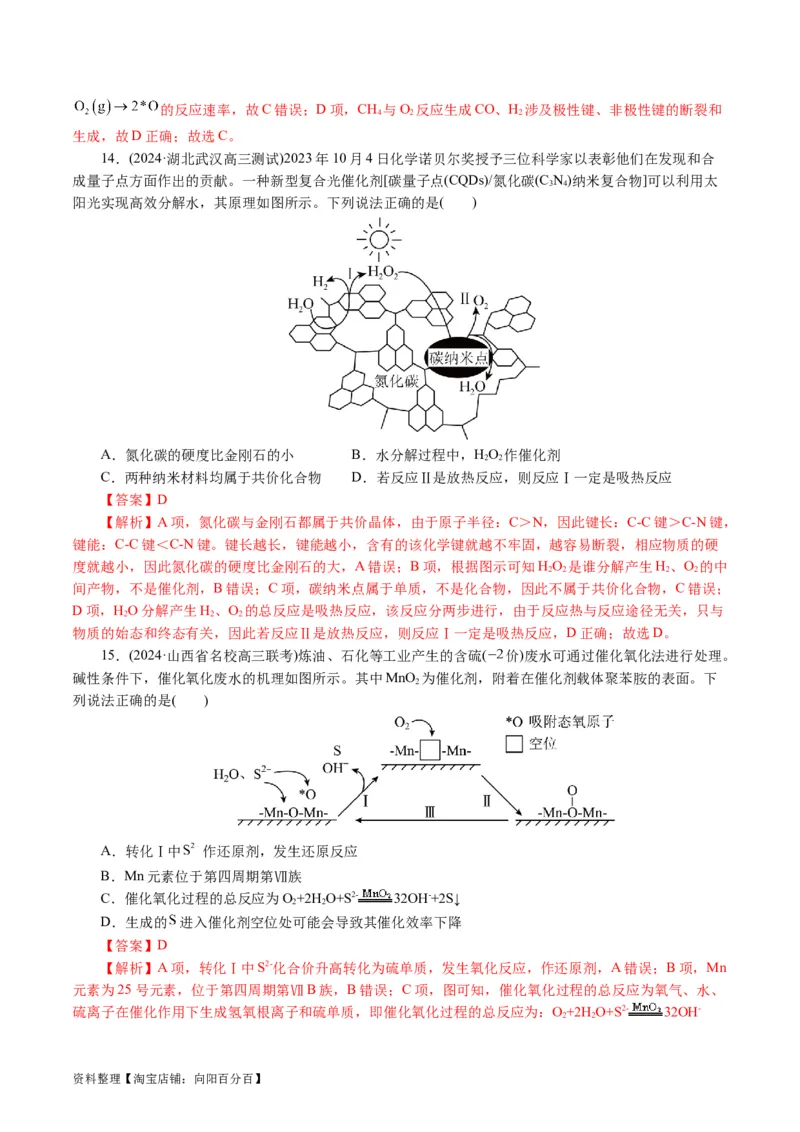
14.(2024·湖北武汉高三测试)2023年10月4日化学诺贝尔奖授予三位科学家以表彰他们在发现和合
成量子点方面作出的贡献。一种新型复合光催化剂[碳量子点(CQDs)/氮化碳(C N)纳米复合物]可以利用太
3 4
阳光实现高效分解水,其原理如图所示。下列说法正确的是( )
A.氮化碳的硬度比金刚石的小 B.水分解过程中,HO 作催化剂
2 2
C.两种纳米材料均属于共价化合物 D.若反应Ⅱ是放热反应,则反应Ⅰ一定是吸热反应
【答案】D
【解析】A项,氮化碳与金刚石都属于共价晶体,由于原子半径:C>N,因此键长:C-C键>C-N键,
键能:C-C键<C-N键。键长越长,键能越小,含有的该化学键就越不牢固,越容易断裂,相应物质的硬
度就越小,因此氮化碳的硬度比金刚石的大,A错误;B项,根据图示可知HO 是谁分解产生H、O 的中
2 2 2 2
间产物,不是催化剂,B错误;C项,碳纳米点属于单质,不是化合物,因此不属于共价化合物,C错误;
D项,HO分解产生H、O 的总反应是吸热反应,该反应分两步进行,由于反应热与反应途径无关,只与
2 2 2
物质的始态和终态有关,因此若反应Ⅱ是放热反应,则反应Ⅰ一定是吸热反应,D正确;故选D。
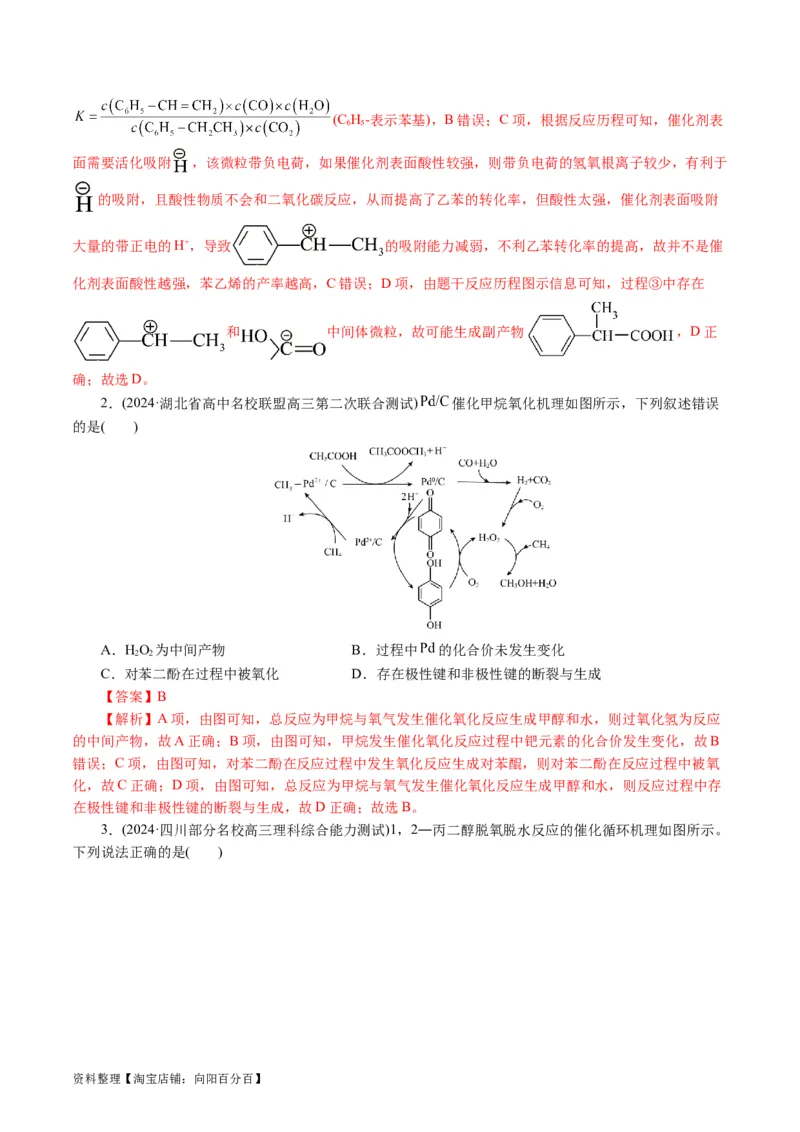
15.(2024·山西省名校高三联考)炼油、石化等工业产生的含硫( 价)废水可通过催化氧化法进行处理。
碱性条件下,催化氧化废水的机理如图所示。其中MnO 为催化剂,附着在催化剂载体聚苯胺的表面。下
2
列说法正确的是( )
A.转化Ⅰ中 作还原剂,发生还原反应
B.Mn元素位于第四周期第Ⅶ族
C.催化氧化过程的总反应为O+2H O+S2- 32OH-+2S↓
2 2
D.生成的 进入催化剂空位处可能会导致其催化效率下降
【答案】D
【解析】A项,转化Ⅰ中S2-化合价升高转化为硫单质,发生氧化反应,作还原剂,A错误;B项,Mn
元素为25号元素,位于第四周期第ⅦB族,B错误;C项,图可知,催化氧化过程的总反应为氧气、水、
硫离子在催化作用下生成氢氧根离子和硫单质,即催化氧化过程的总反应为:O+2H O+S2- 32OH-
2 2
资料整理【淘宝店铺:向阳百分百】+2S↓,C错误; D项,反应中生成硫单质,生成的S覆盖在催化剂表面或进入催化剂内空位处,阻碍了反
应的进行,导致催化剂使用一段时间后催化效率会下降,D正确;故选D。
16.(2024·河北石家庄一中高三月考)我国科技工作者以某含磷化合物作催化剂,利用光催化甲烷直接
合成甲醇的反应机理如图所示。下列说法正确的是( )
A.共价键的键长①<②
B.反应过程中CH 中氢元素被氧化
4
C.该过程催化剂中P元素的化合价发生了改变
D.该过程的总反应方程式为CH+H O→CHOH+ H
4 2 3 2
【答案】C
【解析】A项,P=O键的键长比P-O键的键长短,A错误;B项,反应过程中CH 中氢元素化合价不
4
变,B错误;C项,该过程催化剂中P元素的化合价发生了改变,C正确;D项,该过程的总反应方程式
为2CH+O →2CHOH,D错误;故选C。
4 2 3
题型二 有机反应机理图分析
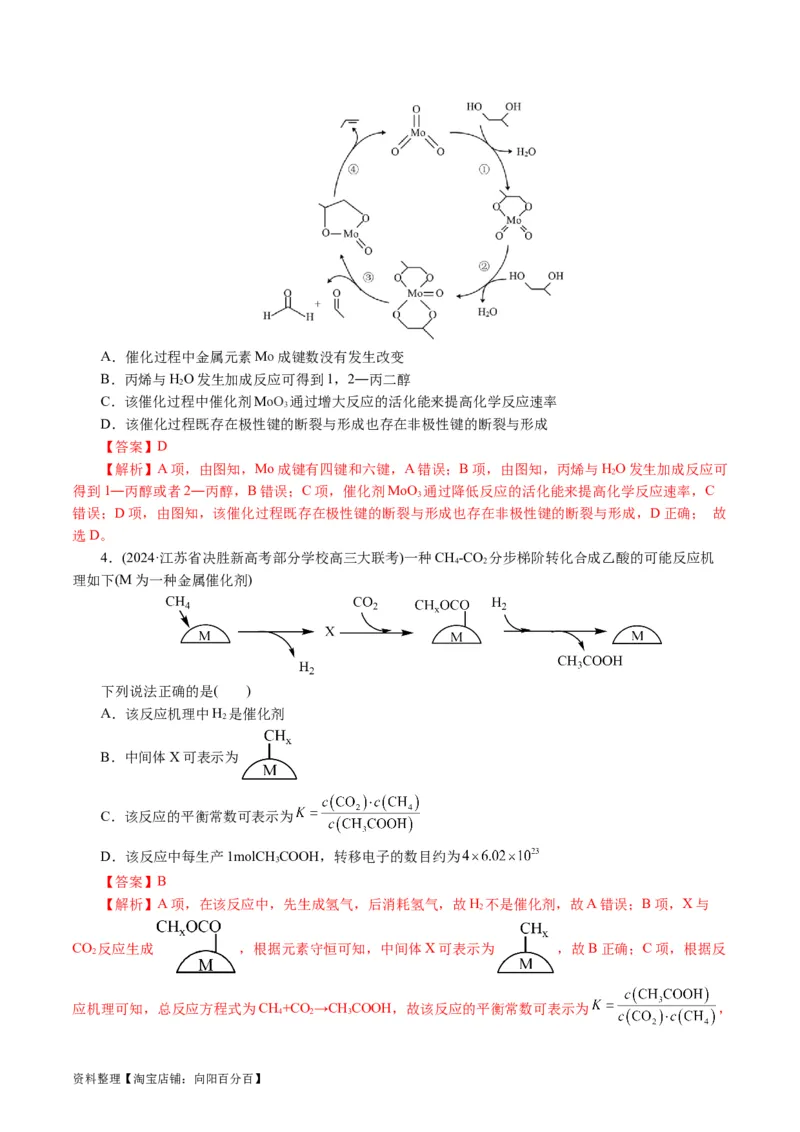
1.(2024·江苏无锡高三期中教学质量调研测试)CO 氧化乙苯脱氢制苯乙烯的反应方程式是:
2
(g)+CO (g) +H O(g)+CO(g),其反应历程如图所示。下列有关
2 2
说法正确的是( )
A.该反应的ΔS<0
B.该反应的平衡常数表达式为 ( -表示苯基)
C.催化剂表面酸性越强,苯乙烯的产率越高
D.过程③可能生成副产物
【答案】D
【解析】A项,由题干反应方程式可知,该反应正反应是一个气体体积增大的方向,故该反应的ΔS>
0,A错误;B项,由题干反应方程式可知,产物中HO为气态,故该反应的平衡常数表达式为
2
资料整理【淘宝店铺:向阳百分百】(C H-表示苯基),B错误;C项,根据反应历程可知,催化剂表
6 5
面需要活化吸附 ,该微粒带负电荷,如果催化剂表面酸性较强,则带负电荷的氢氧根离子较少,有利于
的吸附,且酸性物质不会和二氧化碳反应,从而提高了乙苯的转化率,但酸性太强,催化剂表面吸附
大量的带正电的H+,导致 的吸附能力减弱,不利乙苯转化率的提高,故并不是催
化剂表面酸性越强,苯乙烯的产率越高,C错误;D项,由题干反应历程图示信息可知,过程③中存在
和 中间体微粒,故可能生成副产物 ,D正
确;故选D。
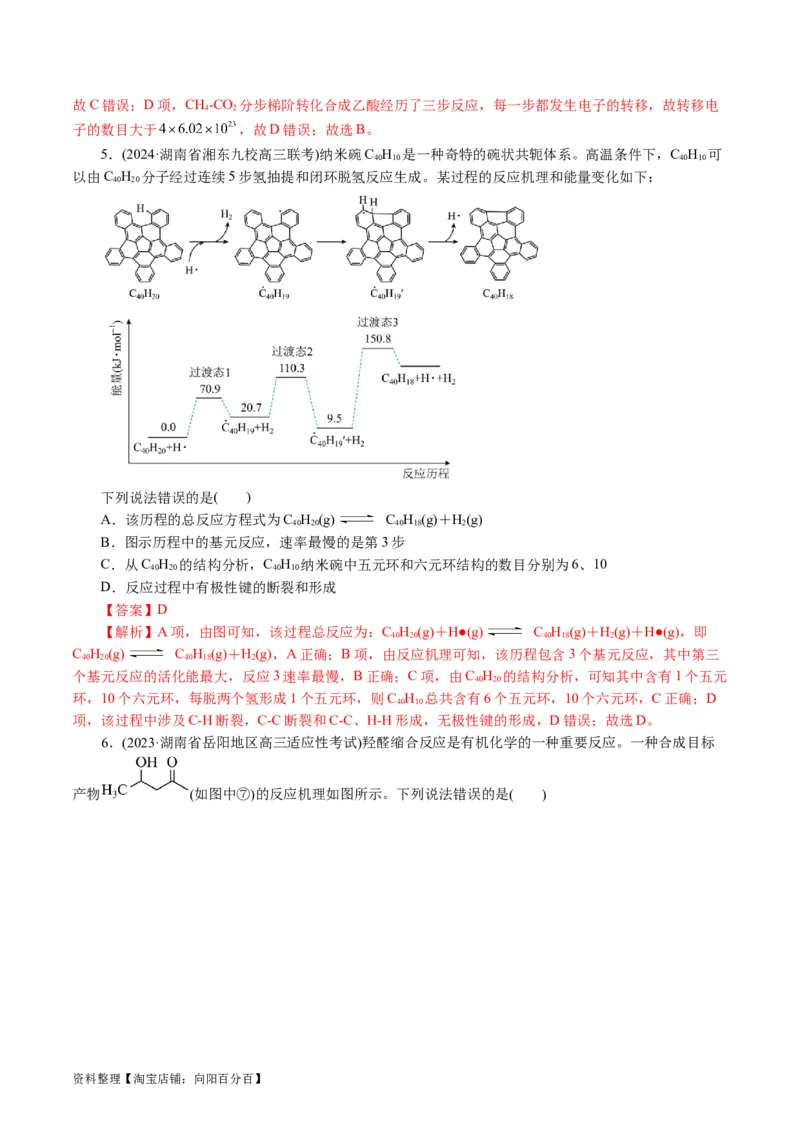
2.(2024·湖北省高中名校联盟高三第二次联合测试) 催化甲烷氧化机理如图所示,下列叙述错误
的是( )
A.HO 为中间产物 B.过程中 的化合价未发生变化
2 2
C.对苯二酚在过程中被氧化 D.存在极性键和非极性键的断裂与生成
【答案】B
【解析】A项,由图可知,总反应为甲烷与氧气发生催化氧化反应生成甲醇和水,则过氧化氢为反应
的中间产物,故A正确;B项,由图可知,甲烷发生催化氧化反应过程中钯元素的化合价发生变化,故B
错误;C项,由图可知,对苯二酚在反应过程中发生氧化反应生成对苯醌,则对苯二酚在反应过程中被氧
化,故C正确;D项,由图可知,总反应为甲烷与氧气发生催化氧化反应生成甲醇和水,则反应过程中存
在极性键和非极性键的断裂与生成,故D正确;故选B。
3.(2024·四川部分名校高三理科综合能力测试)1,2―丙二醇脱氧脱水反应的催化循环机理如图所示。
下列说法正确的是( )
资料整理【淘宝店铺:向阳百分百】A.催化过程中金属元素Mo成键数没有发生改变
B.丙烯与HO发生加成反应可得到1,2―丙二醇
2
C.该催化过程中催化剂MoO 通过增大反应的活化能来提高化学反应速率
3
D.该催化过程既存在极性键的断裂与形成也存在非极性键的断裂与形成
【答案】D
【解析】A项,由图知,Mo成键有四键和六键,A错误;B项,由图知,丙烯与HO发生加成反应可
2
得到1―丙醇或者2―丙醇,B错误;C项,催化剂MoO 通过降低反应的活化能来提高化学反应速率,C
3
错误;D项,由图知,该催化过程既存在极性键的断裂与形成也存在非极性键的断裂与形成,D正确; 故
选D。
4.(2024·江苏省决胜新高考部分学校高三大联考)一种CH-CO 分步梯阶转化合成乙酸的可能反应机
4 2
理如下(M为一种金属催化剂)
下列说法正确的是( )
A.该反应机理中H 是催化剂
2
B.中间体X可表示为
C.该反应的平衡常数可表示为
D.该反应中每生产1molCH COOH,转移电子的数目约为
3
【答案】B
【解析】A项,在该反应中,先生成氢气,后消耗氢气,故H 不是催化剂,故A错误;B项,X与
2
CO 反应生成 ,根据元素守恒可知,中间体X可表示为 ,故B正确;C项,根据反
2
应机理可知,总反应方程式为CH+CO →CHCOOH,故该反应的平衡常数可表示为 ,
4 2 3
资料整理【淘宝店铺:向阳百分百】故C错误;D项,CH-CO 分步梯阶转化合成乙酸经历了三步反应,每一步都发生电子的转移,故转移电
4 2
子的数目大于 ,故D错误;故选B。
5.(2024·湖南省湘东九校高三联考)纳米碗C H 是一种奇特的碗状共轭体系。高温条件下,C H 可
40 10 40 10
以由C H 分子经过连续5步氢抽提和闭环脱氢反应生成。某过程的反应机理和能量变化如下:
40 20
下列说法错误的是( )
A.该历程的总反应方程式为C H (g) C H (g)+H(g)
40 20 40 18 2
B.图示历程中的基元反应,速率最慢的是第3步
C.从C H 的结构分析,C H 纳米碗中五元环和六元环结构的数目分别为6、10
40 20 40 10
D.反应过程中有极性键的断裂和形成
【答案】D
【解析】A项,由图可知,该过程总反应为:C H (g)+H●(g) C H (g)+H(g)+H●(g),即
40 20 40 18 2
C H (g) C H (g)+H(g),A正确;B项,由反应机理可知,该历程包含3个基元反应,其中第三
40 20 40 18 2
个基元反应的活化能最大,反应3速率最慢,B正确;C项,由C H 的结构分析,可知其中含有1个五元
40 20
环,10个六元环,每脱两个氢形成1个五元环,则C H 总共含有6个五元环,10个六元环,C正确;D
40 10
项,该过程中涉及C-H断裂,C-C断裂和C-C、H-H形成,无极性键的形成,D错误;故选D。
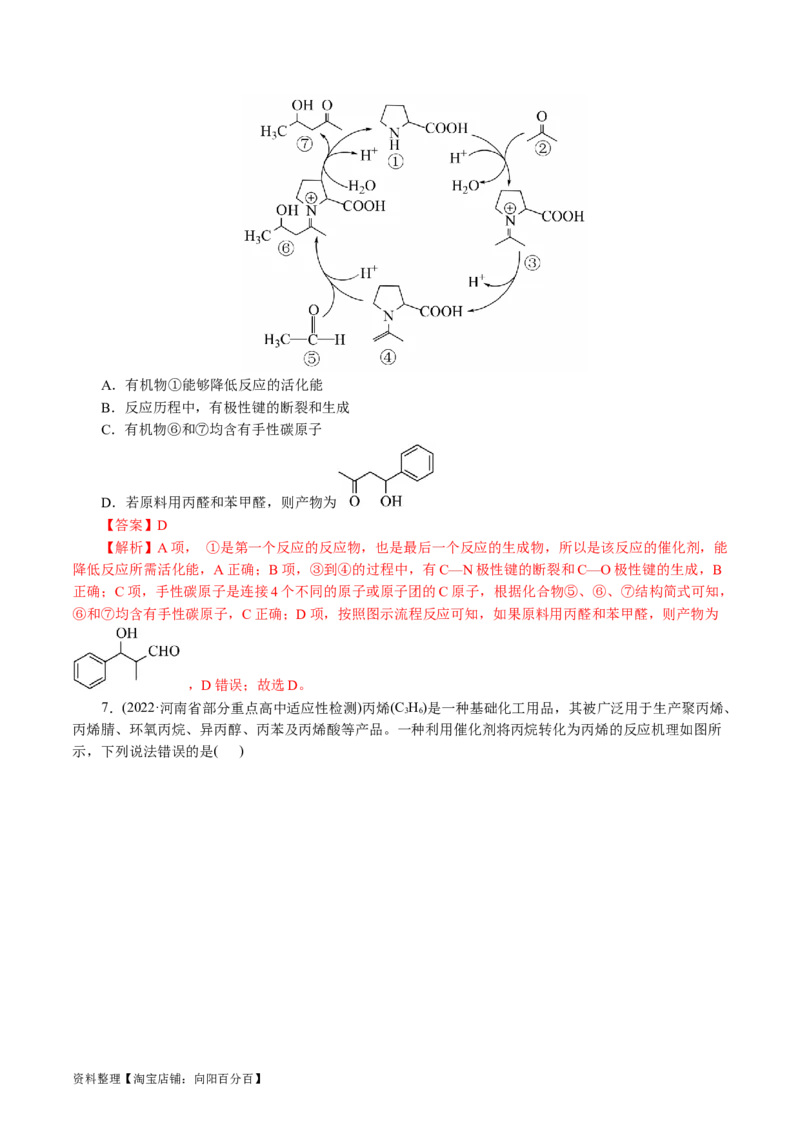
6.(2023·湖南省岳阳地区高三适应性考试)羟醛缩合反应是有机化学的一种重要反应。一种合成目标
产物 (如图中⑦)的反应机理如图所示。下列说法错误的是( )
资料整理【淘宝店铺:向阳百分百】A.有机物①能够降低反应的活化能
B.反应历程中,有极性键的断裂和生成
C.有机物⑥和⑦均含有手性碳原子
D.若原料用丙醛和苯甲醛,则产物为
【答案】D
【解析】A项, ①是第一个反应的反应物,也是最后一个反应的生成物,所以是该反应的催化剂,能
降低反应所需活化能,A正确;B项,③到④的过程中,有C—N极性键的断裂和C—O极性键的生成,B
正确;C项,手性碳原子是连接4个不同的原子或原子团的C原子,根据化合物⑤、⑥、⑦结构简式可知,
⑥和⑦均含有手性碳原子,C正确;D项,按照图示流程反应可知,如果原料用丙醛和苯甲醛,则产物为
,D错误;故选D。
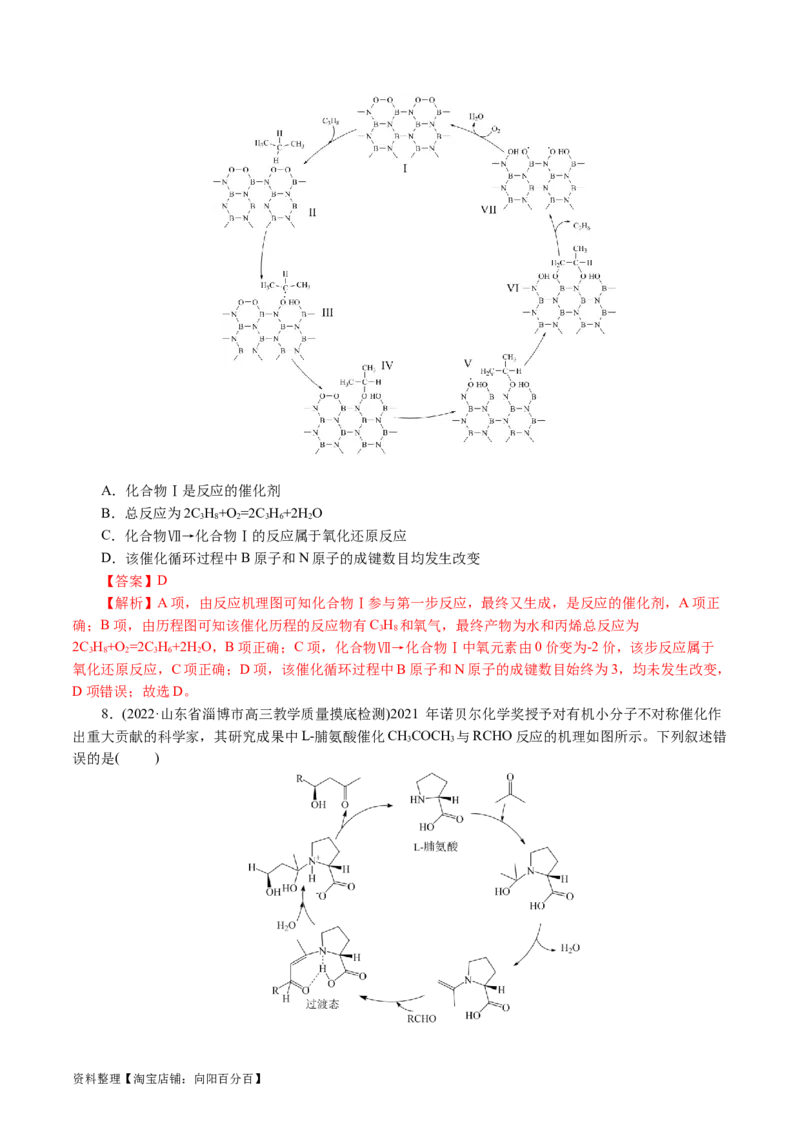
7.(2022·河南省部分重点高中适应性检测)丙烯(C H)是一种基础化工用品,其被广泛用于生产聚丙烯、
3 6
丙烯腈、环氧丙烷、异丙醇、丙苯及丙烯酸等产品。一种利用催化剂将丙烷转化为丙烯的反应机理如图所
示,下列说法错误的是( )
资料整理【淘宝店铺:向阳百分百】A.化合物Ⅰ是反应的催化剂
B.总反应为2C H+O =2C H+2H O
3 8 2 3 6 2
C.化合物Ⅶ→化合物Ⅰ的反应属于氧化还原反应
D.该催化循环过程中B原子和N原子的成键数目均发生改变
【答案】D
【解析】A项,由反应机理图可知化合物Ⅰ参与第一步反应,最终又生成,是反应的催化剂,A项正
确;B项,由历程图可知该催化历程的反应物有C H 和氧气,最终产物为水和丙烯总反应为
3 8
2C H+O =2C H+2H O,B项正确;C项,化合物Ⅶ→化合物Ⅰ中氧元素由0价变为-2价,该步反应属于
3 8 2 3 6 2
氧化还原反应,C项正确;D项,该催化循环过程中B原子和N原子的成键数目始终为3,均未发生改变,
D项错误;故选D。
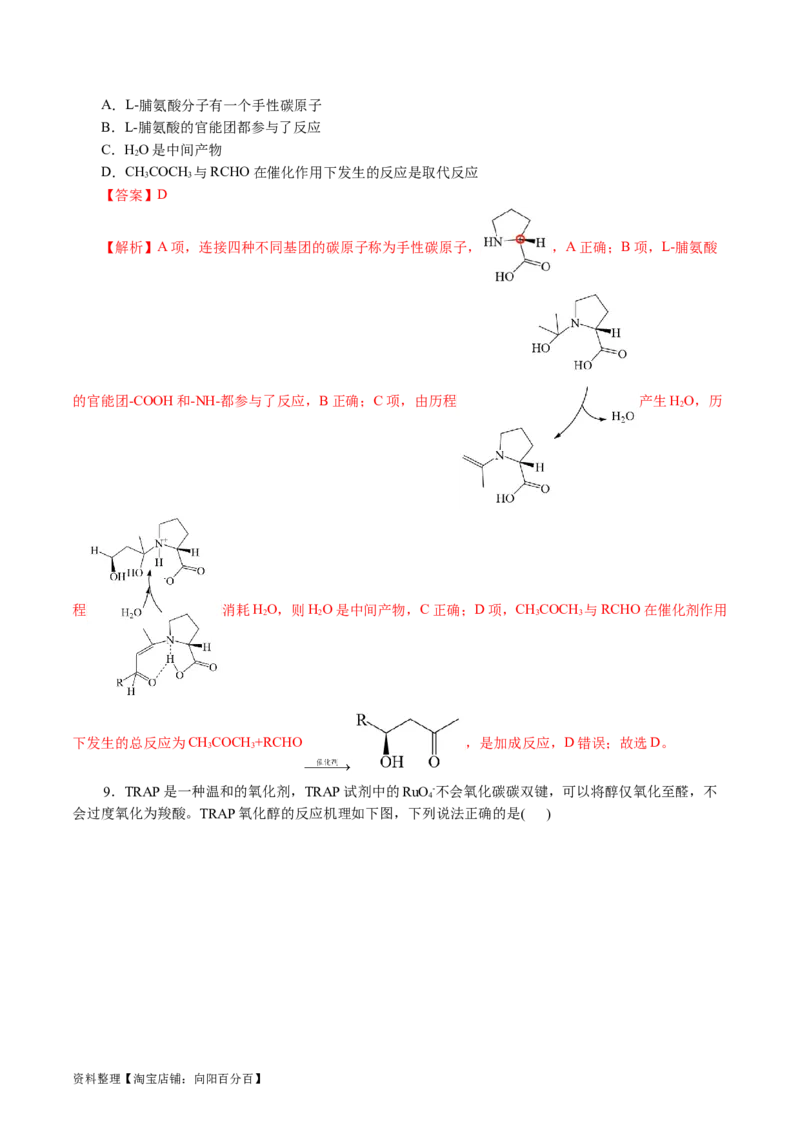
8.(2022·山东省淄博市高三教学质量摸底检测)2021 年诺贝尔化学奖授予对有机小分子不对称催化作
出重大贡献的科学家,其研究成果中L-脯氨酸催化CHCOCH 与RCHO反应的机理如图所示。下列叙述错
3 3
误的是( )
资料整理【淘宝店铺:向阳百分百】A.L-脯氨酸分子有一个手性碳原子
B.L-脯氨酸的官能团都参与了反应
C.HO是中间产物
2
D.CHCOCH 与RCHO在催化作用下发生的反应是取代反应
3 3
【答案】D
【解析】A项,连接四种不同基团的碳原子称为手性碳原子, ,A正确;B项,L-脯氨酸
的官能团-COOH和-NH-都参与了反应,B正确;C项,由历程 产生HO,历
2
程 消耗HO,则HO是中间产物,C正确;D项,CHCOCH 与RCHO在催化剂作用
2 2 3 3
下发生的总反应为CHCOCH +RCHO ,是加成反应,D错误;故选D。
3 3
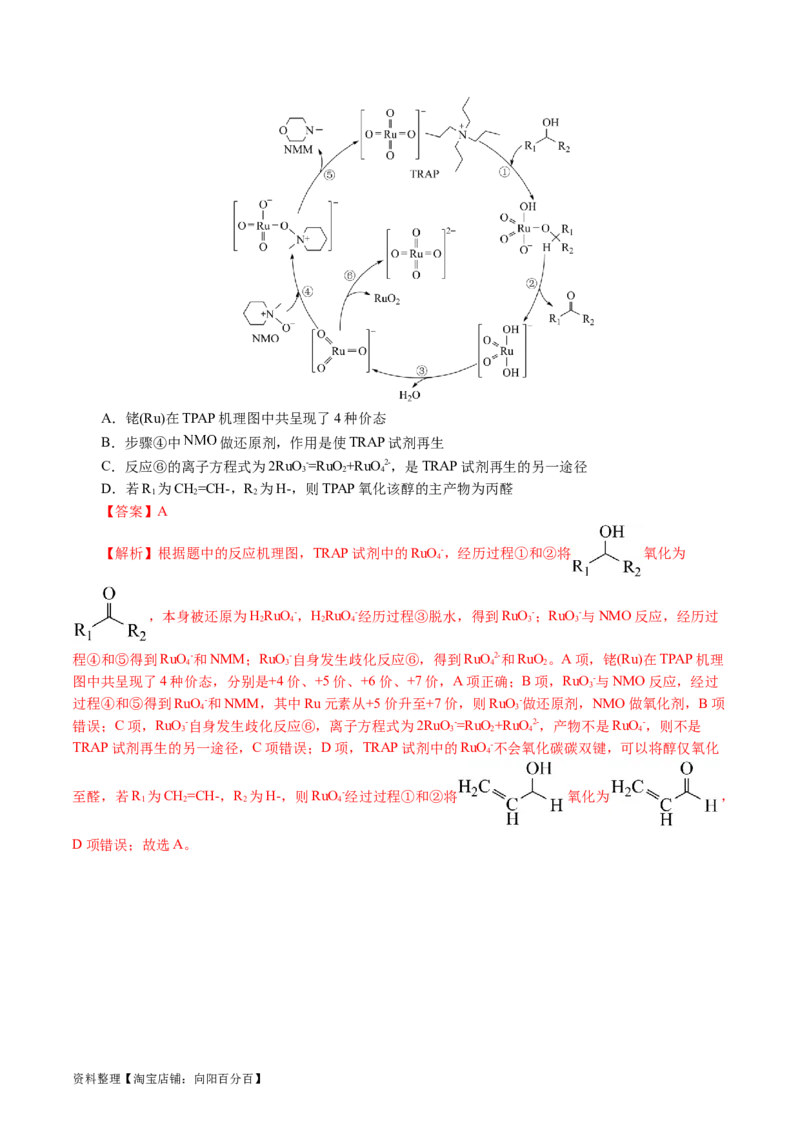
9.TRAP是一种温和的氧化剂,TRAP试剂中的RuO-不会氧化碳碳双键,可以将醇仅氧化至醛,不
4
会过度氧化为羧酸。TRAP氧化醇的反应机理如下图,下列说法正确的是( )
资料整理【淘宝店铺:向阳百分百】A.铑(Ru)在TPAP机理图中共呈现了4种价态
B.步骤④中 做还原剂,作用是使TRAP试剂再生
C.反应⑥的离子方程式为2RuO-=RuO+RuO2-,是TRAP试剂再生的另一途径
3 2 4
D.若R 为CH=CH-,R 为H-,则TPAP氧化该醇的主产物为丙醛
1 2 2
【答案】A
【解析】根据题中的反应机理图,TRAP试剂中的RuO-,经历过程①和②将 氧化为
4
,本身被还原为HRuO-,HRuO-经历过程③脱水,得到RuO-;RuO-与NMO反应,经历过
2 4 2 4 3 3
程④和⑤得到RuO-和NMM;RuO-自身发生歧化反应⑥,得到RuO2-和RuO。A项,铑(Ru)在TPAP机理
4 3 4 2
图中共呈现了4种价态,分别是+4价、+5价、+6价、+7价,A项正确;B项,RuO-与NMO反应,经过
3
过程④和⑤得到RuO-和NMM,其中Ru元素从+5价升至+7价,则RuO-做还原剂,NMO做氧化剂,B项
4 3
错误;C项,RuO-自身发生歧化反应⑥,离子方程式为2RuO-=RuO+RuO2-,产物不是RuO-,则不是
3 3 2 4 4
TRAP试剂再生的另一途径,C项错误;D项,TRAP试剂中的RuO-不会氧化碳碳双键,可以将醇仅氧化
4
至醛,若R 为CH=CH-,R 为H-,则RuO-经过过程①和②将 氧化为 ,
1 2 2 4
D项错误;故选A。
资料整理【淘宝店铺:向阳百分百】