文档内容
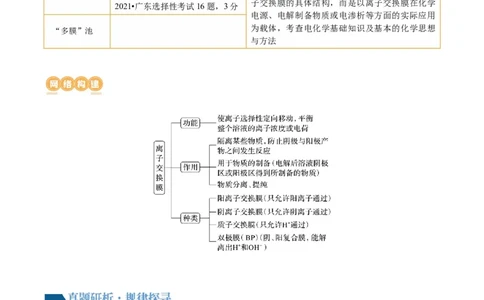
离子交换膜的分析与应用
目 录
1
2
【真题研析·规律探寻】 2
考点一 “单膜”池 2
考点二 “双膜”池 11
考点三 “多膜”池 13
【核心提炼·考向探究】 14
1.隔膜的作用 14
2.离子交换膜的类型 14
3.离子交换膜类型的判断 16
【题型特训·命题预测】 16
题型一 “单膜”池 16
题型二 “双膜”池 30
题型三 “多膜”池 35
考点要求 考题统计 考情分析
2023•湖北省选择性考试10题,3 【命题规律】
分;2023•山东卷 11 题,4 分; 近年来,新型电化学装置中的“膜”层出不穷,
“单膜”池
2022•山东卷13题,4分;2023•浙 高考试题中往往以此为契入点,考查电化学基础
知识。离子交换膜是一种含离子基团的、对溶液
江省6月选考13题,3分;2023•北京卷 5题,3分;2023•全国甲 里的离子具有选择透过能力的高分子膜,又称离子
卷 12 题,6 分;2023•广东卷 16 交换膜。可分三类:(1)阳离子交换膜,简称阳
题,3分;2022•湖南选择性考试8 膜,只允许阳离子通过,即允许H+和其他阳离子
题,3分;2022·浙江省1月选考 通过,不允许阴离子通过;(2)阴离子交换膜,简
21题,2分;2022·浙江省6月选 称阴膜,只允许阴离子通过,不允许阳离子通
考21题,2分;2021•全国甲卷13 过;(3)质子交换膜,只允许H+通过,不允许其他
题,6分;2021•湖北选择性考试 阳离子和阴离子通过。
15题,3分 【命题预测】
预测2024年这类试题将以“文字叙述+离子交换
2021•辽宁选择性考试13题,3
膜+电化学装置图”的方式呈现,考查的并不是离
“双膜”池 分;2021•天津卷11题,3分;
子交换膜的具体结构,而是以离子交换膜在化学
2021•广东选择性考试16题,3分
电源、电解制备物质或电渗析等方面的实际应用
为载体,考查电化学基础知识及基本的化学思想
“多膜”池
与方法
考点一 “单膜”池
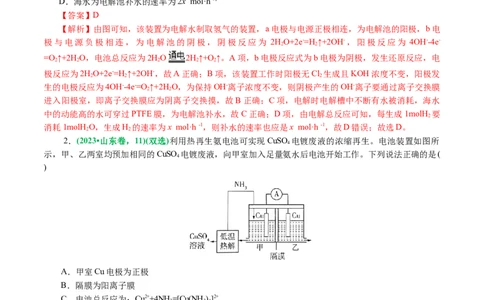
1.(2023•湖北省选择性考试,10)我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的
绿色化。该装置工作时阳极无Cl 生成且KOH溶液的浓度不变,电解生成氢气的速率为x mol·h -1。下列说
2
法错误的是( )A.b电极反应式为2HO+2e-=H ↑+2OH-
2 2
B.离子交换膜为阴离子交换膜
C.电解时海水中动能高的水分子可穿过PTFE膜
D.海水为电解池补水的速率为2x mol·h -1
【答案】D
【解析】由图可知,该装置为电解水制取氢气的装置,a电极与电源正极相连,为电解池的阳极,b电
极与电源负极相连,为电解池的阴极,阴极反应为 2HO+2e-=H ↑+2OH-,阳极反应为 4OH--4e-
2 2
=O ↑+2H O,电池总反应为2HO 2H↑+O ↑。A项,b电极反应式为b电极为阴极,发生还原反应,电
2 2 2 2 2
极反应为2HO+2e-=H ↑+2OH-,故A正确;B项,该装置工作时阳极无Cl 生成且KOH浓度不变,阳极发
2 2 2
生的电极反应为4OH--4e-=O ↑+2H O,为保持OH-离子浓度不变,则阴极产生的OH-离子要通过离子交换膜
2 2
进入阳极室,即离子交换膜应为阴离子交换摸,故B正确;C项,电解时电解槽中不断有水被消耗,海水
中的动能高的水可穿过PTFE膜,为电解池补水,故C正确;D项,由电解总反应可知,每生成1molH 要
2
消耗1molH O,生成H 的速率为x mol·h -1,则补水的速率也应是x mol·h -1,故D错误;故选D。
2 2
2.(2023•山东卷,11)(双选)利用热再生氨电池可实现CuSO 电镀废液的浓缩再生。电池装置如图所
4
示,甲、乙两室均预加相同的CuSO 电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是(
4
)
A.甲室Cu电极为正极
B.隔膜为阳离子膜
C.电池总反应为:Cu2++4NH=[Cu(NH)]2+
3 3 4
D.NH 扩散到乙室将对电池电动势产生影响
3
【答案】CD
【解析】A项,向甲室加入足量氨水后电池开始工作,则甲室 Cu电极溶解,变为铜离子与氨气形成
[Cu(NH )]2+,因此甲室Cu电极为负极,故A错误;B项,再原电池内电路中阳离子向正极移动,若隔膜为
3 4
阳离子膜,电极溶解生成的铜离子要向右侧移动,通入氨气要消耗铜离子,显然左侧阳离子不断减小,明
显不利于电池反应正常进行,故B错误;C项,左侧负极是Cu+4NH-2e- =[Cu(NH)]2+,正极是Cu 2++2e- =
3 3 4
Cu,则电池总反应为:Cu2++4NH=[Cu(NH)]2+,故C正确;D项,NH 扩散到乙室会与铜离子反应生成
3 3 4 3
[Cu(NH )]2+,铜离子浓度降低,铜离子得电子能力减弱,因此将对电池电动势产生影响,故D正确。故选
3 4
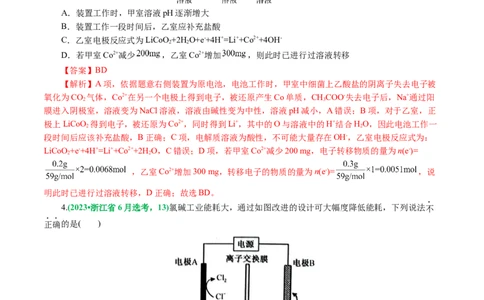
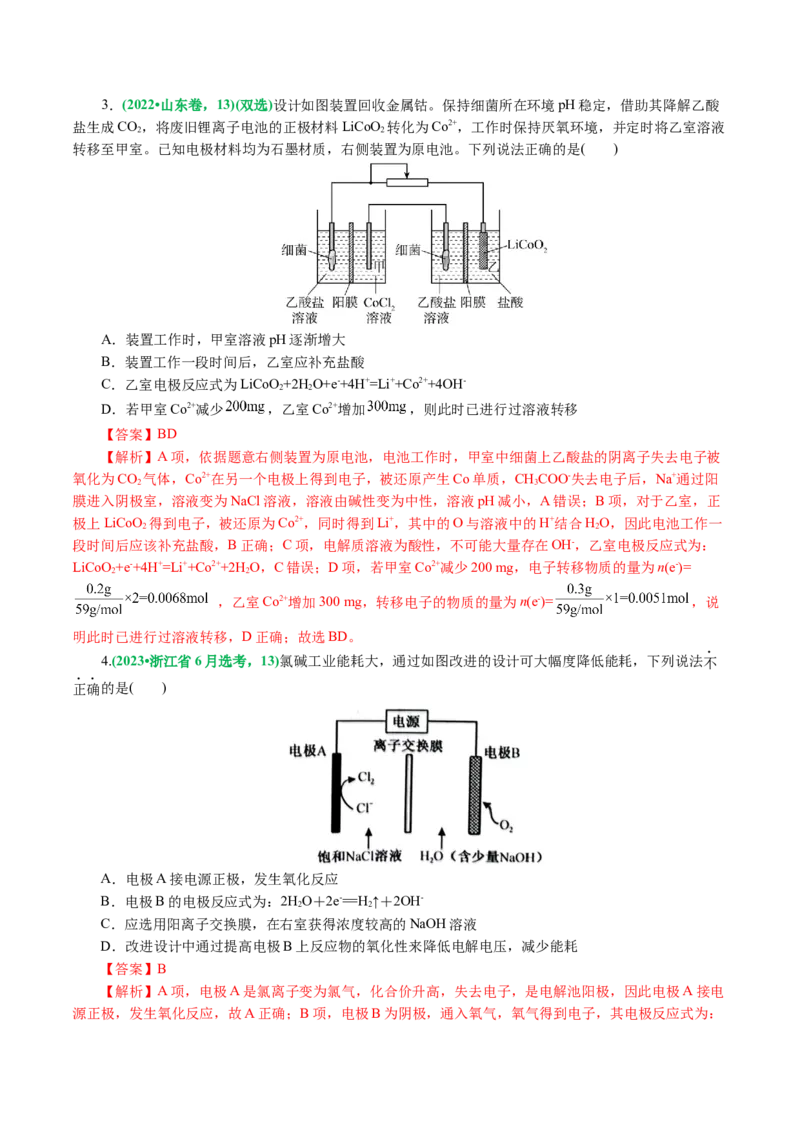
CD。3.(2022•山东卷,13)(双选)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸
盐生成CO,将废旧锂离子电池的正极材料LiCoO 转化为Co2+,工作时保持厌氧环境,并定时将乙室溶液
2 2
转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是( )
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为LiCoO +2H O+e-+4H+=Li++Co2++4OH-
2 2
D.若甲室Co2+减少 ,乙室Co2+增加 ,则此时已进行过溶液转移
【答案】BD
【解析】A项,依据题意右侧装置为原电池,电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被
氧化为CO 气体,Co2+在另一个电极上得到电子,被还原产生Co单质,CHCOO-失去电子后,Na+通过阳
2 3
膜进入阴极室,溶液变为NaCl溶液,溶液由碱性变为中性,溶液pH减小,A错误;B项,对于乙室,正
极上LiCoO 得到电子,被还原为Co2+,同时得到Li+,其中的O与溶液中的H+结合HO,因此电池工作一
2 2
段时间后应该补充盐酸,B正确;C项,电解质溶液为酸性,不可能大量存在OH-,乙室电极反应式为:
LiCoO +e-+4H+=Li++Co2++2H O,C错误;D项,若甲室Co2+减少200 mg,电子转移物质的量为n(e-)=
2 2
,乙室Co2+增加300 mg,转移电子的物质的量为n(e-)= ,说
明此时已进行过溶液转移,D正确;故选BD。
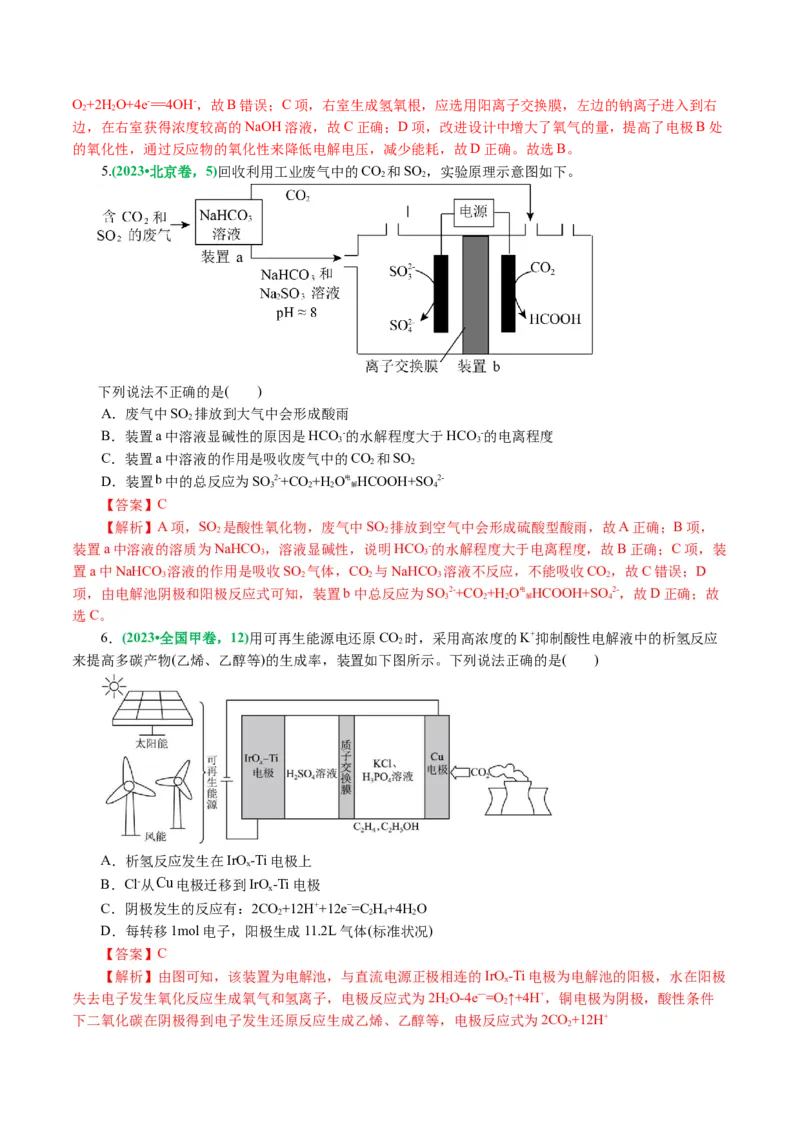
4.(2023•浙江省6月选考,13)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说法不
正确的是( )
A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为:2HO+2e-=H↑+2OH-
2 2
C.应选用阳离子交换膜,在右室获得浓度较高的NaOH溶液
D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗
【答案】B
【解析】A项,电极A是氯离子变为氯气,化合价升高,失去电子,是电解池阳极,因此电极A接电
源正极,发生氧化反应,故A正确;B项,电极B为阴极,通入氧气,氧气得到电子,其电极反应式为:O+2H O+4e-=4OH-,故B错误;C项,右室生成氢氧根,应选用阳离子交换膜,左边的钠离子进入到右
2 2
边,在右室获得浓度较高的NaOH溶液,故C正确;D项,改进设计中增大了氧气的量,提高了电极B处
的氧化性,通过反应物的氧化性来降低电解电压,减少能耗,故D正确。故选B。
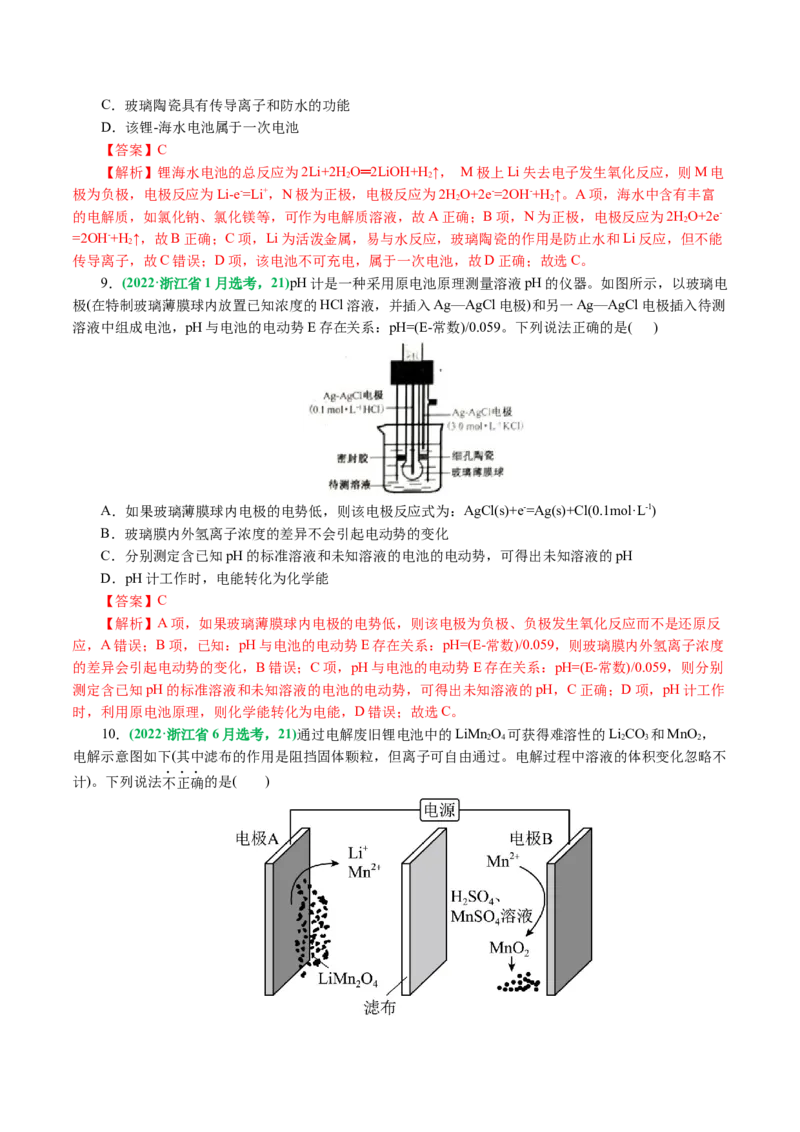
5.(2023•北京卷,5)回收利用工业废气中的CO 和SO ,实验原理示意图如下。
2 2
下列说法不正确的是( )
A.废气中SO 排放到大气中会形成酸雨
2
B.装置a中溶液显碱性的原因是HCO -的水解程度大于HCO -的电离程度
3 3
C.装置a中溶液的作用是吸收废气中的CO 和SO
2 2
D.装置 中的总反应为SO 2-+CO +H O电 HCOOH+SO 2-
3 2 2 解 4
【答案】C
【解析】A项,SO 是酸性氧化物,废气中SO 排放到空气中会形成硫酸型酸雨,故A正确;B项,
2 2
装置a中溶液的溶质为NaHCO ,溶液显碱性,说明HCO -的水解程度大于电离程度,故B正确;C项,装
3 3
置a中NaHCO 溶液的作用是吸收SO 气体,CO 与NaHCO 溶液不反应,不能吸收CO,故C错误;D
3 2 2 3 2
项,由电解池阴极和阳极反应式可知,装置b中总反应为SO 2-+CO +H O电 HCOOH+SO 2-,故D正确;故
3 2 2 解 4
选C。
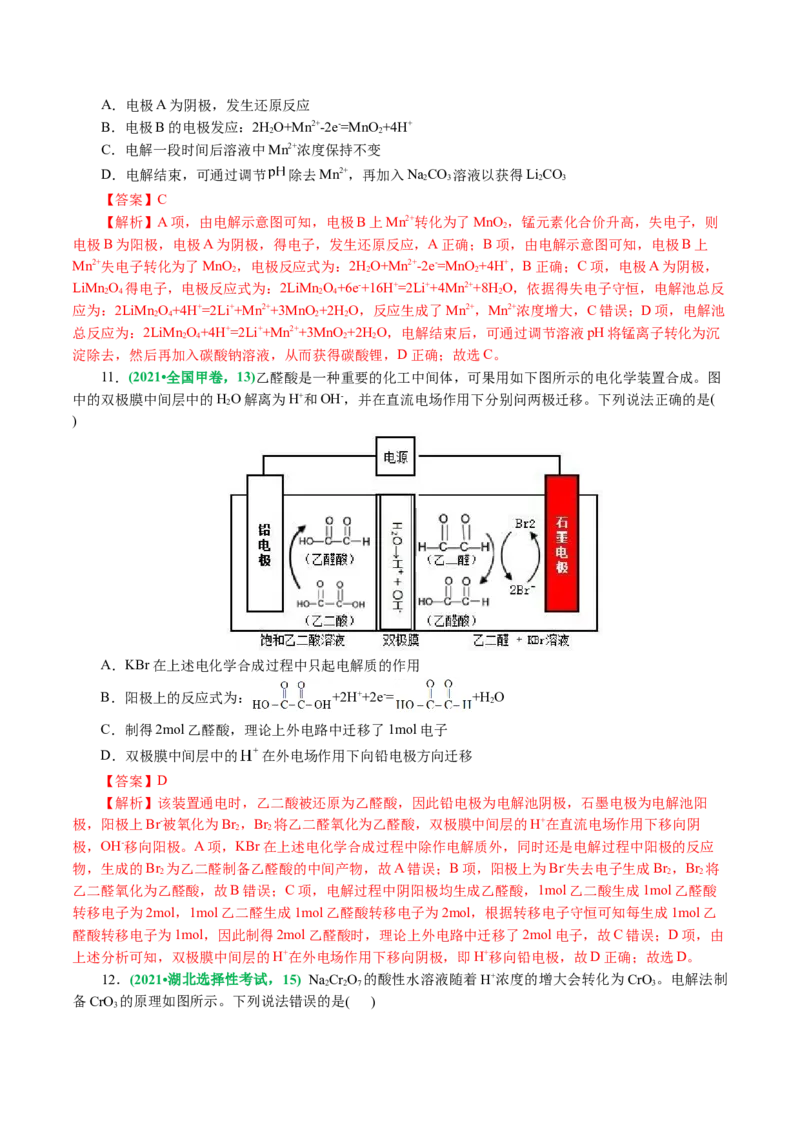
6.(2023•全国甲卷,12)用可再生能源电还原CO 时,采用高浓度的K+抑制酸性电解液中的析氢反应
2
来提高多碳产物(乙烯、乙醇等)的生成率,装置如下图所示。下列说法正确的是( )
A.析氢反应发生在IrO -Ti电极上
x
B.Cl-从 电极迁移到IrO -Ti电极
x
C.阴极发生的反应有:2CO+12H++12e−=C H+4H O
2 2 4 2
D.每转移1mol电子,阳极生成11.2L气体(标准状况)
【答案】C
【解析】由图可知,该装置为电解池,与直流电源正极相连的IrO -Ti电极为电解池的阳极,水在阳极
x
失去电子发生氧化反应生成氧气和氢离子,电极反应式为2HO-4e—=O ↑+4H+,铜电极为阴极,酸性条件
2 2
下二氧化碳在阴极得到电子发生还原反应生成乙烯、乙醇等,电极反应式为2CO+12H+
2+12e−=C H+4H O、2CO+12H++12e−=C HOH+3H O,电解池工作时,氢离子通过质子交换膜由阳极室进
2 4 2 2 2 5 2
入阴极室。A项,析氢反应为还原反应,应在阴极发生,即在铜电极上发生,故A错误;B项,离子交换
膜为质子交换膜,只允许氢离子通过,Cl-不能通过,故B错误;C项,铜电极为阴极,酸性条件下二氧化
碳在阴极得到电子发生还原反应生成乙烯、乙醇等,电极反应式有2CO+12H++12e−=C H+4H O,故C正
2 2 4 2
确;D项,水在阳极失去电子发生氧化反应生成氧气和氢离子,电极反应式为2HO-4e—=O ↑+4H+,每转移
2 2
1mol电子,生成0.25molO,在标况下体积为5.6L,故D错误;故选C。
2
7.(2023•广东卷,16)用一种具有“卯榫”结构的双极膜组装电解池(下图),可实现大电流催化电解
KNO 溶液制氨。工作时,HO在双极膜界面处被催化解离成H+和OH-,有利于电解反应顺利进行。下列
3 2
说法不正确的是( )
A.电解总反应:KNO+3H O= NH ·H O+2O↑+KOH
3 2 3 2 2
B.每生成1mol NH ·H O,双极膜处有9 mol的HO解离
3 2 2
C.电解过程中,阳极室中 的物质的量不因反应而改变
D.相比于平面结构双极膜,“卯榫”结构可提高氨生成速率
【答案】B
【解析】由信息大电流催化电解KNO 溶液制氨可知,在电极a处KNO 放电生成NH ,发生还原反
3 3 3
应,故电极a为阴极,电极方程式为NO - +8e-+7H O= NH·H O+9OH-,电极b为阳极,电极方程式为
3 2 3 2
4OH--4e-=O↑+2HO,“卯榫”结构的双极膜中的H+移向电极a,OH-移向电极b。A项,由分析中阴
2 2
阳极电极方程式可知,电解总反应为KNO+3H O= NH ·H O+2O↑+KOH,故A正确;B项,每生成1mol
3 2 3 2 2
NH ·H O,阴极得8mol e-,同时双极膜处有8mol H+进入阴极室,即有8mol的HO解离,故B错误;C
3 2 2
项,电解过程中,阳极室每消耗4mol OH-,同时有4mol OH-通过双极膜进入阳极室,KOH的物质的量不
因反应而改变,故C正确;D项,相比于平面结构双极膜,“卯榫”结构具有更大的膜面积,有利于HO
2
被催化解离成H+和OH-,可提高氨生成速率,故D正确;故选B。
8.(2022•湖南选择性考试,8)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。
下列说法错误的是( )
A.海水起电解质溶液作用
B.N极仅发生的电极反应:2HO+2e-=2OH-+H ↑
2 2C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
【答案】C
【解析】锂海水电池的总反应为2Li+2HO═2LiOH+H ↑, M极上Li失去电子发生氧化反应,则M电
2 2
极为负极,电极反应为Li-e-=Li+,N极为正极,电极反应为2HO+2e-=2OH-+H ↑。A项,海水中含有丰富
2 2
的电解质,如氯化钠、氯化镁等,可作为电解质溶液,故A正确;B项,N为正极,电极反应为2HO+2e-
2
=2OH-+H ↑,故B正确;C项,Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,但不能
2
传导离子,故C错误;D项,该电池不可充电,属于一次电池,故D正确;故选C。
9.(2022·浙江省1月选考,21)pH计是一种采用原电池原理测量溶液pH的仪器。如图所示,以玻璃电
极(在特制玻璃薄膜球内放置已知浓度的HCl溶液,并插入Ag—AgCl电极)和另一Ag—AgCl电极插入待测
溶液中组成电池,pH与电池的电动势E存在关系:pH=(E-常数)/0.059。下列说法正确的是( )
A.如果玻璃薄膜球内电极的电势低,则该电极反应式为:AgCl(s)+e-=Ag(s)+Cl(0.1mol·L-1)
B.玻璃膜内外氢离子浓度的差异不会引起电动势的变化
C.分别测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH
D.pH计工作时,电能转化为化学能
【答案】C
【解析】A项,如果玻璃薄膜球内电极的电势低,则该电极为负极、负极发生氧化反应而不是还原反
应,A错误;B项,已知:pH与电池的电动势E存在关系:pH=(E-常数)/0.059,则玻璃膜内外氢离子浓度
的差异会引起电动势的变化,B错误;C项,pH与电池的电动势E存在关系:pH=(E-常数)/0.059,则分别
测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH,C正确;D项,pH计工作
时,利用原电池原理,则化学能转化为电能,D错误;故选C。
10.(2022·浙江省6月选考,21)通过电解废旧锂电池中的LiMn O 可获得难溶性的LiCO 和MnO ,
2 4 2 3 2
电解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不
计)。下列说法不正确的是( )A.电极A为阴极,发生还原反应
B.电极B的电极发应:2HO+Mn2+-2e-=MnO+4H+
2 2
C.电解一段时间后溶液中Mn2+浓度保持不变
D.电解结束,可通过调节 除去Mn2+,再加入NaCO 溶液以获得LiCO
2 3 2 3
【答案】C
【解析】A项,由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失电子,则
2
电极B为阳极,电极A为阴极,得电子,发生还原反应,A正确;B项,由电解示意图可知,电极B上
Mn2+失电子转化为了MnO ,电极反应式为:2HO+Mn2+-2e-=MnO+4H+,B正确;C项,电极A为阴极,
2 2 2
LiMn O 得电子,电极反应式为:2LiMn O+6e-+16H+=2Li++4Mn2++8H O,依据得失电子守恒,电解池总反
2 4 2 4 2
应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,反应生成了Mn2+,Mn2+浓度增大,C错误;D项,电解池
2 4 2 2
总反应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,电解结束后,可通过调节溶液pH将锰离子转化为沉
2 4 2 2
淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正确;故选C。
11.(2021•全国甲卷,13)乙醛酸是一种重要的化工中间体,可果用如下图所示的电化学装置合成。图
中的双极膜中间层中的HO解离为H+和OH-,并在直流电场作用下分别问两极迁移。下列说法正确的是(
2
)
A.KBr在上述电化学合成过程中只起电解质的作用
B.阳极上的反应式为: +2H++2e-= +H O
2
C.制得2mol乙醛酸,理论上外电路中迁移了1mol电子
D.双极膜中间层中的 在外电场作用下向铅电极方向迁移
【答案】D
【解析】该装置通电时,乙二酸被还原为乙醛酸,因此铅电极为电解池阴极,石墨电极为电解池阳
极,阳极上Br-被氧化为Br ,Br 将乙二醛氧化为乙醛酸,双极膜中间层的H+在直流电场作用下移向阴
2 2
极,OH-移向阳极。A项,KBr在上述电化学合成过程中除作电解质外,同时还是电解过程中阳极的反应
物,生成的Br 为乙二醛制备乙醛酸的中间产物,故A错误;B项,阳极上为Br-失去电子生成Br ,Br 将
2 2 2
乙二醛氧化为乙醛酸,故B错误;C项,电解过程中阴阳极均生成乙醛酸,1mol乙二酸生成1mol乙醛酸
转移电子为2mol,1mol乙二醛生成1mol乙醛酸转移电子为2mol,根据转移电子守恒可知每生成1mol乙
醛酸转移电子为1mol,因此制得2mol乙醛酸时,理论上外电路中迁移了2mol电子,故C错误;D项,由
上述分析可知,双极膜中间层的H+在外电场作用下移向阴极,即H+移向铅电极,故D正确;故选D。
12.(2021•湖北选择性考试,15) NaCr O 的酸性水溶液随着H浓度的增大会转化为CrO 。电解法制
2 2 7 3
备CrO 的原理如图所示。下列说法错误的是( )
3A.电解时只允许H通过离子交换膜
B.生成O 和H 的质量比为8:1
2 2
C.电解一段时间后阴极区溶液OH的浓度增大
D.CrO 的生成反应为:Cr O2+2H=2CrO+HO
3 2 7 3 2
【答案】A
【解析】左侧电极上产生O ,右侧电极上产生H ,说明左极为阳极,电极反应式为2HO-4e=4H
2 2 2
+O↑,左侧制备三氧化铬:Cr O2+2H=2CrO +HO;右极为阴极,电极反应式为4HO+4e=4OH+
2 2 7 3 2 2
2H↑。在阳极区参与反应制备三氧化铬,故不通过离子交换膜,通过交换膜向阴极区迁移,A项错误;根
2
据电子守恒,产生O、H 的质量之比为32:4=8:1,B项正确;由阴极反应式知,阴极产生OH;如果阴极
2 2
通过交换膜向左侧迁移,OH必然会中和H,与题意相矛盾,所以,钠离子由左侧向右侧迁移,阴极区氢
氧化钠溶液浓度增大,C项正确;根据原料和产物组成知,Cr O2+2H=2CrO+HO;D项正确。
2 7 3 2
考点二 “双膜”池
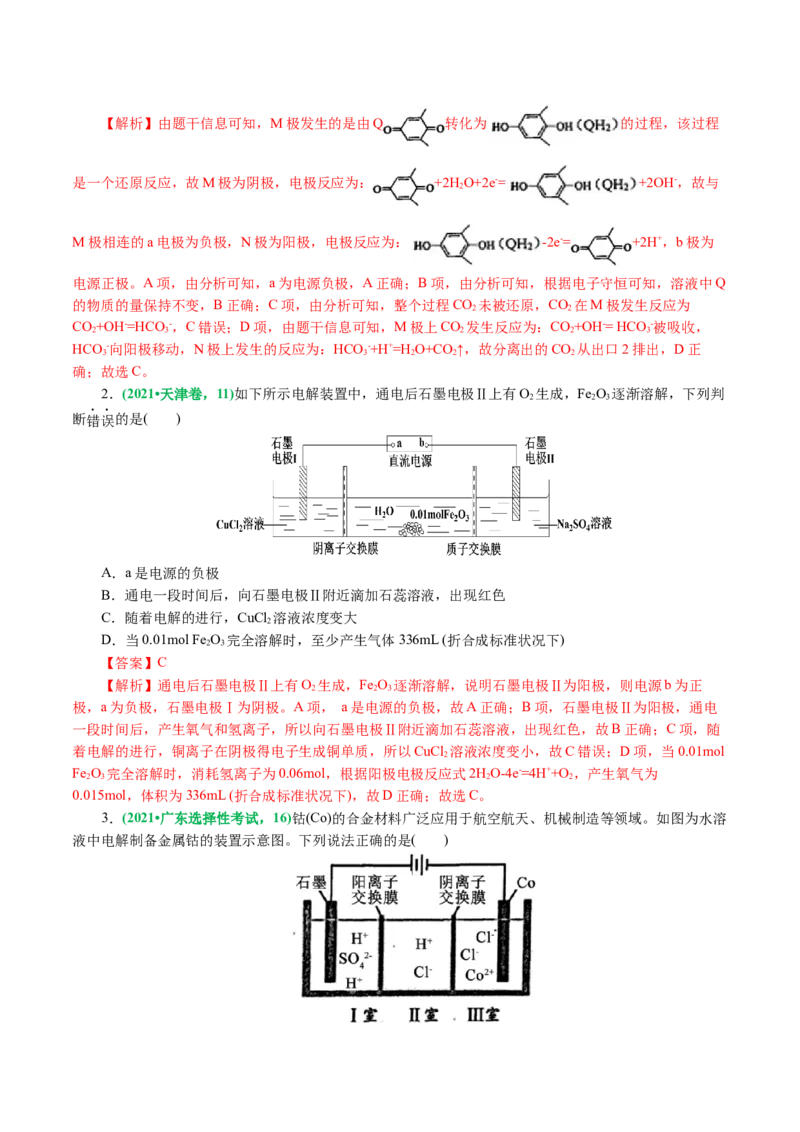
1.(2021•辽宁选择性考试,13)利用 (Q)与 电解转化法从烟气中分离
的原理如图。已知气体可选择性通过膜电极,溶液不能通过。下列说法错误的是( )
A.a为电源负极 B.溶液中Q的物质的量保持不变
C. 在M极被还原 D.分离出的 从出口2排出
【答案】C【解析】由题干信息可知,M极发生的是由Q 转化为 的过程,该过程
是一个还原反应,故M极为阴极,电极反应为: +2H O+2e-= +2OH-,故与
2
M极相连的a电极为负极,N极为阳极,电极反应为: -2e-= +2H+,b极为
电源正极。A项,由分析可知,a为电源负极,A正确;B项,由分析可知,根据电子守恒可知,溶液中Q
的物质的量保持不变,B正确;C项,由分析可知,整个过程CO 未被还原,CO 在M极发生反应为
2 2
CO+OH-=HCO-,C错误;D项,由题干信息可知,M极上CO 发生反应为:CO+OH-= HCO -被吸收,
2 3 2 2 3
HCO -向阳极移动,N极上发生的反应为:HCO -+H+=H O+CO↑,故分离出的CO 从出口2排出,D正
3 3 2 2 2
确;故选C。
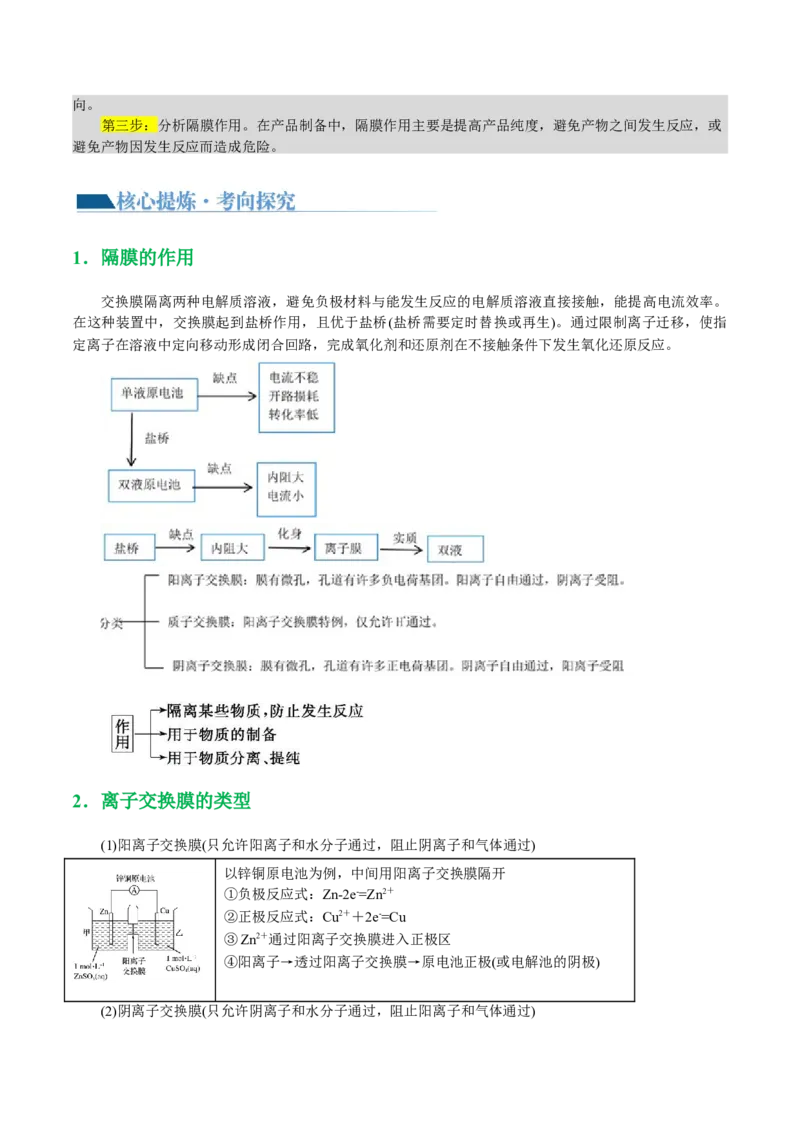
2.(2021•天津卷,11)如下所示电解装置中,通电后石墨电极Ⅱ上有O 生成,Fe O 逐渐溶解,下列判
2 2 3
断错误的是( )
A.a是电源的负极
B.通电一段时间后,向石墨电极Ⅱ附近滴加石蕊溶液,出现红色
C.随着电解的进行,CuCl 溶液浓度变大
2
D.当0.01mol Fe O 完全溶解时,至少产生气体336mL (折合成标准状况下)
2 3
【答案】C
【解析】通电后石墨电极Ⅱ上有O 生成,Fe O 逐渐溶解,说明石墨电极Ⅱ为阳极,则电源b为正
2 2 3
极,a为负极,石墨电极Ⅰ为阴极。A项, a是电源的负极,故A正确;B项,石墨电极Ⅱ为阳极,通电
一段时间后,产生氧气和氢离子,所以向石墨电极Ⅱ附近滴加石蕊溶液,出现红色,故B正确;C项,随
着电解的进行,铜离子在阴极得电子生成铜单质,所以CuCl 溶液浓度变小,故C错误;D项,当0.01mol
2
Fe O 完全溶解时,消耗氢离子为0.06mol,根据阳极电极反应式2HO-4e-=4H++O ,产生氧气为
2 3 2 2
0.015mol,体积为336mL (折合成标准状况下),故D正确;故选C。
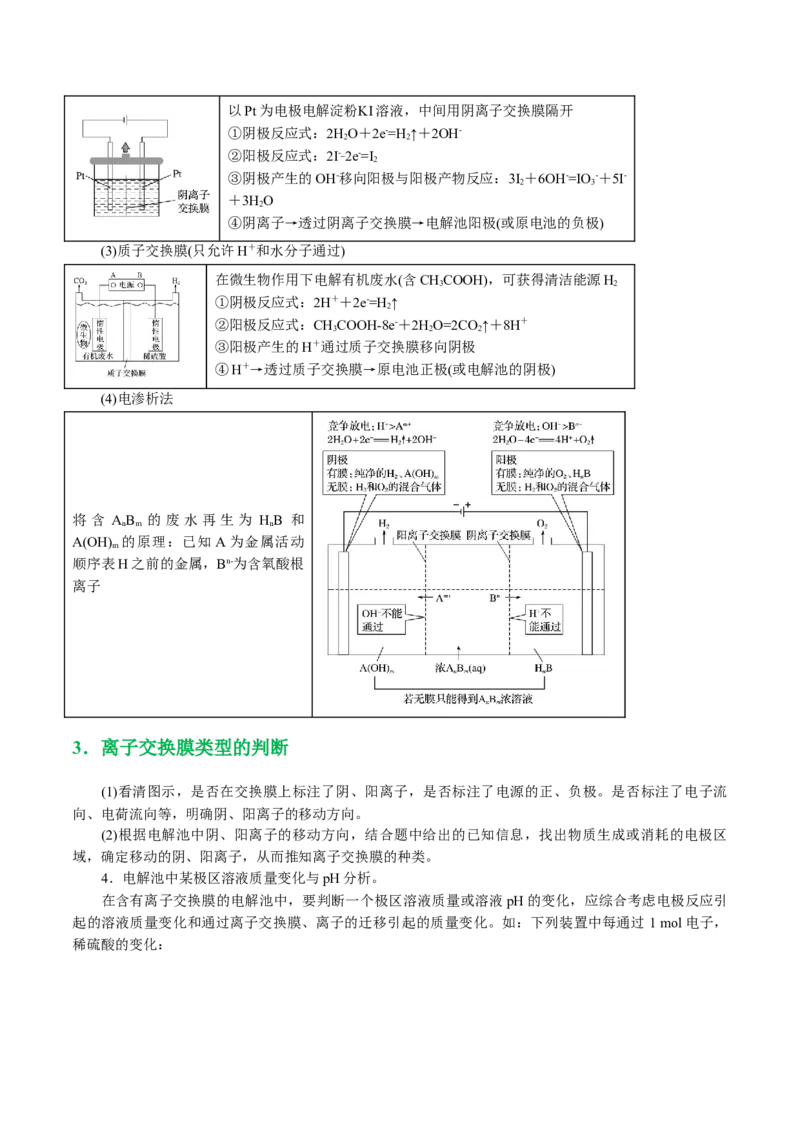
3.(2021•广东选择性考试,16)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶
液中电解制备金属钴的装置示意图。下列说法正确的是( )A.工作时,Ⅰ室和Ⅱ室溶液的pH均增大
B.生成1molCo,Ⅰ室溶液质量理论上减少16 g
C.移除两交换膜后,石墨电极上发生的反应不变
D.电解总反应:为2Co2++2H O 2 Co +O ↑+4H+
2 2
【答案】D
【解析】由图可知,该装置为电解池,石墨电极为阳极,水在阳极失去电子发生氧化反应生成氧气和
氢离子,电极反应式为2HO-4e-=O ↑+4H+,Ⅰ室中阳离子电荷数大于阴离子电荷数,放电生成的氢离子通
2 2
过阳离子交换膜由Ⅰ室向Ⅱ室移动,钴电极为阴极,钴离子在阴极得到电子发生还原反应生成钴,电极反
应式为Co2++2e-=Co,Ⅲ室中阴离子电荷数大于阳离子电荷数,氯离子过阴离子交换膜由Ⅲ室向Ⅱ室移动,
电解的总反应的离子方程式为2Co2++2H O 2 Co +O ↑+4H+。A项,放电生成的氢离子通过阳离子交换膜
2 2
由Ⅰ室向Ⅱ室移动,使Ⅱ室中氢离子浓度增大,溶液pH减小,故A错误;B项,由分析可知,阴极生成
1mol钴,阳极有1mol水放电,则Ⅰ室溶液质量减少18g,故B错误;C项,若移除离子交换膜,氯离子的
放电能力强于水,氯离子会在阳极失去电子发生氧化反应生成氯气,则移除离子交换膜,石墨电极的电极
反应会发生变化,故C错误;D项,由分析可知,电解的总反应的离子方程式为2Co2++2H O 2 Co
2
+O ↑+4H+,故D正确;故选D。
2
考点三 “多膜”池
1.[2014·全国卷Ⅰ,27(4)]HPO 也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴
3 2
膜分别只允许阳离子、阴离子通过):
①写出阳极的电极反应式:______________________________________________________。
②分析产品室可得到HPO 的原因:______________________________________________。
3 2
③早期采用“三室电渗析法”制备 HPO :将“四室电渗析法”中阳极室的稀硫酸用 HPO 稀溶液代
3 2 3 2
替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有____________
杂质。该杂质产生的原因是__________________________________。
【答案】①2HO-4e-===O ↑+4H+
2 2
②阳极室的H+穿过阳膜扩散至产品室,原料室的HPO穿过阴膜扩散至产品室,二者反应生成HPO
2 3 2
③PO HPO或HPO 被氧化
2 3 2
【解析】①阳极发生氧化反应,水中的OH-失去电子,电极反应式为2HO-4e-===O ↑+4H+。②HO
2 2 2
放电产生 H+,H+进入产品室,原料室的 HPO 穿过阴膜扩散至产品室,二者发生反应:H++
2
HPO=H PO 。③如果撤去阳膜,HPO或HPO 可能会被氧化。
2 3 2 2 3 2
第一步:分清隔膜类型。即交换膜属于阳膜、阴膜或质子膜中的哪一种,判断允许哪种离子通过隔
膜。
第二步:写出电极反应式,判断交换膜两侧离子变化,推断电荷变化,根据电荷平衡判断离子迁移方向。
第三步:分析隔膜作用。在产品制备中,隔膜作用主要是提高产品纯度,避免产物之间发生反应,或
避免产物因发生反应而造成危险。
1.隔膜的作用
交换膜隔离两种电解质溶液,避免负极材料与能发生反应的电解质溶液直接接触,能提高电流效率。
在这种装置中,交换膜起到盐桥作用,且优于盐桥(盐桥需要定时替换或再生)。通过限制离子迁移,使指
定离子在溶液中定向移动形成闭合回路,完成氧化剂和还原剂在不接触条件下发生氧化还原反应。
2.离子交换膜的类型
(1)阳离子交换膜(只允许阳离子和水分子通过,阻止阴离子和气体通过)
以锌铜原电池为例,中间用阳离子交换膜隔开
①负极反应式:Zn-2e-=Zn2+
②正极反应式:Cu2++2e-=Cu
③Zn2+通过阳离子交换膜进入正极区
④阳离子→透过阳离子交换膜→原电池正极(或电解池的阴极)
(2)阴离子交换膜(只允许阴离子和水分子通过,阻止阳离子和气体通过)以Pt为电极电解淀粉KI溶液,中间用阴离子交换膜隔开
①阴极反应式:2HO+2e-=H ↑+2OH-
2 2
②阳极反应式:2I-_2e-=I
2
③阴极产生的OH-移向阳极与阳极产物反应:3I+6OH-=IO -+5I-
2 3
+3HO
2
④阴离子→透过阴离子交换膜→电解池阳极(或原电池的负极)
(3)质子交换膜(只允许H+和水分子通过)
在微生物作用下电解有机废水(含CHCOOH),可获得清洁能源H
3 2
①阴极反应式:2H++2e-=H ↑
2
②阳极反应式:CHCOOH-8e-+2HO=2CO↑+8H+
3 2 2
③阳极产生的H+通过质子交换膜移向阴极
④H+→透过质子交换膜→原电池正极(或电解池的阴极)
(4)电渗析法
将 含 AB 的 废 水 再 生 为 HB 和
n m n
A(OH) 的原理:已知A为金属活动
m
顺序表H之前的金属,Bn-为含氧酸根
离子
3.离子交换膜类型的判断
(1)看清图示,是否在交换膜上标注了阴、阳离子,是否标注了电源的正、负极。是否标注了电子流
向、电荷流向等,明确阴、阳离子的移动方向。
(2)根据电解池中阴、阳离子的移动方向,结合题中给出的已知信息,找出物质生成或消耗的电极区
域,确定移动的阴、阳离子,从而推知离子交换膜的种类。
4.电解池中某极区溶液质量变化与pH分析。
在含有离子交换膜的电解池中,要判断一个极区溶液质量或溶液pH的变化,应综合考虑电极反应引
起的溶液质量变化和通过离子交换膜、离子的迁移引起的质量变化。如:下列装置中每通过 1 mol电子,
稀硫酸的变化:(1)b极的电极反应为2HO-4e-=O ↑+4H+,通过1 mol电子时,有0.5 mol HO放电,产生1 mol H+。
2 2 2
(2)通过1 mol电子时,有1 mol H+从稀硫酸中通过阳膜进入产品室。因此通过1 mol电子时,稀硫酸中
反应消耗0.5 mol H O,生成的O 逸出,生成的H+迁移至产品室,则质量减少9 g。稀硫酸中H+的物质的
2 2
量不变,若不考虑溶液体积变化,则溶液pH不变。
题型一 “单膜”池
1.(2024·云南省部分名校高三理科综合能力测试)镍氢电池的工作原理如图所示,放电时,电流由a极
经外电路流向 b极。下列叙述正确的是( )
A.放电时,b极发生还原反应
B.充电时,a极与电流负极连接
C.放电时,a极的电极反应式为 NiO(OH)+e-+H O= Ni(OH) +OH-
2 2
D.充电时,b极的电极反应式为 MH +OH--e-=MH +H O
x x-1 2
【答案】C
【解析】A项,放电时,电流由a极向b极,说明a极为正极,b极为负极,b极发生氧化反应,故A
错误;B项,充电时,a为阳极,与电源正极连接,故B错误;C项,放电时,a极为正极,发生还原反
应,电极反应式为NiO(OH)+e-+H O= Ni(OH) +OH-,故C正确;D项,充电时,b极为阴极,电极反应式
2 2
为MH +HO+e-=MH +OH-,故D错误;故选C。
x-1 2 x
2.(2024·河南·高三湘豫名校联考联盟高三联考)KMnO 是一种重要的化学试剂,电解KMnO 及某种
4 2 4
稀碱性溶液可得到KMnO 、KOH,其工作原理如图所示(电极材料是铁与铂),电解中M电极周围溶液逐渐
4
变成紫红色,下列说法错误的是( )A.电极电势:a>b
B.N电极电极反应式为2HO+2e-=2OH-+H ↑
2 2
C.当电路中有2mol电子转移时,会有78g离子通过X膜
D.M电极是铁、N电极是铂
【答案】D
【解析】由M电极周围溶液颜色的变化可确定有MnO-生成,过程中锰元素价态升高,由此知M是阳
4
极、N是阴极,a是正极、b是负极。A项,由M电极周围溶液颜色的变化可确定有MnO-生成,过程中锰
4
元素价态升高,由此知M是阳极、N是阴极,a是正极、b是负极。正极的电极电势高于负极,A项正
确;B项,阴极上水中+1价氢得到电子转化为H,B项正确;C项,电路中通过的电子所带电量与通过X
2
膜的离子所带电量相同,故有2molK+通过X膜,其质量为78g,C项正确;D项,若铁作阳极,则MnO2-
4
无法放电转化为MnO-,D项错误;故选D。
4
3.(2024·湖北省名校联考高三期中)传统合成氨采用氢气作为氢源,能耗高,我国科研机构采用水作
为氢源,通过如图电化学装置实现了常温下氨的合成。下列说法正确的是( )
A.在阳极池中加入盐酸不影响气体产物的成分
B.隔膜为阳离子交换膜,H+通过该隔膜向左池移动
C.不考虑损耗,理论上氨气和氧气的产出比[ ]为
D.合成氨过程中,电子通过石墨电极流入电源的负极
【答案】B
【解析】结合题意和图可知,左池为电解池的阴极,发生氮气得电子产生氨气的还原反应,因此左池
应该与电源负极相连;而右池则发生水的放电反应,水失去电子生成氧气与氢离子,为阳极,与电源正极
相连。A项,阳极池加入盐酸后,Cl-优先失电子生成Cl,A项错误;B项,电解过程中阳离子向阴极移
2动,B项正确;C项,根据得失电子守恒可知,理论上氨气和氧气的产出比为4∶3,C项错误;D项,石
墨电极为阳极,阳极上面的电子流入电源的正极,D项错误;故选B。
4.(2023·广东省佛山市二模)过硫酸铵[(NH )SO]可用作氧化剂、漂白剂。利用电解法在两极分别生
4 2 2 8
产过硫酸铵和过氧化氢的装置如图所示。下列说法错误的是( )
A.a为外接电源的负极
B.电解总反应:O+2H++2SO2- HO+S O2-
2 4 2 2 2 8
C.阴离子交换膜可用阳离子交换膜替代
D.电解池工作时,I室溶液质量理论上逐渐减小
【答案】C
【解析】S元素化合价由+6价升高为+7价,化合价升高被氧化,故右侧Pt电极为阳极,b为外接电
源正极,a为外接电源负极,左侧Pt电极为阴极。A项,a为外接电源的负极,A正确;B项,阴极氧气被
还原,阳极硫酸根被氧化,电解总反应正确,B正确;C项,根据阳极产物可知,反应需要消耗硫酸根,
阴离子交换膜不可用阳离子交换膜替代,C错误;D项,电解池工作时,I室溶液中氢离子移向阴极,硫酸
根移向阳极,消耗硫酸,I室溶液质量理论上逐渐减小,D正确;故选C。
5.(2024·江苏泰州高三期中)科学家利用氨硼烷设计成原电池装置如题图所示,常温下该电池总反应
为NH ·BH+3H O= NH BO+4H O。下列说法正确的是( )
3 3 2 2 4 2 2
A.b室为该原电池的负极区
B.放电过程中, 通过质子交换膜由b室移向a室
C.a室的电极反应式为NH ·BH+2H O-6e-=4NH++BO -+6H+
3 3 2 4 2
D.其他条件不变时,向HO 溶液中加入适量 溶液能增大电流强度
2 2
【答案】C【解析】氨硼烷中硼元素化合价升高,被氧化,是负极;过氧化氢中氧元素化合价降低,
被还原,是正极。A项,b室为过氧化氢溶液,是正极,A项错误;B项,放电时,氢离子是阳离子,向正
极移动,应有a室移向b室,B项错误;C项,a室为氨硼烷被氧化,失去电子,变成NH BO,C项正
4 2
确;D项,该电解质为酸性溶液,加入NaOH溶液不能增大电流强度,D项错误;故选C。
6.(2023·浙江省杭州地区(含周边)重点中学高三联考化)科学家利用多晶铜高效催化电解CO 制乙烯,
2
原理如图所示。已知:电解前后电解液浓度几乎不变。下列说法正确的是( )A.铂电极为阳极,产生的气体是O 和CO
2 2
B.铜电极的电极反应式为2CO+12HCO-+12e-=C H+12CO 2-+4H O
2 3 2 4 3 2
C.通电过程中,溶液中HCO -通过阴离子交换膜向右槽移动
3
D.当电路中通过0.6 mol电子时,理论上能产生C H1.12L
2 4
【答案】A
【解析】该电解池的总反应方程式为2CO+2H O=C H+3O ,铜电极为阴极,该电极的电极方程式为
2 2 2 4 2
14CO+8H O+12e-=C H+12HCO-,铂电极为阳极,该电极的电极方程式为12HCO --12e-
2 2 2 4 3 3
=12CO ↑+3O ↑+6H O。A项,铂电极为阳极,产生的气体是O 和CO,故A正确;B项,铜电极的电极方
2 2 2 2 2
程式为14CO+8H O+12e-=C H+12HCO-,故B错误;C项,HCO -在铂电极发生反应,并且电解前后电解
2 2 2 4 3 3
液浓度几乎不变,所以溶液中HCO -通过阴离子交换膜向左槽移动,故C错误;D项,由铜电极电极方程
3
式分析可知,当电路中通过0.6 mol电子时,理论上能产生0.05mol C H,在标况下,0.05molC H 的体积
2 4 2 4
为1.12L,该题目没有说明条件为标况,故D错误;故选A。
7.(2024·山东潍坊安丘市三区县高三过程性测试)西北工业大学推出一种新型Zn-NO 电池,通过自供
2
电实现NO -转化为NH ,装置如图所示。下列说法错误的是( )
2 3
A.b电极为原电池的正极
B.装置工作时c极区溶液的pH减小
C.d电极反应式为NO -+5H O+6e-=NH+7OH-
2 2 3
D.装置工作时,若消耗6.5gZn,理论上能得到0.03molNH
3
【答案】C
【解析】根据图知,左侧装置能自发的进行氧化还原反应,则该装置为原电池,Zn易失电子作负极,
b电极为正极,负极的电极反应式为:Zn-2e-=Zn2+,正极的电极反应式为:NO +e-=NO-,b连接石墨c,则
2 2
c为阳极,电极反应式为2HO-4e-=4H++O ↑,d为阴极,电极反应式为NO -+7H++6e-=NH+2H O。A项,根
2 2 2 3 2
据以上分析知,a、b和电解质溶液构成原电池,a为负极,则b为正极,故A正确;B项,c电极上HO失
2
电子生成O 和H+,电极反应式为2HO-4e-=4H++O ↑,有氢离子生成,反应中转移4mol电子同时有
2 2 2
4molH+通过质子交换膜进入d极区,氢离子的物质的量不变,但由于反应消耗水,溶液的pH值减小,故B正确;C项,氢离子由阳极通过质子交换膜进入阴极室,酸性条件下,d电极上NO -得电子生成NH ,
2 3
电极反应式为NO -+7H++6e-=NH+2H O,故C错误;D项,6.5gZn的物质的量为
2 3 2
,由Zn-2e-=Zn2+可知转移0.2mol电子,阴极的电极反应式为:NO -+7H++6e-=NH+2H O,理论上能得到
2 3 2
,故D正确;故选C。
8.(2023届·辽宁省鞍山市普通高中第一次质量监测)工业电解丙烯腈(CH=CHCN)制己二腈
2
[NC(CH )CN]的原理如图所示。相关说法正确的是( )
2 4
A.乙室电极反应:2HO-4e-=O ↑+4H+
2 2
B.该生产过程离子交换膜为阴离子交换膜
C.甲室碳棒为阳极,工作温度较高电极会有损失
D.生产中若收集 气体,转移电子
【答案】A
【解析】根据题意,该装置为电解池装置,依据装置图,乙室中有氧气产生,该电极反应式为2HO-4e-
2
=O ↑+4H+,根据电解原理,该电极为阳极,碳棒为阴极。A项,乙室中有氧气产生,根据电解原理,应是
2
OH-在该电极放电,即电极反应式为2HO-4e-=O ↑+4H+,故A正确;B项,丙烯腈转化成己二腈,其电极
2 2
反应式为2CH=CHCN+2H++2e-= NC(CH )CN,根据电极原理,H+由乙室向甲室移动,因此离子交换膜为
2 2 4
质子交换膜,故B错误;C项,根据上述分析,碳棒为阴极,故C错误;D项,题中没有指明是否是标准
状况,不能直接运用22.4L/mol进行计算,故D错误;故选A。
9.(2023届·安徽省蚌埠市高三第一次教学质量检查)铜基配合物电催化还原CO 的装置原理如图所示,
2
下列说法不正确的是( )
A.石墨烯为阳极,发生电极反应为CO+2e-+2H+=HCOOH
2
B.Pt电极附近溶液的pH值减小
C.每转移2mol电子,阳极室、阴极室溶液质量变化量的差值为28gD.该装置可减少CO 在大气中累积和实现可再生能源有效利用
2
【答案】A
【解析】A项,石墨烯为阴极,A错误;B项,Pt电极上HO失电子转化为O,电极反应为2HO-4e-
2 2 2
=4H++O ↑,所以电极附近溶液的pH减小,B正确;C项,每转移2mol电子,由阴极电极反应式可知生成
2
1molHCOOH,所以阴极室溶液| |=46g/mol×1mol=46g;根据阳极室反应可知每转移2mol电子时阳极消
m阴
耗1mol水,生成0.5mol氧气,同时有2molH+转移至阴极室,所以| |=18g/mol×1mol=18g,所以| ||
m阳 m阴
|=46g-18g=28g,C正确;D项,该装置可减少CO 在大气中累计和实现可再生能源有效利用,D正
m阳 2
确;故选A。
10.(2023届·广东省深圳市光明区一模)某科研小组利用下图装置完成乙炔转化为乙烯的同时为用电器
供电。其中锌板处发生的反应有:①Zn-2e-=Zn2+;②Zn2++4OH-=[Zn((OH) ]2-;③Zn [Zn((OH) ]2-
4 4
=ZnO+2OH-+H O。下列说法不正确的是( )
2
A.电极a的电势高于电极b的电势
B.放电过程中正极区KOH溶液浓度保持不变
C.电极a上发生的电极反应式为C H+2H O+2e-=C H+2OH-
2 2 2 2 4
D.电解足量CuSO 溶液,理论上消耗2.24L(标准状况)C H 时,生成6.4gCu
4 2 2
【答案】B
【解析】由题干可知,锌板处Zn失电子生成Zn2+,为原电池负极,则气体扩散电极a为正极。正极上
C H 得电子与水反应生成C H。A项,由图可知锌板为负极,所以电极a的电势高于电极b的电势,A正
2 2 2 4
确;B项,放电过程中正极区消耗水,导致KOH溶液浓度增大,B错误;C项,电极a上发生的电极反应
式为C H+2H O+2e-=C H+2OH-,C正确;D项,电解硫酸铜时,生成铜的电极反应为Cu2++2e-=Cu,理论
2 2 2 2 4
上消耗2.24LCH(标准状况),即0.1mol,对应电子转移0.2mol,可生成铜6.4g,D正确;故选B。
2 2
11.(2024·山东德州高三期中)我国科学家设计的耦合光催化、电催化分解水的装置如图所示,光照
时,光催化电极产生电子(e-)和空穴(h+)。下列有关说法错误的是( )A.气体X为氢气,气体Y为氧气
B.离子交换膜为阳离子交换膜
C.光催化装置中生成I-的反应为3I - +2h+=I -
3 3
D.每分解0.01molHO光催化装置生成1.905gI-
2 3
【答案】D
【解析】由图可知,光催化装置发生氢离子得到电子发生还原反应:2H++2e-=H ↑、碘离子发生氧化反
2
应:3I - +2h+=I -;电催化装置为电解装置,阴极发生还原反应,电极式I-+2e-=3I-,阳极发生氧化反应,反
3 3
应式为4OH - +4h+= 2HO+O↑。A项,由分析可知,气体X为氢气,气体Y为氧气,A正确; B项,电
2 2
催化装置为电解装置,阴极电极式I-+2e-=3I-,阳极反应式为4OH - +4h+= 2HO+O↑,阴极上阴离子物质
3 2 2
的量增大,阳极上消耗阴离子,根据装置图可知,阳离子迁移到左侧,离子交换膜为阳离子交换膜,B正
确;C项,光催化装置中生成I-的反应为3I - +2h+=I -,C正确;D项,光催化过程中,每分解0.01molHO
3 3 2
则转移0.02mol电子时,生成0.01molI -,质量为0.01mol×381g/mol=3.81g,D错误;故选D。
3
12.(2024·浙江省温州市普通高中高三一模)利用电化学富集海水中锂的电化学系统如图所示。该电化
学系统的工作步骤如下:
①启动电源1,MnO 所在腔室的海水中的Li+进入MnO 结构形成LiMn O;
2 2 2 4
②关闭电源1和海水通道,启动电源2,使LiMnO 中的Li+脱出进入腔室2。
x 2 4
下列说法不正确的是( )
A.启动电源1时,电极1为阳极,发生氧化反应
B.启动电源2时MnO 电极反应式为:2MnO +xLi++xe-=Li MnO
2 2 x 2 4
C.电化学系统提高了腔室2中LiOH的浓度
D.启动至关闭电源1,转化的n(MnO )与生成的n(O )之比为 ,可得LiMnO 中的x=1.2
2 2 x 2 4
【答案】B
【解析】由题意知,启动电源1,使海水中Li+进入MnO 结构形成LiMn O;可知二氧化锰中锰的化
2 2 4
合价降低,为阴极,电极反应式为2MnO +Li++e-=LiMn O,电极1为阳极,连接电源正极;关闭电源1和
2 2 4
海水通道,启动电源2,向电极2上通入空气,使LiMnO 中的Li+脱出进入室2,可知,电极2为阴极,
x 2 4
电极反应式:O+4e-+2H O=4OH-;阳极的电极反应式:LiMnO-xe-=2MnO+xLi+。A项,由分析知,室1
2 2 x 2 4 2
中电极1连接电源1的正极,作阳极,发生氧化反应,故A正确;B项,启动电源2时MnO 作阳极,电极
2
反应式:LiMnO-xe-=2MnO+xLi+,故B错误;C项,电化学系统提高了腔室2中LiOH的浓度,故C正
x 2 4 2
确;D项,根据分析可知,启动至关闭电源1,转化的n(MnO )与生成的n(O )之比为 ,可得LiMnO
2 2 x 2 4
中的x=1.2,故D正确;故选B。13.(2024·浙江省金华市十校选考模拟考试)海水原位直接电解制氢技术是利用海水侧和电解质侧的水
蒸气压力差使海水自然蒸发,并以蒸汽形式通过透气膜扩散到电解质侧重新液化,为电解提供淡水(工作时
KOH溶液的浓度保持不变)。装置如图所示,下列叙述不正确的是( )
A.M电极反应式为4OH―-4e-=O↑+2HO
2 2
B.该技术避免了生成强氧化性的含氯粒子腐蚀电极
C.离子交换膜b为阳离子交换膜
D.当产生标准状况下33.6L H 时,有1.5mol HO(g)透过透气膜a
2 2
【答案】C
【解析】A项,M极生成氧气,M是阳极,M电极反应式为4OH―-4e-=O↑+2HO,故A正确;B
2 2
项,氯离子不能通过透气膜a,所以该技术避免了生成强氧化性的含氯粒子腐蚀电极,故B正确;C项,
M为阳极、N为阴极,若离子交换膜b为阳离子交换膜,钾离子会向右移动,右侧氢氧化钾浓度增大,根
据题意,工作时KOH溶液的浓度保持不变,所以离子交换膜b为阴离子交换膜,故C错误;D项,当产
生标准状况下33.6L H 时,阴极生成氢气的物质的量为1.5mol,阳极生成氧气的物质的量为0.75mol,电解
2
水的物质的量为1.5,工作时KOH溶液的浓度保持不变,所以有1.5mol HO(g)透过透气膜a,故D正确;
2
故选C。
14.(2022·山东省威海市二模)工业上用石墨和铅作电极,用双极膜电解葡萄糖溶液制备甘露醇和葡萄
糖酸盐。已知在直流电场作用下,双极膜将水解离为H+和OH-并实现其定向通过,电解过程如图所示。下
列说法错误的是( )
A.b极材料为石墨,接电源正极
B.通电后双极膜中产生的OH-向b极定向移动
C.生成葡萄糖酸盐的反应为: +BrO -+OH-=HOCH (CHOH) COO-+Br-+H O
3 2 4 2
D.理论上若生成1mol甘露醇,则可生成1mol葡萄糖酸盐
【答案】C
【解析】图示原理为电解葡萄糖溶液制备甘露醇和葡萄糖酸盐。根据b电极反应可知溴离子失去电子
变成溴酸根,故b为阳极,电极反应为Br-+3H O+6e-=BrO -+6H+,在阳极区溴酸根和葡萄糖反应生成葡萄糖
2 3酸盐和溴离子,离子反应为:3 + BrO -+3OH-=3HOCH (CHOH) COO-+Br-+3H O,1mol溴酸
3 2 4 2
根生成溴离子转移电子数为6mol,故1mol葡萄糖生成葡萄糖酸盐转移电子数为2mol,双极膜中产生的氢
氧根向b电极移动。A项,b极为阳极,电极材料不参与反应,故材料为石墨,接电源正极,A正确;B
项,通电后双极膜中产生的OH-向b极(阳极)定向移动,B正确;C项,生成生成葡萄糖酸盐的反应为:3
+BrO -+3OH-=3HOCH (CHOH) COO-+Br-+3H O,C错误;D项,阴极区发生的反应为葡萄
3 2 4 2
糖转变为甘露醇,理论上若生成1mol甘露醇,需消耗1mol葡萄糖,转移2mol电子,在阳极区可生成
1mol葡萄糖酸盐,D正确;故选C。
15.(2022·山东师范大学附中模拟预测)天津大学研究团队以KOH溶液为电解质,CoP和Ni P纳米片
2
为催化电极材料,电催化合成偶氮化合物( )的装置如图所示(R代表烃基)。下列说法不正确的
是( )
A.若用铅蓄电池作为电源,CoP极连接铅蓄电池的铅电极
B.离子交换膜是阴离子交换膜
C.偶氮化合物具有顺反异构体,合成1mol物质,需转移4mol电子
D.Ni P电极反应式为RCHNH —4e—+4OH—= RCN+4HO
2 2 2 2
【答案】C
【解析】由图可知,该装置为电解池,与直流电源负极相连的CoP电极为电解池的阴极,在水分子作
用下硝基苯在阴极得到电子发生还原反应生成 和氢氧根离子,电极反应式为2 +8e—+4H O= +8OH—,Ni P电极为阳极,碱性条件下RCHNH 在阳极失去电子发生氧化反应生成
2 2 2 2
RCN和水,电极反应式为RCHNH —4e—+4OH—= RCN+4HO,电解过程中氢氧根离子通过阴离子交换膜
2 2 2
从左侧阴极室向右侧阳极室移动。A项,该装置为电解池,与直流电源负极相连的CoP电极为电解池的阴
极,则若用铅蓄电池作为电源,CoP极连接铅蓄电池的负极铅电极,故A正确;B项,装置中的离子交换
膜是阴离子交换膜,故B正确;C项,由结构简式可知,偶氮化合物中不饱和氮原子上只连有苯环1个取
代基,不可能存在顺反异构体,由分析可知,合成1mol偶氮化合物,需转移8mol电子,故C错误;D
项,Ni P电极为阳极,碱性条件下RCHNH 在阳极失去电子发生氧化反应生成RCN和水,电极反应式为
2 2 2
RCHNH —4e—+4OH—= RCN+4HO,故D正确;故选C。
2 2 2
16.有一种将乙烯高效转化为环氧乙烷的电化学合成方法,如图所示。反应在KCl电解液的流动池中
进行,电解结束后,将阴阳极电解液输出混合,便可生成环氧乙烷。下列说法正确的是( )
A.泡沫镍电极附近溶液pH减小
B.通电时,图中阴离子从上往下迁移通过阴离子交换膜
C.用该方法制备环氧乙烷的过程总反应为CH=CH +HOCl→ +HCl
2 2
D.当电路中通过2mol电子时,泡沫镍电极上会产生22.4L气体(标准状况)
【答案】D
【解析】由题干信息可知,铂电极上Cl-失电子转化为Cl,铂电极为阳极,阳极反应式为2Cl--2e-
2
=Cl,溶液中发生反应Cl+H O HCl+HOCl,C H+HOCl→HOCH CHCl,ClCH CHOH+OH-
2 2 2 2 4 2 2 2 2
+Cl-+H O,阳极区总反应式为C H-2e-+2OH-→ +H O,镍电极为阴极,阴极反应式为2HO+2e-
2 2 4 2 2
=H ↑+2OH-,制备的总反应式为CH=CH +H O +H ↑。A项,镍电极为阴极,阴极反应式为
2 2 2 2 2
2HO+2e-=H ↑+2OH-,有OH-生成,泡沫镍电极附近溶液pH增大,A错误;B项,铂电极为阳极,镍电极
2 2
为阴极,阴极反应式为2HO+2e-=H ↑+2OH-,阳极溶液中发生反应ClCH CHOH+OH- +Cl-+H O
2 2 2 2 2
需要OH-,OH-从下往上迁移通过阴离子交换膜,B错误;C项,阳极区总反应式为C H-2e-+2OH-→
2 4+H O,阴极反应式为2HO+2e-=H ↑+2OH-,制备的总反应式为CH=CH +H O +H ↑,C错误;D
2 2 2 2 2 2 2
项,当电路中通过2mol电子时,根据电子转移守恒可知,泡沫镍电极上生成氢气为1mol,标准状况下氢
气体积是22.4L,D正确;故选D。
17.(2023届·湖南省长沙一中高三模拟)双极膜电渗析法制备缩水甘油( )的原理:将3-
氯-1,2-丙二醇的水溶液通过膜M与双极膜之间的电渗析室,最终得到的缩水甘油纯度很高(几乎不含无机
盐)。已知:由一张阳膜和一张阴膜复合制成的阴、阳复合膜为双极膜。在直流电场的作用下,双极膜复合
层间的HO解离成OH-和H+并分别通过阴膜和阳膜。下列说法正确的是( )
2
A.装置工作时,3-氯-1,2-丙二醇被氧化
B.通电后,电渗析室内溶液的pH变小
C.膜M为阳离子交换膜
D.装置工作时,阴极上发生的电极反应:2H++2e-=H ↑
2
【答案】D
【解析】根据电荷迁移方向确定双极膜中移向3-氯-1,2-丙二醇的水溶液的只能是带负电荷的OH-,
→ +HCl,OH-中和H+生成HO,Cl-经过膜M向阳极迁移,产品得以纯
2
化。3-氯-1,2-丙二醇未发生氧化还原反应,通电后,双极膜复合层间的HO解离成OH-和H+,OH-中和电
2
渗析室内生成的H+,阴极上H+得到电子生成H。A项,根据电荷迁移方向确定双极膜中移向3-氯-1,2-丙
2
二醇的水溶液的只能是带负电荷的OH-, → +HCl,OH-中和H+生成
HO,Cl-经过膜M向阳极迁移,产品得以纯化,而3-氯-1,2-丙二醇未发生氧化还原反应,A错误;B
2
项,通电后,双极膜复台层间的HO解离成OH-和H+,电渗析室内 →
2
+HCl,OH-中和生成的H+,电渗析室内溶液的pH几乎不变,B错误;C项,电渗析室内产生的Cl-经过膜M向阳极迁移,膜M为阴离子交换膜,C正确;D项,装置工作时,阴极上发生的电极反应为氢离子得到
电子生成氢气,反应为:2H++2e-=H ↑,D正确;故选D。
2
18.(2023届·湖南省益阳市高三教学质量调研)锂离子电池具有质量小、体积小、储存和输出能量大等
特点,是多种便携式电子设备和交通工具的常用电池。一种锂离子电池的结构及工作原理如图所示,电解
质溶液为LiPF (六氟磷酸锂)的碳酸酯溶液(无水)。下列说法错误的是( )
6
A.放电时电极a为电池的正极,充电时电极b作阳极
B.放电时负极反应式为:LiC -xe-=xLi++C
x y y
C.电池放电时总反应为:LiC + Li CoO=LiCoO+C
x y 1-x 2 2 y
D.放电充电时,锂离子往返于电池的正极负极之间,完成化学能与电能的相互转化
【答案】A
【解析】根据图中信息可知,放电时阳离子Li+向电极a移动,则电极a为正极,则电极b为负极,当充
电时,电极b为阴极,电解时Li+向阴极移动。A项,根据图中信息可知,放电时阳离子Li+向电极a移
动,则电极a为正极,则电极b为负极,当充电时,电极b为阴极,A错误;B项,放电时电极b为负极,
负极上LiC 失电子产生Li+和C ,电极反应式为LiC -xe-=xLi++C ,B正确;C项,电池放电时正极反应式
x y y x y y
为Li CoO+xe-+xLi+=LiCoO,结合选项B可知,总反应为:LiC + Li CoO=LiCoO+C ,C正确;D项,
1-x 2 2 x y 1-x 2 2 y
根据图中信息可知,放电充电时,锂离子往返于电池的正极负极之间,完成化学能与电能的相互转化,D
正确;故选A。
题型二 “双膜”池
1.(2024·黑龙江省龙东五地市高三联考)一种成本低、稳定性好的全碱性多硫化物-空气液流二次电池
工作时,原理如图所示,下列说法错误的是( )A.膜a为阳离子交换膜,膜b为阴离子交换膜
B.连接负载时,X极的电极反应式为2S2--2e-=S 2-
2 4
C.连接电源时,Ⅰ室的 数目增加
D.连接电源时,电路中每通过 电子,生成 的质量为20g
【答案】D
【解析】由图可知,连接负载时,该装置为原电池,X极为负极,S2-在负极失去电子发生氧化反应生
2
成S2-,溶液中钠离子通过阳离子交换膜进入Ⅱ室,Y极为正极,氧气在正极得到电子发生还原反应生成氢
4
氧根离子,溶液中氢氧根离子通过阴离子交换膜进入Ⅱ室;连接电源时,该装置为电解池,与直流电源负
极相连的X极为阴极、Y极为阳极。A项,由分析可知,膜a为允许钠离子通过的阳离子交换膜,膜b为
允许氢氧根离子通过的阴离子交换膜,故A正确;B项,连接负载时,该装置为原电池,X极为负极,S2-
2
在负极失去电子发生氧化反应生成S2-,电极反应式为2S2--2e-=S 2-,故B正确;C项,连接负载时,Ⅰ室
4 2 4
溶液中钠离子通过阳离子交换膜进入Ⅱ室,则连接电源时,该装置为电解池,Ⅱ室溶液中钠离子通过阳离
子交换膜进入Ⅰ室,溶液中钠离子数目增加,故C正确;D项,连接负载时,Ⅰ室溶液中钠离子通过阳离
子交换膜进入Ⅱ室,正极区溶液中氢氧根离子通过阴离子交换膜进入Ⅱ室,则连接电源时,该装置为电解
池,Ⅱ室溶液中钠离子通过阳离子交换膜进入Ⅰ室,溶液中氢氧根离子通过阴离子交换膜进入阳极区,Ⅱ
室没有氢氧化钠生成,而是消耗氢氧化钠,故D错误;故选D。
2.(2023届·江苏省南通市高三期初教学质量调研)一种水性电解液Zn-MnO 离子选择双隔膜电池如下图
2
所示。(已知在KOH溶液中,Zn2+以Zn(OH )2-存在)。下列叙述不正确的是( )
4
A.放电时Zn作负极
B.a为阳离子交换膜,b为阴离子交换膜
C.放电时MnO 电极上发生的反应:MnO +4H++2e- =Mn2++2H O
2 2 2
D.电路中每通过1 mol电子,Zn电极的质量减小32.5g
【答案】B
【解析】根据题意可知,此装置为原电池,Zn为负极,发生氧化反应,电极反应为Zn-2e-+4OH-=
Zn(OH )2-,负极区K+剩余,通过隔膜迁移到II区;MnO 电极为正极,发生还原反应:MnO +2e-
4 2 2
+4H+=Mn2++2H O,正极区SO 2-过量,通过隔膜迁移到II区,故II区中KSO 溶液的浓度增大。A项,Zn
2 4 2 4
为负极,发生氧化反应,电极反应为Zn-2e-+4OH-= Zn(OH ) 2-,故A正确;B项,I区的SO 2-通过隔膜向Ⅱ
4 4
区迁移,a为阴离子交换膜,K+从III区通过隔膜迁移到II区,b为阳离子交换膜,故B错误;C项,MnO
2
电极做正极,电极反应为:MnO +4H++2e-═Mn2++2H O,故C正确;D项,Zn电极反应式为Zn-2e-+4OH-=
2 2
Zn(OH )2-,所以电路中通过1 mol电子,负极锌溶解的质量为0.5×65=32.5g,故D正确;故选B。
4
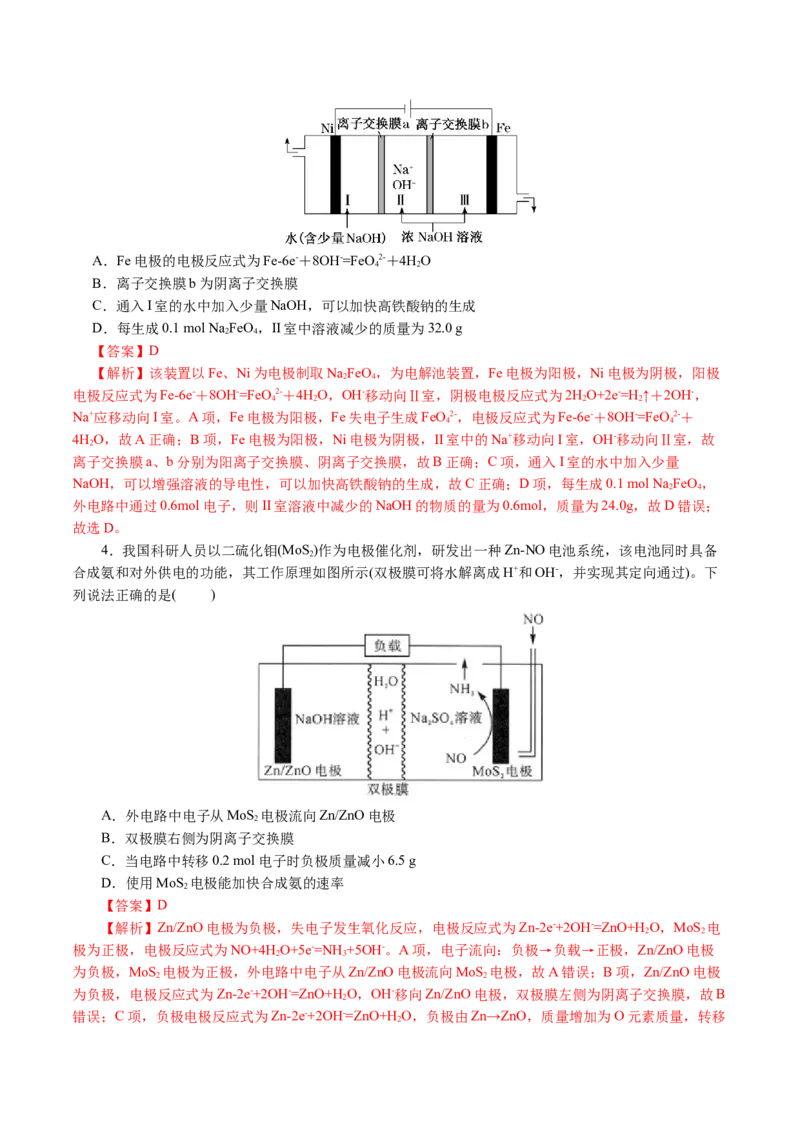
3.(2023届·辽宁省沈阳市第一二〇中学高三模拟)高铁酸钠(Na FeO)是一种新型的消毒剂,以Fe、Ni
2 4
为电极制取NaFeO 的原理如图所示。下列叙述错误的是( )
2 4A.Fe电极的电极反应式为Fe-6e-+8OH-=FeO 2-+4HO
4 2
B.离子交换膜b为阴离子交换膜
C.通入I室的水中加入少量NaOH,可以加快高铁酸钠的生成
D.每生成0.1 mol Na FeO,II室中溶液减少的质量为32.0 g
2 4
【答案】D
【解析】该装置以Fe、Ni为电极制取NaFeO,为电解池装置,Fe电极为阳极,Ni电极为阴极,阳极
2 4
电极反应式为Fe-6e-+8OH-=FeO 2-+4HO,OH-移动向Ⅱ室,阴极电极反应式为2HO+2e-=H ↑+2OH-,
4 2 2 2
Na+应移动向I室。A项,Fe电极为阳极,Fe失电子生成FeO2-,电极反应式为Fe-6e-+8OH-=FeO 2-+
4 4
4HO,故A正确;B项,Fe电极为阳极,Ni电极为阴极,II室中的Na+移动向I室,OH-移动向Ⅱ室,故
2
离子交换膜a、b分别为阳离子交换膜、阴离子交换膜,故B正确;C项,通入I室的水中加入少量
NaOH,可以增强溶液的导电性,可以加快高铁酸钠的生成,故C正确;D项,每生成0.1 mol Na FeO,
2 4
外电路中通过0.6mol电子,则II室溶液中减少的NaOH的物质的量为0.6mol,质量为24.0g,故D错误;
故选D。
4.我国科研人员以二硫化钼(MoS )作为电极催化剂,研发出一种Zn-NO电池系统,该电池同时具备
2
合成氨和对外供电的功能,其工作原理如图所示(双极膜可将水解离成H+和OH-,并实现其定向通过)。下
列说法正确的是( )
A.外电路中电子从MoS 电极流向Zn/ZnO电极
2
B.双极膜右侧为阴离子交换膜
C.当电路中转移0.2 mol电子时负极质量减小6.5 g
D.使用MoS 电极能加快合成氨的速率
2
【答案】D
【解析】Zn/ZnO电极为负极,失电子发生氧化反应,电极反应式为Zn-2e-+2OH-=ZnO+H O,MoS 电
2 2
极为正极,电极反应式为NO+4H O+5e-=NH+5OH-。A项,电子流向:负极→负载→正极,Zn/ZnO电极
2 3
为负极,MoS 电极为正极,外电路中电子从Zn/ZnO电极流向MoS 电极,故A错误;B项,Zn/ZnO电极
2 2
为负极,电极反应式为Zn-2e-+2OH-=ZnO+H O,OH-移向Zn/ZnO电极,双极膜左侧为阴离子交换膜,故B
2
错误;C项,负极电极反应式为Zn-2e-+2OH-=ZnO+H O,负极由Zn→ZnO,质量增加为O元素质量,转移
20.2 mol电子时增加0.1mol氧原子,负极质量增加m=nM=0.1mol×16g/mol=1.6 g,故C错误;D项,结合提
示,科研人员以二硫化钼MoS 作为电极催化剂,催化剂可以降低反应活化能,加快合成氨的反应速率,
2
故D正确;故选D。
5.双极膜电渗析法制疏基乙酸(HSCH COOH)和高纯度NaOH溶液的原理如图所示,其中a,b为离子
2
交换膜,双极膜在直流电压下可解离出H+和OH-。
已知:双极膜复合层间 HO能解离为H+和OH-,且实现H+和OH-的定向通过。下列说法正确的是
2
( )
A.M极连接电源的正极,电极反应式为2HO-4e-=4H++O↑
2 2
B.膜a和膜b均为阳离子交换膜,Na+经膜a由盐室移向碱室1
C.电解一段时间后,碱室2中NaOH溶液浓度变大
D.若将盐室中原料换成NaSO 溶液,当外电路中通过2mol e-时,可生成2molH SO
2 4 2 4
【答案】C
【解析】根据双极膜中H+和OH-的移动方向知,左侧为阴极,故M极连接电源的负极,N极连接电源
的正极。A项,根据双极膜中H+和OH-的移动方向知,M极连接电源的负极,其电极反应式为2HO+2e-=
2
2OH-+H↑,A错误;B项,根据题意分析可知,膜a和膜b均为阳离子交换膜,盐室中Na+经膜a由盐室
2
移向碱室l,碱室1中产生OH-,使碱室1中NaOH溶液浓度变大,碱室2中Na+经膜b移向纯水室生成
NaOH溶液,B正确;C项,由B项分析知,碱室2中NaOH溶液浓度变小,C错误;D项,外电路有
2mol电子通过时,盐室中有2mol Na+移向碱室1,双极膜中有2molH+移向盐室,即得到1molH SO ,D错
2 4
误。故选C。
6.(2024·山东省普通高中高三联合质量测评)利用热再生氨电池可实现(CuSO 电镀废液的浓缩再生,
4
同时利用该电池电解NaSO 溶液(a、b电极均为石墨电极),可以制得O、H、HSO 和NaOH装置如图所
2 4 2 2 2 4
示,甲、乙两室均预加相同的CuSO 电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是(
4
)
A.隔膜为阳离子膜
B.当电路中转移2mol电子时,1mol SO 2-通过膜d向右移动
4
C.电池总反应为:Cu 2++4NH=[Cu(NH )]2+
3 3 4
D.M、P、X、Y对应的物质分别是稀硫酸、稀NaOH溶液、H、O
2 2【答案】C
【解析】向甲室加入足量氨水后电池开始工作,则甲室电极溶解,铜失去电子发生氧化反应变为铜离
子与氨气形成[Cu(NH )]2+,Cu -2e- +4NH=[Cu(NH )]2+,因此甲室电极为负极,乙室电极为正极。A项,硫
3 4 3 3 4
酸根离子向通过隔膜向负极移动,进入甲室,则隔膜为阴离子膜,A错误;B项,b为阴极,电解池中阴
离子向阳极移动,B错误;C项,左侧负极是Cu -2e- +4NH=[Cu(NH )]2+,正极铜极上铜离子得到电子发生
3 3 4
还原反应生成铜:Cu2+ -2e- =[Cu,则电池总反应为:Cu 2++4NH=[Cu(NH )]2+,C正确;D项,结合分析可
3 3 4
知,Y为阴极,X为阳极,该装置为电解硫酸钠的装置,在阳极产生氧气和硫酸,在阴极产生氢气和氢氧
化钠,D错误;故选C。
7.(2024·浙江省宁波市高三选考模拟考试)电解硫酸钠溶液制取电池正极材料 的前驱
体 ,其工作原理如图所示:
下列说法不正确的是( )
A.a是直流电源的正极,石墨电极发生氧化反应
B.交换膜A是阴离子交换膜,通电一段时间,Ⅰ室pH降低
C.当产生 的 时,标准状况下纯钛电极上至少产生 气体
D.若将纯钛电极直接放入Ⅱ室,则纯钛电极上会有金属与前驱体附着而使产率降低
【答案】C
【解析】由图可知,前驱体在III室生成,则II室的金属阳离子进入III室,交换膜B为阳离子交换
膜,则右侧纯钛电极为阴极,电极反应式为2HO+2e-=H ↑+2OH-,OH-与金属阳离子结合得到前驱体,为
2 2
保持电荷守恒,交换膜A为阴离子交换膜,左侧石墨电极为阳极,电极反应式为2HO-4e-=O ↑+4H+,所以
2 2
电解过程实际上是电解水。A项,石墨为阳极,发生氧化反应,则a为电源的正极,故A正确;B项,交
换膜A为阴离子交换膜,左侧电极反应式为2HO-4e-=O ↑+4H+,产生H+,故pH降低,故B正确;C项,
2 2
每生成0.1mol的 ,就相当于生成0.2mol OH-,由电极反应式2HO+2e-=H ↑+2OH-可知,
2 2
会生成0.1mol H ,在标准状况下的体积为2.24L,故C错误;D项,纯钛电极若直接放入II室,会导致接
2
受电子的物质不是水而是金属离子,导致金属单质的生成,附着在前驱体上导致产率的降低,故D正确;
故选C。
题型三 “多膜”池
1.(2023届·湖南省永兴县第一中学高三模拟)一种电解法制备Ca(HPO ) 并得到NaOH等副产物的示意
2 4 2
装置如图,下列说法正确的是( )A.与a、b相连的分别是电源的负极、正极
B.NaOH溶液中石墨电极上的反应为2HO+2e-=H ↑+2OH-
2 2
C.A膜、C膜均为阴离子交换膜,B膜为阳离子交换膜
D.产品室中的Ca2+和原料室的 物质的量浓度同等程度增大
【答案】B
【解析】由图可知,产品Ca(HPO ) 在产品室生成,左侧石墨作阳极,氯离子放电,电极反应式为
2 4 2
2Cl--2e-=Cl↑,阳极室的Ca2+透过A膜进入产品室,A膜为阳离子交换膜,HPO -透过B膜进入产品室与
2 2 4
Ca2+结合生成Ca(HPO ),B膜为阴离子交换膜,右侧石墨极为阴极,水放电,电极反应式为2HO+2e-
2 4 2 2
=H ↑+2OH-,Na +透过C膜进入阴极室,C膜为阳离子交换膜。A项,左侧电极为阳极,应连接电源正极,
2
即a、b相连的分别是电源的正极、负极,故A错误;B项,右侧石墨极为阴极,水放电,电极反应式为
2HO+2e-=H ↑+2OH-,故B正确;C项,A膜、C膜为阳离子交换膜,B膜为阴离子交换膜,故C错误;D
2 2
项,阳极室的Ca2+透过A膜进入产品室,产品室中的Ca2+离子浓度增大,Na+透过C膜进入阴极室,原料
室的Na+浓度减小,故D错误;故选B。
2.(2023届·河北省曲阳县第一高级中学高三模拟)目前,应用电渗析法进行海水淡化是解决淡水资源医
乏的有效途径之一,该方法是利用电解原理通过多组电渗析膜实现,工作原理如图所示(以NaCl溶液代替
海水),同时获得产品Cl、H、NaOH。下列说法正确的是( )
2 2
A.a是直流电源的负极
B.阳极区溶液浓度几乎不变
C.膜pq、st分别为阳离子交换膜、阴离子交换膜
D.出口I、II分别接收NaCl浓溶液、淡水
【答案】B
【解析】由图可知,N极生成氢气,说明为氢离子放电发生还原反应,为电解池阴极,则M为阳极。A
项,a连接阳极,是直流电源的正极,A错误;B项,阳极区反应为2Cl--2e-=Cl↑,I中氯离子通过阴离子
2
膜pq进入阳极区,溶液浓度几乎不变,B正确;C项,I中氯离子通过阴离子膜pq进入阳极区,钠离子通
过阳极膜st进入阴极区,C错误;D项,I中氯离子向左侧运动,钠离子向右侧运动,氯化钠溶液浓度减
小,使I口对应区域形成淡水,II口对应区域形成NaCl浓溶液,D错误;故选B。
3.(2022·浙江省五校高三联考)双极膜电解法制巯基乙酸(HSCH COOH)和高纯NaOH溶液原理如图所
2示,其中a、b为离子交换膜,双极膜在直流电压下可解离出H+和OH-。下列说法正确的是( )
A.膜a和膜b均为阳离子交换膜
B.双极膜解离出的H+在双极膜的右侧
C.碱室1和碱室2的NaOH溶液可以循环使用,电解过程不产生其他副产物
D.若将盐室的原料换成NaSO 溶液,当外电路通过2mole-时,可生成2molH SO
2 4 2 4
【答案】A
【解析】根据装置图,该装置为电解池装置,根据电解原理,左边电极为阴极,电极反应式为
2HO+2e-=H ↑+2OH-,HSCH COONa中Na+向阴极移动,膜a为阳离子交换膜,右边电极为阳极,电极反
2 2 2
应式为4OH--4e-=O ↑+2H O,碱室2中Na+向左移,膜b为阳离子交换膜。A项,根据上述分析,膜a、b均
2 2
为阳离子交换膜,故A说法正确;B项,根据上述分析,双极膜解离出的H+在双极膜的左侧,故B说法错
误;C项,根据上述分析,碱室1和碱室2的NaOH溶液循环使用,副产品还有氢气和氧气,故C说法错
误;D项,外电路有2mol电子通过,盐室中有2molNa+移向碱室1,双极膜中有2molH+移向盐室,即得到
1molH SO ,故D说法错误;故选A。
2 4
4.我国力争2030年前实现碳达峰,2060年前实现碳中和。某高校研究团队提出,利用TiO 基催化剂
2
光催化还原CO 转化为甲醇(CHOH),并利用利用双极膜电渗析法制取盐酸和氢氧化钠的装置如下图所
2 3
示。下列说法不正确的是( )
A.电极c的电势高于电极d的电势
B.N表示阴离子交换膜
C.甲室流出的为盐酸溶液
D.相比现有氯碱工业制取氢氧化钠,该方法更环保
【答案】C
【解析】据图分析,电极c由CO 转化为CHOH,碳元素化合价降低,为原电池的正极,电极 d是
2 3
HO中杨转化为O ,氧元素化合价升高,为电池的负极。A项,如图分析,电极c由CO 转化为CHOH,
2 2 2 3
碳元素化合价降低,为原电池的正极,电极d是HO中杨转化为O ,氧元素化合价升高,为电池的负极,
2 2
正极电极比负极高,A正确;B项,由图可知,左边石墨为阴极,右边石墨为阳极,电流方向由右向左,
阳离子方向由右向左,阴离子方由左向右。氯离子由乙室向丙室迁移,N为阴离子交换膜,B正确; C项,钠离子由乙室向甲室迁移,OH-由双极膜向甲室迁移,甲室流出的为氢氧化钠溶液,C错误;D项,相
比现有氯碱工业制取氢氧化钠,该方法无氯气产生,更环保,D正确;故选C。
5.一种双阴极微生物燃料电池装置如图所示。该装置可以同时进行硝化和反硝化脱氮,下列叙述正
确的是( )
A.电池工作时,H+的迁移方向:左→右
B.电池工作时,“缺氧阴极”电极附近的溶液pH减小
C.“好氧阴极”存在反应:NH +-6e-+ 8OH-=NO-+ 6H O
4 2 2
D.“厌氧阳极”区质量减少28.8g时,该电极输出电子2.4mol
【答案】D
【解析】如图所示,“厌氧阳极”上,C H O 失去电子生成CO 和H+,电极反应式为
6 12 6 2
C H O+6H O-24e-=6CO ↑+24H+;“缺氧阴极”上,NO -得到电子生成NO ,NO 再转化为N,电极反应
6 12 6 2 2 3 2 2 2
式分别为:NO -+e-+2H+=NO↑+H O,2NO +8e-+8H+=N ↑+4H O;“好氧阴极”上,O 得到电子生成HO,
3 2 2 2 2 2 2 2
电极反应式为O+4H++4e-=2H O,同时O 还能氧化NH +生成NO -,NO -还可以被O 氧化为NO -,反应方
2 2 2 4 2 2 2 3
程式分别为2 NH++3O =2 NO -+2H O+4H+,2 NO-+O =2 NO -。A项,电池工作时,“厌氧阳极”失去的
4 2 2 2 2 2 3
电子沿外电路流向“缺氧阴极”和“好氧阴极”,则“厌氧阳极”产生的H+通过质子交换膜向“缺氧阴
极”和“好氧阴极”迁移,故H+的迁移方向既有左(“厌氧阳极”)→右(“好氧阴极”),又有右(“厌氧阳
极”)→左(“缺氧阴极”),A错误;B项,电池工作时,“缺氧阴极”上消耗H+,其附近的溶液pH增大,
B错误;C项,“好氧阴极”上的反应有O+4H++4e-=2H O,2 NH++3O =2 NO -+2H O+4H+,2 NO-+O =2
2 2 4 2 2 2 2 2
NO -,C错误;D项,“厌氧阳极”的电极反应式为C H O+6H O-24e-=6CO ↑+24H+,每1mol C H O 反
3 6 12 6 2 2 6 12 6
应,消耗6mol HO,转移24mol电子,“厌氧阳极”区质量减少288g,故“厌氧阳极”区质量减少28.8g
2
时,该电极输出电子2.4mol,D正确;故选D。
6.使用交替排列的单价选择性阳离子交换膜和阴离子交换膜的电渗析过程如图所示。电渗析分离离
子的原理是单价阳离子(例如:Li+、Na+、K+)通过单价选择性阳离子交换膜迁移到浓缩室,而二价阳离子
(例如:Ca2+、Mg2+)被阻挡,留在脱盐室,达到富集锂的目的。下列说法错误的是( )
A.电极W连接电源正极,电极N连接电源负极B.X口流出的是富Li+盐水,Y口流出的是贫Li+盐水
C.选择性离子交换膜是电渗析技术应用于盐湖卤水提锂的关键
D.该电渗析过程总的电解方程式为2HO 2H↑+O ↑
2 2 2
【答案】B
【解析】A项,由图可知,Cl-向W电极方向移动,Li+向N电极方向移动,则W极是和电源正极相连
的阳极,N极是和电源负极相连的阴极,故A正确;B项,X口流出盐水所对应的两个交换膜之间,所含
的Li+通过单价选择性阳离子交换膜移向右边隔壁的两个膜之间,则X口流出的是贫Li+盐水,而Y口流出
盐水所对应的两个交换膜之间,则多了左边两个膜之间渗透移动过来的Li+,则Y口流出的是富Li+盐水,
故B错误;C项,通过对图分析,从盐湖卤水提锂,可利用图中的单价选择性阳离子交换膜和阴离子交换
膜通过电渗析法使盐湖卤水中所含的锂离子富集起来,然后再提取锂,故C正确;D项,从W电极和N
电极的产物结合电解池电极离子的放电顺序可知,W电极是OH-放电,N电极是H+放电,而OH-和H+均来
自水分子的电离,则整个电渗析过程中,被电解的是水,故D正确;故选B。
7.如图所示电解装置中,通电后Ⅱ室溶液底部 逐渐溶解,下列判断正确的是( )
A.a是电源的正极
B.通电一段时间后,向石墨电极Ⅱ附近滴加酚酞溶液,出现红色
C.随着电解的进行,Ⅰ室溶液的pH变大
D.当0.01mol Fe O 全溶解时,至少产生气体672mL(标准状况下测得)
2 3
【答案】C
【解析】通电后石墨电极Ⅱ室底部Fe O 逐渐溶解,说明石墨电极Ⅱ附近水电离的氢氧根离子放电产
2 3
生氢离子,为阳极,则电源b为正极,a为负极,石墨电极Ⅰ为阴极。A项,由分析可知,a是电源的负
极,故A错误;B项,石墨电极Ⅱ为阳极,电极反应式为2HO-4e-=O ↑+4H+,4H+向室Ⅱ移动需要一定时
2 2
间,所以石墨电极Ⅱ附近显酸性,滴加酚酞溶液,不变色,故B错误;C项,CuCl 溶液因水解显酸性,
2
随着电解的进行,Ⅰ室铜离子在阴极得电子生成铜单质,所以CuCl 溶液浓度变小,酸性减弱,pH增大,
2
故C正确;D项,Fe O 溶解的反应为Fe O+6H+=2Fe3++3H O,当0.01mol Fe O 完全溶解时,消耗氢离子
2 3 2 3 2 2 3
为0.06mol,根据阳极电极反应式2HO - 4e−=O ↑+ 4H+,产生氧气为0.015mol,体积为336mL (折合成标准
2 2
状况下),故D错误;故选C。
8.(2024·浙江省绍兴市高三选考科目诊断性考试)以四甲基氯化铵[(CH )NCl]水溶液为原料,利用光
3 4
伏并网发电装置制备四甲基氢氧化铵[(CH )NOH],下列叙述不正确的是( )
3 4A.a极电极发生还原反应
B.保持电流恒定,增大NaCl稀溶液浓度,制备(CH)NOH的反应速率增大
3 4
C.c为阳离子交换膜,d为阴离子交换膜
D.b极收集2.24L(标况)气体时,溶液中有0.4mol离子透过交换膜
【答案】B
【解析】据de池中浓度变化得出,钠离子从b极池通过e膜,氯离子从cd池通过d膜,由电解池中阳
离子向阴极移动,阴离子向阳极移动,则a为阴极,b为阳极,a与N型半导体相连,b与P型半导体相
连,所以N型半导体为负极,P型半导体为正极。A项,由题中信息可知,a为阴极,发生得电子的还原反
应,A正确;B项,保持电流恒定,则单位时间a极得到的电子数目是恒定的,增大NaCl的浓度,电极反
应的速率不变,B错误;C项,由题中图示信息可知, Cl-通过d膜,(CH)N+通过c膜,所以c膜为阳离
3 4
子交换膜,d为阴离子交换膜,C正确;D项,b极电极反应式为4OH--4e-=O ↑+2H O,收集氧气0.1mol
2 2
时,转移电子0.4mol,Na+离子通过e膜,Cl-通过d膜,(CH)N+通过c膜,这些离子均带1个单位电荷,
3 4
通过的离子的物质的量为0.4mol,D正确;故选B。