文档内容
题型 02 阿伏加德罗常数的判断
目录
【考向一】有关物质的量等基本概念和公式的规范应用................................................................................1
【考向二】一定物质中原子、中子、质子、电子等数目计算........................................................................4
【考向三】一定量的物质中化学键的计算........................................................................................................6
【考向四】有关特殊微观粒子的考查................................................................................................................9
【考向五】混合物中微粒数的计算..................................................................................................................11
【考向六】氧化还原反应中电子转移数目的计算..........................................................................................13
【考向七】物质转化中的隐含反应..................................................................................................................16
【考向八】溶液中微粒数的计算......................................................................................................................19
......................................................................................................................................21
【考向一】有关物质的量等基本概念和公式的规范应用
【典例1】N 为阿伏加德罗常数的值。下列说法错误的是_____________。
A
A.(2023·全国甲卷) 的 溶液中 的数目为
B.(2023·海南卷)5.6g铁粉与 的HCl的溶液充分反应,产生的气体分子数目为
C.(2023·浙江6月)向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
D.(2023·广东卷) 含有的共价键数目为
E.(2023·辽宁卷) 含 键数目为
F.(2022·全国甲卷)25℃、101kPa下,28L氢气中质子的数目为2.5N
A
G.(2021·天津卷)1L1mol/LHCl溶液中,HCl分子的数目为N
A
H.(2023·全国甲卷)标准状况下, 中电子的数目为
I.(2022·辽宁卷)pH=12的NaCO 溶液中OH-数目为0.01N
2 3 A
J.(2021·福建卷)1.12L C H 所含极性共价键的数目为0.2N
2 4 A
K.0.1mol·L-1 HClO 溶液中含有的H+数为0.1N
4 A
L.(2021·广东卷)11.2LNO与11.2LO 混合后的分子数目为N
2 A
M.(2022·浙江6月)11.2L乙烷和丙烯的混合气体中所含碳氢键数为3N
A
1.物质的量只能衡量微观粒子,必须指明具体粒子的种类或化学式。如1 molH和1 molNaCl。
2.物质的量是物理量,摩尔是物质的量的单位,不是物理量。
3.6.02×1023是个纯数值,没有任何物理意义,而阿伏加德罗常数(N )是指1 mol任何微粒所含的粒子
A
数,数值约为6.02×1023;N 6.02×1023/mol。
A
4.摩尔质量、相对原子(或分子)质量的含义不同,不是同一个物理量。二者单位也不同,摩尔质量的单位是g·mol-1或kg·mol-1,相对原子(或分子)质量的单位为1,当摩尔质量以g·mol-1为单位时,二者在
数值上相等。
5.对具体的物质,其摩尔质量是确定的,不随物质的量的多少而变化,也不随物质的聚集状态而变
化。
6.气体摩尔体积(22.4 L·mol-1)应用的“五大误区”
(1)使用“条件”是标准状况,即0 ℃、101 kPa,而不是常温、常压。
(2)使用对象必须是气体物质,可以是单一气体,也可以是混合气体。
标准状况下不是气体而又常在题中出现的物质有:水、苯、SO 、HF、CCl 、己烷、CS、CHCl 、
3 4 2 3
Br 、乙醇等。
2
(3)标准状况下的气体摩尔体积约为22.4 L·mol-1,其他条件下V 一般不是22.4 L·mol-1。
m
(4)22.4 L气体,在标准状况下的物质的量是1 mol,在非标准状况下,可能是1 mol,也可能不是1
mol。
(5)物质的质量、物质的量一定时,所含微粒数与物质处于何种条件无关。
如常温常压下32 g O 所含的原子数目是2N 。注意不要形成定势思维,看到“常温常压”就排除选
2 A
项。
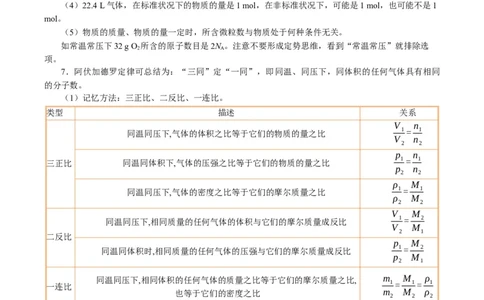
7.阿伏加德罗定律可总结为:“三同”定“一同”,即同温、同压下,同体积的任何气体具有相同
的分子数。
(1)记忆方法:三正比、二反比、一连比。
类型 描述 关系
V n
同温同压下,气体的体积之比等于它们的物质的量之比
1= 1
V n
2 2
p n
三正比 同温同体积下,气体的压强之比等于它们的物质的量之比
1= 1
p n
2 2
ρ M
同温同压下,气体的密度之比等于它们的摩尔质量之比
1= 1
ρ M
2 2
V M
同温同压下,相同质量的任何气体的体积与它们的摩尔质量成反比
1= 2
V M
2 1
二反比
p M
同温同体积时,相同质量的任何气体的压强与它们的摩尔质量成反比
1= 2
p M
2 1
同温同压下,相同体积的任何气体的质量之比等于它们的摩尔质量之比, m M ρ
一连比
1= 1= 1
也等于它们的密度之比 m M ρ
2 2 2
(2)应用阿伏加德罗定律推论时可通过pV=nRT及n=、ρ=导出。
8.必须能够算出某微粒的物质的量,才能判断其个数为多少N 。
A
(1)缺少体积,如常温下,pH=2的HSO 溶液中含有的H+数目为0.01N 。
2 4 A
(2)缺少温度压强,如由HO 制得2.24LO ,转移的电子数目为0.2N 。
2 2 2 A
(3)缺少具体反应,如1molCl 参加反应,转移电子数一定为2N 。
2 A
(4)概念的思维定势:等物质的量不能代替具体的物质的量。
【变式1-1】(2023-2024高三上·福建福州·期中)设N 为阿伏加德罗常数的值。下列叙述正确的是
AA.N 个P 分子与22.4 L甲烷(标准状况)分子所含共价键数目之比为1:1
A 4
B.N 个CO 分子中共用电子对的数目为2N
A 2 A
C.浓硝酸热分解生成NO 、NO 共23 g时,转移电子数为0.5N
2 2 4 A
D.0.1 mol/L KAl(SO ) 溶液中,Al3+的个数小于为0.1N
4 2 A
【变式1-2】(2023-2024高三上·山东烟台·期中) 为阿伏加德罗常数的值。下列说法正确的是
A. 与足量水反应,转移电子数为
B.标准状况下, 中氧原子的数目为
C. 的 溶液中 的数目为
D.标准状况下, 通入水中,溶液中氯离子数为
【考向二】一定物质中原子、中子、质子、电子等数目计算
【典例2】N 为阿伏加德罗常数的值。下列说法正确的是_____________。
A
A.(2023·全国卷)标准状况下, 中电子的数目为
B.(2023·广东卷) 和 的混合物中含 ,则混合物中质子数为
18
C.(2022·辽宁卷)1.8g O中含有的中子数为N
8 A
D.(2022·浙江6月)8g CH 含有中子数为3N
4 A
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3N
A
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6N
A
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18N
A
I.(2021·湖北卷)23gCHCHOH中sp3杂化的原子数为N
3 2 A
J.(2021·湖北卷)0.5molXeF 中氙的价层电子对数为3N
4 A
K.(2021·湖南卷)18gH18O含有的中子数为10N
2 A
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3N
A
M.(2021·海南卷)0.1mol肼(HN-NH )含有的孤电子对数为0.2N
2 2 A
N.(2021·全国甲卷)18g重水(DO)中含有的质子数为10N
2 A
1.常见的原子
1 12 14 16 35
符号
1H 6C 7N 8O 17Cl
2.质量数、质子数、中子数和电子数之间的数量关系
(1)质量数=质子数+中子数≈原子的相对原子质量
(2)质子数=各微粒原子序数之和
(3)中子数=各微粒中子数之和
(4)电子数=各微粒电子数之和±电荷数(5)电中性微粒:中子、原子、分子和取代基,质子数=电子数
3.1mol下列微粒所含的质子数、电子数及中子数
质子数 电子数 中子数
HO 10N 10N 8N
2 A A A
NH 10N 10N 7N
3 A A A
Na+ 11N 10N 12N
A A A
F- 9N 10N 10N
A A A
NH + 11N 10N 7N
4 A A A
OH- 9N 10N 8N
A A A
【变式2-1】(2023-2024高三上·黑龙江伊春·期中)用 表示阿伏加德罗常数的值,下列说法正确的是
A. 溶于水形成的氨水中质子数约为
B. 完全水解生成的 胶体粒子数目为
C.高温下,铁粉与水蒸气反应,固体的质量增加 ,则转移电子数目为
D.质量分数为46%的乙醇水溶液中所含氢原子数为
【变式2-2】(2023-2024高三上·浙江舟山·联考)设 为阿伏伽德罗常数的值,下列说法不正确的是
A.2 g H18O与D16O的混合物中所含中子、电子数目均为
2 2
B.42 g C H 最多含有σ键的数目为
6 12
C.22.4 L CO 与NaOH溶液完全反应,则
2
D.足量的浓盐酸与8.7 g MnO 反应,转移电子的数目为
2
【考向三】一定量的物质中化学键的计算
【典例3】 为阿伏加德罗常数的值。下列叙述正确的是
A.(2023·全国卷) 异丁烷分子中共价键的数目为
B.(2023·广东卷) 含有的共价键数目为
C.(2023·湖北卷)1molSi含Si-Si键的数目约为
D.(2023·辽宁卷) 含 键数目为
E.(2022·浙江卷)32g甲醇的分子中含有C—H键的数目为4N
A
F.(2022·浙江卷) 乙烷和丙烯的混合气体中所含碳氢键数为G.(2021·全国卷) 环状 ( )分子中含有的 键数为
1.化学键与物质类别的关系
(1)只含共价键的物质。
①同种非金属元素构成的单质,如I 、N 、P 、金刚石、晶体硅等;
2 2 4
②不同种非金属元素构成的共价化合物,如HCl、NH 、SiO 、CS 等。
3 2 2
(2)只含有离子键的物质:活泼非金属元素与活泼金属元素形成的化合物,如Na S、K O等。
2 2
(3)既含有离子键又含有共价键的物质:如Na O 、NH Cl、NaOH等。
2 2 4
(4)无化学键的物质:惰性气体等。
(5)碳碳双键中,存在一个σ键,一个π键,而碳碳三键中,存在一个σ键,两个π键。
2.物质的化学键
(1)某些特殊物质中所含化学键。
物质 白磷 金刚石/晶体硅 SiO 石墨
2
结构
化学键 P—P C—C/Si—Si Si—O C—C
化学键数 6 2 4 1.5
(2)苯:苯环中的碳碳键是介于单键和双键之间的一种独特的键,不含有碳碳双键,含有 6个C—
H。
(3)1 mol Na O、CaC 中含O 、C分别是1 mol。
2 2 2
(4)HO、C H 中化学键的数目为3、3n+1。
2 2 n 2n+2
(5)注意同分异构体中所含化学键数目可能不同。
结构式1 结构式2
C HO
2 6
碳碳键
1 0
数
碳氢键
5 6
数
碳氧键
1 2
数
(6)同一通式,连接方式不同,化学键数目不同。
C H 链状结构 环状结构
n 2n
碳碳单键数 n-2 n
碳碳双键数 1 0
碳氢单键数 2n 2n【变式3-1】(2023-2024高三上·湖南常德·阶段考)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.11 g的D18O中含有的中子数为5N
2 A
B.1 L pH=2的HSO 溶液中H+的数目为0.02N
2 4 A
C.将0.5 mol Cl 溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为N
2 A
D.标准状况下,2.24 L C H 和N 的混合气体中含有的π键数为0.2N
2 2 2 A
【变式3-2】(2023-2024高三上·重庆·期中)已知: , 为
阿伏加德罗常数的值。下列说法正确的是
A. 的 溶液中所含 数目为
B.1L 的 溶液中所含 的数目为
C.22.4L(标准状况下) 参加反应,转移的电子数目为
D.常温下,27g 中含有的共价键数目为
【考向四】有关特殊微观粒子的考查
【典例4】设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.(2022·浙江卷)1.8g重水(D O)中所含质子数为N
2 A
B.(2022·海南卷) 含有的中子数为1.3NA
C.(2022·辽宁卷) 中含有的中子数为
D.(2021·湖南卷) 含有的中子数为
E.(2021·湖北卷)0.5molXeF 中氙的价层电子对数为3N
4 A
F.(2021·海南卷) 中含有的共价键的数目为0.1
G.(2021·福建卷) 晶体中阴、阳离子总数为
此类题型要求同学们对物质的微观构成要非常熟悉,弄清楚微粒中相关粒子数(质子数、中子数、电子
数)及离子数、电荷数、化学键之间的关系。
先计算出一个物质中所含微观粒子数目,再根据题目条件计算出该物质的物质的量,进而计算出物质
中所含微观粒子数目的物质的量,最后根据微粒数、物质的量、N 三者之间的数学关系,确定微观粒子的
A
数目。
1.一些特殊微粒
(1)Ne:是单原子分子;
(2)臭氧(O )、白磷(P ):多原子分子中的原子个数;
3 4
(3)DO:H( H)、D( H)、T( H)三者中的中子数不同;
2(4)16O、17O、18O;16O、17O、18O;35Cl、37Cl中的中子数不同;
2 2 2
(5)NaO、NaO、KO 中的阴、阳离子个数比。
2 2 2 2
2.特殊的离子组成
(1)共价化合物中不含离子。
(2)固体离子化合物中含有离子,但不含自由离子。
(3)离子化合物XY 中所含的离子。
a b
非金属Y的价态 最低负价 非最低负价
所含离子 Xb+和Ya- Xb+和Ya-
b
(4)酸式盐在不同状态下所含离子。
不同状态 弱酸的酸式盐NaHCO 强酸的酸式盐NaHSO
3 4
固体 Na+和HCO - Na+和HSO -
3 4
熔融 Na+和CO2- Na+和HSO -
3 4
水溶液 Na+和HCO - Na+、H+和SO 2-
3 4
【变式4-1】(2023-2024高三上·天津·期中)设 为阿伏加德罗常数的值。下列有关叙述正确的是
A.10 g 60%的乙酸水溶液中含有的氧原子总数为0.2
B.常温常压下,15g甲基碳正离子( )所含的电子数为8
C.0.5 mol的 和 混合物中,所含阴离子数为
D.标准状况下,22.4 L 参加反应时,转移电子数为2
【变式4-2】(2023-2024高三上·黑龙江齐齐哈尔·期中)用 表示阿伏加德罗常数的值,下列叙述错误的
是
A.2.0g 与 的混合物中所含质子数、中子数均为
B.标准状况下,11.2L 中含有S原子的数目为
C.1mol 中含阴、阳离子总数为
D.浓硝酸受热分解生成 、 共23g,转移电子数为
【考向五】混合物中微粒数的计算
【典例5】用 表示阿伏加德罗常数的值,下列叙述错误的是
A.(2023·广东卷) 和 的混合物中含 ,则混合物中质子数为
B.(2022·浙江卷) 乙烷和丙烯的混合气体中所含碳氢键数为
C.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
D.(2021·湖南卷) 与 在密闭容器中充分反应后的分子数为
E.(2021·浙江卷)CH 和C H 混合气体2.24L(标准状况)完全燃烧,则消耗O 分子数目为0.25N
4 2 4 2 A1.若物质为混合物,先求混合物中各物质的最简式。
(1)若最简式相同,可先求最简式的物质的量,然后求解目标粒子数目。
(2)若最简式不同,可先计算两物质的摩尔质量是否相同,当摩尔质量相同时,可先求两物质的总
物质的量,然后求解目标粒子的数目。
如:14 g乙烯与丙烯中所含的碳原子数为N ;22 g CO 和NO 混合物中所含的原子数为1.5N ;常考
A 2 2 A
查的还有O 和O,NO 和NO 等。
2 3 2 2 4
2.若混合气体能发生反应且反应可逆,因为可逆反应进行不完全,当没给出转化率时,不能求出准确
的目标粒子数目。
【变式5-1】(2023-2024高三上·辽宁丹东·期中)“天宫一号”和“神舟八号”是我国航天事业发展的里
程碑。运载火箭的推进剂引燃后发生反应: 。用 表示阿伏加德
罗常数的值,下列有关说法正确的是
A. 中含有的共用电子对数为
B. 混合物中含有的质子数为
C.相同质量的 和 含有的氮原子数相等
D.当生成 时转移电子数为
【变式5-2】(2023-2024高三上·福建福州·期中)N 为阿伏加德罗常数的值。下列说法正确的是
A
A.4.2g乙烯和丙烯混合气体中含有的极性键数目为0.6N
A
B.1L 1mol/L熔融的NaHSO 中含有的阳离子数目为2N
4 A
C.0.1mol乙醇与0.3mol乙酸在浓硫酸作用下充分反应生成乙酸乙酯分子数为0.1N
A
D.晶体B的结构单元为 ,则11g晶体B含有0.6N 个三角形(相邻原子构成)
A
【考向六】氧化还原反应中电子转移数目的计算
【典例6】 代表阿伏加德罗常数的值。下列说法正确的是
A.(2023·海南卷)2.4g镁条在空气中充分燃烧,转移的电子数目为
B.(2023·辽宁卷)我国古代四大发明之一黑火药的爆炸反应为:
,每生成 转移电子数目为
C.(2023·重庆卷)已知反应: ,若消耗 (标准状况) ,转移
的电子数为
D.(2022·全国卷)电解熔融 ,阴极增重 ,外电路中通过电子的数目为E.(2022·浙江卷)足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
F.(2022·河北卷)3.9gNa O 与足量水反应,转移电子个数为0.1N
2 2 A
G.(2021·全国卷) 的 与 完全反应时转移的电子数为
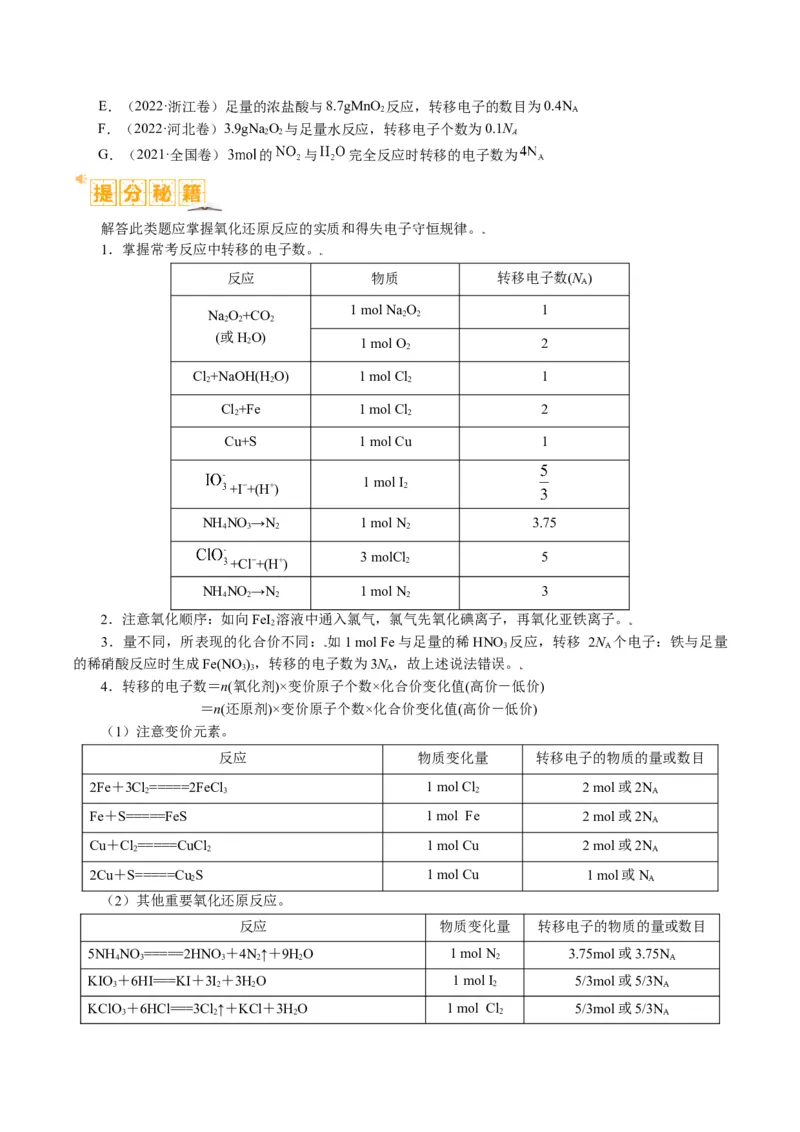
解答此类题应掌握氧化还原反应的实质和得失电子守恒规律。
1.掌握常考反应中转移的电子数。
反应 物质 转移电子数(N )
A
1 mol Na O 1
NaO+CO 2 2
2 2 2
(或HO)
2 1 mol O 2
2
Cl+NaOH(H O) 1 mol Cl 1
2 2 2
Cl+Fe 1 mol Cl 2
2 2
Cu+S 1 mol Cu 1
1 mol I
+I−+(H+) 2
NH NO →N 1 mol N 3.75
4 3 2 2
3 molCl 5
+Cl−+(H+) 2
NH NO →N 1 mol N 3
4 2 2 2
2.注意氧化顺序:如向FeI 溶液中通入氯气,氯气先氧化碘离子,再氧化亚铁离子。
2
3.量不同,所表现的化合价不同:如1 mol Fe与足量的稀HNO 反应,转移 2N 个电子:铁与足量
3 A
的稀硝酸反应时生成Fe(NO ),转移的电子数为3N ,故上述说法错误。
3 3 A
4.转移的电子数=n(氧化剂)×变价原子个数×化合价变化值(高价-低价)
=n(还原剂)×变价原子个数×化合价变化值(高价-低价)
(1)注意变价元素。
反应 物质变化量 转移电子的物质的量或数目
2Fe+3Cl=====2FeCl 1 mol Cl 2 mol或2N
2 3 2 A
Fe+S=====FeS 1 mol Fe 2 mol或2N
A
Cu+Cl=====CuCl 1 mol Cu 2 mol或2N
2 2 A
2Cu+S=====Cu S 1 mol Cu 1 mol或N
2 A
(2)其他重要氧化还原反应。
反应 物质变化量 转移电子的物质的量或数目
5NH NO =====2HNO+4N↑+9HO 1 mol N 3.75mol或3.75N
4 3 3 2 2 2 A
KIO +6HI===KI+3I+3HO 1 mol I 5/3mol或5/3N
3 2 2 2 A
KClO+6HCl===3Cl↑+KCl+3HO 1 mol Cl 5/3mol或5/3N
3 2 2 2 A2HO===2HO+O↑ 1 mol H O 1 mol或N
2 2 2 2 2 2 A
3Fe+2O=====Fe O 3mol Fe 8 mol或8N
2 3 4 A
3Fe+4HO(g)=====Fe O+4H(g) 3mol Fe 8 mol或8N
2 3 4 2 A
Fe+2HCl===FeCl +H↑ 1 mol Fe 2 mol或2N
2 2 A
4Na+O===2Na O 1 mol Na 1 mol或N
2 2 A
2Na+O=====NaO 1 mol Na 1 mol或N
2 2 2 A
NaO+SO ===Na SO 1 mol NaO 2 mol或2N
2 2 2 2 4 2 2 A
【变式6-1】(2023-2024高三上·福建福州·期中)在化工生产中常利用某分子筛作催化剂,催化 脱除
废气中的 和 ,生成两种无毒物质,其反应历程如图所示。设 为阿伏加德罗常数的值,下列说
法中正确的是
A. 溶液中含有 的数目为
B.标况下, 二氧化氮气体中含有的分子数为
C.总反应中生成 (标准状况)时转移电子数为
D. 中含有相同键能的 共价键的数目为
【变式6-2】(2023-2024高三上·辽宁沈阳·期中)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.1 mol[Cu(NH )CO]+中σ键的个数为14N
3 3 A
B.标准状况下,22.4L氮气中含有7N 个中子
A
C.5.6gFe与稀硝酸发生反应时,转移电子数一定为0.3N
A
D.0.2mol•L-1 Na SO 溶液中,Na+的数目为0.4N
2 4 A
【考向七】物质转化中的隐含反应
【典例7】设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.(2022·全国卷) 溶液中, 的数目为B.(2022·全国卷)电解熔融 ,阴极增重 ,外电路中通过电子的数目为
C.(2022·浙江卷) 和 于密闭容器中充分反应后, 分子总数为
D.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
E.(2021·河北卷)电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
F.(2021·广东卷) 与 混合后的分子数目为
G.(2021·浙江卷)0.1 mol CH COOH与足量CHCHOH充分反应生成的CHCOOCH CH 分子数目
3 3 2 3 2 3
为0.1N
A
1.可逆反应类型
因为可逆反应进行不完全,当没给出转化率时,不能求出准确的目标粒子数目。
如某密闭容器盛有0.1 mol N 和0.3 mol H ,在一定条件下充分反应,转移的电子数目为0.6N :该反
2 2 A
应为可逆反应,进行程度不确定,无法准确求解转移的电子数目,故错误。
常见的可逆反应有:
①2SO +O 2SO ,
2 2 3
②N +3H 2NH 。
2 2 3
③Cl+HO HCl+HClO。
2 2
④NH+HO NH ·H O NH+OH-。
3 2 3 2
⑤2NO NO。
2 2 4
⑥H +I 2HI。
2 2
⑦CH COOH+C HOH CHCOOC H+HO。
3 2 5 3 2 5 2
2.溶液浓度变化使反应停止的类型
因为酸的浓度变化使反应停止,难以求出准确的目标粒子数目。
(1)浓度变小,反应停止:数据为无效数据。
①铜和浓硫酸加热先放二氧化硫,后反应停止。
②碳和浓硫酸加热先放二氧化硫和二氧化碳,后反应停止。
③碳和浓硝酸加热先放二氧化氮和二氧化碳,后反应停止。
④二氧化锰和浓盐酸加热先放氯气,后反应停止。
(2)浓度变小,反应变化:数据为有效数据。
①锌和浓硫酸常温先放二氧化硫,后放氢气。
②铜和浓硝酸常温先放二氧化氮,后放一氧化氮。
3.物质组成不能确定的类型
当某些物质混合或反应进行一段时间后,产物的种类变化或物质的量不定,难以求出准确的目标粒子
数目。
如标准状况下,5.6 L NO和5.6 L O 混合后的分子总数为0.5N :两种气体混合后生成NO ,若不考虑
2 A 2NO 部分转化为NO ,气体的体积为8.4 L,物质的量为0.375 mol,事实上,混合气体中存在可逆反应
2 2 4
2NO NO,故无法准确求解分子数目,错误。
2 2 4
如下列为常见的隐含反应:
(1)隐含的可逆反应:2NO NO;△H<0。
2 2 4
(2)铝、铁常温下遇到浓硫酸、浓硝酸发生钝化。
(3)溶液中生成的可溶性气体会部分溶解,如电解氯化钠溶液,逸出的氯气的体积比氢气的小。
(4)活泼电极作阳极,电极参与反应,溶液中的离子不放电。
(5)电解精炼中,阳极生成多种金属离子,阴极只生成一种金属。
①阳极减重量与转移的电子数间无确定的关系。
②阴极增重量与转移的电子数间有确定的关系。
【变式7-1】(2023-2024高三上·河北张家口·联考)N 为阿伏加德罗常数的值。下列说法正确的是
A
A.常温常压下,23gNO 和NO 混合气体含有的分子数为0.5N
2 2 4 A
B.1 mol Cu与足量的S反应,转移电子数为2N
A
C.标准状况下,22.4L乙炔与氢气完全加成,破坏的共用电子对数为3N
A
D.9.2gNa与含0.1 mol HCl的稀盐酸充分反应,转移电子数为0.4N
A
【变式7-2】(2023-2024高三上·北京海淀·期中)用 代表阿伏加德罗常数的值。下列说法正确的是
A.1mol羟基含有的电子数目为
B.56g Fe与足量稀 反应转移的电子数目为
C.2L 的 溶液中, 的数目为
D.1mol 与5mol 充分反应可生成 数目为
【考向八】溶液中微粒数的计算
【典例8】用 代表阿伏加德罗常数的值。下列说法不正确的是
A.(2023·海南卷) 完全溶于 所得溶液, 微粒数目为
B.(2023·浙江卷)向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
C.(2023·浙江卷)标准状况下,11.2LCl 通入水中,溶液中氯离子数为0.5N
2 A
D.(2023·广东卷)体积为 的 溶液中, 数目为
E.(2021·天津卷)1mol/LHCl溶液中,HCl分子的数目为N
A
F.(2021·浙江卷) 的 水溶液中含有氧原子数为
此类题的解题思路如下:
已知量(溶液的体积及溶质的物质的量浓度)→物质的量→分析粒子种类及个数(溶质的电离、水
解、溶剂所含粒子等)→目标粒子数目;解题时的几个易错点:
(1)“已知浓度缺体积”及“已知体积缺浓度”:以上两种情况均无法求解溶液中所含目标粒子的
数目;
如25 ℃ 时,pH=13的NaOH溶液中所含OH−的数目为 0.1N :因为缺少溶液的体积无法计算OH−的
A
数目,故此说法错误。
(2)电离:当溶质为弱电解质时,其在溶液中部分电离,溶液中所含的分子数及电离出的离子数目
均无法直接求解;
如1 L 1 mol·L−1的氨水中有N 个NH+ :一水合氨为弱电解质,不能全部电离,故氨水中所含NH+ 的
A 4 4
数目小于N ,错误。
A
(3)水解:当电解质在溶液中发生水解时,溶液中发生水解的离子数目无法直接求解;
如将0.1 mol FeCl 配成1 L溶液,所得溶液含有0.1N 个Fe3+:Fe3+部分水解导致所配溶液中的Fe3+减
3 A
少,从而使溶液中的Fe3+数目小于0.1N ,错误。
A
(4)溶剂:当溶剂中也含有所求的粒子时,往往习惯性地只考虑溶质中所含粒子,而忽视了溶剂中
所含粒子导致出错。
如50 g质量分数为46%的乙醇水溶液中,含氢原子数目为3N :由于陷入思维定式,忽视溶剂水中也
A
含有氢原子而出错。
(5)胶体中微粒:是多个微粒的聚合体
如0.1L1mol/L的饱和氯化铁溶液滴入沸水中,生成的胶体含胶粒数目小于0.1N 。
A.
【变式8-1】(2023-2024高三上·福建·莆田二中期中) 为阿伏加德罗常数的值,下列说法正确的是
A.1mol 中含有的碳氢键数目不一定为
B.0.1mol 与0.1mol 反应时生成的 分子数为
C. 溶液中含有的 的总数为
D.22.4L 发生反应 ,转移的电子数为
【变式8-2】(2023-2024高三上·重庆南开中学期中)氨氮是水体的污染物之一,工业上可用次氯酸钠作处
理剂,反应方程式为: 。设阿伏加德罗常数的值为N ,下列说法正确
A
的是
A.1 L 0.1mol/L NaClO 溶液中含有0.1N 个 ClO⁻
A
B.18 g HO 中含有的孤电子对数目为2N
2 A
C.生成11.2 L N,转移的电子数为 3N
2 A
D.0.5 L0.1 mol/L 氨水中含有1.(2023·全国甲卷) 为阿伏加德罗常数的值。下列叙述正确的是
A. 异丁烷分子中共价键的数目为
B.标准状况下, 中电子的数目为
C. 的 溶液中 的数目为
D. 的 溶液中 的数目为
2.(2023·浙江卷)N 为阿伏加德罗常数的值,下列说法正确的是
A
A.4.4gC HO中含有σ键数目最多为0.7N
2 4 A
B.1.7gH O 中含有氧原子数为0.2N
2 2 A
C.向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
D.标准状况下,11.2LCl 通入水中,溶液中氯离子数为0.5N
2 A
3.(2023·辽宁卷)我国古代四大发明之一黑火药的爆炸反应为: 。
设 为阿伏加德罗常数的值,下列说法正确的是
A. 含 键数目为 B.每生成 转移电子数目为
C. 晶体中含离子数目为 D. 溶液中含 数目为
4.(2022·全国卷) 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
5.(2022·浙江卷)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
6.(2022·浙江卷) 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为
C. 含有中子数为
D. 和 于密闭容器中充分反应后, 分子总数为
7.(2022·海南卷)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常数的值,下列
A
说法正确的是
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
8.(2022·河北卷)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.3.9gNa O 与足量水反应,转移电子个数为0.1N
2 2 AB.1.2gMg在空气中燃烧生成MgO和MgN,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 A
D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1N
2 A
9.(2022·辽宁卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的中子数为
B. 分子中含有的 键数目为
C.标准状况下, 气体中 数目为
D. 的 溶液中 数目为0.01N
A
10.(2022·福建卷)常温常压下,电化学还原制氨气的总反应方程式: ,
设 为阿伏加德罗常数的值,下列说法正确的是
A. 水中含有的孤电子对数为
B.每产生 失去的电子数为
C. 氨水中,含有的 分子数少于
D.消耗 (已折算为标况)时,产生的 分子数为
11.(2022·重庆卷)工业上用N 和H 合成NH ,N 代表阿伏加德罗常数的值,下列说法正确的是
2 2 3 A
A.消耗14gN 生成NH 分子数为2 N
2 3 A
B.消耗1molH ,生成N-H键数为2 N
2 A
C.生成标准状况下22.4LNH ,电子转移数为2 N
3 A
D.氧化1molNH 生成NO,需O 分子数为2 N
3 2 A
12.(2021·全国卷) 为阿伏加德罗常数的值。下列叙述正确的是
A. 重水( )中含有的质子数为
B. 的 与 完全反应时转移的电子数为
C. 环状 ( )分子中含有的 键数为
D. 的 溶液中 离子数为
13.(2021·天津卷)设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.1mol/LHCl溶液中,HCl分子的数目为N
A
B.22.4L氢气中,H 分子的数目为N
2 A
C.180g葡萄糖中,C原子的数目为6N
A
D.1molN 中,σ键的数目为3N
2 A
14.(2021·河北卷)N 是阿伏加德罗常数的值,下列说法错误的是
A
A.22.4L(标准状况)氟气所含的质子数为18N
A
B.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
D.1L1mol•L-1溴化铵水溶液中NH 与H+离子数之和大于N
A15.(2021·重庆卷)葡萄酒中含有CHCHOH、CHCOOH、 SO 和CO 等多种成分。若N 代表阿伏加
3 2 3 2 2 A
德罗常数的值,下列说法正确的是
A.46gCHCHOH中含有C-H键数为5N
3 2 A
B.1L1 mol·L-1CHCOOH溶液中含有氢离子数为N
3 A
C.1 mol SO 与1 mol O 完全反应转移的电子数为4 N
2 2 A
D.11.2L (标准状况) CO 完全溶于水后溶液中HCO 分子数为0.5N
2 2 3 A
16.(2021·湖南卷) 为阿伏加德罗常数的值。下列说法正确的是
A. 含有的中子数为
B. 溶液中含有的 数为
C. 与 在密闭容器中充分反应后的分子数为
D. 和 (均为标准状况)在光照下充分反应后的分子数为
17.(2021·湖北卷)N 为阿伏加德罗常数的值。下列说法错误的是
A
A.23gCHCHOH中sp3杂化的原子数为N
3 2 A
B.0.5molXeF 中氙的价层电子对数为3N
4 A
C.1mol[Cu(H O) ]2+中配位键的个数为4N
2 4 A
D.标准状况下,11.2LCO和H 的混合气体中分子数为0.5N
2 A
18.(2021·广东卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 含有 键的数目为
B. 的盐酸含有阴离子总数为
C. 与 混合后的分子数目为
D. 与足量 反应生成的 分子数目为
1.(2023-2024高三上·湖南·联考) 是阿伏加德罗常数的值,下列说法正确的是
A. 二氧化硅晶体中含有的硅氧键数目为
B. 碘蒸气和 氢气在密闭容器中充分反应,生成的碘化氢分子数等于
C. 铁与水蒸气在高温条件下完全反应失去电子数为
D.标准状况下, 己烷在 中完全燃烧,生成的二氧化碳分子数目为
2.(2023-2024高三上·北京丰台·期中)用N 表示阿伏加德罗常数。下列说法正确的是
A
A.同温同压下,相同体积的O 和CO 所含的原子数相同
2 2
B.质量相同的HO和DO所含的分子数相同
2 2
C.标准状况下,22.4L乙炔中σ键数为3N ,π键数为2N
A A
D.12g金刚石中C-C键数为4N
A
3.(2023-2024高三上·湖北·联考)设 为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下, 所含离子总数为
B.标准状况下, 含有 个质子C. 苯中含有 个碳碳双键
D. 中含有的中子数为
4.(2023-2024高三上·四川成都·成都实外校考)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.9.2g甲苯( )中所含碳碳双键数目为0.3N
A
B.常温常压下,5.6g乙烯和环丁烷(C H)的混合气体中含有的碳原子数为0.4N
4 8 A
C.常温下,1LpH=13的Ba(OH) 溶液中由水电离的OH-数目为0.1N
2 A
D.1L0.1 mol·L-1KCr O 酸性溶液中所含 的数目为0.1 N
2 2 7 A
5.(2023-2024高三上·陕西师大附中校考)设 表示阿伏加德罗常数的值,下列说法正确的是
A. 分子式为 的烃分子中,共用电子对数目一定为
B. 羟基( )和 所含的质子数和电子数均为
C. 与一定量的 恰好完全反应,则转移的电子数一定为
D. 的 溶液中 和 离子数之和为
6.(2023-2024高三上·安徽·宣城联考)设 为阿伏加德罗常数的值,下列说法正确的是
A. 溶液中含 分子的数目小于
B.标准状况下, 与 充分反应,生成的 分子数目为
C. ( )与 ( )的混合物中所含的共价键数目为
D.标准状况下,22.4L氯气与甲烷的混合气体,光照时充分反应生成的HCl分子数为
7.(2023-2024高三上·广东广州·执信中学校考)设 代表阿伏加德罗常数的值。下列说法正确的是
A.78gNaO 与足量水完全反应,电子转移数为
2 2
B.1L0.1mol·L﹣1的NaCO 溶液含 的数目为
2 3
C.1mol 分子中所含σ键数为
D.标准状况下,2.24LCCl 所含氯原子数为
4
8.(2023-2024高三上·新疆乌鲁木齐·兵团二中期中)设 为阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下22.4L NO与11.2L 混合后气体的分子总数为
B.质量分数为46%的乙醇水溶液中所含氢原子数为
C.在反应 中,每生成4mol ,转移的电子数为
D.标准状况下11.2L 全溶于水,溶液中的 、 、 的数目之和为
9.(2023-2024·河南·校联考一模)设 为阿伏加德罗常数的值,下列说法错误的是
A.常温、常压下,1.4g环丁烷与环丙烷混合气体中含有的氢原子数为B.标准状况下,22.4L氯气、氢气和一氧化碳的混合气体中含有 个原子
C.100g32%的甲醇溶液中含有的氢原子数为
D.两份质量均为5.6g的铁粉分别与足量硫粉、碘单质充分反应,转移的电子数均为
10.(2023-2024·广西·校联考一模)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.常温常压下,23g钠在足量的氧气中燃烧,转移的电子数为2N
A
B.1molH O中,中心原子的孤电子对数为2N
2 A
C.标准状况下,0.1molHF的体积约为2.24L
D.1L0.1mol•L-1的(NH )SO 溶液中,含有NH 的数目为0.2N
4 2 3 A
11.(2023-2024高三上·黑龙江·大庆实验中学期中)用N 表示阿伏加德罗常数的数值,下列说法错误的
A
是
A.28 g乙烯和丙烯的混合气体充分燃烧,消耗的O 分子数为3N
2 A
B.0.2 mol FeCl 水解形成的Fe(OH) 胶体粒子数小于0.2N
3 3 A
C.标准状况下,2.24 L新戊烷中电子的数目为3.4N
A
D.含0.2 mol HSO 的浓硫酸与足量的镁反应,转移的电子数大于0.2N
2 4 A
12.(2023-2024高三上·浙江金华·第一中学校考)设 为阿伏加德罗常数的值,下列叙述正确的是
A.4.6g 完全燃烧,一定有 个C-H键断裂
B.0.1mol丙烯酸( )中含有 个 键
C.含0.5mol 的酸性溶液与足量 反应生成 ,转移电子数
D.0.2mol 完全水解形成的 胶体粒子数等于
13.(2023-2024高三上·重庆·期中)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.120g由NaHSO 和MgSO 组成的混合固体中 数目为N
4 4 A
B.标准状况下,22.4LCC1 中C-Cl键的数目为4N
4 A
C.12.8gCu与足量S完全反应,转移的电子数为0.2N
A
D.1mol I (g)和1mol H 在密闭容器中充分反应,所得混合气体的分子数小于2N
2 2 A
14.(2023-2024高三上·河北保定·期中)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,0.5 mol 、 、 、HF含有电子均为
B.标准状况下,2.24 L 与水反应转移电子
C.42 g Fe完全溶于一定量的稀硝酸,则生成气体的分子数为
D.电解NaCl溶液在阴极产生11.2 L(标准状况下)气体时,有 个电子通过溶液进入阳极
15.(2023-2024高三上·湖北武汉·第六中学校考)N 代表阿伏加德罗常数的值。 下列说法正确的是
A
A.常温下,0.1 mol∙L−1的 溶液中氮原子数目为0.2N
A
B.7.8gNa O 与足量的水( )反应生成的氧气所含的中子数为0.8N
2 2 A
C.电解精炼铜的过程中,电路中每通过 N 个电子,阳极溶解铜32g
AD.标准状况下,22.4LNO 含有的原子数目为3N
2 A