文档内容
题型 08 元素周期律推断
目录
.............................................................................................................................1
【考向一】原子结构与性质推断......................................................................................................................1
【考向二】性质与位置推断..............................................................................................................................4
【考向三】“片段结构”与性质推断..............................................................................................................7
【考向四】“序、层”规律推断....................................................................................................................10
【考向五】“序、价”规律推断....................................................................................................................13
【考向六】性质递变型推断............................................................................................................................15
【考向七】性质图像表达推断........................................................................................................................18
【考向八】无机框图推断................................................................................................................................24
【考向九】给定微粒组成推断........................................................................................................................28
...........................................................................................................................32
【考向一】原子结构与性质推断
【典例1】(2023·全国·模拟预测)科学家利用 粒子(即氦核 )进行多种核反应: 、
。已知 和 都具有放射性,下列说法错误的是
A.X元素位于元素周期表的第二周期第ⅥA族
B. 和 互为同位素,化学性质相同
C. 、 都可作为示踪原子
D.核反应产生的能量可用于发电,属于化学能转化为电能
【答案】D
【解析】A.因为核反应过程中电子数不变,由题意可推出 ,所以X是O,位于元素周期表中第二周
期第ⅥA族,A正确;
B.同位素的化学性质几乎相同,B正确;C.由于 、 都具有放射性,所以均可作为示踪原子,C正确;
D.核反应不属于化学反应的范畴,利用核反应产生的能量发电是将核能转化为电能,D错误;
故选D。
1.1~18号元素原子核外电子排布的特点
(1)电子层排布: x 或2,x或2,8,x
(2)次外层电子数为2或8;内层电子数为2或10
(3)简单离子的最外层电子数为0或2或8
2.原子结构与元素的性质的关系
元素 最外层电子数 得失电子能力 化学性质 主要化合价
较稳定,一般
稀有气 一般不易
8(He为2) 不参与化学反 0
体元素 得失电子
应
金属元素 <4 易失电子 金属性 只有正价,一般是+1→+3
非金属元
≥4 易得电子 非金属性 既有正价又有负价
素
3.微粒符号及意义
4.1~20号元素原子核外电子排布的特点
(1)原子核中无中子的原子:H。
(2)最外层只有一个电子的原子:H、Li、Na、K;
最外层有两个电子的原子:He、Be、Mg、Ca。
(3)最外层电子数等于次外层电子数的原子:Be、Ar;
最外层电子数是次外层电子数2倍的原子:C;
最外层电子数是次外层电子数3倍的原子:O。
(4)电子层数与最外层电子数相等的原子:H、Be、Al;
最外层电子数是电子层数2倍的原子:He、C、S;
最外层电子数是电子层数3倍的原子:O。
(5)次外层电子数是最外层电子数2倍的原子:Li、Si。
(6)内层电子总数是最外层电子数2倍的原子:Li、P。
(7)与He原子电子层结构相同的离子:H-、Li+、Be2+。
(8)次外层电子数是其他各层电子总数2倍的原子:Li、Mg。(9)次外层电子数与其他各层电子总数相等的原子:Be、S。
5.核反应变化历程
(1)概念:原子核发生变化的过程,即质子数或中子数发生变化的反应
(2)变化类型:核变化
2 3 4 1
①核聚变:1 H+1H 2 He+0n
14 14 0
②核裂变: 6C 7N+-1e-
n b d f
(3)遵循规律:mX+a Y c Z+e W
①质子数守恒:m+a=c+e
②质量数守恒:n+b=d+f
(4)常见的重要核素及其应用
235 14 12 2 3 18
92U 6C 6C 1 H(D) 1H(T) 8O
用于考古断 相对原子质量的标准
核燃料 制氢弹 示踪原子
代 阿伏伽德罗常数基准
【变式1-1】(2023·河北石家庄·校联考模拟预测)核反应产生的能量可作为未来新能源,现有两个核反应:
① ;② ,其中Y的核外电子数等于(m+2)。下列说法错误的是
A. B.原子半径:
C.最高价含氧酸的酸性: D.M、X都可与Y形成多种化合物
【答案】A
【分析】根据质量守恒可知,m=6,n=12得M微粒为 ,依据Y的电子数等于(m+2),得Y微粒为O,从
而得出X微粒为N,据此分析解题。
【解析】A.依据质量守恒,4+b=d+1,即b=d-3,故A说法错误;
B.C、N、O为同周期主族元素,随原子序数递增,原子半径逐渐减小,故B说法正确;
C.HNO 为强酸,H CO 为弱酸,故C说法正确;
3 2 3
D.C、N与O可形成CO、CO 、NO、NO 等多种化合物,故D说法正确;
2 2
答案为A。
【变式1-2】(2023·山东济宁·统考三模)用 粒子( )分别轰击 和 ,发生核反应:
和 ,其中基态 原子的能级数与未成对电子数相等。下列说法
正确的是
A.用 粒子轰击 发生的是化学变化B.X、Y、Z的单质均为分子晶体
C.基态X和Y原子核外未成对电子数之比为1:1
D.Y、Z简单氢化物的还原性ZW>R
B.含氧酸的酸性:R>Z
C.Y和R形成的化合物是离子化合物
D.第三电离能:W>X
【答案】A
【分析】W的气态氢化物常用作制冷剂,则W为N,W、X、Y、Z、R的原子序数依次增大,Y是同周期主
族元素中离子半径最小的,则Y为Al;ZXR 能与水剧烈反应,观察到液面上有白雾生成,证明有HCl生成,
2
并有无色刺激性气味的气体逸出,该气体能使品红溶液褪色,证明有二氧化硫气体生成,确定ZXR 为
2
SOCl ,因此X为O、Z为S、R为Cl;故W为N、X为O、Y为Al、Z为S、R为Cl。
2
【解析】A.NH 中形成氢键比H S的沸点高,水常温下是液态其余两种氢化物常温是气态,简单气态氢化
3 2
物的沸点:X>W>R,故A正确;
B.HClO的酸性比硫酸弱不能说含氧酸的酸性:R>Z,故B错误;
C.AlCl 是共价化合物,因此不能说Y和R形成的化合物是离子化合物,故C错误;
3
D.O半径小于N因此第三电离能:W<X,故D错误;故选A。
1.非金属性强:周期表右上角的F最强
(1)单质与氢气容易化合,气态氢化物稳定。
(2)最高价含氧酸的酸性强(HClO 最强),相应盐的碱性弱。
4
(3)相应阴离子及气态氢化物的还原性弱。
(4)在化合物中显负价元素的非金属性强。
(5)共用电子对偏向的一方元素的非金属性强。
(6)特殊情况。
①N 与H 很难化合,但氮元素的非金属性很强。
2 2
②2C+SiO Si+2CO↑不能说明碳元素的非金属性比硅的强。
2
2.金属性强:周期表左下角的Na最强
(1)单质与酸或水反应剧烈。
(2)最高价碱的碱性强,相应盐的酸性弱。
(3)相应阳离子的氧化性弱。
(4)能够从盐溶液中置换出其他金属的金属。
(5)特殊情况。
①活泼性:Ca>Na,但钠和水反应更剧烈。
②反应Na(l)+KCl(l) NaCl(l)+K(g),不能说明金属性Na>K。
③按周期律Pb比Sn活泼,按金属活动顺序表Sn比Pb活泼。
3.元素及其化合物的一些特征性质可以成为推断的突破口
特征 元素
形成化合物种类最多的元素、单质是自然界中硬度最大的物质的元
C
素或气态氢化物中氢的质量分数最高的元素
空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素 N
地壳中含量最多的元素、氢化物沸点最高的元素或氢化物在通常情
O
况下呈液态的元素
单质密度最小的;元密度最小的金属元素 H、Li
单质在常温下呈液态的,非金属元素、金属元素 Br、Hg
最高价氧化物及其水化物既能与强酸反应,又能与强碱反应的元素 Al
元素的气态氢化物和它的最高价氧化物对应的水化物能起化合反应
N、S
的元素、能起氧化还原反应的元素
元素的单质在常温下能与水反应放出气体的短周期元素 Li、Na、F
单质是重要的半导体材料、氧化物可用作光导纤维 Si
短周期中金属性最强的元素、非金属性最强的元素 Na、F单质最活泼的非金属元素或无正价的元素或无含氧酸的非金属元素
或无氧酸(气态氢化物)可腐蚀玻璃的元素或气态氢化物最稳定的元 F
素或阴离子的还原性最弱的元素
4.元素推断题六大误区
误认为最高正化合价和最低负化合价绝对值相等的元素只有第IVA族的元素。忽视了第IA族的
误区1
氢元素的最高正化合价为+1价,最低负化合价为-1价
误区2 误认为主族元素的最高正化合价一定等于其族序数。忽视了氧一般不显正价,氟无正价
误认为元素的非金属性越强,其氧化物对应水化物的酸性就越强。但酸性HCIOX>Y
B.简单氢化物的还原性:X>Y
C.常温下,Z的单质能够与水剧烈反应
D.由W、X、Y三种元素组成的化合物的水溶液可能呈酸性
【答案】A
【分析】由题给信息,短周期主族元素W、X、Y、Z、M的原子序数依次增大,X和Y位于同一周期且能组
成红棕色的大气污染物,则红棕色大气污染物为 ,则X为N,Y为O,金属元素M的单质与冷水几乎
不反应,但可与热水发生置换反应生成W的单质,则M为Mg,W为H, 原子序数依次增大,Z可能为F
或Na,则W、X、Y、M四种元素分别为H、N、O、Mg,Z可能为 或 ;
【解析】A.简单离子半径: (或 ),A项错误;,
B.同周期 从左到右,非金属性增强,氢化物的还原性减弱,则简单氢化物的还原性: ,B项正
确,
C.常温下, 或 均能的与水剧烈反应,C项正确;
D.由W、X、Y三种元素组成的 的水溶液显碱性,组成的 显酸性,D项正确。
答案选A。
【考向三】“片段结构”与性质推断
【典例3】(2022·广东卷)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧
化物对应的水化物为强酸。下列说法不正确的是
甲 乙
丙 丁 戊
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
【答案】C
【分析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或高氯酸,若是高
氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊为S,甲为C、乙为O、丙为Si、丁为
P。
【解析】A.根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故A正确;B.根据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;
C.甲的氢化物可能为氨气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产生;若是甲烷、
乙烷等,则遇氯化氢不反应,没有白烟生成,故C错误;
D.丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强碱反应,故D正确。
综上所述,答案为C。
1.根据“片段结构”推断元素的思维模式
给出一小部分元素周期表推断元素是一种常见题型,需要根据题目明确给出的信息或周期表结构中“隐
藏”的信息进行推断。如第一周期只有两端有元素,如果某元素上方有相邻元素,则或为第三周期元素或
为Li或为Ne。解题时,应先根据题示信息推出某种元素,然后顺藤摸瓜,由元素的位置关系确定其他元
素。
(1)元素周期表中第一周期只有两种元素H和He,H元素所在的第ⅠA族左侧无元素分布;
(2)He为0族元素,0族元素为元素周期表的右侧边界,0族元素右侧没有元素分布。
利用这个关系可以确定元素所在的周期和族。
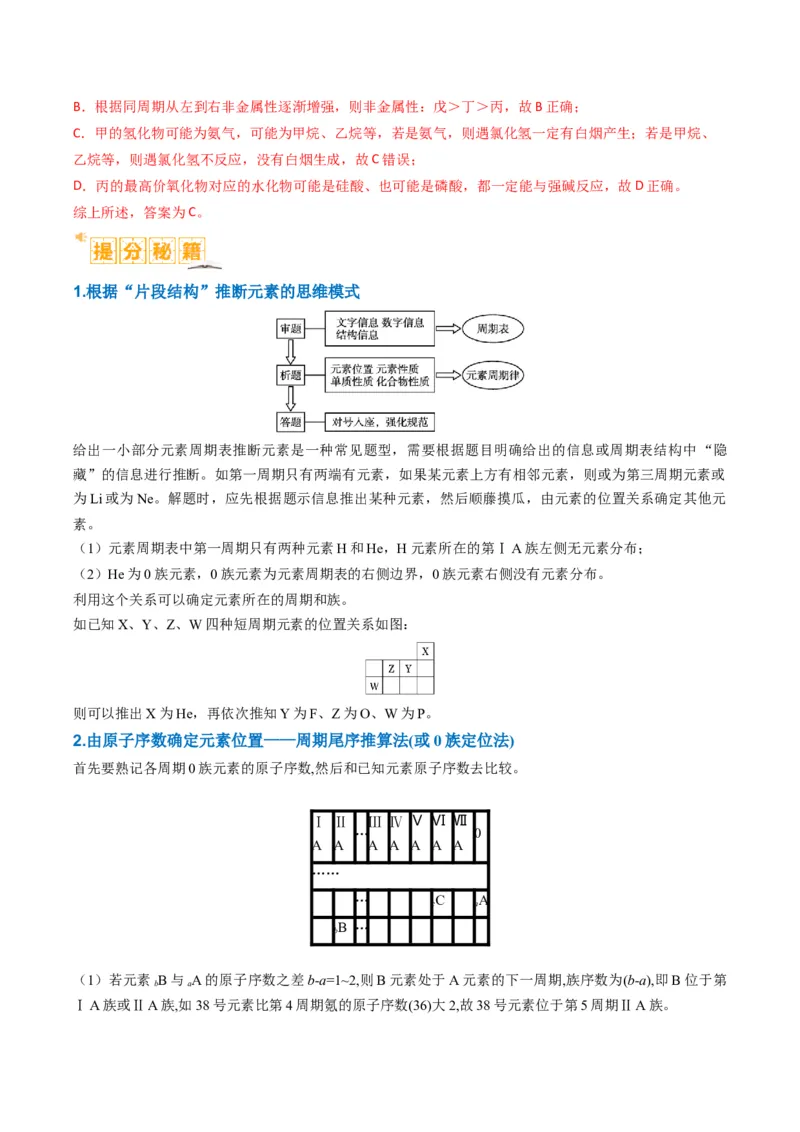
如已知X、Y、Z、W四种短周期元素的位置关系如图:
则可以推出X为He,再依次推知Y为F、Z为O、W为P。
2.由原子序数确定元素位置——周期尾序推算法(或0族定位法)
首先要熟记各周期0族元素的原子序数,然后和已知元素原子序数去比较。
Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ Ⅵ Ⅶ
… 0
A A A A A A A
……
… C A
c a
B …
b
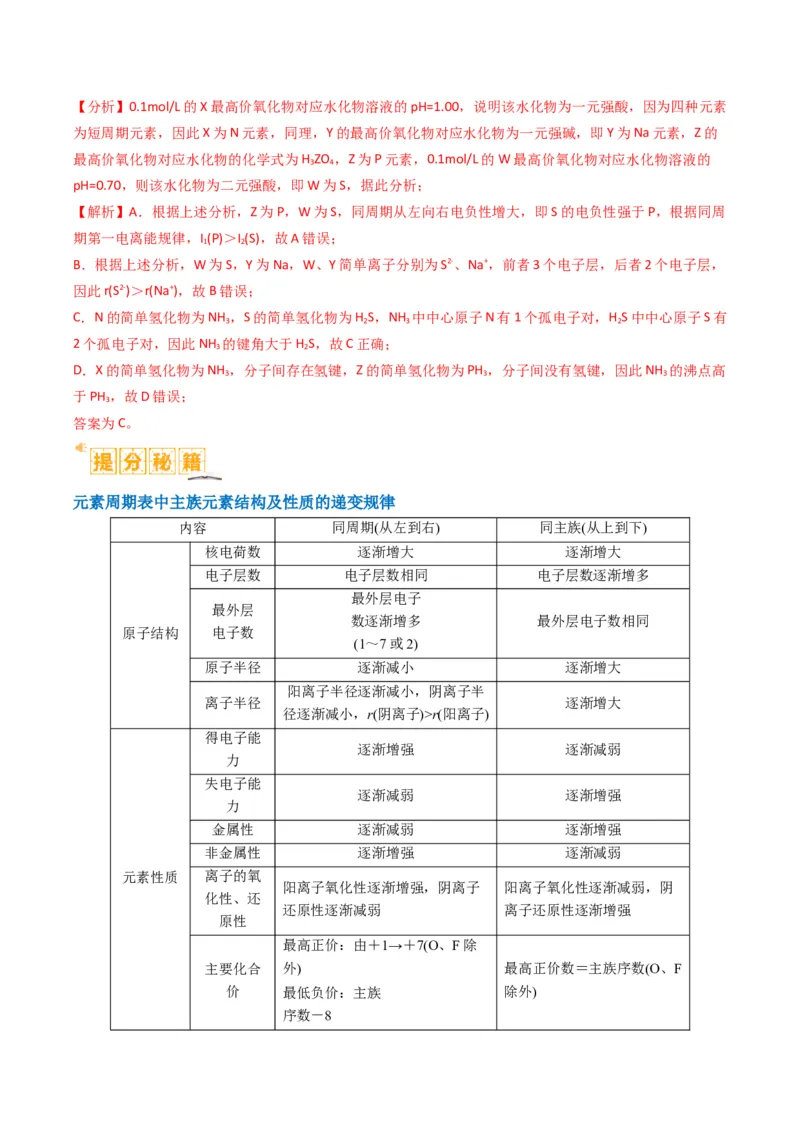
(1)若元素 B与 A的原子序数之差b-a=1~2,则B元素处于A元素的下一周期,族序数为(b-a),即B位于第
b a
ⅠA族或ⅡA族,如38号元素比第4周期氪的原子序数(36)大2,故38号元素位于第5周期ⅡA族。(2)若元素 A与 C的原子序数之差a-c=1~5,则C元素位于A元素所在周期,族序数为[8-(a-c)],即C位于第
a c
ⅢA~ⅦA族,如49号元素比第5周期的氙(54号)原子序数小5,因此该元素处在第5周期ⅢA族。
①ⅠA族元素不等同于碱金属元素,氢元素不属于碱金属元素。
②元素周期表中第18列是0族,不是ⅧA族,第8、9、10三列是Ⅷ族,不是ⅧB族。
③根据元素周期表的构成特点,可分析每个族的元素种类,含元素种类最多的族是ⅢB族,共有32种元素。
④过渡元素全部是金属元素,原子最外层电子数不超过2个(1~2个)。
⑤由于镧系和锕系的原因,第6、7周期的ⅡA族和ⅢA族元素原子序数差为25。
3.短周期元素推断的数量突破口
(1)序差关系:短周期同主族相邻元素除了H和Li差2外,其余都差8
X
Z-8
Y W M
Z-1 Z Z+1
(2)等量关系:质子数=核电荷数=原子序数=核外电子总数
【变式3-1】W、X、Y、Z四种短周期元素,在元素周期表中的位置如图所示,其中W元素的原子序数为Z
元素原子序数的两倍,则下列说法正确的是
A.X位于元素周期表中的第三周期第VI 族
B.X、Y、Z三种元素对应原子的半径依次减小
C.XZ 和YZ 的结构和化学性质相似
2 2
D.利用Y的含氧酸酸性强于W的含氧酸酸性,可证明非金属性W强于Y
【答案】B
【分析】由元素在周期表中的位置可知Y、Z位于第二周期,X、W位于第三周期,W元素的原子序数为Z
元素原子序数的两倍,则W应为S元素,Z为O元素,由相对位置可知Y为N元素,X为Si元素。由以上
分析可知X为Si元素、Y为N元素、Z为O元素,W为S元素。
【解析】A.X为Si元素,位于元素周期表中的第三周期第IVA族,故A错误;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径为X>Y>Z,故B正确;
C.SiO 是共价晶体,NO 是分子晶体,二者结构不相似,化学性质也不相似,故C错误;
2 2
D.非金属性越强,对应最高价含氧酸的酸性越强,不是最高价含氧酸不能通过酸性比较非金属性,故D
错误。
故选B。
【变式3-2】(2023上·四川成都·高三成都七中校考)下图为元素周期表短周期的一部分,Z原子的电子层
数为n,最外层电子数为2n+l。下列叙述错误的是
R W XY Z
A.氢和R、W三种元素形成的阴离子有3种以上
B.RY 分子中每个原子的最外层均为8电子结构
2
C.X、Z的简单氢化物的热稳定性和还原性都是X的强
D.R、Y、Z的最高价氧化物对应水化物的酸性依次增强
【答案】C
【分析】Z原子的电子层数为n,最外层电子数为2n+l,则Z为Cl,根据图示依次推出R、W、X、Y分别为
C、O、F、S。
【解析】A.氢和C、O三种元素形成的阴离子有3种以上,绝大多数为有机酸酸根离子,故A正确;
B.CS 的结构类似于CO ,每个原子都达到了最外层8电子结构,故B正确;
2 2
C.F的非金属性强于Cl,HCl的还原性强于HF,故C错误;
D.C、S、Cl的非金属性依次增强,对应最高价氧化物水化物的酸性依次增强,故D正确;
故选C。
【考向四】“序、层”规律推断
【典例4】(2023·四川成都·石室中学校考模拟预测)A、B、C、D、E是原子序数依次增大的五种短周期元
素且B、C元素相邻,D元素原子的最外层电子数与核外电子层数相等;A元素可以与B、C、E元素分别形
成甲、乙、丙三种物质且甲、乙均为10电子化合物,丙为18电子化合物。已知:甲+E =丙+B ,甲+丙=丁。
2 2
下列说法一定正确的是
A.离子半径:E>D>C>B
B.常温下,含D元素的盐溶液pH<7
C.丁物质均由非金属元素组成,只含共价键
D.一元弱酸AEC,其结构式为A-C-E
【答案】D
【分析】由题意A元素可以与B、C、E元素分别形成甲、乙、丙三种物质且甲、乙均为10电子化合物,可
推测甲、乙、丙均为氢化物,故A为H,B、C是第二周期的元素,丙为18电子氢化物,故E为Cl,丙为
HCl;又因为甲+E =丙+B ,故甲是NH ,B为N;且B、C元素相邻,故C为O,乙为H O;甲+丙=丁,即
2 2 3 2
NH +HCl=NH Cl;D元素原子的最外层电子数与核外电子层数相等且在氧元素之后,故D位于第三周期,为
3 4
Al。
【解析】A.据分析离子半径排序为:D>E>B>C,故A项错误;
B.含D元素的盐溶液可分为铝盐和偏铝酸盐,常温下,前者的溶液中铝离子水解导致溶液pH<7,后者的
溶液中偏铝酸根水解导致溶液显碱性故pH>7,故B项错误;C.丁是NH Cl,均右非金属元素组成,但氯化铵中既含有离子键又含有共价键,故C项错误;
4
D.据分析故一元弱酸AEC为HClO,中心原子为氧原子,杂化方式为sp3,有两个孤电子对,故该分子为直
线形分子,其结构为:H-O-Cl,既A-C-E,故D项正确。
故答案选D。
1.理清“序、层”规律
(1)若一种阳离子与一种阴离子电子层数相同,则“阴前右,阳后左”,即阴离子在前一周期右侧,阳
离子在后一周期左侧,阳离子的原子序数大。如核外电子排布相同的主族元素的相对位置判断方法:
若短周期主族元素的简单离子:A+、B2+、C-、D2-具有相同的电子层结构,则A、B、C、D四种元素在
元素周期表中的相对位置如下:
故原子序数:B>A>C>D
原子半径:A>B>D>C
离子半径:D2->C->A+>B2+
(2)同周期元素的简单阳离子与阴离子相比,阴离子原子序数大。
2.微粒半径的比较
(1)相同电性微粒半径大小的比较
①原子半径:左下角的Na最大
②阳离子半径:左下角的Na+最大
③阴离子半径:左下角的P3-最大
(2)不同电性微粒半径大小的比较
①同周期:阴离子半径>阳离子半径,如Na+<Cl-
②同元素:电子数越多,微粒半径越大,如Fe2+>Fe3+
③同电子层结构:原子序数越大,离子半径越小,如Na+<O2-
(3)常见10电子微粒半径大小比较:N3->O2->Na+>Mg2+>Al3+
(4)常见18电子微粒半径大小比较:P3->S2->K+>Ca2+
【变式4-1】W、X、Y、Z是原子序数依次增大的前三周期主族元素,W与其他元素不在同一周期,X、Y、
Z处于同一周期。X的价电子排布为nsnnpn,Z的第一电离能都小于同周期相邻元素。下列说法不正确的是
A.Z的氢化物的沸点不一定大于X的氢化物的沸点
B.Z元素对应的单质一定是非极性分子
C.W、X、Y、Z原子半径大小:X>Y>Z>W
D.X、Z两种元素形成化合物时,Z总显负价,说明非金属性:Z>X【答案】B
【分析】X的价电子排布为nsnnpn即可推知n=2,即X为C元素;Z的第一电离能都小于同周期相邻元素,
又Z处于第二周期,可推知Z为O元素,则Y为N元素;W与其他元素不在同一周期,即W只能为第一周
期,为H元素;
【解析】A.Z和X的简单氢化物分别为H O和CH ,由于水分子间有氢键,即水的沸点一定大于甲烷,但
2 4
中没有说明Z的简单氢化物,可能液态或固态的烃,选项A正确;
B.Z为O,氧气是非极性分子,但臭氧是极性分子,选项B错误;
C.W、X、Y、Z原子半径大小:C>N>O>H,选项C正确;
D.X为C、Z为O,二者都是非金属元素,原子之间通过共价键结合形成化合物。元素非金属性越强,在
形成化合物时,共用电子对就偏向吸引电子能力强的O元素,该元素化合价就显负价,吸引电子能力弱的
形成化合物时元素显正价,因此可根据X、Z两种元素形成化合物时,Z总显负价,判断元素的非金属性:
Z>X,选项D正确;
答案选B。
【变式4-2】甲、乙、丙、丁4种物质分别含2种或3种元素,它们的分子中均含18个电子,甲是气态氢
化物,在水中分步电离出两种阴离子,下列推断正确的是
A.甲通入硫酸铜溶液中产生黑色沉淀,甲能与碱反应
B.乙被称为“绿色氧化剂”,则乙分子空间构型为直线形
C.若丙中含有第二周期IVA族的元素,则丙与甲烷中碳氢个数比不同
D.丁的溶液为强酸,用铜做电极电解丁溶液两极都有气体产生
【答案】A
【解析】A.有18个电子的气态氢化物是H S,通入硫酸铜生成硫化铜黑色沉淀,且其为二元弱酸,能与
2
碱反应,故A正确;
B.含有18电子的绿色氧化剂是H O ,空间构型不是直线型,故B错误;
2 2
C.有第二周期IVA族的元素的18电子是C H 或CH O,可能与甲烷中碳氢个数比相同,故C错误;
2 4 4
D.含有18电子且是强酸的是HCl,用铜做电极电解盐酸,阳极发生Cu-2e-=Cu2+没有气体产生,故D错误;
故选A。
【考向五】“序、价”规律推断
【典例5】根据表中短周期元素的有关信息判断,下列说法错误的是
元素编号 E F G H I J K L
原子半径/nm 0.037 0.074 0.082 0.099 0.102 0.143 0.160 0.186
最高化合价或最低化合价 +1 -2 +3 -1 -2 +3 +2 +1A.最高价氧化物对应水化物的酸性:HK>J
D.J、K、L的单质可以通过电解法冶炼获得
【答案】A
【分析】F、I的最低负化合价都为-2,应该为第ⅥA族元素,根据原子半径可知F为O,I为S;E、L的最
高正化合价为+1,结合原子半径大小可知E为H,L为Na;K的最高正化合价为+2,结合原子半径可知K为
Mg;G、J的最高正化合价为+3,结合原子半径可知G为B,J为Al;H的最低化合价为-1,为第ⅦA族元素,
其原子半径大于F,则H为Cl。
【解析】A.Cl的最高价氧化物对应的水化物为高氯酸,S的最高价氧化物对应的水化物为硫酸,由于非金
属性:Cl>S,则高氯酸的酸性大于硫酸,故A错误;
B.Mg2+、O2-电子层结构相同,核电荷数越大离子半径越小,故离子半径:Mg2+Mg>Al,故C正确;
D.钠、镁和铝都是活泼金属,都是通过电解其熔融的化合物获得的,故D正确;
故选:A。
1.熟记“序、价”规律。
在短周期元素中,元素的原子序数与其主要化合价的数值在奇偶性上一般一致,“价奇序奇,价偶序偶”。
2.化合价规律
(1)常用等量关系。
①主族元素最高正价=最外层电子数=主族序数=价电子数。
②主族元素的最高正价+|最低负价|=8或2(氢)。
(2)化合价的范围:+1≤最高价≤+7,-4≤最低价≤-1。
(3)化合价的特殊点。
①氟元素没有正化合价。
②氧元素有正化合价,但是没有所在族的最高正化合价。
③金属元素、硼元素没有负化合价。
(4)最高正化合价与其最低负化合价代数和。
①等于0的短周期元素:氢、碳、硅。
②等于2的短周期元素:氮、磷。
③等于4的短周期元素:硫。
④等于6的短周期元素:氯。【变式5-1】短周期主族元素X、Y、Z、W的原子半径和元素最低化合价的关系如图所示。下列叙述正确的
是
A.第一电离能:
B.简单氢化物的沸点:
C.最高价氧化物对应水化物的酸性:
D. 的空间结构为平面三角形
【答案】C
【分析】X、Y、Z、W均为短周期主族元素,据图可知,W原子半径最大,且最低化合价为1,则W为氯
元素,所以Z为氟元素,由于X、Y的原子半径大于氟,根据最低化合价可知X为碳元素,Y为氮元素。
【解析】A.同一周期,第一电离能从左到右呈增大趋势,基态N原子2p能级轨道半充满较稳定,其第一
电离能大于相邻元素,则第一电离能:F>N>C,即Z>Y>X,A项错误;
B.HF和 分子间存在氢键,由于电负性:F>N,因此HF的氢键强于 , 分子间不存在氢键,所
以HF、 、 的沸点依次降低,即简单氢化物的沸点:Z>Y>X,B项错误;
C.N元素的非金属性比碳元素强,所以 酸性大于 ,最高价氧化物对应水化物的酸性:Y>X,C
项正确;
D. 分子中心N原子价层电子对数为 ,采取sp3杂化,孤电子对数为1,则它的空间
结构为三角锥形,D项错误;
故选C。
【变式5-2】(2023上·山东菏泽·高三山东省鄄城县第一中学校考)以化合价为纵坐标,物质类别为横坐标
的图像称为价类二维图,在地壳中的含量仅次于铝,居第四位的元素价类二维图如图所示,下列说法错误
的是A.a与水常温下几乎不发生反应,但在高温下可反应
B.b和c可分别与水发生反应生成e和d
C.e在潮湿的空气中容易转变为d
D.h的某种盐是具备净水和消毒双重功能的水处理剂
【答案】B
【解析】由题中信息可知,在地壳中的含量仅次于铝,居第四位的元素是Fe元素;
【分析】A.Fe与水常温下几乎不发生反应,但在高温下 ,选项A正确;
B.b为FeO,c为 ,FeO和 均不溶于水,均不能直接与水反应生成相应的碱 和 ,
选项B错误;
C. 在潮湿的空气中容易转变为 ,即: ,选项C正确;
D.h为高铁酸盐即含 , 具有强氧化性,能够杀菌消毒,+6价的铁被还原成+3价,又 形成
氢氧化铁胶体具有较大表面积,吸附悬浮杂质可以做净水剂,选项D正确;
答案选B。
【考向六】性质递变型推断
【典例6】(2022上·云南保山·高三统考期中)短周期元素X、Y、Z、W的原子序数依次增大。用表中信息
判断下列说法正确的是
元素 X Y Z W
最高价氧化物的水化物 H ZO
3 4
0.lmo1/L溶液对应的pH(25℃) 1.00 13.00 1.57 0.70
A.元素电负性、第一电离能:ZW D.简单氢化物的沸点:Xr(阳离子)
得电子能
逐渐增强 逐渐减弱
力
失电子能
逐渐减弱 逐渐增强
力
金属性 逐渐减弱 逐渐增强
非金属性 逐渐增强 逐渐减弱
元素性质 离子的氧
阳离子氧化性逐渐增强,阴离子 阳离子氧化性逐渐减弱,阴
化性、还
还原性逐渐减弱 离子还原性逐渐增强
原性
最高正价:由+1→+7(O、F除
主要化合 外) 最高正价数=主族序数(O、F
价 最低负价:主族 除外)
序数-8气态氢化
物 依次减弱 依次增强
的还原性
非金属元
素
气态氢化
气态氢化物的形成越来越容易, 气态氢化物形成越来越困
化合物的 物
其稳定性逐渐增强 难,其稳定性逐渐减弱
性质 的形成难
易
及稳定性
最高价氧
化物对应 酸性逐渐增强 酸性逐渐减弱
水化物的 碱性逐渐减弱 碱性逐渐增强
酸碱性
【变式6-1】(2023下·江苏南通)X、Y、Z、W、R属于元素周期表中前20号主族元素,且原子序数依次
增大。X和Z的基态原子的2p能级上各有两个未成对电子,W与Z同族。R的最外层电子数与最内层电子
数相等。下列说法正确的是
A.元素第一电离能:
B.简单离子半径:
C.简单气态氢化物的热稳定性:
D.最高价氧化物对应水化物的酸性:
【答案】A
【分析】X、Y、Z、W、R属于元素周期表中前20号主族元素,且原子序数依次增大,X和Z的基态原子的
2p能级上各有两个未成对电子,分别为2p2、2p4,即X为C元素,Z为O,则Y为N元素;W与Z同族,则
W为S元素;R的最外层电子数与最内层电子数相等,即最外层电子数为2,且原子序数大于16,则R为
Ca元素,综上,X、Y、Z、W、R分别为C、N、O、S、Ca元素;由上述分析可知,X、Y、Z、W、R分别为
C、N、O、S、Ca元素;
【解析】A.N、O位于第二周期元素,但N原子的2p3结构属于半充满的稳定结构,舍去1个电子所需能
量大,所以元素第一电离能: I (N) > I (O),选项A正确;
1 1
B.S2-、Ca2+的核外电子数均为18,二者核外电子排布相同,但Ca2+的质子数多,对最外层电子数的引力强,
电子Ca2+ 的半径小于S2-,即离子半径:S2- > Ca2+,选项B错误;
C.非金属性: O > S,非金属性越强,其简单气态氢化物的热稳定性越强,则热稳定性:H O > H S,选项C错
2 2
误;
D.碳酸是弱酸,硫酸是强酸,即最高价氧化物对应水化物的酸性: H SO > H CO ,选项D错误;
2 4 2 3答案选A。
【变式6-2】(2022·四川南充·四川省南充高级中学校考一模)主族元素Q、X、Y、Z、W的原子序数依次
增大,且均不大于20。Q的简单氢化物和其最高价含氧酸可以化合成盐,X与Z同主族且Z的原子序数是X
的两倍;Q、Y、W原子的最外层电子数之和为9,下列说法一定正确的是
A.简单氢化物的还原性:ZY
2
【答案】A
【分析】浓度均为0.01mol/L的溶液,W、Y、Z的最高价氧化物对应的水化物的pH都小于7,W、Y、Z的
最高价氧化物对应的水化物是酸,说明W、Y、Z都是非金属元素,W、Z最高价氧化物对应的水化物的
pH=2,为一元强酸,原子序数Z>W,则Z是Cl、W是N;Y的最高价氧化物对应的水化物的pH<2,应该为
二元强酸硫酸,则Y是S;X的最高价氧化物对应的水化物的pH=12,应该为一元强碱氢氧化钠, 则X是
Na;由以上分析可知,W、X、Y、Z分别为N、Na、S、Cl元素;
【解析】A.WZ 为NCl ,NCl 中N原子成3个σ键,有一对未成键的孤对电子,杂化轨道数为4,采取sp3
3 3 3
型杂化,空间构型是三角锥形,选项A错误;
B.Na是非常活泼的金属,工业上采用电解法冶炼Na,选项B正确;
C.ClO 具有强氧化性,能使蛋白质变性,可作为自来水的消毒剂,选项C正确;
2
D.非金属性越强最简单气态氢化物的稳定性越强,故最简单气态氢化物稳定性:Z>Y,选项D正确;
答案选A。
【变式7-2】(2023·江西南昌·统考二模)元素周期表中前20号元素R、X、Y、Z的原子序数依次增大。R
和Y位于同主族,X的简单离子半径在同周期元素中最小。由这四种元素组成一种化合物Q,在Q的溶液
中滴加Ba(OH) 溶液。产生沉淀的物质的量与Ba(OH) 的物质的最的关系如图所示,下列说法正确的是
2 2A.简单离子半径:Z>Y
B.简单气态氯化物的热稳定性:Y>R
C.Q的水溶液显酸性、可作为净水剂
D.M点沉淀物有2种,且物质的量之比为4:1
【答案】C
【分析】元素周期表中前20号元素R、X、Y、Z的原子序数依次增大。R和Y位于同主族,X的简单离子半
径在同周期元素中最小。由这四种元素组成一种化合物Q,在Q的溶液中滴加Ba(OH) 溶液。产生沉淀的
2
物质的量与Ba(OH) 的物质的最的关系如图所示,则X为Al, 1mol氢氧化钡会溶解2mol氢氧化铝,但实
2
际只有1mol沉淀 ,说明还生成了另外的1mol沉淀,加入3mol氢氧化钡会生成2mol氢氧化铝沉淀和
3mol其他沉淀,则另外3mol沉淀是硫酸钡和碳酸钡沉淀,又根据R和Y位于同主族,则R为O,Y为S,Z
为K,Q为硫酸铝钾。
【解析】A.根据同电子层结构核多径小,则简单离子半径:Y>Z,故A错误;
B.根据非金属性越强,其气态氢化物越稳定,则简单气态氯化物的热稳定性:R>Y,故B错误;
C.Q为硫酸铝钾,铝离子水解生成氢氧化铝和氢离子,因此其水溶液显酸性、可作为净水剂,故C正确;
D.M点沉淀物有2种,1mol硫酸铝钾溶液中加入3mol氢氧化钡得到3mol硫酸钡和1mol氢氧化铝,其物
质的量之比为3:1,故D错误。
综上所述,答案为C。
【考向八】无机框图推断
【典例8】(2023上·湖北武汉·高三校联考阶段练习)短周期元素W、X、Y、Z原子序数依次递增,X、Z同
主族,W、Y同主族。由上述元素组成的物质甲~已转化关系如图,乙、丙、丁、戊都是二元化合物,丁的
焰色反应为黄色,已为淡黄色单质。下列说法错误的是
A.只有甲的水溶液为碱性 B.X和Z能形成多种酸根离子
C.沸点:戊 乙 D.电负性:
【答案】A
【分析】丁的焰色反应为黄色,丁中含有Na元素,己为淡黄色单质,己是S单质,W、X、Y、Z原子序数
依次递增,X、Z同主族,W、Y同主族,则Z是S元素、Y是Na元素、W是H元素、X是O元素。甲是
NaOH、乙是H S、丙是SO 、丁是Na S、戊是H O、己是S单质。
2 2 2 2【解析】A.NaOH、Na S的水溶液都为碱性,故A错误;
2
B.O和S能形成 等多种酸根离子,故B正确;
C.H O分子间能形成氢键,沸点:H O H S,故C正确;
2 2 2
D.非金属性越强,电负性越大,电负性: ,故D正确;
选A。
一、解题策略
解题的关键是仔细审题,依物质的特性或特征转化来确定“突破口”,顺藤摸瓜,进而完成全部未知物的
推断。我们可以将推断题的解题方法及推理过程表示如下:
推断题――→――→――→结论―→验证
二、解题“突破口”
1.物质的特殊颜色
相关知识:
(1)有色固体
①红色:Cu、Cu O、Fe O;
2 2 3
②红褐色:Fe(OH) ;
3
③黄色:AgI、Ag PO ;
3 4
④浅黄色:S、NaO 或AgBr;
2 2
⑤蓝色:Cu(OH) ;
2
⑥黑色:炭粉、CuO、FeO、FeS、CuS、Ag S、PbS;
2
⑦紫黑色:KMnO 、I;
4 2
⑧白色:Fe(OH) 、CaCO 、BaSO、AgCl、BaSO。
2 3 4 3
(2)有色溶液:
Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)、MnO(紫红色)、Fe3+与苯酚(紫色)、Fe3+与SCN-(红色)、I 与淀粉
2
(蓝色)等。
水(溶剂) 苯(溶剂) CCl (溶剂)
4
Br 黄→橙 黄→红棕
2
I 深黄→褐 淡紫→紫红 紫→深紫
2
(3)有色气体:
Cl(黄绿色)、Br (g)(红棕色)、NO (红棕色)、I(g)(紫色)、O(淡蓝色)等。
2 2 2 2 3
(4)火焰颜色:
①焰色反应:Na+(黄色)、K+(紫色)、Ca2+(砖红色)等;②蓝色:CO在空气中燃烧;
③淡蓝色:S、H、HS、CH 等在空气中燃烧;④苍白色:H 在Cl 中燃烧。
2 2 4 2 2
2.物质的特征性质相关知识
(1)能使品红溶液褪色的气体:
SO (加热后又恢复红色)、Cl(加热后不恢复红色)。
2 2
(2)沉淀特殊的颜色变化:
①白色沉淀先变灰绿色,再变红褐色:Fe(OH) ――→Fe(OH) ;
2 3
②白色沉淀迅速变棕褐色:AgOH→Ag O。
2
(3)在空气中变为红棕色:NO(无色)――→NO (红棕色)。
2
(4)能使澄清石灰水变浑浊的气体:CO、SO 。
2 2
(5)通入CO 气体变浑浊的溶液:石灰水(过量则变澄清)、NaSiO 溶液、饱和NaCO 溶液、浓苯酚钠溶
2 2 3 2 3
液、NaAlO 溶液等。
2
(6)使湿润的红色石蕊试纸变蓝的气体:NH 。
3
(7)使湿润的淀粉碘化钾试纸变蓝:NO 、Cl、Br 、FeCl 等。
2 2 2 3
(8)能与SO 、Cl、O 等氧化性较强的气体(或其水溶液)反应析出淡黄色沉淀:HS。
2 2 2 2
(9)在一定条件下具有漂白性的物质:NaO、HO、SO 、氯水、O、活性炭等。
2 2 2 2 2 3
(10)能溶解SiO 固体的物质:氢氟酸和NaOH溶液。
2
(11)能与浓硫酸、铜片共热产生红棕色气体(NO )的溶液:硝酸盐(或硝酸)溶液。
2
(12)滴入沸水中可得到红褐色胶体的溶液:含Fe3+的盐溶液。
(13)烟雾现象:
①棕(黄)色的烟:Cu或Fe在Cl 中燃烧;
2
②白烟:Na在Cl 或P在空气中燃烧;NH 遇到HCl气体;
2 3
③白雾:由HX等极易溶于水的气体产生;
④白色烟雾:P在Cl 燃烧。
2
3.物质之间的特征转化关系
相关知识:
(1)连续氧化反应:A――→B――→C――→D(酸或碱)。
①NH (g)――→N――→NO――→NO ――→HNO;
3 2 2 3
②HS(g)――→S――→SO ――→SO ――→HSO ;
2 2 3 2 4
③CH(g)――→C――→CO――→CO――→HCO;
4 2 2 3
④Na(s)――→NaO――→NaO――→2NaOH。
2 2 2
(2)
X可能为弱酸的铵盐:(NH )CO 或NH HCO ;(NH )S或NH HS;(NH )SO 或NH HSO 等。
4 2 3 4 3 4 2 4 4 2 3 4 3
(3)三角转化关系:(4)化合物+化合物→单质+化合物
这类反应主要有:CO+HO(g)=====CO+H、Fe O+3CO=====2Fe+3CO 等。
2 2 2 2 3 2
(5)化合物A+单质B→化合物C+单质D。
这类反应主要有:
CO+2Mg=====2MgO+C;Fe O+3H=====2Fe+3HO;
2 2 3 2 2
Fe+2HCl===FeCl +H↑;C+HO(g)=====CO+H;
2 2 2 2
3Fe+4HO(g)=====Fe O+4H 等。
2 3 4 2
【变式8-1】(2023·天津滨海新·高三校联考开学考试)原子序数依次增大的短周期元素X、Y、Z、R,化合
物 是海水中含量最高的盐类物质,Z的质子数是X质子数的2倍,X、Y、Z三种元素组成两种化合物
A、B的性质如下图。下列说法正确的是
A.简单氢化物沸点: B.简单离子半径:
C.Y与X形成的一种化合物含有离子键和非极性键D.化合物A和B的水溶液皆呈中性
【答案】C
【解析】原子序数依次增大的短周期元素X、Y、Z、R,化合物 是海水中含量最高的盐类物质,可知Y
为Na、R为Cl;X、Y、Z三元素组成两种化合物A、B,A与HCl反应生成的气体可使品红褪色,可知该气
体为二氧化硫,A为亚硫酸钠;A与R (Cl )或X的氢化物反应生成B,则B为硫酸钠,则X为O,Z为S元
2 2
素;结合分析可知,X为O,Y为Na,Z为S,R为Cl元素;
A.水分子之间存在氢键,导致水的沸点较高,即简单氢化物沸点Zb
B.丙中既有离子键又有极性共价键
C.b、c形成的化合物中阴、阳离子数目之比为1∶2
D.a、b、d形成的化合物adb 中,d的杂化方式是sp3
4
【答案】A
【分析】A为单质,丁常用于消毒、漂白,推测A为Cl ,丁为NaClO,常温下乙为液体,推测乙为H O,
2 2
则A+丙的反应为 ,甲可以和水生成NaOH,则甲为Na O,由此a、b、
2
c、d分别为H、O、Na、Cl元素。
【解析】A.b、c对应的离子分别为O2-和Na+,具有相同的核外电子排布,核电荷数越大离子半径越小,
则离子半径:O2->Na+,即b>c, A错误;
B.丙为NaOH,由Na+和OH-构成,则含有离子键和极性共价键, B正确;
C.b为O元素、c为Na元素,二者组成的Na O和Na O 中阴、阳离子数目之比均为1∶2, C正确;
2 2 2
D.a、b、d形成的化合物adb 即为HClO ,Cl原子的价层电子对数为 =4,则Cl的杂化方式
4 4
是sp3, D正确;
答案选A。
【考向九】给定微粒组成推断
【典例9】(2023·辽宁卷)某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。W、X、Y、Z、Q
是核电荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电子数的2倍。
下列说法错误的是A.W与X的化合物为极性分子 B.第一电离能
C.Q的氧化物是两性氧化物 D.该阴离子中含有配位键
【答案】A
【分析】W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W形成1条单键且核电荷数最小,W为H,
X形成4条键,核电荷数大于H,且小于其他三种元素,X为C,Y形成2条单键,核电荷数大于C,Y为
O,W、Y原子序数之和等于Z,Z为F,Y原子价电子数为Q原子价电子数的2倍,Q为Al。
【解析】A.W与X的化合物不一定为极性分子,如CH 就是非极性分子,A错误;
4
B.同周期元素从左到右第一电离能呈增大趋势,则第一电离能F>O>C,B正确;
C.Q为Al,Al O 为两性氧化物,C正确;
2 3
D.该阴离子中L与Q之间形成配位键,D正确;
故答案选A。
1.常见元素的成键数
主族 IA IIA IIIA IVA VA VIA VIIA
元素符号 H Be B、Al C、Si N、P O、S F、Cl
最外层电子数 1 2 3 4 5 6 7
正常的成键数 1 2 3 4 3 2 1
特殊的成键数 4 5(P) 6(S)
2.判断共价型微粒中原子最外层电子数
(1)若分子中含氢原子,则一定不满足8e-稳定结构
(2)共价型微粒:N(e-)=原子的价电子数+成键数±电荷数
①PCl :N(e-) =5+3=8,N(e-) =7+1=8
3 P Cl
②NH +:N(e-) =5+4-1=8,N(e-) =1+1=2
4 N H
③AlCl -:N(e-) =3+4+1=8,N(e-) =7+1=8
4 Al Cl
④COCl :N(e-) =4+4=8,N(e-) =6+2=8,N(e-) =7+1=8(Cl- -Cl)
2 C O Cl
3.离子化合物X Y 中是否含共价键的判断
a b
非金属Y的价态 所含阴离子 是否含共价键
最低价 Ya- 不含
非最低价 Y a- 含有
b
(1)Na S 是由 Na + 和S2-构成的
2 x x
(2)NaBr 是由 Na + 和Br -构成的
3 3(3)K C 是由 K + 和C 3-构成的
3 60 60
(4)Na O 是由 Na + 和O 2-构成的
2 2 2
(5)CaCl 是由 Ca 2+ 和 C l - 构成的
2
(6)Mg N 是由 Mg 2+ 和 N 3 - 构成的
3 2
4.常见化合物的组成
构型 常见化合物
CO 、NO 、SO 、SiO 、CS 、ClO 、CaC 、MgX 、
2 2 2 2 2 2 2 2
AB 型
2
CaX 、BeCl 、KO 、CaO 、BaO 等。
2 2 2 2 2
A B 型 H O 、Na O 、C H 、Na S 、H S 等
2 2 2 2 2 2 2 2 2 2 2 2
A B型 H O、H S、Na O、Na S、N O
2 2 2 2 2 2
A B 型 Mg N
3 2 3 2
Al O 、Al S 、B O 、B S 、N O 、P O 、C O (乙
2 3 2 3 2 3 2 3 2 3 2 3 2 3
A B 型
2 3
二酸酐)。
NH 、SO 、PH 、PCl 、AlCl 、FeCl 、BCl 、BF 、
3 3 3 3 3 3 3 3
AB 型
3
AlF 等
3
AB 型 CH 、SiH 、CCl 、SiCl 、SiF 、CF 等
4 4 4 4 4 4 4
A B 型 C H 、N O
2 4 2 4 2 4
【变式9-1】(2024上·黑龙江哈尔滨·高三哈尔滨三中校考期末)某化合物结构如图所示,其中X、Y、Z、
W为原子序数依次增大的短周期非金属元素,Y是有机分子的骨架元素,M位于元素周期表ds区,下列说
法不正确的是
①第一电离能:
②氢化物沸点:YX,A正确;
B.N最高正价为+5价,O无最高正价,最高正价N大于O,B错误;
C.Na和O形成的过氧化钠中含有非极性共价键,C正确;
D.非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性N大于C,硝酸酸性强于碳酸,D正确;
故选B。
2.(2022·湖南卷)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增大
的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是
A.原子半径: B.非金属性:C.Z的单质具有较强的还原性 D.原子序数为82的元素与W位于同一主族
【答案】C
【分析】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1个共价键,X、
Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和,则X为C元素、Y
为O元素、Z为F元素、W为Si元素。
【解析】A.同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大小顺序为C>O>F,故A
正确;
B.同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元素的非金属性依次减弱,
则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;
C.位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;
D.原子序数为82的元素为铅元素,与硅元素都位于元素周期表ⅣA族,故D正确;
故选C。
3.(2023·湖南卷)日光灯中用到的某种荧光粉的主要成分为3W (ZX ) ∙WY 。已知:X、Y、Z和W为原子
3 4 2 2
序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基
态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
A.电负性:X>Y>Z>W
B.原子半径:XX>Z>W,A错误;
B.同一周期原子半径从左到右依次减小,同一主族原子半径从上到下依次增大,故四种原子的原子半径
大小为:YY B.简单氢化物的还原性:X>Y
C.同周期元素形成的单质中Y氧化性最强 D.同周期中第一电离能小于X的元素有4种
【答案】D
【分析】Y位于第三周期,且最高正价与最低负价的代数和为6,则Y是Cl元素,由X、Y形成的阴离子和
阳离子知,X与Y容易形成共价键,根据化合物的形式知X是P元素。
【解析】A.P与Cl在同一周期,则P半径大,即X>Y,A项不符合题意;
B.两者对应的简单氢化物分别是PH 和HCl,半径是P3->Cl-,所以PH 的失电子能力强,还原性强,即
3 3
X>Y,B项不符合题意;
C.同周期元素从左往右,金属性减弱,非金属性增强,各元素对应的金属单质还原性减弱,非金属单质
的氧化性增强,所以Cl 的氧化性最强,C项不符合题意;
2
D.同一周期,从左到右,第一电离能呈现增大的趋势,第VA族元素的第一电离能大于相邻元素的第一电
离能;所以第三周期第一电离能从小到大依次为Na、Al、Mg、Si、S、P、Cl,所以有5种,D项符合题意;
故选D。
6.(2021·湖南卷)W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与X的原子
序数之和,Z的最外层电子数为K层的一半,W与X可形成原子个数比为2:1的 分子。下列说法正确
的是
A.简单离子半径:B.W与Y能形成含有非极性键的化合物
C.X和Y的最简单氢化物的沸点:
D.由W、X、Y三种元素所组成化合物的水溶液均显酸性
【答案】B
【分析】Z的最外层电子数为K层的一半,则Z的核外有3个电子层,最外层电子数为1,即为Na,W与X
能形成原子个数比为2:1的18电子的分子,则形成的化合物为N H ,所以W为H,X为N,Y的原子序数
2 4
是W和X的原子序数之和,则Y为O。据此分析解答。
【解析】由分析可知,W为H,X为N,Y为O,Z为Na。
A.离子的电子层数相同时,原子序数越小,半径越大,即离子半径大小为:N3->O2->Na+,即简单离子半
径为:X>Y>Z,故A错误;
B.W为H,Y为O,能形成H O ,含有极性共价键和非极性共价键,故B正确;
2 2
C.X的最简单氢化物为氨气,Y的最简单氢化物为水,水的沸点高于氨气,即最简单氢化物的沸点为Y>
X,故C错误;
D.由W、X、Y三种元素形成的化合物有硝酸,硝酸铵,氨水等,硝酸,硝酸铵显酸性,氨水显碱性,故
由W、X、Y三种元素形成的化合物不一定都是酸性,故D错误;
故选B。
7.(2021·浙江卷)现有4种短周期主族元素X、Y、Z和Q,原子序数依次增大,其中Z、Q在同一周期。
相关信息如下表:
元素 相关信息
X 最外层电子数是核外电子总数的一半
Y 最高化合价和最低化合价之和为零
Z 单质为淡黄色固体,常存在于火山喷口附近
Q 同周期元素中原子半径最小
下列说法正确的是
A.常温时,X单质能与水发生剧烈反应
B.Y与Q元素组成的YQ 分子,空间构型为正四面体
4
C.Y、Z、Q最高价氧化物对应水化物的酸性依次减弱
D.第五周期且与Q同主族元素的单质在常温常压下呈液态
【答案】B
【分析】X原子的最外层电子数是核外电子总数的一半,由于最外层电子数不超过8个,因此X只能是第
二周期的Be;Y元素的最高化合价和最低化合价之和为零,位于第ⅣA族,Y是C或Si;Z单质为淡黄色固
体,常存在于火山喷口附近,因此Z是S;Q是同周期元素中原子半径最小,且Z和Q位于同一周期,因此
Q是Cl,据此解答。
【解析】根据以上分析可知X是Be,Y是C或Si,Z是S,Q是Cl。则A.Be的金属性弱于Mg,常温时镁和冷水不反应,因此Be单质不能与水发生剧烈反应,A错误;
B.Y与Q元素组成的CCl 或SiCl 分子,空间构型均为正四面体,B正确;
4 4
C.Y、Z、Q三种元素的非金属性逐渐增强,非金属性越强,最高价含氧酸的酸性越强,则最高价氧化物对
应水化物的酸性依次增强,C错误;
D.第五周期且与Cl同主族元素的单质是碘,在常温常压下呈固态,D错误;
答案选B。
8.(2021·江苏卷)前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y
的周期序数与族序数相等,基态时Z原子3p原子轨道上有5个电子,W与Z处于同个主族。下列说法正确
的是
A.原子半径:r(X)O>C,故B正确;
C.同一周期从左到右原子半径逐渐减小,同一主族从上到下原子半径逐渐增大,电子层越多半径越大,
所以原子半径:Cl>C>F,故C错误;
D.OF 中,F为-1价,则O的化合价为+2价,故D正确;
2
答案选C。1.(2023上·新疆阿克苏·高三新疆维吾尔自治区阿克苏地区第二中学校考)W、X、Y是三种短周期主族元
素且分别位于三个周期,X和Y位于同一主族且原子序数存在2倍关系。 (M=278g/mol)的热重
曲线(空气中加热)如图所示。下列说法不正确的是
A.X和Y的简单氢化物稳定性:X>Y
B.W和金属钠形成的化合物为离子化合物
C.最终曲线Q所得到的物质为Z X
3 4
D.热重曲线的第1、2、3个拐点失去的都是
【答案】C
【分析】根据“W、X、Y是三种短周期主族元素且分别位于三个周期”推出其中一定有H;又根据“X和Y
位于同一主族且原子序数存在2倍关系”推出X和Y为O和S,则W为H,结合化合物的化学式,知X为
O,Y为S。根据 (M=278g/mol),推出Z的摩尔质量为 ,故Z为Fe,该物质为
。
【解析】A.同一主族元素自上而下非金属性减弱,则简单氢化物的热稳定性逐渐减弱,故稳定性:
,A正确;
B.NaH是由Na+和H-构成的离子化合物,B正确;
C.8.34g的 的物质的量为0.03mol,其中全部结晶水为0.21mol、质量为3.78g,结合M、N、
P的质量计算,第一个拐点失去0.09mol ,第二个拐点失去0.09mol ,第三个拐点失去0.03mol
,最终剩余的是Fe的氧化物,其中Fe的物质的量为0.03mol,质量为1.68g,则O的质量为0.72g,物
质的量0.045mol, ,故最终曲线Q所得物质为 ,C错误;
D.结合选项C可知,热重曲线的第1、2、3个拐点失去的都是 , D正确;
故选C。
2.X、Y、Z、W为原子序数依次增大的短周期主族元素,X与W同主族,Y、Z同周期。四种元素组成的某
化合物M的结构如图所示。下列叙述错误的是A.电负性:XY>Z>W
D.X、Z两种元素形成化合物时,Z总显负价,说明非金属性:Z>X
【答案】B
【分析】X的价电子排布为nsnnpn即可推知n=2,即X为C元素;Z的第一电离能都小于同周期相邻元素,
又Z处于第二周期,可推知Z为O元素,则Y为N元素;W与其他元素不在同一周期,即W只能为第一周
期,为H元素;
【解析】A.Z和X的简单氢化物分别为H O和CH ,由于水分子间有氢键,即水的沸点一定大于甲烷,但
2 4
中没有说明Z的简单氢化物,可能液态或固态的烃,选项A正确;
B.Z为O,氧气是非极性分子,但臭氧是极性分子,选项B错误;
C.W、X、Y、Z原子半径大小:C>N>O>H,选项C正确;
D.X为C、Z为O,二者都是非金属元素,原子之间通过共价键结合形成化合物。元素非金属性越强,在
形成化合物时,共用电子对就偏向吸引电子能力强的O元素,该元素化合价就显负价,吸引电子能力弱的
形成化合物时元素显正价,因此可根据X、Z两种元素形成化合物时,Z总显负价,判断元素的非金属性:
Z>X,选项D正确;答案选B。
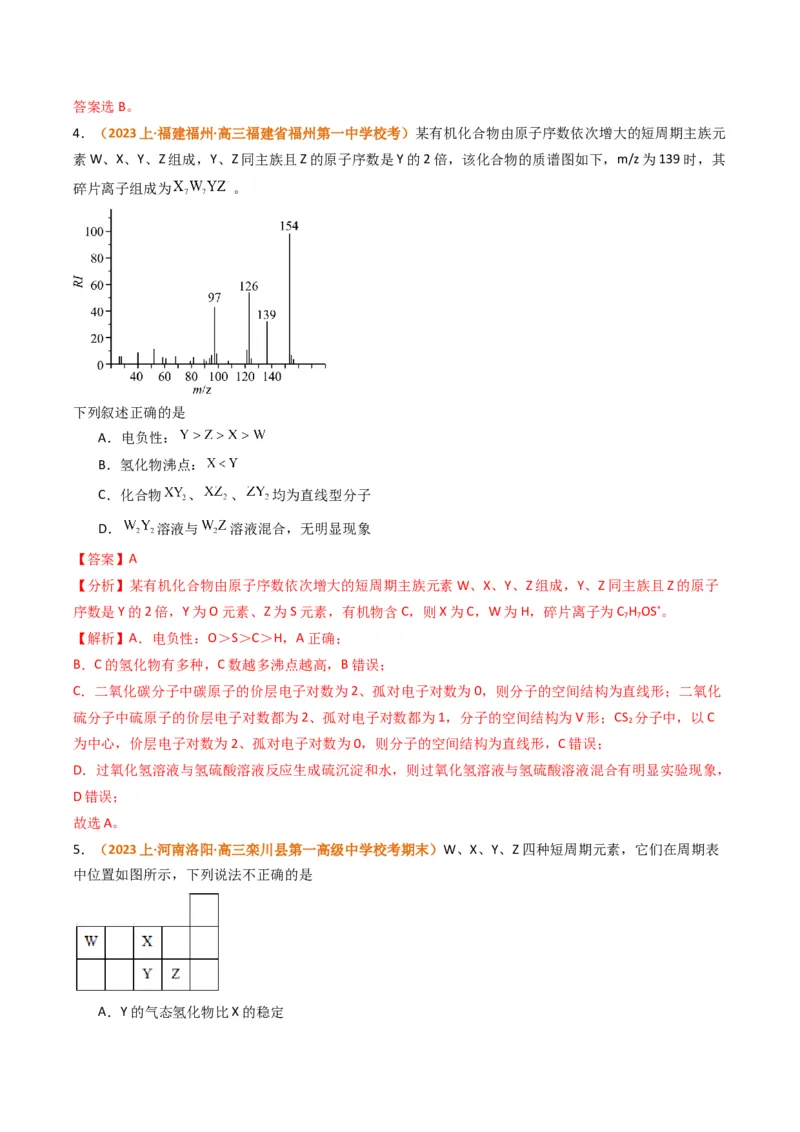
4.(2023上·福建福州·高三福建省福州第一中学校考)某有机化合物由原子序数依次增大的短周期主族元
素W、X、Y、Z组成,Y、Z同主族且Z的原子序数是Y的2倍,该化合物的质谱图如下,m/z为139时,其
碎片离子组成为 。
下列叙述正确的是
A.电负性:
B.氢化物沸点:
C.化合物 、 、 均为直线型分子
D. 溶液与 溶液混合,无明显现象
【答案】A
【分析】某有机化合物由原子序数依次增大的短周期主族元素W、X、Y、Z组成,Y、Z同主族且Z的原子
序数是Y的2倍,Y为O元素、Z为S元素,有机物含C,则X为C,W为H,碎片离子为C H OS+。
7 7
【解析】A.电负性:O>S>C>H,A正确;
B.C的氢化物有多种,C数越多沸点越高,B错误;
C.二氧化碳分子中碳原子的价层电子对数为2、孤对电子对数为0,则分子的空间结构为直线形;二氧化
硫分子中硫原子的价层电子对数都为2、孤对电子对数都为1,分子的空间结构为V形;CS 分子中,以C
2
为中心,价层电子对数为2、孤对电子对数为0,则分子的空间结构为直线形,C错误;
D.过氧化氢溶液与氢硫酸溶液反应生成硫沉淀和水,则过氧化氢溶液与氢硫酸溶液混合有明显实验现象,
D错误;
故选A。
5.(2023上·河南洛阳·高三栾川县第一高级中学校考期末)W、X、Y、Z四种短周期元素,它们在周期表
中位置如图所示,下列说法不正确的是
A.Y的气态氢化物比X的稳定B.Z、Y、W的最高价氧化物对应水化物的酸性依次降低
C.WH 与Z元素的单质在一定条件下可能发生化学反应
4
D.W的位置是第二周期、第ⅣA族
【答案】A
【分析】W、X、Y、Z四种短周期元素,它们在周期表中位置如表所示,Z位于第三周期ⅦA族,为Cl元素,
结合各元素的相对位置可知,Y为S元素,X为O元素,W为C元素,以此分析解答。
【解析】A.由分析可知,X为O元素,Y为S元素,非金属性越强,气态氢化物越稳定,非金属性SS>C,所以Z、Y、W的最高价氧化物对应水化物的酸性依次降低,B项正确;
C.由分析可知, 为 ,Z为Cl元素, 与 在光照条件下可能发生取代反应,C项正确;
D.由分析可知,W为C元素,在周期表中位于第二周期第ⅣA族,D项正确;
故选A。
6.(2024上·河北石家庄·高三石家庄外国语学校阶段考)“祝融号”火星车发回的遥测信号显示,火星的
气体及岩石中富含原子序数依次递增的四种短周期主族元素X、Y、Z、W,它们分属长两个周期,且只含
一种金属元素,X、W同主族,四种元素的原子最外层电子数之和为16,Y元素是地壳中含量最多的元素。
下列判断错误的是
A.一定条件下Z可以与XY 发生反应
2
B.简单氢化物沸点:XW>Y>X
D.Y与Z形成的化合物中可能含有非极性键
【答案】C
【分析】由Y元素是地球地壳中含量最高的元素,可知Y为O;X、Y、Z、W原子序数递增的四种短周期主
族元素,X、W同主族,设X的最外层电子数为m,Z的最外层电子数为n,则与X同主族的W的最外层电
子数也为m,根据四种元素的原子最外层电子数之和为16可得2m+n+6=16,可得2m+n=10,若m=1,则
n=8(Z的最外层电子数为8,不符合短周期主族元素要求,舍弃);若m=2,则n=6(X、W分别为Be、
Mg,不符合只含一种金属元素的要求,舍弃);若m=3,=4(W、Z分别为Al和Si,不符合原子序数递增
的规律,舍弃);若m=4,n=2,则X是C元素,W是Si元素,Z是Mg元素,符合题意。综上分析可知,
X、Y、Z、W分别为C、O、Mg、Si。
【解析】A.Mg可以在CO 中燃烧置换出C,故A正确;
2
B.X、Y的简单氢化物分别是CH 、H O,H O能形成分子间氢键,CH 则没有,故沸点:CH Si>C>O,故C错误;
D.Y与Z形成的MgO 中可能含有O-O非极性键,故D正确;
2故答案选C。
7.(2023上·江苏泰州·高三姜堰中学校考期中)W、X、Y、Z是原子序数依次增大的四种短周期主族元素,
W基态原子只有一种自旋取向的电子,X最高正化合价与最低负化合价代数和为零,Y的单质在空气中含
量最高,Z位于第三周期,其基态原子s能级上的电子总数与p能级上的电子总数相等。下列说法正确的是
A.第一电离能 :Z>X>Y
B.简单气态氢化物的热稳定性:X>Y
C.X、Y均能与W形成含有非极性键的化合物
D.工业上制备Z单质是通过电解其氯化物的水溶液而获得
【答案】C
【分析】W基态原子只有一种自旋取向的电子,则W为H,X最高正化合价与最低负化合价代数和为零,
则X为C,Y的单质在空气中含量最高,则Y为N,Z位于第三周期,其基态原子s能级上的电子总数与p
能级上的电子总数相等,则Z为Mg,据此回答。
【解析】A.第一电离能 :N>C>Mg,A错误;
B.简单气态氢化物的热稳定性:NH >CH ,B错误;
3 4
C.C、N均能与H形成C H 、N H 等含有非极性键的化合物,C正确;
2 4 2 4
D.工业上制备Mg单质是通过电解其熔融氯化物而获得,D错误;
故选C。
8.常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01mol/L)的pH和
原子半径、原子序数的关系如图所示。下列说法不正确的是
A.电负性:Z>Y>X
B.简单离子的乎径:Y>Z>W>X
C.同浓度氢化物水溶液的酸性:ZY>X>W,C正确;
D.元素Z为F元素,F元素无正化合价,D错误;
答案选C。
11.(2023上·浙江嘉兴·高三统考阶段练习)X、Y、Z、R、Q是元素周期表中原子序数依次增大的前四周期
元素,X是宇宙中含量最多的元素;Y与Z同周期,Y基态原子有3个未成对电子,Z元素原子的价层电子
排布为 ;R元素简单离子在同周期离子中半径最小;Q元素最高能层只有1个电子,其余能层均充
满电子。下列说法不正确的是
A. 是含有极性键和非极性键的极性分子
B.第一电离能:
C.Q在周期表的ds区
D.电负性:
【答案】D
【分析】结合题意可推知:X是宇宙中含量最多的元素即H,Y与Z同周期,Y基态原子有3个未成对电子,
Z元素原子的价层电子排布为 ,n只能取2,故Z价层电子排布为2s22p4,为O元素,故Y为N元素;
R元素简单离子在同周期离子中半径最小,R为Al;Q元素最高能层只有1个电子,其余能层均充满电子,
故Q为Cu。
【解析】A.结合题意及分析可知, 为H O ,是含有极性键和非极性键的极性分子,A正确;
2 2
B.第一电离能同周期从左往右逐渐增大,同主族从上到下逐渐减小,故: ,B正确;
C.Q为Cu,第四周期第IB族,位于周期表的ds区,C正确;
D.同周期主族元素自左而右电负性增大,N、O在它们的氢化物中都表现负价,说明二者的电负性都比氢
元素大,则电负性:H<N<O,而AlH 钠元素显正价,故电负性H>Al,故电负性: ,D错
3误;
故选D。
12.(2024·河北·校联考模拟预测)化合物[Z (YX ) •W X]是一种重要的矿物资源,可用于制造含Y化肥。
3 4 2 2
W、X、Y、Z为元素周期表前20号元素,原子序数依次增加,只有一种金属元素,其中元素Z与X质子数
之和是Y与W质子数之差的2倍。下列说法错误的是
A.Y的最高价氧化物的水化物是中强酸
B.X的简单氢化物的稳定性比Y的强
C.简单离子的半径:Z>Y>X>W
D.Z与X可以形成既有离子键又有共价键的化合物
【答案】C
【分析】W、X、Y、Z为元素周期表前20号元素,原子序数依次增加,只有一种金属元素,结合
Z (YX ) •W X化学式可知,推测W为氢、X为氧;可用于制造含Y化肥,且Z (YX ) •W X中Z为+2价、YX 原
3 4 2 2 3 4 2 2 4
子团显-3价,则Y为磷;其中元素Z与X质子数之和是Y与W质子数之差的2倍,则XZ的质子数之和为
28,那么Z为钙;检查推理正确;
【解析】A.Y的最高价氧化物的水化物是磷酸,磷酸为中强酸,A正确;
B.非金属性越强,其简单氢化物稳定性越强,则O的简单氢化物的稳定性比P的强,B正确;
C.电子层数越多半径越大,电子层数相同时,核电荷数越大,半径越小;简单离子的半径:P3->Ca2+>O2-
>H+,C错误;
D.Z与X可以形成既有离子键又有共价键的化合物,例如过氧化钙CaO ,D正确;
2
故选C。