文档内容
题型 15 沉淀溶解平衡及图像分析
目录
.....................................................................................................................................1
【考向一】沉淀溶解平衡及其影响因素..........................................................................................................1
【考向二】沉淀溶解平衡的应用......................................................................................................................3
【考向三】K 概念及其影响因素.....................................................................................................................4
sp
【考向四】K 的计算类型.................................................................................................................................6
sp
【考向五】溶液离子的沉淀顺序实验分析......................................................................................................7
【考向六】沉淀溶解平衡图像分析..................................................................................................................9
【考向七】沉淀滴定的图像分析....................................................................................................................12
...................................................................................................................................14
【考向一】沉淀溶解平衡及其影响因素
【典例1】如图所示,有T、T 两种温度下两条BaSO 在水中的沉淀溶解平衡曲线,在T 温度下,下列说
1 2 4 1
法不正确的是
A.加入NaSO 可使溶液由a点变到b点
2 4
B.在T 曲线上方区域(不含曲线)任意一点时,均有BaSO 沉淀生成
1 4
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点1.沉淀溶解平衡的特点
2.影响沉淀溶解平衡的因素
①内因:难溶电解质本身的性质,这是决定因素。
②外因:
【变式1-1】(2023下·上海宝山·高三)某温度下硫酸钡与水组成的混合物中加入少量硫酸钠固体,下列说
法错误的是
A.BaSO 的电离程度减小 B.BaSO 溶解的量减小
4 4
C.c(Ba2+)与c(SO )的乘积不变 D.溶液的导电能力增强
【变式1-2】(2023·海南海口·统考模拟预测)已知:向难溶电解质饱和溶液中加入与该电解质没有相同离
子的强电解质时,使难溶物溶解度增大的效应称为盐效应。常温下,在含大量BaSO 固体的浊液中加入
4
0.01mol下列物质(忽略体积变化),溶液中c(Ba2+)由大到小的排序正确的是
①BaSO ②Na SO ③KNO
4 2 4 3
A.②①③ B.③②① C.③①② D.①③②【考向二】沉淀溶解平衡的应用
【典例2】在温热气候条件下,浅海地区有厚层的石灰石沉积,而深海地区却很少。下列解析不正确的是
A.与深海地区相比,浅海地区水温较高,有利于游离的CO 增多、石灰石沉积
2
B.与浅海地区相比,深海地区压强大,石灰石岩层易被CO 溶解,沉积少
2
C.深海地区石灰石岩层的溶解反应为CaCO (s)+HO(l)+CO(aq)=Ca(HCO )(aq)
3 2 2 3 2
D.海水呈弱碱性,大气中CO 浓度增加,会导致海水中 浓度增大
2
沉淀溶解平衡的应用
1.沉淀的生成
当溶液中离子积(Q)大于溶度积(K )时有沉淀生成。
c sp
①调节pH法:如除去NH Cl溶液中的FeCl 杂质,可加入氨水调节pH至4左右,离子方程式为Fe3++
4 3
3NH ·H O===Fe(OH) ↓+3NH。
3 2 3
②沉淀剂法:如用HS沉淀Cu2+,离子方程式为Cu2++HS===CuS↓+2H+。
2 2
2.沉淀的溶解
当溶液中离子积(Q)小于溶度积(K )时,沉淀可以溶解。
c sp
①酸溶解:用离子方程式表示CaCO 溶于盐酸:CaCO +2H+===Ca2++CO↑+HO。
3 3 2 2
②盐溶解:用离子方程式表示Mg(OH) 溶于NH Cl溶液:Mg(OH) +2NH===Mg2++2NH ·H O。
2 4 2 3 2
③配位溶解:用离子方程式表示AgCl溶于氨水:
AgCl+2NH ·H O===[Ag(NH )]++Cl-+2HO。
3 2 3 2 2
④氧化还原溶解:如不溶于盐酸的硫化物Ag S溶于稀HNO。
2 3
3.沉淀的转化
通常,一种沉淀可以转化为更难溶的沉淀,两种难溶物的溶解能力差别越大,这种转化的趋势就越大。
①实质:沉淀溶解平衡的移动。
②实例:AgNO 溶液――→AgCl――→AgBr,则K (AgCl)>K (AgBr)。
3 sp sp
③应用:
锅炉除垢:将CaSO 转化为CaCO ,离子方程式为CaSO+CO===CaCO +。
4 3 4 3
矿物转化:CuSO 溶液遇ZnS转化为CuS,离子方程式为ZnS+Cu2+===CuS+Zn2+。
4
废水处理:利用FeS除废水中的重金属离子,如Hg2+,离子方程式为FeS+Hg2+===HgS+Fe2+。
提醒:
(1)由于沉淀的生成取决于Q 与K 的相对大小,而溶解度与相对分子质量有关,有可能溶解度大的物质
c sp
转化为溶解度小的。
(2)用沉淀法除杂不可能将杂质离子全部通过沉淀除去。一般认为残留在溶液中的离子浓度小于 1×10-5mol·L-1时,沉淀已经完全。
【变式2-1】(2023上·江西宜春·高三江西省宜丰中学校考)将浓盐酸加到NaCl饱和溶液中,会析出NaCl
晶体,对这种现象正确的解释是
A.由于c (Cl-)增加,使溶液中c (Na+)·c (Cl-)>K (NaCl),故产生NaCl晶体
平 平 平 sp
B.HCl是强酸,所以它能使NaCl沉淀出来
C.由于c (Cl-)增加,使NaCl的溶解平衡向析出NaCl的方向移动,故有NaCl沉淀析出
平
D.酸的存在,降低了盐的溶解度
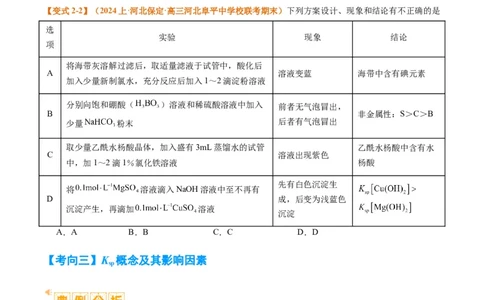
【变式2-2】(2024上·河北保定·高三河北阜平中学校联考期末)下列方案设计、现象和结论有不正确的是
选
实验 现象 结论
项
将海带灰溶解过滤后,取适量滤液于试管中,酸化后
A 溶液变蓝 海带中含有碘元素
加入少量新制氯水,充分反应后加入1~2滴淀粉溶液
分别向饱和硼酸( )溶液和稀硫酸溶液中加入 前者无气泡冒出,
B 非金属性:S>C>B
少量 粉末 后者有气泡冒出
取少量乙酰水杨酸晶体,加入盛有3mL蒸馏水的试管 乙酰水杨酸中含有水
C 溶液出现紫色
中,加1~2滴1%氯化铁溶液 杨酸
先有白色沉淀生
将 溶液滴入NaOH溶液中至不再有
D 成,后变为浅蓝色
沉淀产生,再滴加 溶液
沉淀
A.A B.B C.C D.D
【考向三】K 概念及其影响因素
sp
【典例3】(2023上·辽宁葫芦岛)下列有关 沉淀溶解平衡的说法中错误的是
A. 的溶度积常数表达式
B. 难溶于水,溶液中没有 和SO
C.升高温度, 的溶解度增大
D.向 悬浊液中加入 固体, 溶解的量减少1.溶度积和浓度商
以A B (s) mAn+(aq)+nBm-(aq)为例:
m n
溶度积 浓度商
概念 沉淀溶解的平衡常数 溶液中有关离子浓度幂的乘积
符号 K Q
sp c
K (A B )= Q(A B )=
sp m n c m n
表达式 cm(An+)·cn(Bm-),式中的浓度都是平衡 cm(An+)·cn(Bm-),式中的浓度
浓度 是任意浓度
判断在一定条件下沉淀能否生成或溶解:
①Q>K :溶液过饱和,有沉淀析出;
c sp
应用
②Q=K :溶液饱和,处于平衡状态;
c sp
③QC>Si 液体变浑浊
A.A B.B C.C D.D
【考向六】沉淀溶解平衡图像分析
【典例6】(2024上·山东菏泽·高三山东省鄄城县第一中学校考) 在不同温度下的沉淀溶解平衡曲
线如图所示( )。下列说法不正确的是
A.温度为 时, B. 的溶解度:
C. 的溶解过程吸收能量 D.将Z溶液升温可以得到Y溶液
1.解沉淀溶解平衡图像题的三步骤
第一步:明确图像中纵、横坐标的含义
纵、横坐标通常是难溶物溶解后电离出的离子浓度。
第二步:理解图像中线上点、线外点的含义(1)以氯化银为例,在该沉淀溶解平衡图像上,曲线上任意一点都达到了沉淀溶解平衡状态,此时Q=K 。在
sp
温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变化,不会出现在曲线以外。
(2)曲线上方区域的点均为过饱和溶液,此时Q>K 。
sp
(3)曲线下方区域的点均为不饱和溶液,此时QCaCO >MnCO;
4 3 3
③X点对于CaSO 来说要析出沉淀,对于CaCO 来说是不饱和溶液,能继续溶解CaCO ;
4 3 3
④Y点:[SO2- ]>[Ca2+],二者浓度的乘积等于10-5;Z点:[CO2-
]<[Mn2+],二者浓度的乘积等于10-10.6。
4 3
3.氢氧化物的溶解平衡图像(1)K [Fe(OH)]<K [Cu(OH)]
sp 3 sp 2
(2)a点到b点可加入碱性物质
(3)d点对于Fe3+可沉淀,对于Cu2+不可沉淀
4.图像分析应注意下列四点
(1)曲线上任一点均为饱和溶液,线外的点为非饱和溶液,可根据Q与K 的大小判断。
sp
(2)求K 时可找曲线上合适的一点确定离子浓度进行计算,曲线上任一点的K 相同。
sp sp
(3)若坐标表示浓度的对数时,要注意离子浓度的换算,如lgc(X-)=a,则c(X-)=10a。
(4)若坐标表示浓度的负对数[pX=-lgc(X-)]时,pX越大,c(X-)越小,c(X-)=10-pX。
【变式6-1】(2023上·河南周口·高三项城市第一高级中学校联考)常温下, 、 和
在水中达沉淀溶解平衡时的pM-pH关系如图所示 ,M代表 、 或 ;
时可认为M离子沉淀完全,已知 , 。
下列叙述正确的是
A.ⅰ曲线代表的是
B.a、b两点对应物质的 和溶解度均相同
C. 、 的混合溶液中 时二者能同时沉淀
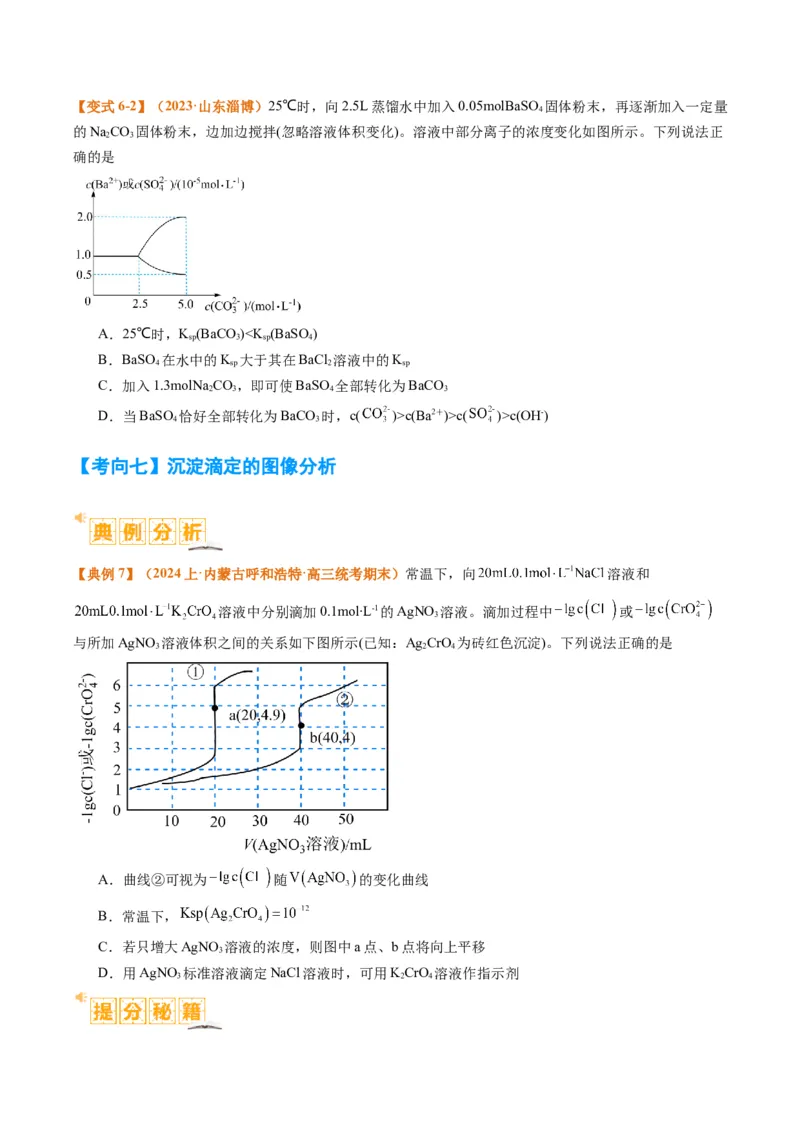
D.“沉铜”时,若将pH从5.0提高到5.5,则铜损失的量降低至原来的10%【变式6-2】(2023·山东淄博)25℃时,向2.5L蒸馏水中加入0.05molBaSO 固体粉末,再逐渐加入一定量
4
的NaCO 固体粉末,边加边搅拌(忽略溶液体积变化)。溶液中部分离子的浓度变化如图所示。下列说法正
2 3
确的是
A.25℃时,K (BaCO)c(Ba2+)>c( )>c(OH-)
4 3
【考向七】沉淀滴定的图像分析
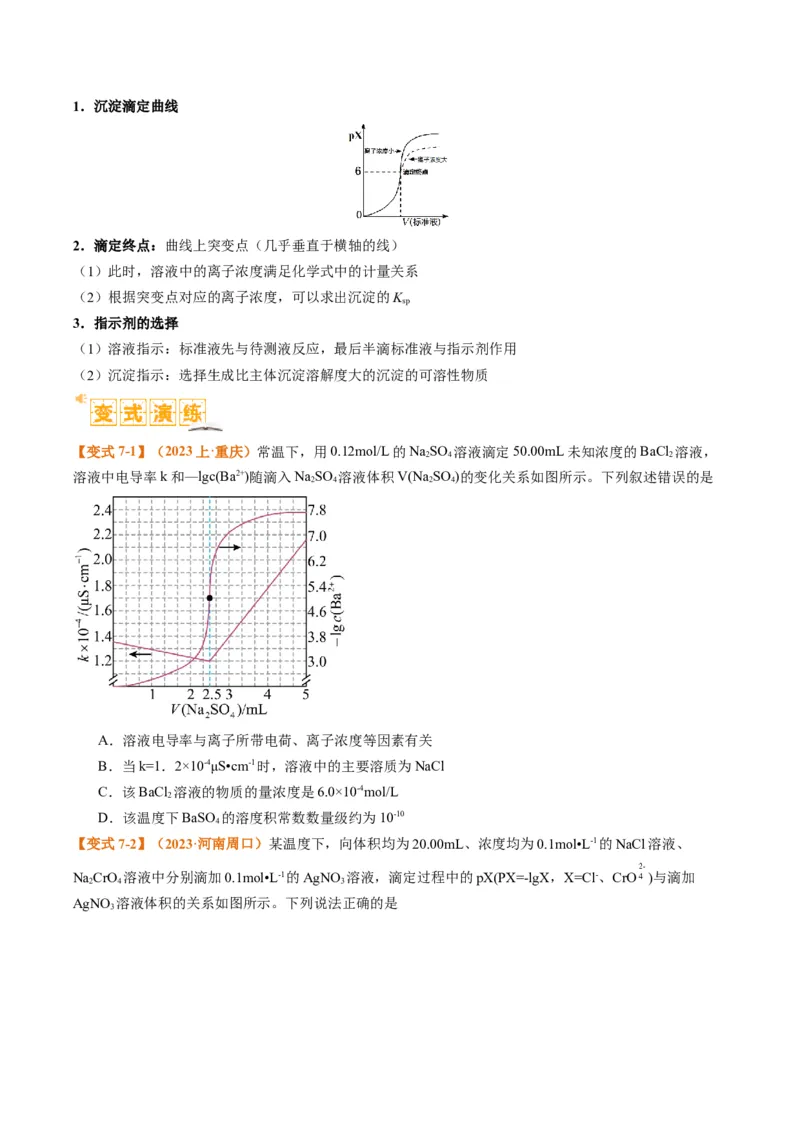
【典例7】(2024上·内蒙古呼和浩特·高三统考期末)常温下,向 溶液和
溶液中分别滴加0.1mol∙L-1的AgNO 溶液。滴加过程中 或
3
与所加AgNO 溶液体积之间的关系如下图所示(已知:Ag CrO 为砖红色沉淀)。下列说法正确的是
3 2 4
A.曲线②可视为 随 的变化曲线
B.常温下,
C.若只增大AgNO 溶液的浓度,则图中a点、b点将向上平移
3
D.用AgNO 标准溶液滴定NaCl溶液时,可用KCrO 溶液作指示剂
3 2 41.沉淀滴定曲线
2.滴定终点:曲线上突变点(几乎垂直于横轴的线)
(1)此时,溶液中的离子浓度满足化学式中的计量关系
(2)根据突变点对应的离子浓度,可以求出沉淀的K
sp
3.指示剂的选择
(1)溶液指示:标准液先与待测液反应,最后半滴标准液与指示剂作用
(2)沉淀指示:选择生成比主体沉淀溶解度大的沉淀的可溶性物质
【变式7-1】(2023上·重庆)常温下,用0.12mol/L的NaSO 溶液滴定50.00mL未知浓度的BaCl 溶液,
2 4 2
溶液中电导率k和—lgc(Ba2+)随滴入NaSO 溶液体积V(Na SO )的变化关系如图所示。下列叙述错误的是
2 4 2 4
A.溶液电导率与离子所带电荷、离子浓度等因素有关
B.当k=1.2×10-4μS•cm-1时,溶液中的主要溶质为NaCl
C.该BaCl 溶液的物质的量浓度是6.0×10-4mol/L
2
D.该温度下BaSO 的溶度积常数数量级约为10-10
4
【变式7-2】(2023·河南周口)某温度下,向体积均为20.00mL、浓度均为0.1mol•L-1的NaCl溶液、
NaCrO 溶液中分别滴加0.1mol•L-1的AgNO 溶液,滴定过程中的pX(PX=-lgX,X=Cl-、CrO )与滴加
2 4 3
AgNO 溶液体积的关系如图所示。下列说法正确的是
3A.曲线II表示AgNO 溶液滴定NaCl溶液的过程
3
B.K (Ag CrO)=10-2b
sp 2 4
C.其他条件不变,如果NaCl溶液浓度改为0.05mol•L-1,则滴定终点向上移动
D.若a=5 b=4,则用AgNO 标准液滴定NaCl时可用KCrO 溶液做指示剂
3 2 4
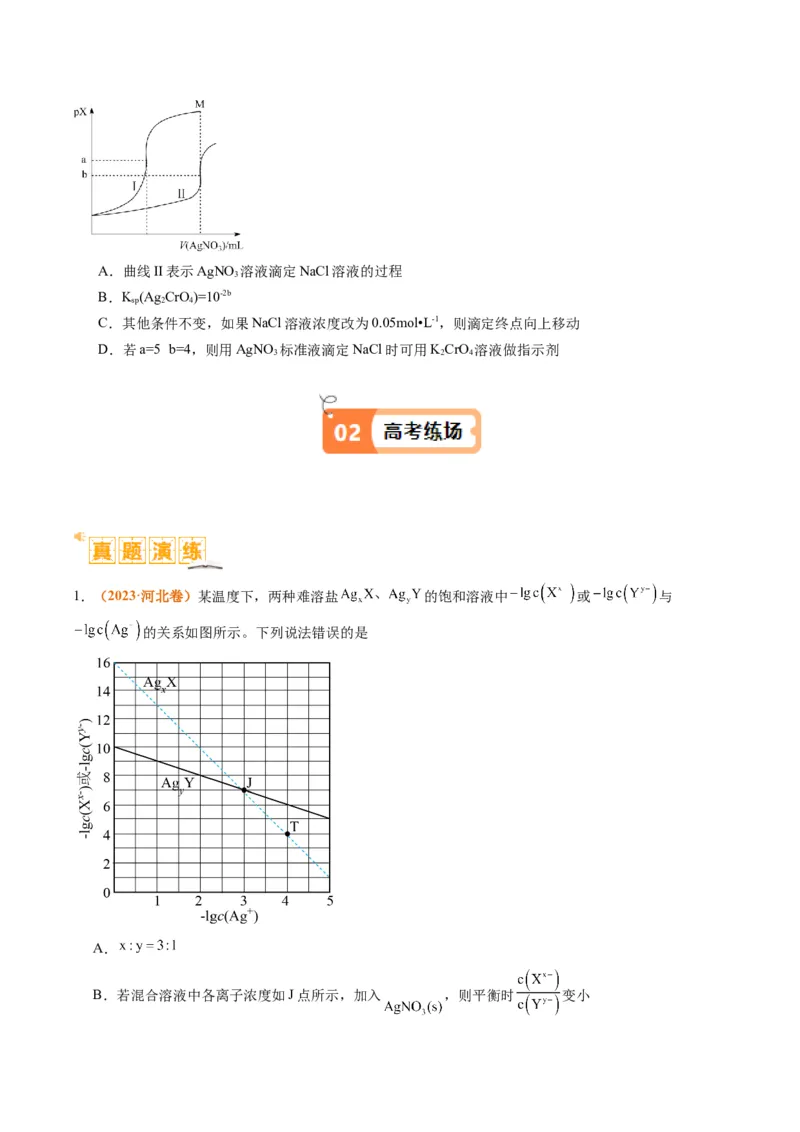
1.(2023·河北卷)某温度下,两种难溶盐 的饱和溶液中 或 与
的关系如图所示。下列说法错误的是
A.
B.若混合溶液中各离子浓度如J点所示,加入 ,则平衡时 变小C.向 固体中加入 溶液,可发生 的转化
D.若混合溶液中各离子起始浓度如T点所示,待平衡时
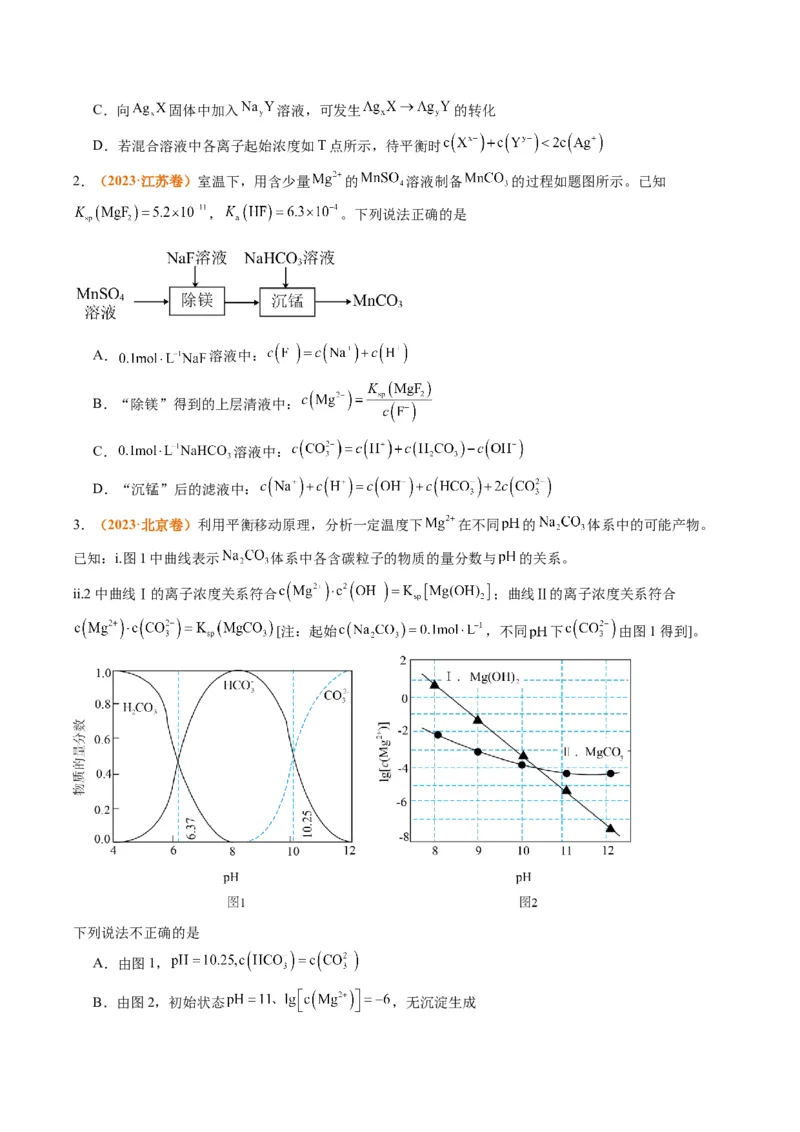
2.(2023·江苏卷)室温下,用含少量 的 溶液制备 的过程如题图所示。已知
, 。下列说法正确的是
A. 溶液中:
B.“除镁”得到的上层清液中:
C. 溶液中:
D.“沉锰”后的滤液中:
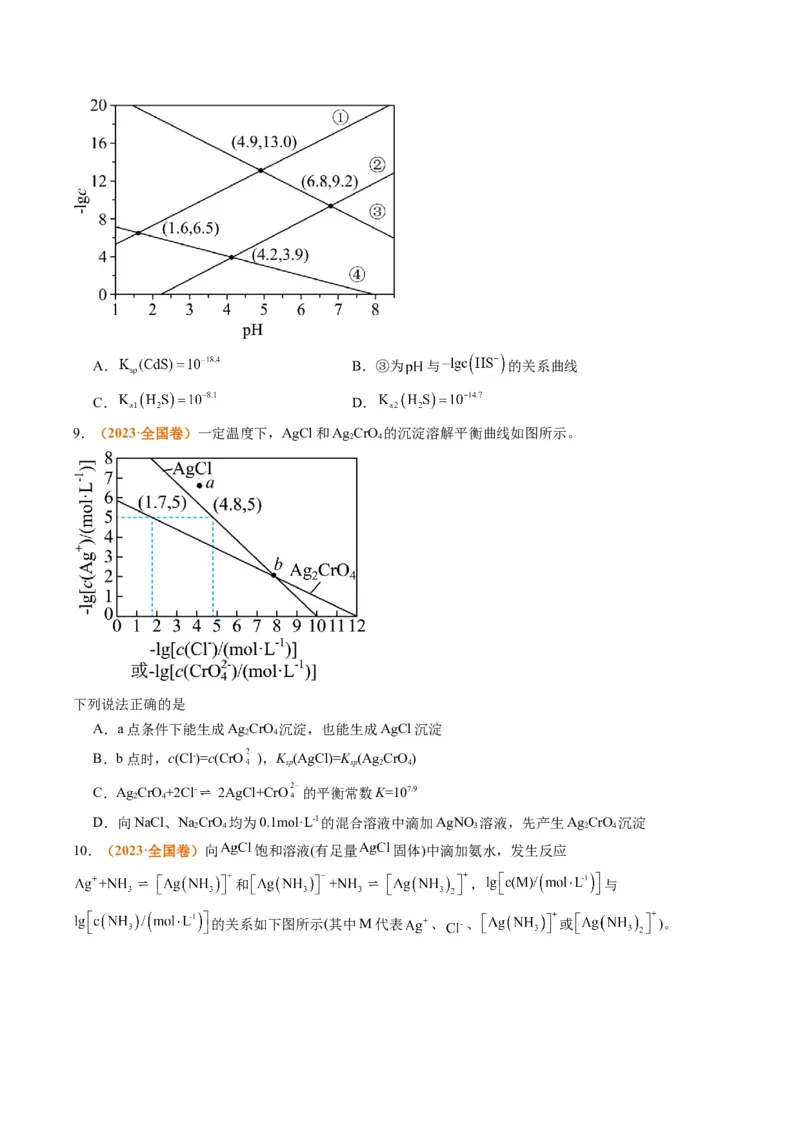
3.(2023·北京卷)利用平衡移动原理,分析一定温度下 在不同 的 体系中的可能产物。
已知:i.图1中曲线表示 体系中各含碳粒子的物质的量分数与 的关系。
ii.2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同 下 由图1得到]。
下列说法不正确的是
A.由图1,
B.由图2,初始状态 ,无沉淀生成C.由图2,初始状态 ,平衡后溶液中存在
D.由图1和图2,初始状态 、 ,发生反应:
4.(2023·浙江卷)探究卤族元素单质及其化合物的性质,下列方案设计、现象和结论都正确的是
实验方案 现象 结论
分层,下层由紫红色 碘在浓 溶液中的溶解
A 往碘的 溶液中加入等体积浓 溶液,振荡 变为浅粉红色,上层 能力大于在 中的溶
呈棕黄色
解能力
B 用玻璃棒蘸取次氯酸钠溶液点在 试纸上 试纸变白 次氯酸钠溶液呈中性
向 溶液中先滴加4滴
先产生白色沉淀,再 转化为 ,
C
溶液,再滴加4滴 溶
产生黄色沉淀 溶解度小于 溶解度
液
取两份新制氯水,分别滴加 溶液和淀粉 前者有白色沉淀,后 氯气与水的反应存在限
D
溶液 者溶液变蓝色 度
A.A B.B C.C D.D
5.(2023·浙江卷)草酸( )是二元弱酸。某小组做如下两组实验:
实验I:往 溶液中滴加 溶液。
实验Ⅱ:往 溶液中滴加 溶液。
[已知: 的电离常数 ,溶液混合后体积变化忽略不
计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中 时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中 时,溶液中
6.(2023·湖南卷)处理某铜冶金污水(含 )的部分流程如下:已知:①溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
物质
开始沉淀 1.9 4.2 6.2 3.5
完全沉淀 3.2 6.7 8.2 4.6
② 。
下列说法错误的是
A.“沉渣Ⅰ”中含有 和
B. 溶液呈碱性,其主要原因是
C.“沉淀池Ⅱ”中,当 和 完全沉淀时,溶液中
D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水
7.(2023·湖北卷)下列化学事实不符合“事物的双方既相互对立又相互统一”的哲学观点的是
A.石灰乳中存在沉淀溶解平衡
B.氯气与强碱反应时既是氧化剂又是还原剂
C.铜锌原电池工作时,正极和负极同时发生反应
D.Li、Na、K的金属性随其核外电子层数增多而增强
8.(2023·辽宁卷)某废水处理过程中始终保持HS饱和,即 ,通过调节pH使 和
2
形成硫化物而分离,体系中 与 关系如下图所示,c为 和 的浓度,单位为
。已知 ,下列说法正确的是A. B.③为 与 的关系曲线
C. D.
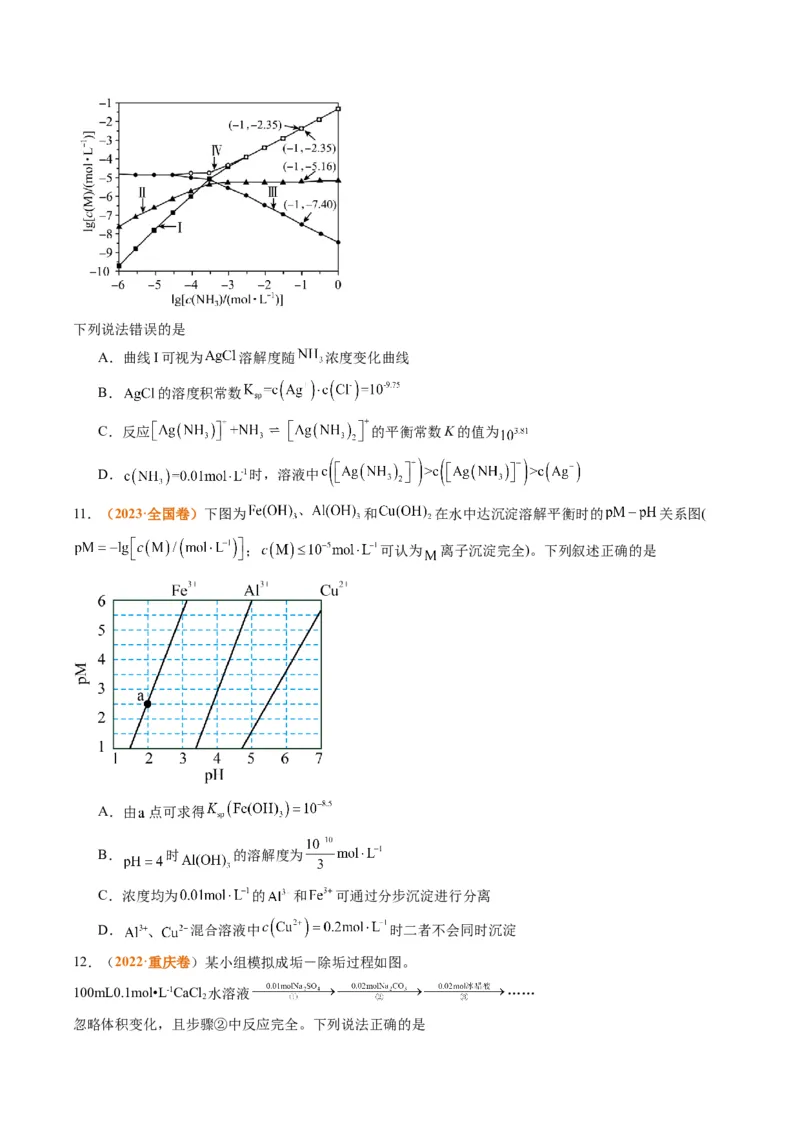
9.(2023·全国卷)一定温度下,AgCl和Ag CrO 的沉淀溶解平衡曲线如图所示。
2 4
下列说法正确的是
A.a点条件下能生成Ag CrO 沉淀,也能生成AgCl沉淀
2 4
B.b点时,c(Cl-)=c(CrO ),K (AgCl)=K (Ag CrO)
sp sp 2 4
C.Ag CrO+2Cl- 2AgCl+CrO 的平衡常数K=107.9
2 4
D.向NaCl、NaCrO 均为0.1mol·L-1的混合溶液中滴加AgNO 溶液,先产生Ag CrO 沉淀
2 4 3 2 4
10.(2023·全国卷)向 饱和溶液(有足量 固体)中滴加氨水,发生反应
和 , 与
的关系如下图所示(其中M代表 、 、 或 )。下列说法错误的是
A.曲线I可视为 溶解度随 浓度变化曲线
B. 的溶度积常数
C.反应 的平衡常数K的值为
D. 时,溶液中
11.(2023·全国卷)下图为 和 在水中达沉淀溶解平衡时的 关系图(
; 可认为 离子沉淀完全)。下列叙述正确的是
A.由 点可求得
B. 时 的溶解度为
C.浓度均为 的 和 可通过分步沉淀进行分离
D. 混合溶液中 时二者不会同时沉淀
12.(2022·重庆卷)某小组模拟成垢-除垢过程如图。
100mL0.1mol•L-1CaCl 水溶液 ……
2
忽略体积变化,且步骤②中反应完全。下列说法正确的是A.经过步骤①,溶液中c(Ca2+)+c(Na+)=c(Cl-)
B.经过步骤②,溶液中c(Na+)=4c(SO )
C.经过步骤②,溶液中c(Cl-)=c(CO )+c(HCO )+c(H CO)
2 3
D.经过步骤③,溶液中c(CHCOOH)+c(CH COO-)=c(Cl-)
3 3
1.(2023上·上海松江)下列对“难溶”的理解正确的是
A.“难溶”是指物质常温时在水中溶解的质量小于0.01g
B.在水中难溶的物质,也难溶于其他溶剂
C.只有难溶的物质才能建立溶解平衡
D.相同条件下,难溶的物质更容易形成饱和溶液
2.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag+
+2NH·H O Ag(NH) +2H O。下列分析不正确的是
3 2 3 2
A.浊液中存在沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl-(aq)
B.实验可以证明NH 结合Ag+能力比Cl-强
3
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
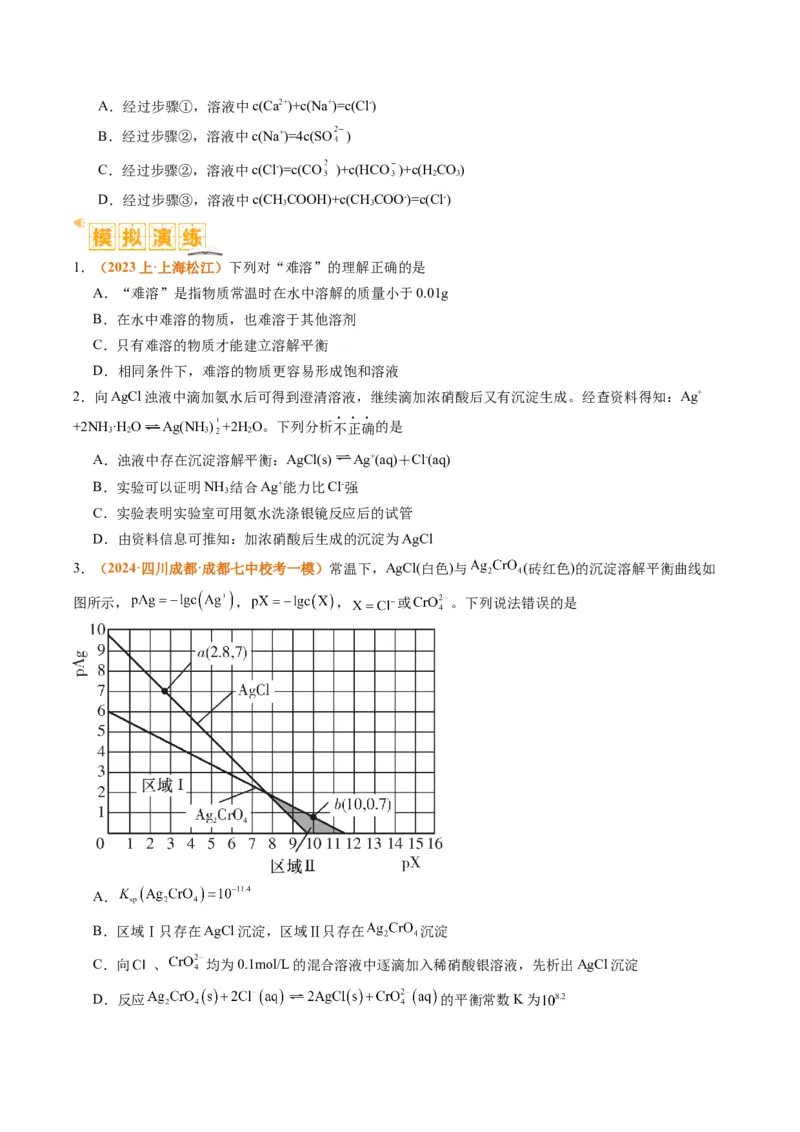
3.(2024·四川成都·成都七中校考一模)常温下,AgCl(白色)与 (砖红色)的沉淀溶解平衡曲线如
图所示, , , 或 。下列说法错误的是
A.
B.区域Ⅰ只存在AgCl沉淀,区域Ⅱ只存在 沉淀
C.向 、 均为0.1mol/L的混合溶液中逐滴加入稀硝酸银溶液,先析出AgCl沉淀
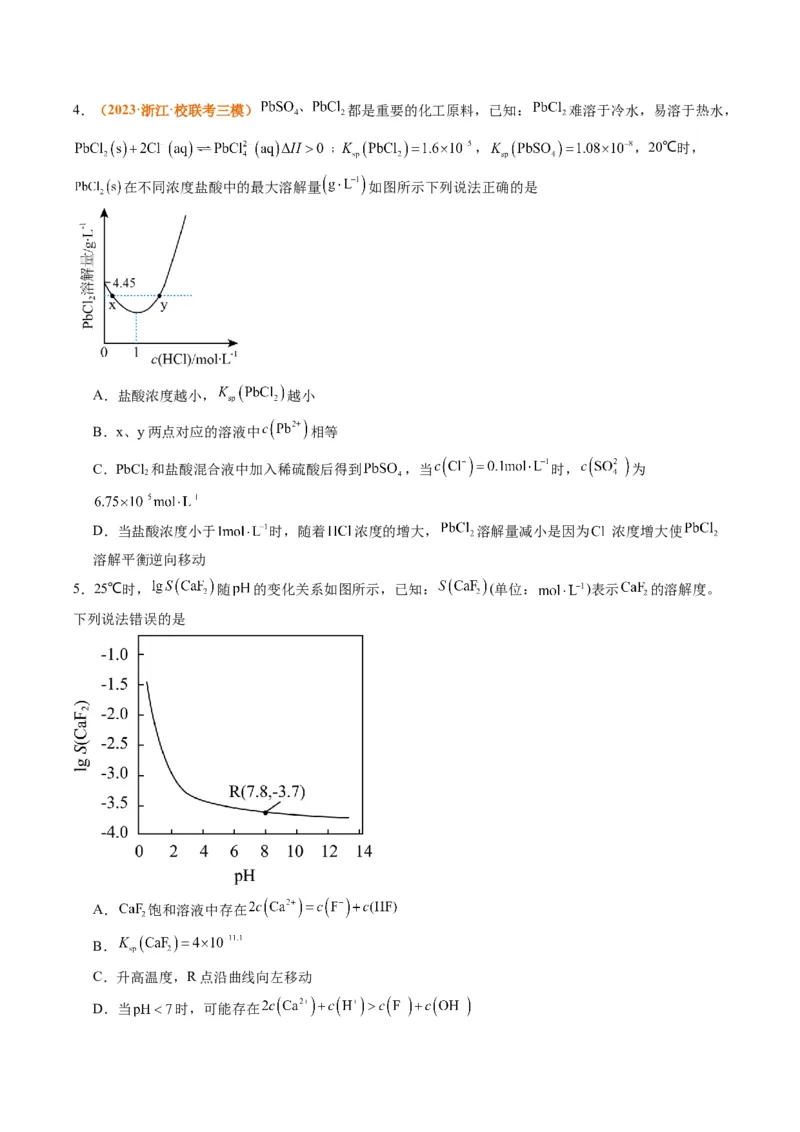
D.反应 的平衡常数K为4.(2023·浙江·校联考三模) 都是重要的化工原料,已知: 难溶于冷水,易溶于热水,
﹔ , ,20℃时,
在不同浓度盐酸中的最大溶解量 如图所示下列说法正确的是
A.盐酸浓度越小, 越小
B.x、y两点对应的溶液中 相等
C.PbCl 和盐酸混合液中加入稀硫酸后得到 ,当 时, 为
2
D.当盐酸浓度小于 时,随着 浓度的增大, 溶解量减小是因为 浓度增大使
溶解平衡逆向移动
5.25℃时, 随 的变化关系如图所示,已知: (单位: )表示 的溶解度。
下列说法错误的是
A. 饱和溶液中存在
B.
C.升高温度,R点沿曲线向左移动
D.当 时,可能存在6.已知25℃时,CaSO 在水中的沉淀溶解平衡曲线如图所示,向100mL该条件下的CaSO 饱和溶液中加
4 4
入400mL0.01mol·L-1NaSO 溶液,下列叙述正确的是
2 4
A.溶液中析出CaSO 固体沉淀,最终溶液中[ ]比原来的小
4
B.溶液中无沉淀析出,溶液中[Ca2+]、[ ]都变小
C.溶液中析出CaSO 固体沉淀,溶液中[Ca2+]、[ ]都变小
4
D.溶液中无沉淀析出,但最终溶液中[ ]比原来的大
7.(2024上·山东菏泽·高三山东省鄄城县第一中学校考)已知:常温下 , 。
向10 0.10 溶液中滴加0.10 的 溶液,滴加过程中 (M表示金属)与加
入的溶液体积(V)的关系如图所示,下列说法正确的是
A.常温下, 的平衡常数
B.常温下, 饱和溶液中 的数量级为
C.b点体系中, 的溶解速率大于其生成速率
D.若用 代替 (其他不变),则c点应向下移动
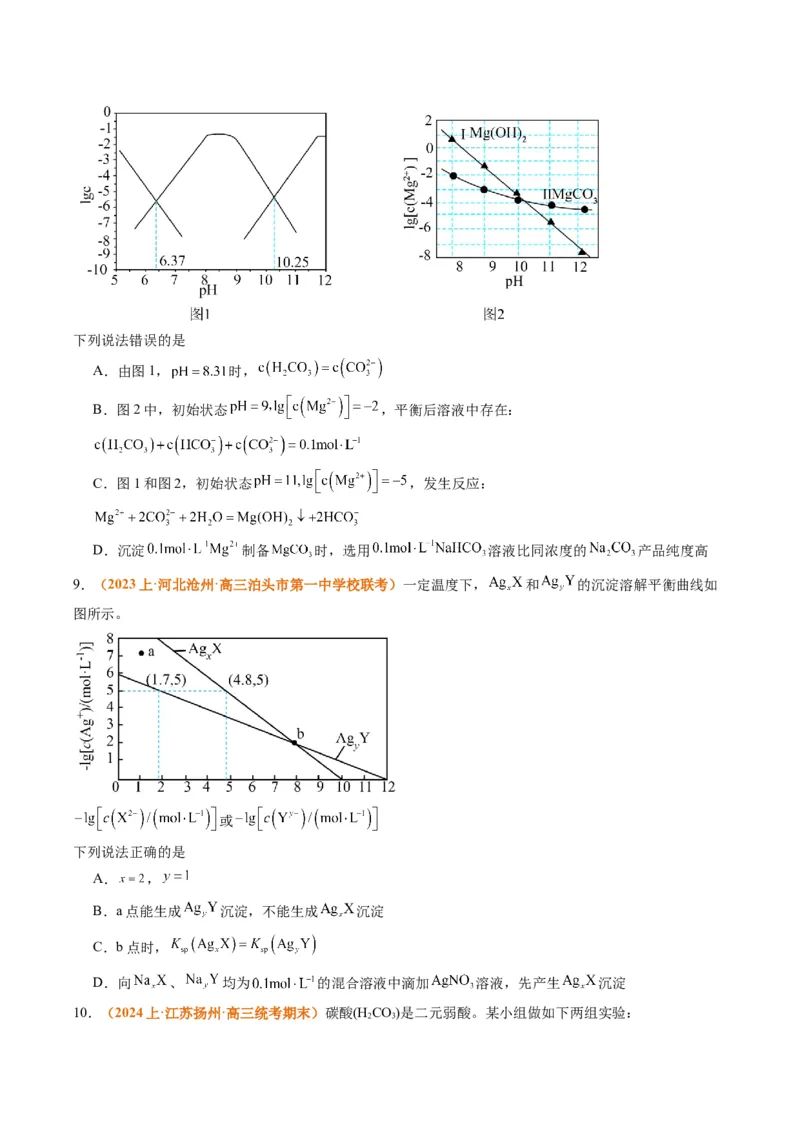
8.(2024上·山东济宁·高三统考期末)利用平衡移动原理,分析一定温度下 在不同 的 体
系中的可能产物。已知:图1中曲线表示 体系中各含碳粒子的 与 的关系;图2中曲线Ⅰ的
离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[起始 ,不同 下含碳粒子的浓度由图1得到]。下列说法错误的是
A.由图1, 时,
B.图2中,初始状态 ,平衡后溶液中存在:
C.图1和图2,初始状态 ,发生反应:
D.沉淀 制备 时,选用 溶液比同浓度的 产品纯度高
9.(2023上·河北沧州·高三泊头市第一中学校联考)一定温度下, 和 的沉淀溶解平衡曲线如
图所示。
或
下列说法正确的是
A. ,
B.a点能生成 沉淀,不能生成 沉淀
C.b点时,
D.向 、 均为 的混合溶液中滴加 溶液,先产生 沉淀
10.(2024上·江苏扬州·高三统考期末)碳酸(H CO)是二元弱酸。某小组做如下两组实验:
2 3实验I:往20mL0.1mol·L−1HCO 溶液中滴加0.1mol·L−1氨水。
2 3
实验Ⅱ:往20mL0.1mol·L−1NaHCO 溶液中滴加0.1mol·L−1CaCl 溶液。
3 2
[已知:K (H CO)=4.5×10−7,K (H CO)=5.6×10−11,K (NH ·H O)=1.8×10-5,K (CaCO)=3.6×10−9,溶液混
a1 2 3 a2 2 3 b 3 2 sp 3
合后体积变化忽略不计],下列说法正确的是
A.实验I中V(氨水)=20mL时,存在c(H CO)<c(CO )+c(NH ·H O)
2 3 3 2
B.实验I中pH=8时,存在c(H CO)>c(CO )
2 3
C.实验Ⅱ中V(CaCl )=10mL时,发生反应HCO +Ca2+=CaCO ↓+H+
2 3
D.实验Ⅱ中V(CaCl )=80mL时,沉淀后的上层清液中:c(Ca2+)c(CO )>K (CaCO)
2 sp 3
11.(2023上·黑龙江·高三校联考期末) 时,用 溶液分别滴定等物质的量浓度的
三种溶液pM[p表示负对数, 表示 ]随溶液 变
化的关系如图所示。已知:常温下, 。下列推断正确的是
A.曲线③代表 与 的关系曲线
B.调节 时,可将废水中 完全沉淀
C.滴定 溶液至X点时,溶液中:
D.经计算, 能完全溶于HR溶液
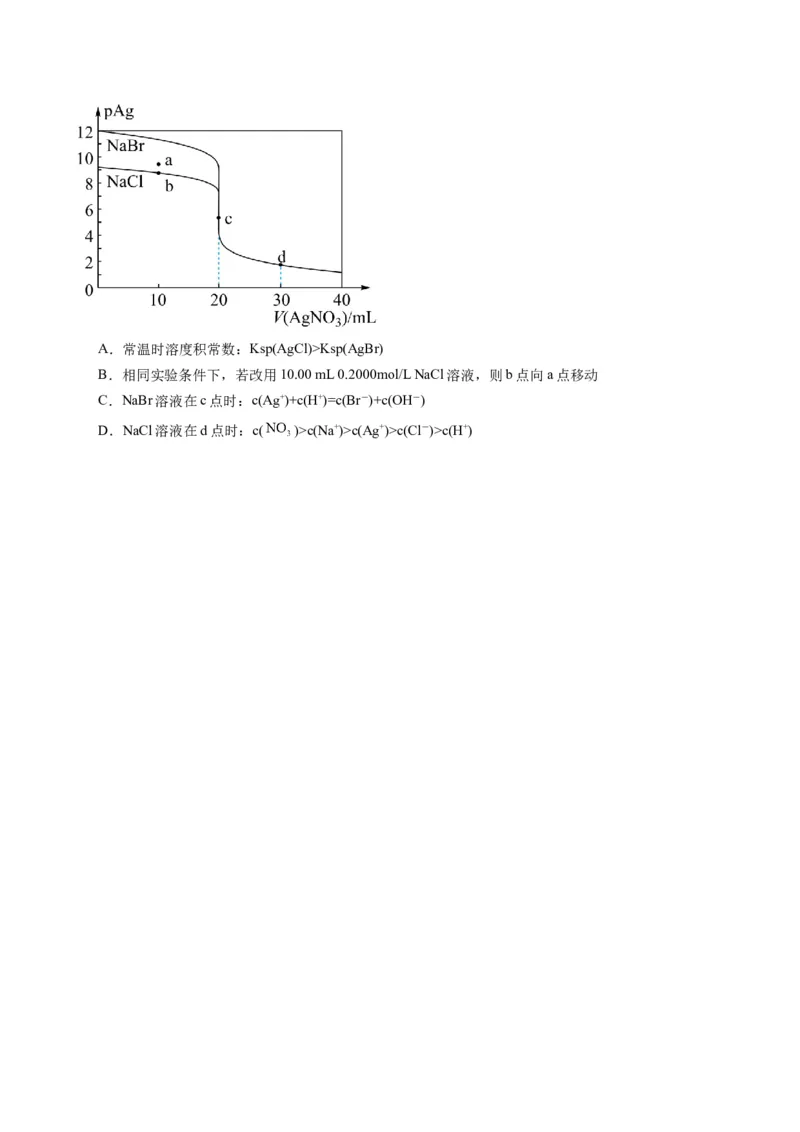
12.(2023上·四川成都·高三石室中学校考)常温下,用0.1000mol/L AgNO 标准溶液(pH≈5)分别滴定
3
20.00 mL 0.1000mol/L的NaCl溶液和NaBr溶液,混合溶液的pAg[定义为pAg= -lgc(Ag+)]与AgNO 溶液
3
体积的变化关系如图所示。下列说法不正确的是A.常温时溶度积常数:Ksp(AgCl)>Ksp(AgBr)
B.相同实验条件下,若改用10.00 mL 0.2000mol/L NaCl溶液,则b点向a点移动
C.NaBr溶液在c点时:c(Ag+)+c(H+)=c(Br-)+c(OH-)
D.NaCl溶液在d点时:c( )>c(Na+)>c(Ag+)>c(Cl-)>c(H+)