文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖北专用)
黄金卷04
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 O 16 Na 23 S 32 Cl 35.5 Ni 59 As 75
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.从古至今,人类的生活、生产都离不开材料的应用。下列说法正确的是
A.三星堆祭祀坑内发现了大量丝绸朽化后的残留物,丝绸的主要成分是蛋白质
B.人民币票面文字处采用了含 的磁性油墨, 常用作红色颜料
C.北斗卫星上使用的硅太阳能电池阵,利用 将太阳能转化为电能
D.“奋斗者号”潜水器使用的固体浮力材料,由空心玻璃微球填充在高强度树脂中制成,属于无机非金
属材料
2.哲学中“对立与统一”同时发生规律广泛存在于化学中。下列叙述中不符合“对立与统一”规律的是
A.工业合成氨中,吸热反应和放热反应同时发生
B.在化学反应中,浓硝酸挥发性和氧化性同时表现
C.原电池中正极反应和负极反应同时发生
D.C、N、O的电负性随其核电荷数的增大而增大
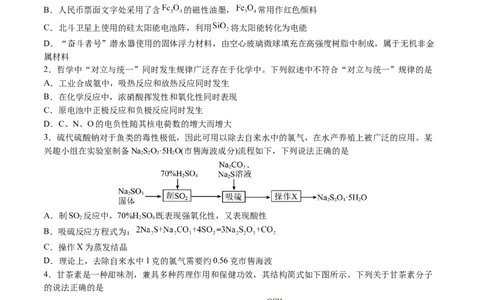
3.硫代硫酸钠对于鱼类的毒性极低,因此可用以除去自来水中的氯气,在水产养殖上被广泛的应用。某
兴趣小组在实验室制备NaSO·5H O(市售海波成分)流程如下,下列说法正确的是
2 2 3 2
A.制SO 反应中,70%H SO 既表现强氧化性,又表现酸性
2 2 4
B.吸硫反应方程式为:
C.操作X为蒸发结晶
D.理论上,去除自来水中1克的氯气需要约0.56克市售海波
4.甘茶素是一种甜味剂,兼具多种药理作用和保健功效,其结构简式如下图所示。下列关于甘茶素分子
的说法正确的是
A.分子式为
B.能发生加成反应
C.所有原子共平面
D.苯环上的一氯代物有7种
5.化学用语可以表达化学过程,下列化学用语的表达正确的是A.邻羟基苯甲醛中加入足量浓溴水:
B.向次氯酸钙溶液中通入 :
C.用电子式表示HCl的形成过程:
D.尿素与甲醛制备线型脲醛树脂:
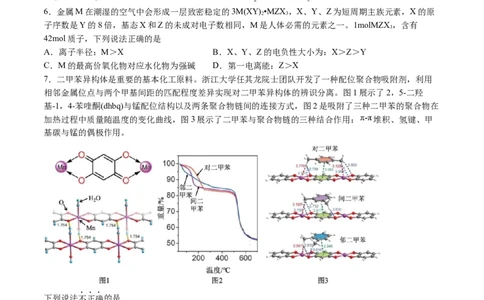
6.金属M在潮湿的空气中会形成一层致密稳定的3M(XY) •MZX ,X、Y、Z为短周期主族元素,X的原
2 3
子序数是Y的8倍,基态X和Z的未成对电子数相同,M是人体必需的元素之一。1molMZX ,含有
3
42mol质子,下列说法正确的是
A.离子半径:M>X B.X、Y、Z的电负性大小为:X>Z>Y
C.M的最高价氧化物对应水化物为强碱 D.第一电离能:Z>X
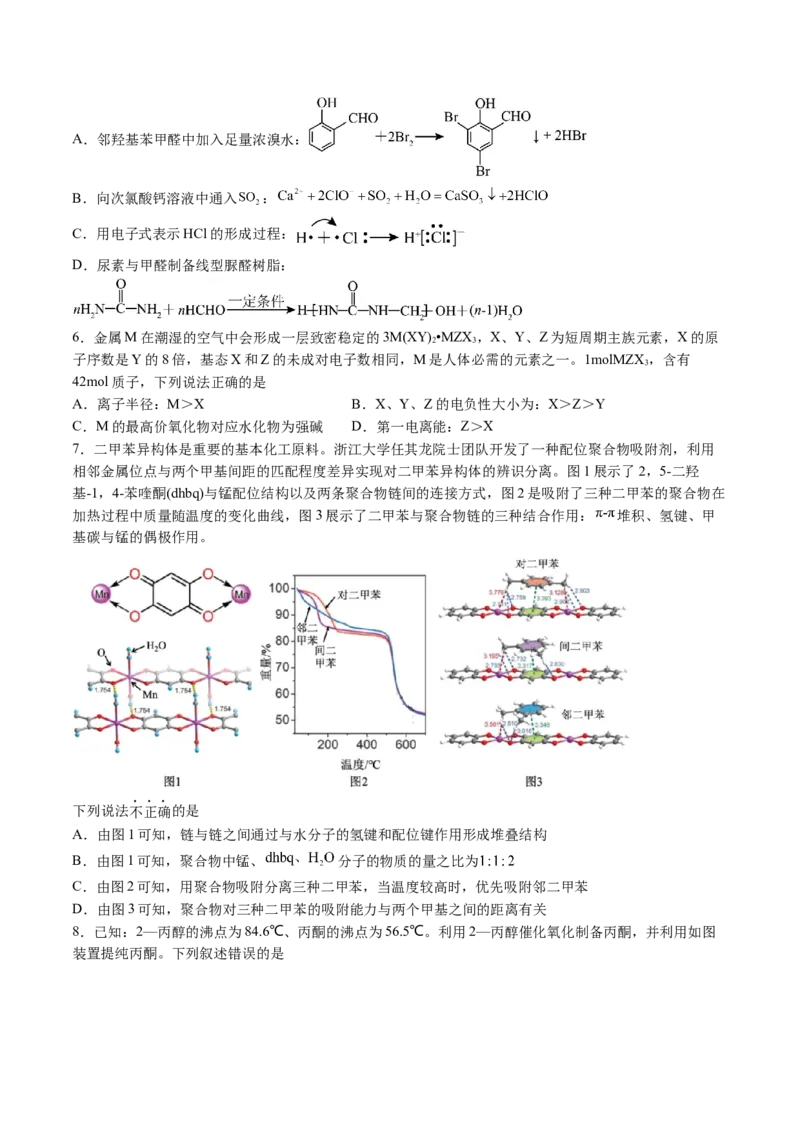
7.二甲苯异构体是重要的基本化工原料。浙江大学任其龙院士团队开发了一种配位聚合物吸附剂,利用
相邻金属位点与两个甲基间距的匹配程度差异实现对二甲苯异构体的辨识分离。图1展示了2,5-二羟
基-1,4-苯喹酮(dhbq)与锰配位结构以及两条聚合物链间的连接方式,图2是吸附了三种二甲苯的聚合物在
加热过程中质量随温度的变化曲线,图3展示了二甲苯与聚合物链的三种结合作用: 堆积、氢键、甲
基碳与锰的偶极作用。
下列说法不正确的是
A.由图1可知,链与链之间通过与水分子的氢键和配位键作用形成堆叠结构
B.由图1可知,聚合物中锰、 分子的物质的量之比为
C.由图2可知,用聚合物吸附分离三种二甲苯,当温度较高时,优先吸附邻二甲苯
D.由图3可知,聚合物对三种二甲苯的吸附能力与两个甲基之间的距离有关
8.已知:2—丙醇的沸点为84.6℃、丙酮的沸点为56.5℃。利用2—丙醇催化氧化制备丙酮,并利用如图
装置提纯丙酮。下列叙述错误的是A.采用热水浴加热
B.毛细玻璃管与液面接触的地方能形成汽化中心
C.克氏蒸馏头能防止液体冲入冷凝管
D.温度计指示温度为84.6℃
9.将氟气通入氢氧化钠溶液中,可得 。 是一种无色、几乎无味的剧毒气体,主要用于氧化氟化反
应、火箭工程助燃剂等。下列说法错误的是
A. 中O的化合价为 价
B. 的VSEPR模型为四面体
C.与 分子相比, 分子的极性大
D.与 分子相比, 分子的键角小
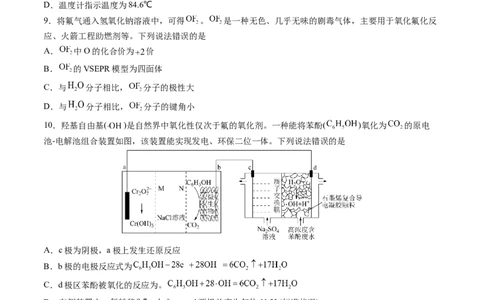
10.羟基自由基( )是自然界中氧化性仅次于氟的氧化剂。一种能将苯酚( )氧化为 的原电
池-电解池组合装置如图,该装置能实现发电、环保二位一体。下列说法错误的是
A.c极为阴极,a极上发生还原反应
B.b极的电极反应式为
C.d极区苯酚被氧化的反应为。
D.右侧装置中,每转移 ,c、d两极共产生气体11.2L(标准状况)
11.下列对有关事实的解释正确的是
选项 事实 解释
A 某些金属盐灼烧呈现不同焰色 电子从低能轨道跃迁至高能轨道时吸收光波长不同
B CH 与NH 分子的空间结构不同 二者中心原子杂化轨道类型不同
4 3
C 白磷为正四面体分子 白磷分子中P﹣P键间的夹角是109.5°
D HF的热稳定性比HCl强 H﹣F比H﹣Cl的键能大12.2021年诺贝尔化学奖授予本杰明·李斯特、大卫·麦克米兰,以表彰他们在“不对称有机催化的发展”
中的贡献,用脯氨酸催化合成酮醇反应如图。下列说法错误的是
A.C的分子式为C H NO B.理论上,该反应原子利用率为100%
10 11 4
C.脯氨酸与 互为同分异构体 D.可用酸性高锰酸钾溶液鉴别b和c
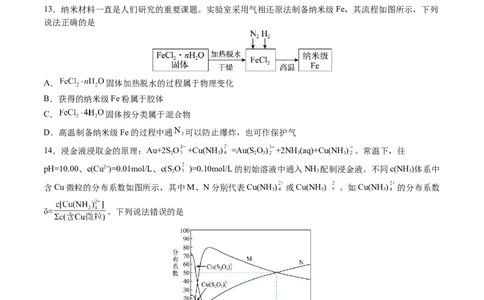
13.纳米材料一直是人们研究的重要课题。实验室采用气相还原法制备纳米级Fe,其流程如图所示,下列
说法正确的是
A. 固体加热脱水的过程属于物理变化
B.获得的纳米级Fe粉属于胶体
C. 固体按分类属于混合物
D.高温制备纳米级Fe的过程中通 可以防止爆炸,也可作保护气
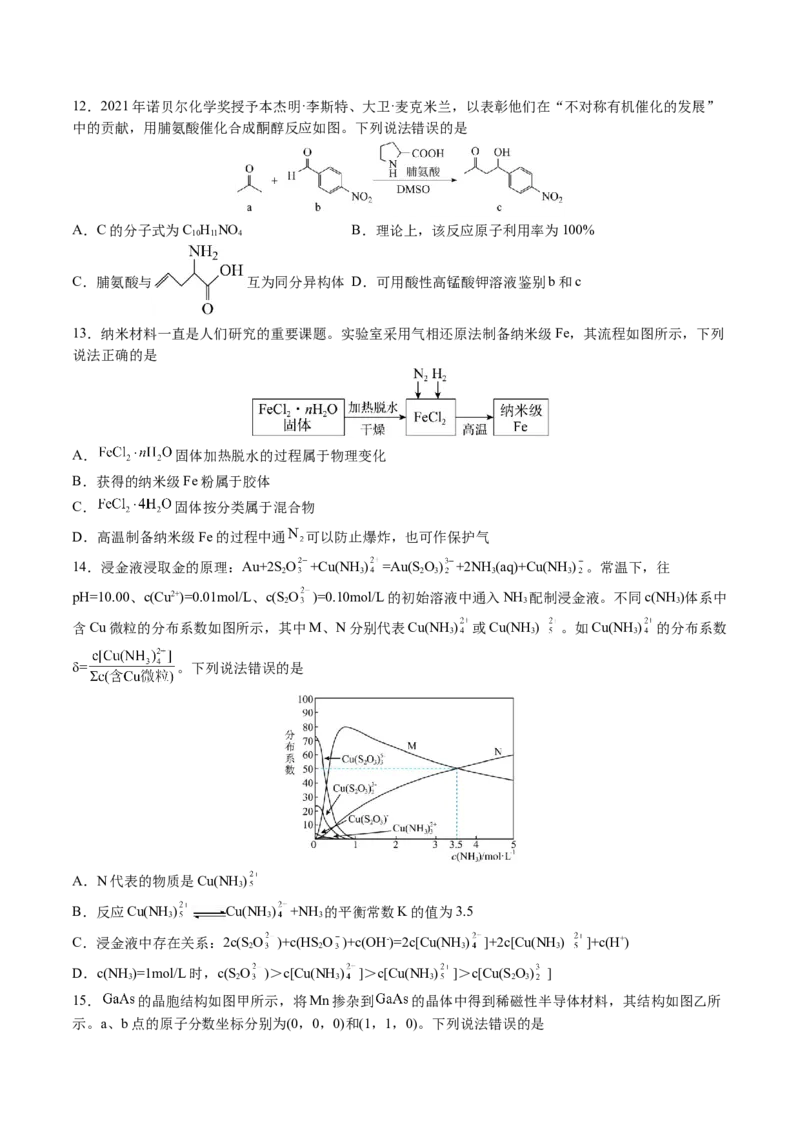
14.浸金液浸取金的原理:Au+2SO +Cu(NH) =Au(SO) +2NH(aq)+Cu(NH) 。常温下,往
2 3 2 3 3 3
pH=10.00、c(Cu2+)=0.01mol/L、c(SO )=0.10mol/L的初始溶液中通入NH 配制浸金液。不同c(NH )体系中
2 3 3
含Cu微粒的分布系数如图所示,其中M、N分别代表Cu(NH ) 或Cu(NH ) 。如Cu(NH ) 的分布系数
3 3 3
δ= 。下列说法错误的是
A.N代表的物质是Cu(NH )
3
B.反应Cu(NH ) Cu(NH ) +NH 的平衡常数K的值为3.5
3 3 3
C.浸金液中存在关系:2c(SO )+c(HSO )+c(OH-)=2c[Cu(NH) ]+2c[Cu(NH) ]+c(H+)
2 2 3 3
D.c(NH )=1mol/L时,c(SO )>c[Cu(NH ) ]>c[Cu(NH ) ]>c[Cu(SO) ]
3 2 3 3 2 3
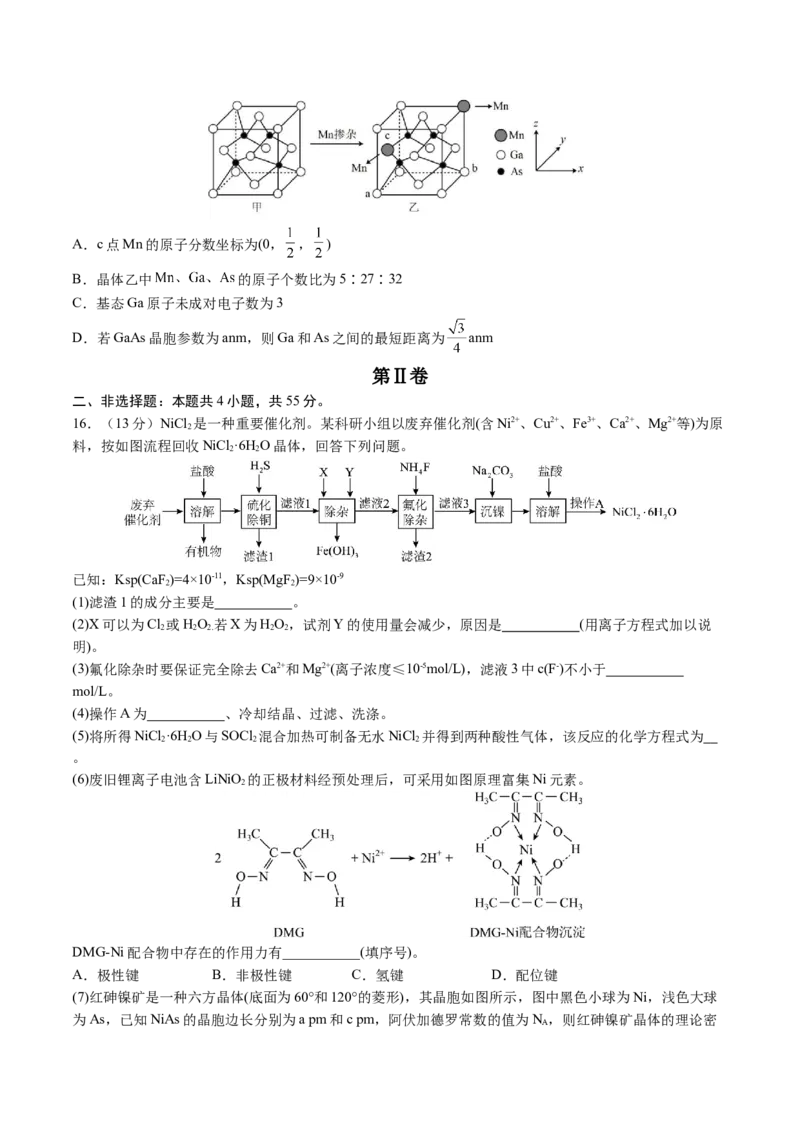
15. 的晶胞结构如图甲所示,将Mn掺杂到 的晶体中得到稀磁性半导体材料,其结构如图乙所
示。a、b点的原子分数坐标分别为(0,0,0)和(1,1,0)。下列说法错误的是A.c点Mn的原子分数坐标为(0, , )
B.晶体乙中 的原子个数比为5∶27∶32
C.基态Ga原子未成对电子数为3
D.若GaAs晶胞参数为anm,则Ga和As之间的最短距离为 anm
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
16.(13分)NiCl 是一种重要催化剂。某科研小组以废弃催化剂(含Ni2+、Cu2+、Fe3+、Ca2+、Mg2+等)为原
2
料,按如图流程回收NiCl ·6H O晶体,回答下列问题。
2 2
已知:Ksp(CaF )=4×10-11,Ksp(MgF)=9×10-9
2 2
(1)滤渣1的成分主要是 。
(2)X可以为Cl 或HO 若X为HO,试剂Y的使用量会减少,原因是 (用离子方程式加以说
2 2 2. 2 2
明)。
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于
mol/L。
(4)操作A为 、冷却结晶、过滤、洗涤。
(5)将所得NiCl ·6H O与SOCl 混合加热可制备无水NiCl 并得到两种酸性气体,该反应的化学方程式为
2 2 2 2
。
(6)废旧锂离子电池含LiNiO 的正极材料经预处理后,可采用如图原理富集Ni元素。
2
DMG-Ni配合物中存在的作用力有___________(填序号)。
A.极性键 B.非极性键 C.氢键 D.配位键
(7)红砷镍矿是一种六方晶体(底面为60°和120°的菱形),其晶胞如图所示,图中黑色小球为Ni,浅色大球
为As,已知NiAs的晶胞边长分别为a pm和c pm,阿伏加德罗常数的值为N ,则红砷镍矿晶体的理论密
A度为ρ= g·cm-3(写出表达式,需化简)
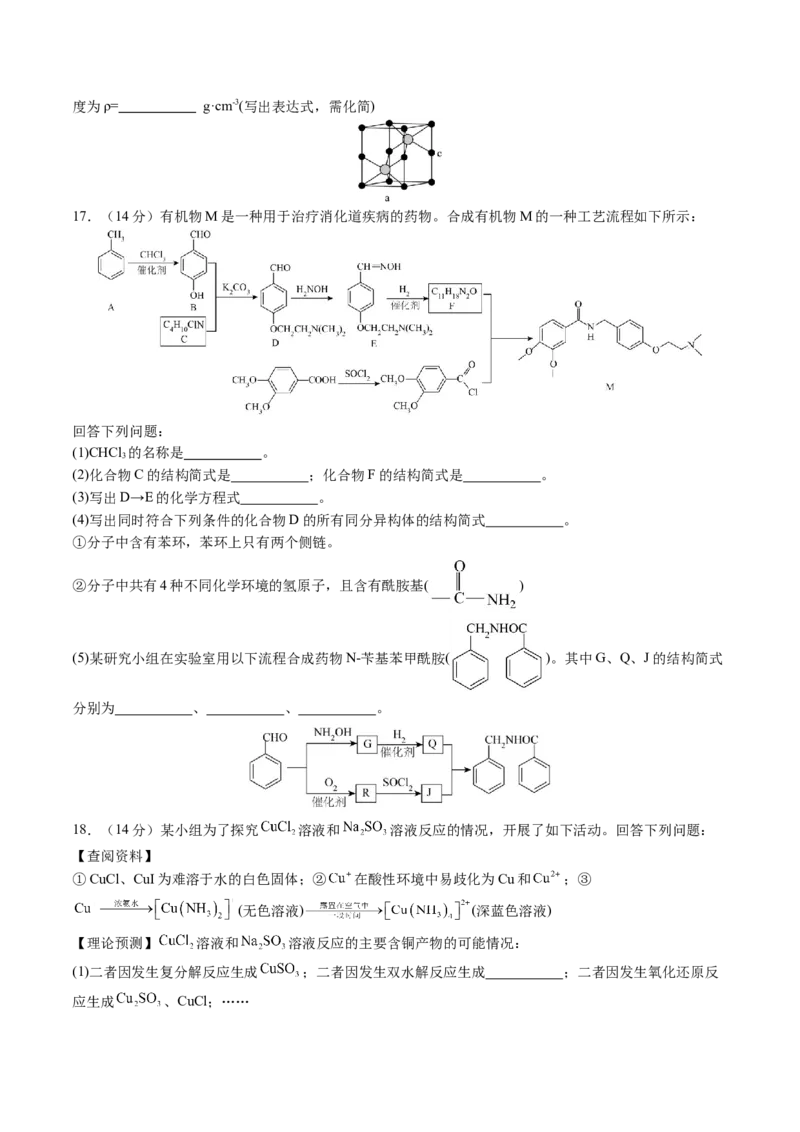
17.(14分)有机物M是一种用于治疗消化道疾病的药物。合成有机物M的一种工艺流程如下所示:
回答下列问题:
(1)CHCl 的名称是 。
3
(2)化合物C的结构简式是 ;化合物F的结构简式是 。
(3)写出D→E的化学方程式 。
(4)写出同时符合下列条件的化合物D的所有同分异构体的结构简式 。
①分子中含有苯环,苯环上只有两个侧链。
②分子中共有4种不同化学环境的氢原子,且含有酰胺基( )
(5)某研究小组在实验室用以下流程合成药物N-苄基苯甲酰胺( )。其中G、Q、J的结构简式
分别为 、 、 。
18.(14分)某小组为了探究 溶液和 溶液反应的情况,开展了如下活动。回答下列问题:
【查阅资料】
①CuCl、CuI为难溶于水的白色固体;② 在酸性环境中易歧化为Cu和 ;③
(无色溶液) (深蓝色溶液)
【理论预测】 溶液和 溶液反应的主要含铜产物的可能情况:
(1)二者因发生复分解反应生成 ;二者因发生双水解反应生成 ;二者因发生氧化还原反
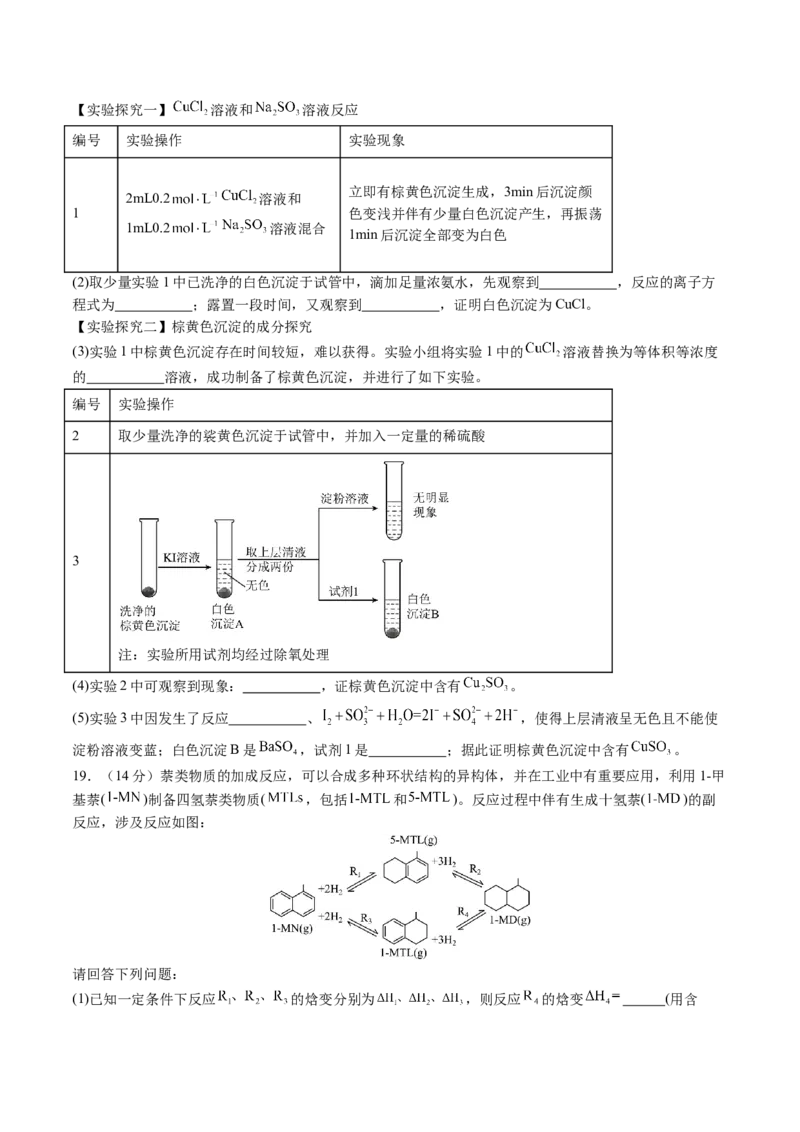
应生成 、CuCl;……【实验探究一】 溶液和 溶液反应
编号 实验操作 实验现象
立即有棕黄色沉淀生成,3min后沉淀颜
2mL0.2 溶液和
1 色变浅并伴有少量白色沉淀产生,再振荡
1mL0.2 溶液混合
1min后沉淀全部变为白色
(2)取少量实验1中已洗净的白色沉淀于试管中,滴加足量浓氨水,先观察到 ,反应的离子方
程式为 ;露置一段时间,又观察到 ,证明白色沉淀为CuCl。
【实验探究二】棕黄色沉淀的成分探究
(3)实验1中棕黄色沉淀存在时间较短,难以获得。实验小组将实验1中的 溶液替换为等体积等浓度
的 溶液,成功制备了棕黄色沉淀,并进行了如下实验。
编号 实验操作
2 取少量洗净的裟黄色沉淀于试管中,并加入一定量的稀硫酸
3
注:实验所用试剂均经过除氧处理
(4)实验2中可观察到现象: ,证棕黄色沉淀中含有 。
(5)实验3中因发生了反应 、 ,使得上层清液呈无色且不能使
淀粉溶液变蓝;白色沉淀B是 ,试剂1是 ;据此证明棕黄色沉淀中含有 。
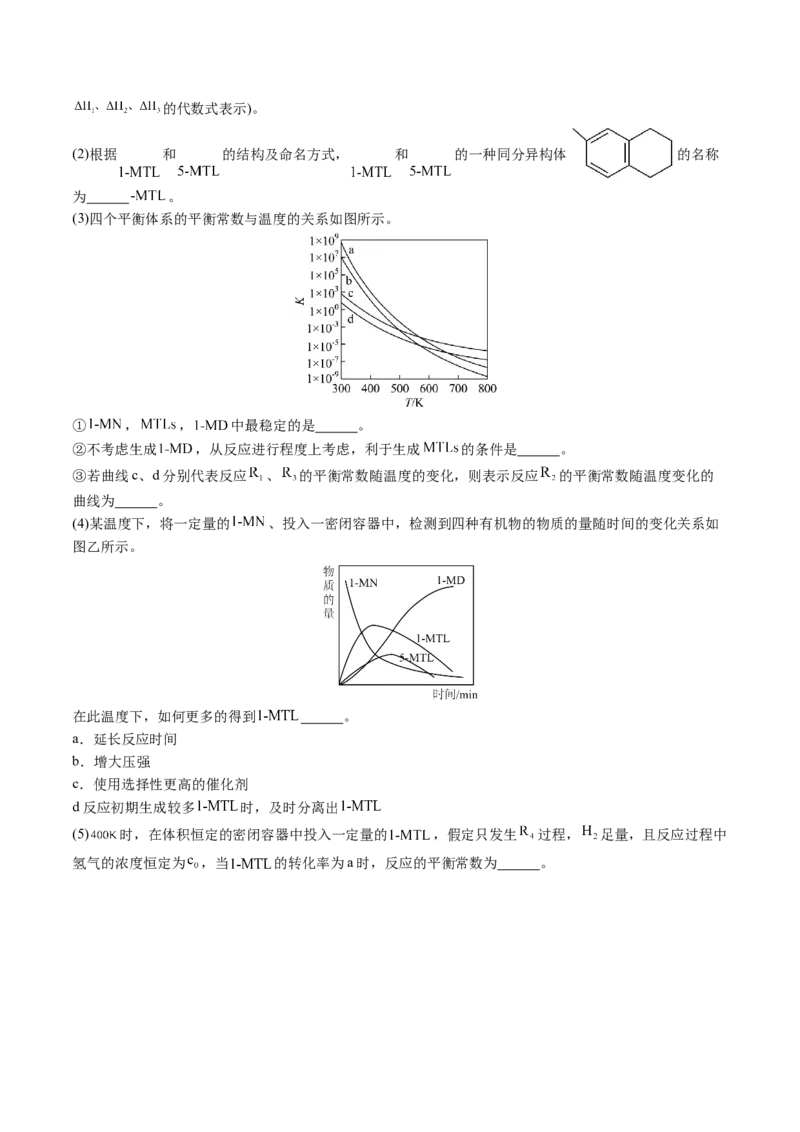
19.(14分)萘类物质的加成反应,可以合成多种环状结构的异构体,并在工业中有重要应用,利用1-甲
基萘( )制备四氢萘类物质( ,包括 和 )。反应过程中伴有生成十氢萘( )的副
反应,涉及反应如图:
请回答下列问题:
(1)已知一定条件下反应 的焓变分别为 ,则反应 的焓变 (用含的代数式表示)。
(2)根据 和 的结构及命名方式, 和 的一种同分异构体 的名称
为 。
(3)四个平衡体系的平衡常数与温度的关系如图所示。
① , , 中最稳定的是 。
②不考虑生成 ,从反应进行程度上考虑,利于生成 的条件是 。
③若曲线c、d分别代表反应 、 的平衡常数随温度的变化,则表示反应 的平衡常数随温度变化的
曲线为 。
(4)某温度下,将一定量的 、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如
图乙所示。
在此温度下,如何更多的得到 。
a.延长反应时间
b.增大压强
c.使用选择性更高的催化剂
d反应初期生成较多 时,及时分离出
(5) 时,在体积恒定的密闭容器中投入一定量的 ,假定只发生 过程, 足量,且反应过程中
氢气的浓度恒定为 ,当 的转化率为a时,反应的平衡常数为 。