文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟║天津专用
黄金卷05
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Mg -24 Fe-56
一、选择题:本题共12小题,每小题3分,共36分。每小题给出的四个选项中,只有一项符合题目要
求.
1.化学与生产、生活密切相关,下列说法不正确的是
A.游泳馆常用硫酸铜作池水消毒剂
B.硅胶可用作商品包装袋内的干燥剂,也可以用作催化剂的载体
C.小苏打是制作馒头和面包等糕点的膨松剂,也是治疗胃酸过多的一种药剂
D.光导纤维、棉花、油脂、ABS树脂都是由高分子化合物组成的物质
2.下列说法错误的是
A.糖类、橡胶和蛋白质都属于天然高分子
B.淀粉和纤维素属于多糖,淀粉在人体中水解的最终产物是葡萄糖,纤维素可刺激肠道蠕动
C.油和脂肪是根据含不饱和烃基和饱和烃基的相对含量不同引起的熔点不同进行区分的
D.氨基酸和蛋白质都具有两性,氨基酸是组成蛋白质的基本结构单位,没有蛋白质就没有生命
3.下列实验合理的是
A.用新制氢氧化铜悬浊液(必要时可加热)鉴别甲酸与乙酸
B.用澄清石灰水鉴别SO 与CO
2 2
C.用淀粉-KI试纸鉴别碘水与FeCl 溶液
3
D.用湿润的pH试纸测定CHCOONa的pH
3
4.物质的性质决定用途,下列两者对应关系不正确的是
A.Al(OH) 有弱碱性,可用于治疗胃酸过多
3
B.生铁硬度大、抗压性强,可用于铸造机器底座
C.稀硝酸有强氧化性,可清洗附着在试管内壁的银镜
D.单晶硅是良好的半导体材料,常用于制备光导纤维
5.CrSi、Ge-GaAs、ZnGeAs 和SiC都是重要的半导体化合物,下列说法错误的是
2A.原子半径:r(Ga)>r(Ge)>r(As)
B.碳单质、晶体硅、SiC均为共价晶体
C.可在周期表中元素Si附近寻找新半导体材料
D.第一电离能:I(C)>I (Si)>I (Ge)
1 1 1
6. 可用于水处理, 约为8时, 可与 反应生成 、 和 。 可用于烟气(含 、 、
、 等)脱硫。下列物质结构与性质或物质性质与用途具有对应关系的是
A. 分子间作用力较大,易液化
B. 常温下呈固态,可用于烟气脱硫
C. 分子间存在氢键, 的热稳定性强于
D. 的溶解度比 大,可用于饮用水消毒杀菌
7.据文献报道,钒催化某反应的反应机理如图所示,下列叙述正确的是
A.HO参与了该催化循环
2
B.该反应利用了NH 的还原性除去NO,减少了空气污染
3
C.该过程只断裂了极性共价键
D.该催化循环过程中V的价态变化为+5→+4
8.如图物质是一种重要的有机合成中间体。下列关于该物质的说法正确的是
A.该物质的分子式为 ,分子中碳原子的杂化方式有 、B.该物质属于芳香烃, 该芳香烃最多能与 加成
C.该物质最多有18个原子共面
D.该物质能使溴水和酸性高锰酸钾溶液褪色
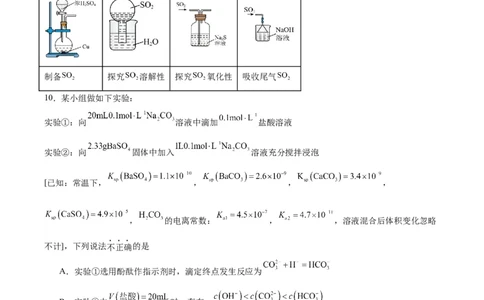
9.实验室进行 制备和性质探究,下列实验原理和装置不能达到实验目的的是
A B C D
制备 探究 溶解性 探究 氧化性 吸收尾气
10.某小组做如下实验:
实验①:向 溶液中滴加 盐酸溶液
实验②:向 固体中加入 溶液充分搅拌浸泡
[已知:常温下, , , ,
, 的电离常数: , ,溶液混合后体积变化忽略
不计],下列说法不正确的是
A.实验①选用酚酞作指示剂时,滴定终点发生反应为
B.实验①中 时,存在:
C.实验②中再加入 溶液,可将 完全转化为
D.实验②静置,向上层清液中滴加 溶液,会析出 和
11.砷可用于制取新型半导体材料砷化镓,砷化镓晶胞如图所示。下列说法正确的是
A. 、 的空间构型均为平面三角形
B.基态As原子的核外电子排布式为
C. 的沸点比 高的原因是 能形成分子间氢键
D.砷化镓晶胞中每个As原子周围与它最近且距离相等的Ga原子有6个
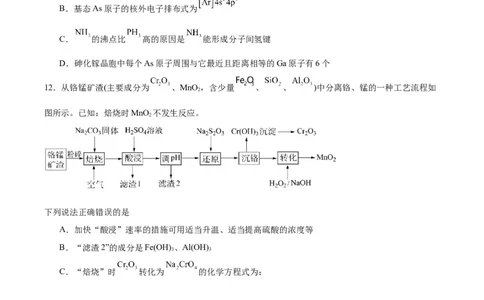
12.从铬锰矿渣(主要成分为 、MnO ,含少量 、 、 )中分离铬、锰的一种工艺流程如
2
图所示。已知:焙烧时MnO 不发生反应。
2
下列说法正确错误的是
A.加快“酸浸”速率的措施可用适当升温、适当提高硫酸的浓度等
B.“滤渣2”的成分是Fe(OH) 、Al(OH)
3 3
C.“焙烧”时 转化为 的化学方程式为:
D.流程中加入 的作用为作氧化剂,S元素被还原为
二、非选择题:本题共4小题,共64分。
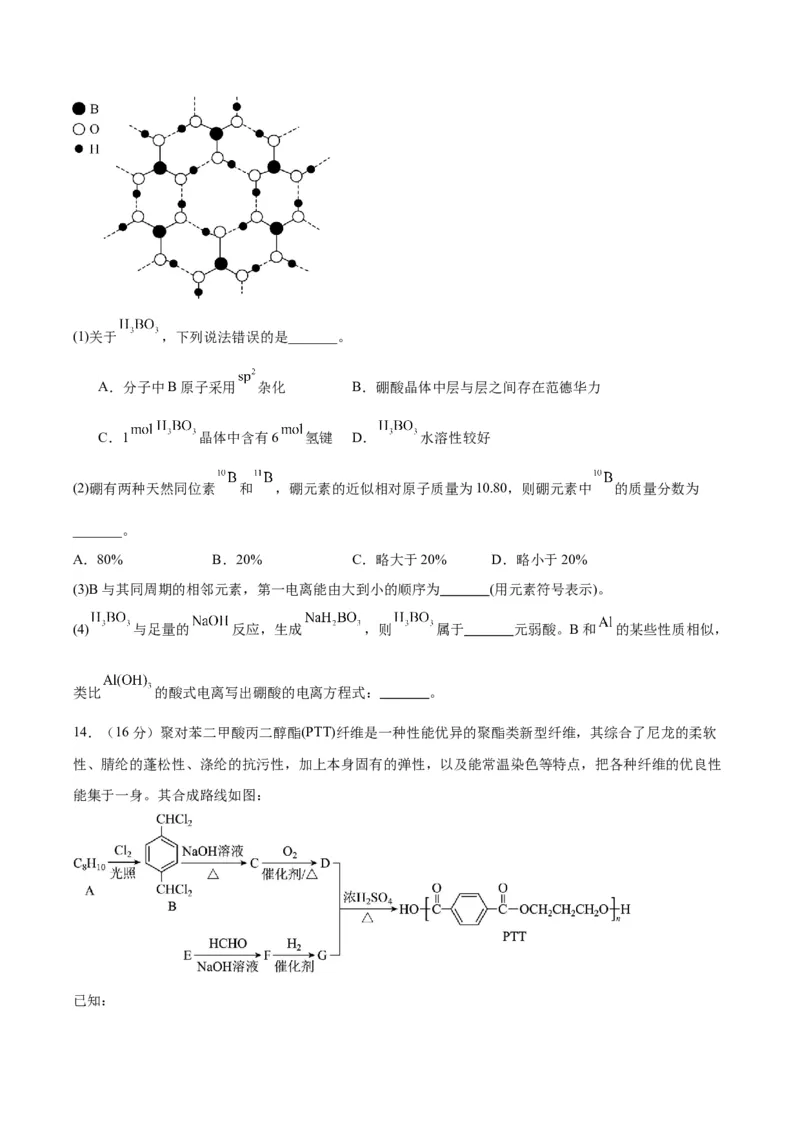
13.(16分)硼酸( )为白色晶体,晶体结构为层状,其二维平面结构如图所示。(1)关于 ,下列说法错误的是_______。
A.分子中B原子采用 杂化 B.硼酸晶体中层与层之间存在范德华力
C.1 晶体中含有6 氢键 D. 水溶性较好
(2)硼有两种天然同位素 和 ,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为
_______。
A.80% B.20% C.略大于20% D.略小于20%
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为 (用元素符号表示)。
(4) 与足量的 反应,生成 ,则 属于 元弱酸。B和 的某些性质相似,
类比 的酸式电离写出硼酸的电离方程式: 。
14.(16分)聚对苯二甲酸丙二醇酯(PTT)纤维是一种性能优异的聚酯类新型纤维,其综合了尼龙的柔软
性、腈纶的蓬松性、涤纶的抗污性,加上本身固有的弹性,以及能常温染色等特点,把各种纤维的优良性
能集于一身。其合成路线如图:
已知:①两个―OH连在同一个碳原子上会形成 ;
②
回答下列问题:
(1)A的化学名称为 。,它能发生的有机反应类型有 (填序号)。
①取代反应 ②加成反应 ③氧化反应 ④水解反应 ⑤消去反应
(2)C中官能团的名称为 ;C→D的反应类型为 。
(3)E→F的化学方程式为 。
(4)D+G→PTT的化学方程式为 。
(5)有机物H是D的同分异构体,写出符合条件的H的结构简式 。
①属于芳香族化合物;
②能够发成水解反应,且水解产物之一能与 溶液发生显色反应;
③核磁共振氢谱峰面积之比为1∶1。
(6)参照上述合成路线,以苯甲醛和乙炔为原料设计合成高分子 的合成路线 (其他试剂任
选)。
15.(16分)I.含氯物质在生产生活中有重要应用。
(1)实验室沿用舍勒的方法制取 的化学方程式为 。
(2)实验室制取干燥 时,净化与收集 所需装置的接口连接顺序为 。
其中NaOH溶液的作用是 ,其原理是 (用离子方程式表示)。
(3)某氯水久置后不能使品红溶液褪色,可推测氯水中 已分解。检验此久置氯水中 存在的操
作及现象是 。II.某研究性学习小组的同学为了制取NO并探究其性质,进行了如下实验。
试回答下列问题:
(4)某同学用图甲装置进行实验,收集到无色气体,由此确定铜和稀硝酸反应生成NO气体。该同学的推断
不合理的理由是 (用化学方程式表示)。
(5)另一名同学设计了图乙装置进行实验,步骤如下:①在大试管中放入适量石灰石,加入过量稀硝酸;②
待石灰石反应完全,将铜丝浸入过量的稀硝酸中;③一段时间后,观察到大试管中气体始终为无色,收集
反应产生的气体。其中步骤①的作用是 。
(6)当过量的铜与稀硝酸完全反应后,再加入20%的稀硫酸,铜片上又有气泡产生,稀硫酸的作用是
(填选项编号),反应的离子方程式为 。
a.还原剂 b.氧化剂 c.提供氢离子 d.提供热能
16.(16分)HDS催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙烧——水浸取法从HDS
废催化剂(主要成分为MoS、NiS、 、 等)中提取贵重金属钒和钼,其工艺流程如图所示。
已知:Ⅰ.焙烧时 、 、 均可与纯碱反应生成对应的钠盐,而NiO不行。
Ⅱ.高温下 易分解,分解产物含氮元素的气体有两种,二者均非氧化物。
Ⅲ. ; 、 。
请回答下列问题:
(1)流程的“气体”中含有二氧化碳,写出二氧化碳的一种用途: 。
(2)请写出“焙烧”过程中 及MoS分别与纯碱反应的化学方程式: , 。(3)“浸渣”的成分为 (填化学式);“滤液2”中的成分除了 外,还含有 (填
化学式)。
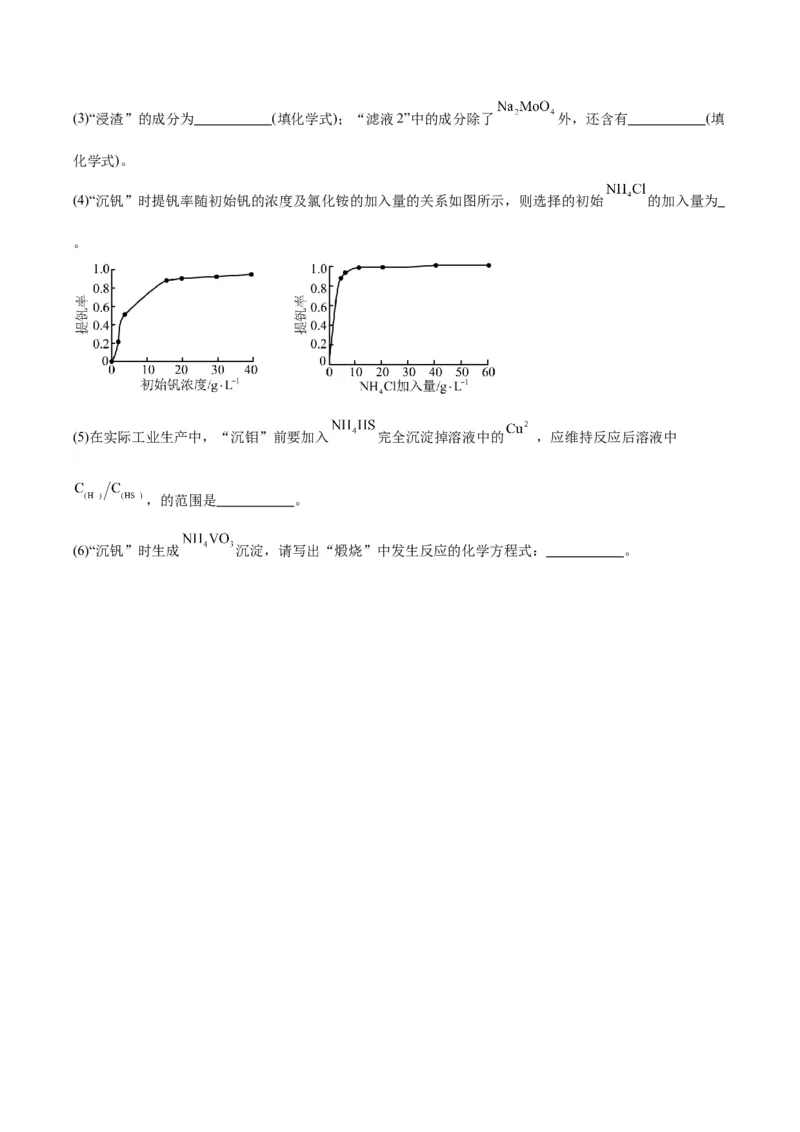
(4)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始 的加入量为
。
(5)在实际工业生产中,“沉钼”前要加入 完全沉淀掉溶液中的 ,应维持反应后溶液中
,的范围是 。
(6)“沉钒”时生成 沉淀,请写出“煅烧”中发生反应的化学方程式: 。