文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟║天津专用
黄金卷08
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Mg -24 Fe-56
一、选择题:本题共12小题,每小题3分,共36分。每小题给出的四个选项中,只有一项符合题目要
求.
1.化学与生产、生活、科技密切相关。下列说法正确的是
A.“天宫二号”空间站的太阳能电池帆板,其主要材料为晶体硅
B.“长征七号”采用液氧、煤油等作为推进剂,液氧、煤油是纯净物
C.C919大飞机上使用了芳纶纤维,芳纶属于天然纤维
D.杭州亚运会上的礼仪服饰用丝绸作为面料,丝绸属于糖类
2.下列关于你身边的化学叙述正确的是
A.硫的氧化物、氮的氧化物都是造成酸雨的主要因素
B.汽油、花生油、牛油都属于酯类
C.毛发、蚕丝、涤纶都属于天然高分子化合物
D.温室效应只与 有关
3.下列鉴别或检验能达到实验目的的是
A.用金属钠检验乙醇中混有少量的水
B.用硝酸银溶液鉴别氯苯与溴苯
C.用酸性高锰酸钾溶液鉴别Vc水溶液与葡萄糖溶液
D.用BaCl 溶液鉴别SO 和SO
2 2 3
4.下列有关物质的性质上用途具有对应关系的是
A.晶体硅硬度大,可用于制作半导体材料
B.二氧化硅难溶于水,可用于制作光导纤维
C.二氧化氯具有强氧化性,可用作自来水消毒剂
D.浓盐酸具有挥发性,可用于实验室制备氯气5.H、Li、Na、K位于周期表中ⅠA族。下列说法正确的是
A.离子半径大小: B.电负性大小:
C.第一电离能: D.碱性强弱:
6.反应 可制含氯消毒剂。下列说法正确的是
A.HCl和NaCl所含化学键类型相同
B. 是由极性键构成的非极性分子
C. 的空间结构为三角锥形
D.中子数为18的Cl原子:
7. 可作为光催化水生产物质X的高效催化剂,反应部分机理如题图所示。下列说法正确
的是
A.Co元素位于元素周期表IB族
B.在激光作用下, 发生氧化反应
C.物质X为
D.工业上煅烧 制备 的反应:
8.我国科学家提出的聚集诱导发光机制已成为研究热点之一。一种具有聚集诱导发光性能的物质,其分
子结构如图所示。下列说法不正确的是A.分子中N原子有sp2、sp3两种杂化方式
B.1mol该有机物最多可以消耗2molNaOH
C.该物质既有酸性又有碱性
D.该物质可发生取代反应、加成反应
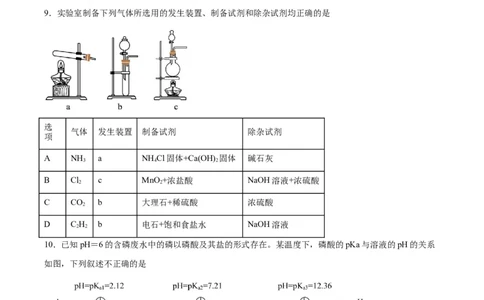
9.实验室制备下列气体所选用的发生装置、制备试剂和除杂试剂均正确的是
选
气体 发生装置 制备试剂 除杂试剂
项
A NH a NH Cl固体+Ca(OH) 固体 碱石灰
3 4 2
B Cl c MnO +浓盐酸 NaOH溶液+浓硫酸
2 2
C CO b 大理石+稀硫酸 浓硫酸
2
D C H b 电石+饱和食盐水 NaOH溶液
2 2
10.已知pH=6的含磷废水中的磷以磷酸及其盐的形式存在。某温度下,磷酸的pKa与溶液的pH的关系
如图,下列叙述不正确的是
A.该废水中离子浓度存在关系:
B.若逐渐增大该废水的pH,溶液中 将先增大后减小
C.向废水中加入 生成 沉淀除磷后,溶液 将增大D.室温下, 的平衡常数
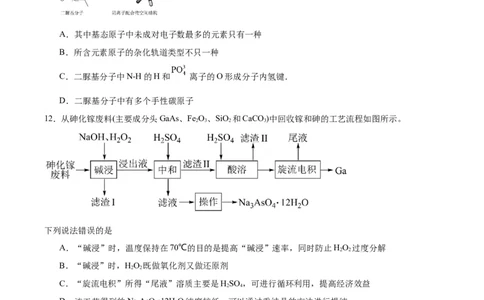
11.阴离子 和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如图所示(图中省略阴离
子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
A.其中基态原子中未成对电子数最多的元素只有一种
B.所含元素原子的杂化轨道类型不只一种
C.二脲基分子中N-H的H和 离子的O形成分子内氢键.
D.二脲基分子中有多个手性碳原子
12.从砷化镓废料(主要成分头GaAs、Fe O、SiO 和CaCO )中回收镓和砷的工艺流程如图所示。
2 3 2 3
下列说法错误的是
A.“碱浸”时,温度保持在70℃的目的是提高“碱浸”速率,同时防止HO 过度分解
2 2
B.“碱浸”时,HO 既做氧化剂又做还原剂
2 2
C.“旋流电积”所得“尾液”溶质主要是HSO ,可进行循环利用,提高经济效益
2 4
D.该工艺得到的NaAsO •12H O纯度较低,可以通过重结晶的方法进行提纯
3 4 2
二、非选择题:本题共4小题,共64分。
13.(16分)含碘的物质广泛应用于生活中。如(CHNH )PbI 作为典型的有机金属卤化物,一直是太阳能
3 3 3
电池研究的宠儿;AgI可用于显影剂和人工增雨。
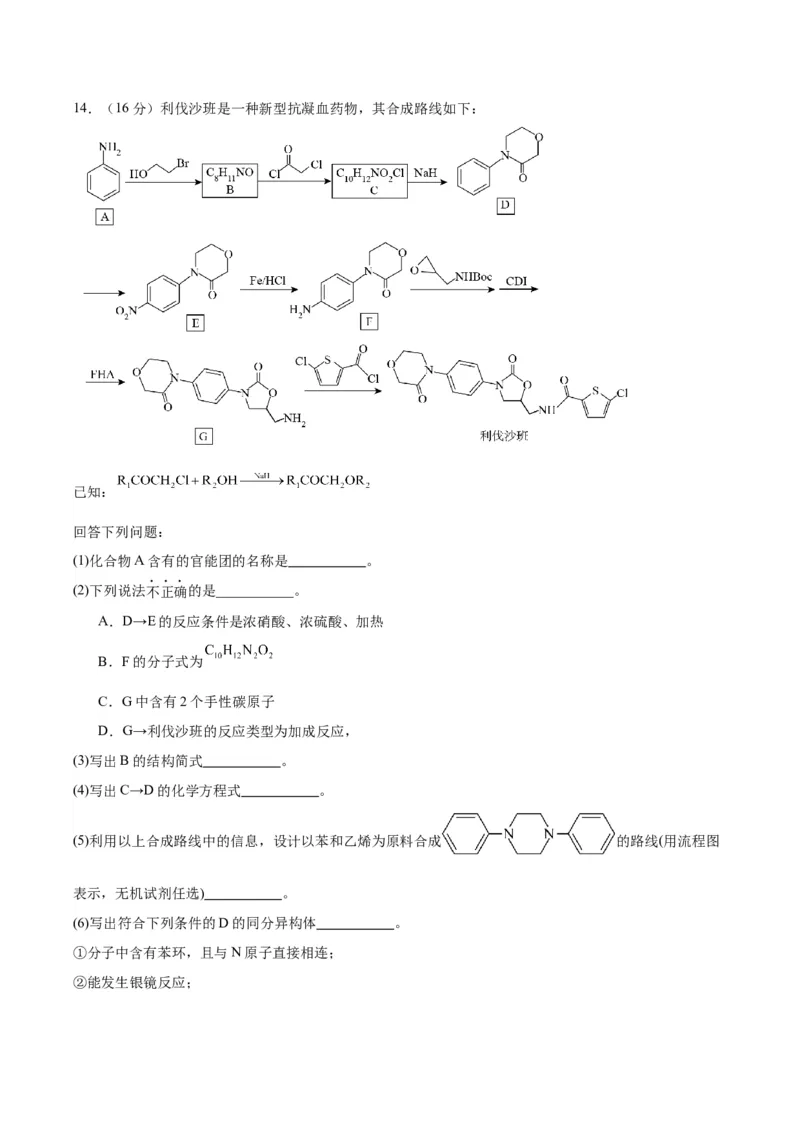
(1)基态碘原子的价电子排布式为 。
(2)CH NH 中所含元素电负性从大到小的顺序为 。
3(3)I 的VSEPR模型如下图,中心I原子的杂化方式是 (填“sp3”、“sp”、“sp3d”或“sp3d2”)。I
的空间构型为 。
(4)Ti的四卤化物熔点如下表所示。由此可推知,TiF 中的化学键类型是 TiCl 至TiI 熔点依次
4 4 4
升高,原因是 。
化合物 TiF TiCl TiBr TiI
4 4 4 4
熔点/℃ 377 -24.12 38.3 155
(5)(CH NH )PbI 晶体属于钙钛矿型结构(如图所示)。Pb2+周围距离最近且相等的I-数目有 个;
3 3 3
晶胞中A、B之间的距离为apm,(CHNH )PbI 式量为M,该物质的密度ρ= g·cm-3(列出计算式,
3 3 3
设N 为阿伏加德罗常数的值)。
A
(6)在离子晶体中,当0.414