文档内容
氯及其化合物
【学习目标】
1.了解氯气的物理性质
2.了解氯气与单质、水和碱的反应
3.了解氯气的实验室制取方法和原理
4.了解氯离子检验的方法
【学习重难点】
氯气的化学性质、氯水的主要性质
氯气的实验室制法、氯离子的检验方法
【课前复习】
钠与氯气反应的方程式为 ;自然界中
氯元素的主要存在形式是 。
【学习过程】
【第一课时】
氯及其化合物
一、氯气
1.氯气的物理性质:氯气是 有 的气体,可溶于水,易
,有一定的毒性,密度 。遇氯气泄漏时,人员应该迅速撤离至 ,
且尽量居于 。
2.氯气的化学性质:氯原子的最外层有 个电子,容易得到 个电子达到8电子
的稳定结构,所以氯气应该具有 。
(1)氯气与单质的反应:
【演示实验】在空气中点燃氢气,将点燃的氢气深入盛有氯气的集气瓶中,观察现象。
现象:氢气在氯气中 ,发出 ,生成的
HCl气体在集气瓶口与空气中的水蒸气结合,形成 。
方程式:
1 / 7氢气在氯气中能燃烧,说明燃烧需要的条件是
燃烧的本质是
(2)氯气与水的反应:氯气在水中的溶解度为
【演示实验】向试管中加入一定量的氯水,滴加硝酸银溶液观察现象。
现象: ;这说明
氯气溶于水时,部分氯气会与水反应,方程式为:
。HClO是 ,该物质具有 ,能够杀死水中的病菌起到消
毒的作用,因此很多自来水厂会用氯气消毒杀菌。近期有科学家提出,用氯气进行自来水消
毒时会产生对人体有害的 ,因此国家规定了自来水中余氯含量
的标准,同时也在积极研究新型自来水消毒剂( 等)。
【演示实验】向分别装有干燥红色布条和湿润红色布条的试剂瓶中通入氯气,观察现象。
现象:
结论:有漂白性的是
过氧化钠为什么具有漂白性?( )
次氯酸不稳定,光照分解的方程式为
(3)与碱的反应
根据氯气与水的反应,氯气与氢氧化钠溶液反应的方程式是
离子方程式为 用双线桥分析离子方程式。
将氯气通入氢氧化钠溶液会得到 ,
这样的混合溶液称为 ,其有效成分为 。
氯气与氢氧化钙溶液反应的方程式
将氯气通入 中会得到以次氯酸钙为有效成分的 ,若氯
气与氢氧化钙充分反应使 成为主要成分,就得到了 。
漂白液、漂白粉、漂粉精都是常用的 。
【第二课时】
二、 氯气
1.原理:实验室制备氯气的化学方程式为
该实验过程中使用的盐酸必须是
【思考与交流】根据初中学习过的气体实验室制法填写下表:
气 制取原理(方 反应物
反应条件 装置图
体 程式) 状态
2 / 7固体+固体加热的反应会选取的仪器是 ,固体+液体
不加热的反应会选取的仪器是 。
氯气的实验室制取是 ,选取的仪器是
组装的气体发生装置,具体装置图为: 。
在分液漏斗中加入 ,圆底烧瓶中加入 。
氯气应该使用 法进行收集,用 试剂进行尾气
吸收。按照这种方法得到的氯气会有 杂质,为了得到纯净的
氯气应该对制取的氯气进行净化除杂,氯气中的水蒸气可以用 除去,HCl可
以用
除去;应该先除去 杂质。由上,实验室得到较纯净的氯气的
实验装置为:
实验室制取气体的装置一般包括发生装置和收集装置,还有可能有除杂装置和尾气处理
装置。如果这些装置都需要,其顺序是
【思考与交流】请根据上述实验室制取氯气装置的选择,互相讨论,填写下表:
装置 选择装置的根据
发生装置
除杂装置
收集装置
尾气处理装置
【练习】已知实验室可以用亚硫酸钠(Na SO )固体和浓硫酸加热反应制取二氧化硫
2 3
(SO ),SO 属于酸性氧化物,在水中的溶解度为1:40,根据上述原则,画出实验室制取
2 2
二氧化硫的装置图。
如果再考虑到二氧化硫溶解度太大,则尾气处理装置有可能发生 ,可以将
尾气处理装置改为防倒吸装置如: 。
三、氯离子检验
【演示实验】在三支试管中分别加入稀盐酸、氯化钠溶液和碳酸钠溶液,再各滴入几滴
硝酸银溶液,观察现象,再加入稀硝酸观察现象。
3 / 7稀盐酸中加入硝酸银溶液现象为 ,再加稀硝酸
氯化钠溶液中加入硝酸银溶液现象为 ,再加稀硝酸
碳酸钠溶液中加入硝酸银溶液现象为 ,再加稀硝酸
上述实验过程中发生的所有反应的离子方程式有:
加盐溶液中的氯离子的方法是:
【检测反馈】
【第一课时】
1.下列说法不正确的是( )
A.氯元素在自然界中存在游离态,只是量极少
B.海水中的氯元素主要以NaCl等盐的形式存在
C.人体血液中含有NaCl,其浓度大约为0.9%
D.NaCl对维持人体的生理功能有着重要作用
2.氯的原子结构示意图是( )
A. B. C. D.
3.下列各种物理性质中,对氯气来说不正确的是( )
A.黄绿色的气体 B.密度比空气小
C.能溶于水 D.有刺激性气味
4.将氯气用软管通到田鼠洞中可消灭田鼠,这是利用了氯气下列性质中的( )
①黄绿色 ②密度比空气大 ③有毒 ④易液化 ⑤溶于水
A.①② B.②③ C.①②③ D.③④⑤
5.下列现象不属于H 在Cl 中燃烧现象的是( )
2 2
A.苍白色火焰 B.瓶口有白雾 C.集气瓶内气体颜色变浅 D.爆炸
6.下列含氯化合物中,不能由金属单质和氯气直接反应得到的是( )
A.FeCl B、CuCl C.AlCl D.AgCl
2 2 3
7.用自来水养金鱼时,我们通常先将自来水日晒一段时间后,再注入鱼缸,其目的是(
)
A.利用日光中紫外线杀死水中的细菌 B.提高水温,有利于金鱼生长
4 / 7C.增加水中氧气的含量 D.促使水中的次氯酸分解
8.用玻璃棒蘸取新制氯水滴在蓝色石蕊试纸中部,观察到的现象是( )
9.(1)游泳池水中的含氯气量应该控制在0.5 mg/L至1.0 mg/L之间,写出氯气溶于水
的化学方程式_______________________________________________________________。溶于
水后产生的________可杀菌消毒。
(2)下图显示一星期中每天19时泳池水中的氯气含量,哪几天使用泳池不安全____。
(3)你认为哪几天的天气火热、阳光强烈________,说出一种理由是______________
____________________________________________________________。
(4)若把一片紫色的花瓣放入氯水中,可观察到的现象是____________________。
【答案】1.A 2.C 3.B 4.B 5.D 6.A 7.D 8.C
9.(1)Cl +H O===HCl+HClO
2 2
HClO
(2)星期六、星期日
(3)星期四、星期六
这两天中Cl 含量变化较大
2
(4)花瓣褪色
【第二课时】
1.检验Cl-时,所用试剂硝酸的作用是( )
A.防止CO的干扰
B.防止Cl-的干扰
C.生成Ag CO 沉淀
2 3
D.防止NO干扰
2.证明某白色固体中含有Cl-的正确方法是( )
5 / 7A.加入AgNO 溶液和稀硝酸,看是否有白色沉淀生成
3
B.溶于水后加入AgNO 溶液,看是否有白色沉淀生成
3
C.加入AgNO 溶液,看是否有白色沉淀生成
3
D.溶于水后先加入Ba(NO ) 溶液,过滤,再加入AgNO 溶液和稀硝酸,看是否有白色
3 2 3
沉淀生成
3.下列微粒或物质中,化学性质最活泼的是( )
A.氯离子 B.氯原子
C.氯分子 D.液氯
4.能证明某溶液中含有NaCl的是( )
A.焰色反应是黄色
B.溶液有咸味
C.取少量溶液于试管中,滴加稀硝酸酸化的硝酸银溶液,出现白色沉淀
D.焰色反应是黄色,同时又能与稀硝酸酸化的硝酸银溶液反应生成白色沉淀
5.右图是一种检验某气体化学性质的实验装置,图中B为开关,如先打开B,在A处通
入干燥氯气,C中红色布条颜色无变化,当关闭B时,C处红色布条颜色褪去。则D瓶中盛
有的溶液是( )
A.浓H SO 溶液 B.饱和NaCl溶液
2 4
C.浓NaOH溶液 D.浓Ba(OH) 溶液
2
6.有一包白色固体,它可能是KCl、K CO KNO 中的一种或几种,进行下列实验:
2 3. 3
①溶于水,得无色溶液;
②在所得溶液中滴入AgNO 溶液,生成白色沉淀;
3
③再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是________,可能含有的成分是________。
(2)请写出上述实验中有关反应的离子方程式________________________________
________________________________________________________________________
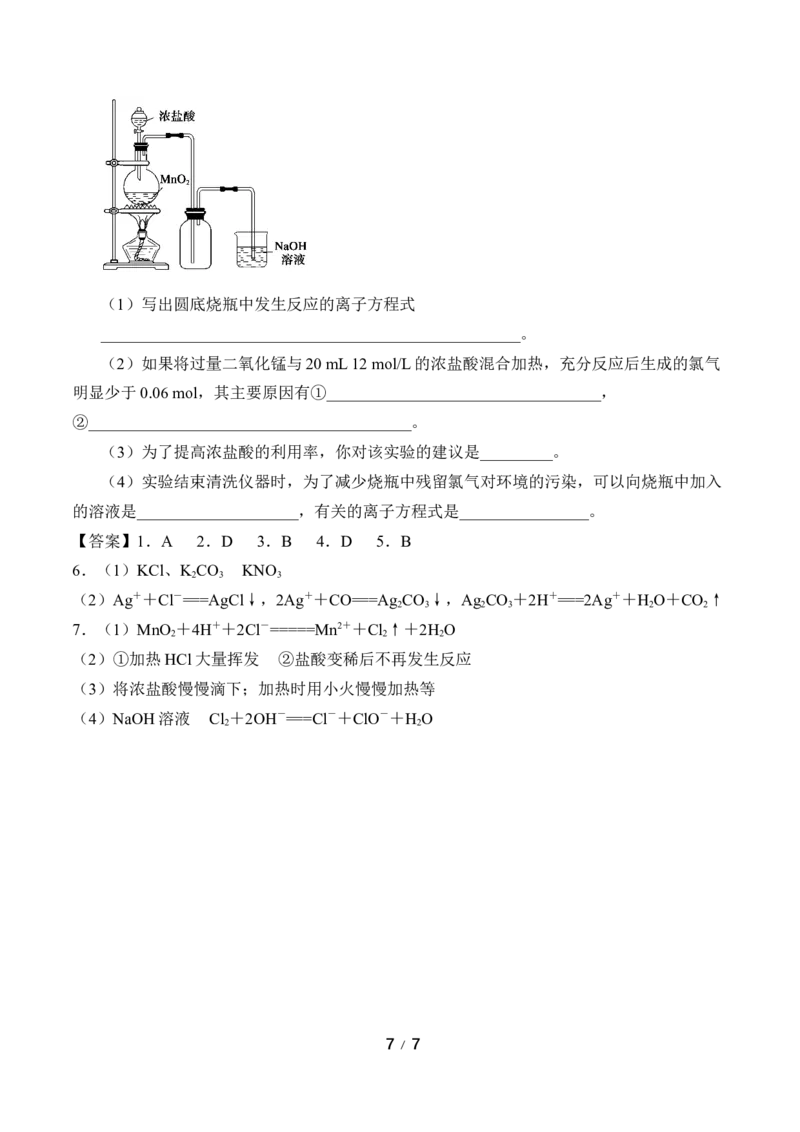
7.实验室中常用MnO 氧化浓盐酸的方法制取氯气,实验装置如图所示。
2
6 / 7(1)写出圆底烧瓶中发生反应的离子方程式
____________________________________________________。
(2)如果将过量二氧化锰与20 mL 12 mol/L的浓盐酸混合加热,充分反应后生成的氯气
明显少于0.06 mol,其主要原因有①__________________________________,
②________________________________________。
(3)为了提高浓盐酸的利用率,你对该实验的建议是_________。
(4)实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入
的溶液是____________________,有关的离子方程式是________________。
【答案】1.A 2.D 3.B 4.D 5.B
6.(1)KCl、K CO KNO
2 3 3
(2)Ag++Cl-===AgCl↓,2Ag++CO===Ag CO ↓,Ag CO +2H+===2Ag++H O+CO ↑
2 3 2 3 2 2
7.(1)MnO +4H++2Cl-=====Mn2++Cl ↑+2H O
2 2 2
(2)①加热HCl大量挥发 ②盐酸变稀后不再发生反应
(3)将浓盐酸慢慢滴下;加热时用小火慢慢加热等
(4)NaOH溶液 Cl +2OH-===Cl-+ClO-+H O
2 2
7 / 7