文档内容
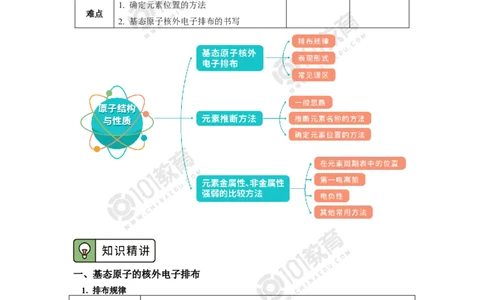
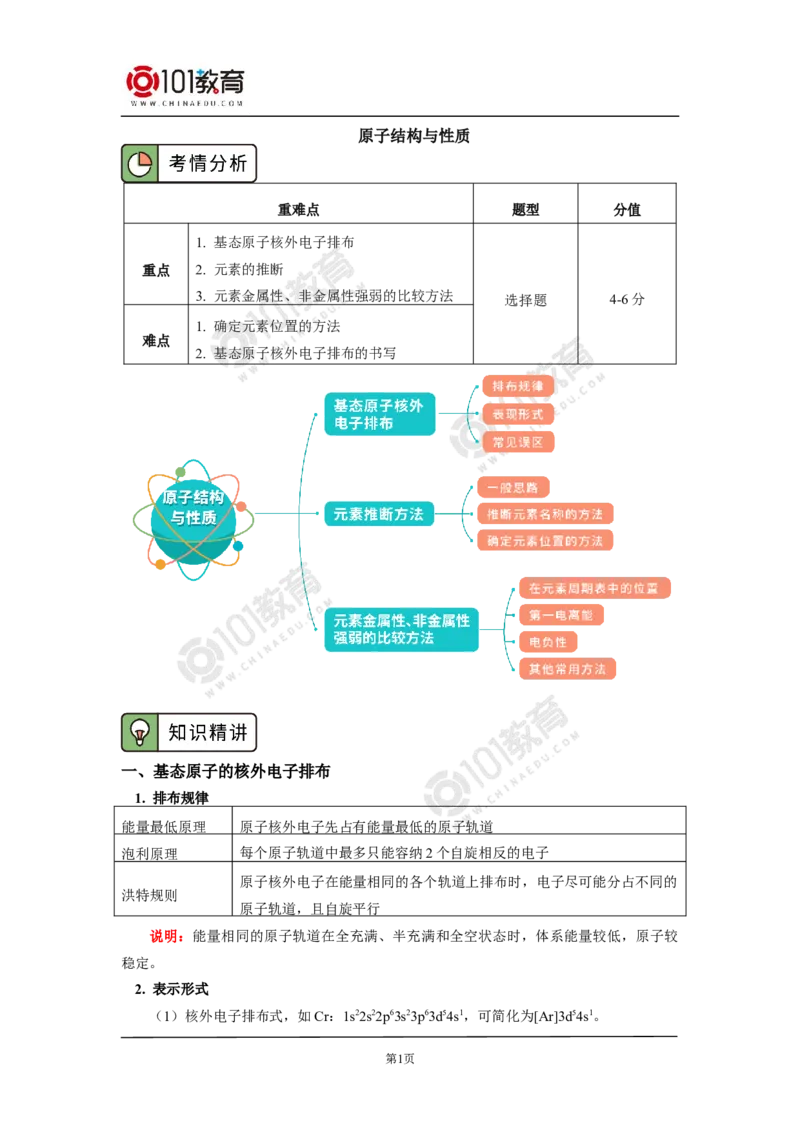
原子结构与性质
重难点 题型 分值
1. 基态原子核外电子排布
重点 2. 元素的推断
3. 元素金属性、非金属性强弱的比较方法 选择题 4-6分
1. 确定元素位置的方法
难点
2. 基态原子核外电子排布的书写
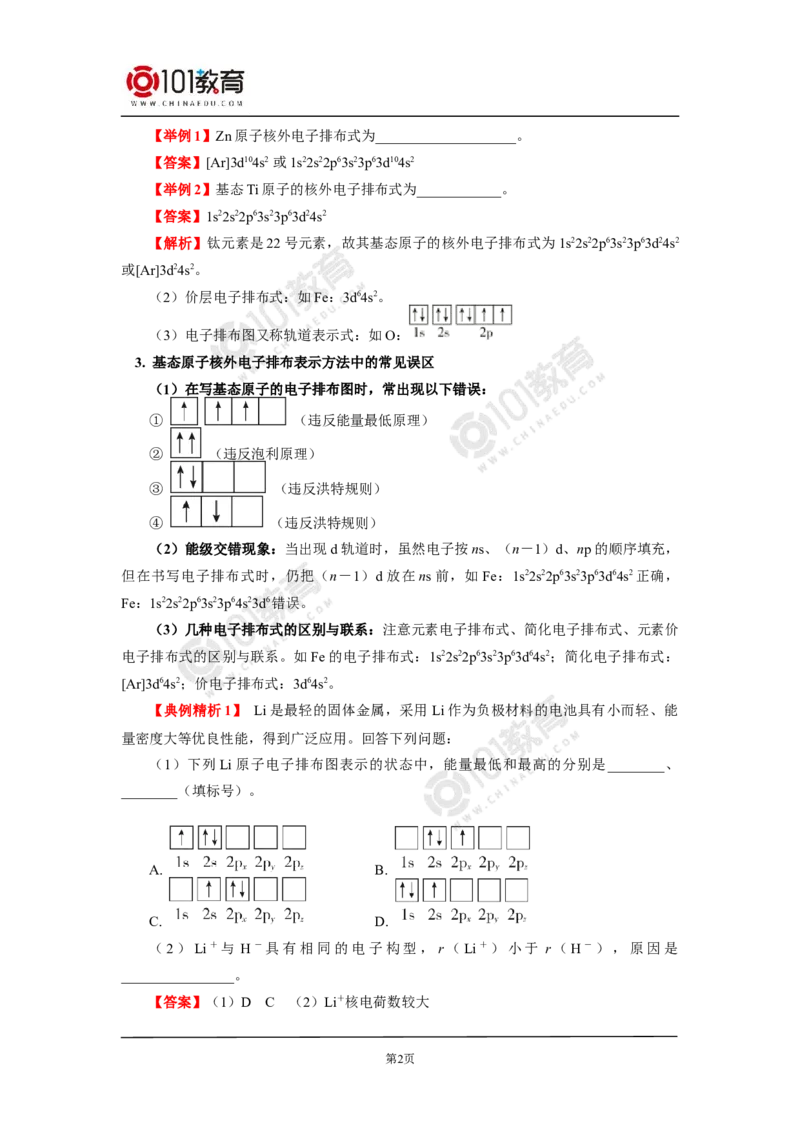
一、基态原子的核外电子排布
1. 排布规律
能量最低原理 原子核外电子先占有能量最低的原子轨道
泡利原理 每个原子轨道中最多只能容纳2个自旋相反的电子
原子核外电子在能量相同的各个轨道上排布时,电子尽可能分占不同的
洪特规则
原子轨道,且自旋平行
说明:能量相同的原子轨道在全充满、半充满和全空状态时,体系能量较低,原子较
稳定。
2. 表示形式
(1)核外电子排布式,如Cr:1s22s22p63s23p63d54s1,可简化为[Ar]3d54s1。
第1页【举例1】Zn原子核外电子排布式为____________________。
【答案】[Ar]3d104s2 或1s22s22p63s23p63d104s2
【举例2】基态Ti原子的核外电子排布式为____________。
【答案】1s22s22p63s23p63d24s2
【解析】钛元素是22号元素,故其基态原子的核外电子排布式为1s22s22p63s23p63d24s2
或[Ar]3d24s2。
(2)价层电子排布式:如Fe:3d64s2。
(3)电子排布图又称轨道表示式:如O:
3. 基态原子核外电子排布表示方法中的常见误区
(1)在写基态原子的电子排布图时,常出现以下错误:
① (违反能量最低原理)
② (违反泡利原理)
③ (违反洪特规则)
④ (违反洪特规则)
(2)能级交错现象:当出现d轨道时,虽然电子按ns、(n-1)d、np的顺序填充,
但在书写电子排布式时,仍把(n-1)d放在ns前,如Fe:1s22s22p63s23p63d64s2正确,
Fe:1s22s22p63s23p64s23d6错误。
(3)几种电子排布式的区别与联系:注意元素电子排布式、简化电子排布式、元素价
电子排布式的区别与联系。如Fe的电子排布式:1s22s22p63s23p63d64s2;简化电子排布式:
[Ar]3d64s2;价电子排布式:3d64s2。
【典例精析1】 Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能
量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别是________、
________(填标号)。
A. B.
C. D.
(2)Li+与 H-具有相同的电子构型,r(Li+)小于 r(H-),原因是
________________。
【答案】(1)D C (2)Li+核电荷数较大
第2页【解析】(1)根据核外电子排布规律可知Li的基态核外电子排布式为1s22s1,则D中
能量最低;C中有2个电子处于2p能级上,能量最高。
(2)由于锂的核电荷数较大,原子核对最外层电子的吸引力较大,因此Li+的半径小
于H-。
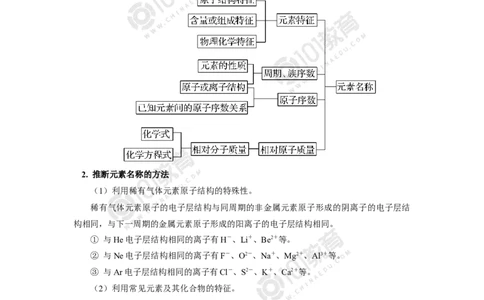
二、元素的推断方法
1. 元素推断的一般思路
2. 推断元素名称的方法
(1)利用稀有气体元素原子结构的特殊性。
稀有气体元素原子的电子层结构与同周期的非金属元素原子形成的阴离子的电子层结
构相同,与下一周期的金属元素原子形成的阳离子的电子层结构相同。
① 与He电子层结构相同的离子有H-、Li+、Be2+等。
② 与Ne电子层结构相同的离子有F-、O2-、Na+、Mg2+、Al3+等。
③ 与Ar电子层结构相同的离子有Cl-、S2-、K+、Ca2+等。
(2)利用常见元素及其化合物的特征。
① 形成化合物种类最多的元素之一、单质是自然界中硬度最大的物质的元素:C。
② 空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素;N。
③ 地壳中含量最多的元素或氢化物在通常情况下呈液态的元素;O。
④ 单质密度最小的元素:H;单质密度最小的金属元素:Li。
⑤ 单质在常温下呈液态的非金属元素:Br;金属元素:Hg。
⑥ 最高价氧化物及其对应水化物既能与强酸反应,又能与强碱反应的元素:Be、
Al。
⑦ 元素的气态氢化物和它的最高价氧化物对应水化物能发生化合反应的元素:N;能
第3页发生氧化还原反应的元素:S。
⑧ 元素的单质在常温下能与水反应放出气体的短周期元素:Li、Na、F。
3. 确定元素位置的方法
(1)由基态原子的价电子排布式给元素定位。
周期序数 = 电子层数(能层序数)= 最高能层序数
主族元素的族序数 = 价电子数
第ⅢB族~第ⅦB族的价电子排布式为(n-1)d1-10ns1~2(镧系、锕系除外),族序
数=价电子数。如锰的价电子排布式为3d54s2,它位于元素周期表中第四周期第ⅦB族。
第ⅠB族和第ⅡB族的价电子排布式为(n-1)d10ns1~2,族序数=ns轨道上的电子数。
(2)根据原子序数以0族为基准给元素定位:
稀有气体元素在周期表中的位置
稀有气体元素 He Ne Ar Kr Xe Rn Og
周期序数 一 二 三 四 五 六 七
原子序数 2 10 18 36 54 86 118
判断方法:减数定位法。即由与稀有气体元素的原子序数之差确定元素在周期表中的
位置。
① 当原子序数与稀有气体原子序数相近且小时:
第一步先确定纵列数从而确定族数:原子序数-稀有气体元素的原子序数(相近且
小)= 元素所在的纵列数。
已知在元素周期表中:第1、2纵列为第ⅠA族、ⅡA族,第3~7纵列为第ⅢB族~
第ⅦB族,第8~10纵列为第Ⅷ族,第11、12纵列为第ⅠB族、ⅡB族,第13~17纵列
为第ⅢA族~第ⅦA族。
第二步确定周期数:该元素的周期数 = 稀有气体元素的周期数+1。
【举例】如判断原子序数为41的元素在元素周期表中的位置。
【分析】41与36接近,有41-36=5,故该元素位于第五周期第ⅤB族。
当原子序数与稀有气体原子序数相近且大时:
稀有气体元素的原子序数(相近且大)-原子序数=18-该元素所在纵列数。
如判断新发现的114号元素在元素周期表中的位置。
分析:118-114=18-该元素所在纵列数,该元素所在纵列数=14,为顺数第14纵列或
倒数第5纵列,故114号元素位于第七周期第ⅣA族。
【典型例题2】A、B、C、D、E是元素周期表前四周期中五种常见的元素,其相关信
息如下表:
元素 相关信息
第4页A 原子核外L层电子数是K层的2倍
B 其一种单质可构成地球生物的“保护伞”
C 原子的第一电离能在第三周期中最小
D 基态原子最外层电子排布式为(n+1)sn(n+1)p(n+2)
E 可形成多种氧化物,其中一种为具有磁性的黑色晶体
请回答下列问题:
(1)C在元素周期表中位于第________周期、第________族;E的基态原子核外电子
排布式是_____________________________。
(2)B、C、D 的简单离子半径由大到小的顺序为(用化学符号表示,下同)
________________,B、D的简单气态氢化物中稳定性较强的是________。
(3)B、C的单质按物质的量之比为1∶2形成的化合物中化学键的类型为________。
【答案】(1)三 ⅠA 1s22s22p63s23p63d64s2或[Ar]3d64s2 (2)S2->O2->Na+ HO
2
(3)共价键、离子键
三、元素金属性、非金属性强弱的比较方法
方法 元素金属性强弱的判断 元素非金属性强弱的判断
同周期从左到右元素非金属性增
在元素周期表中 同周期从左到右元素金属性减弱,
强,同主族从上到下元素非金属性
的位置 同主族从上到下元素金属性增强
减弱
第一电离能越小,元素金属性越强 第一电离能越大,元素非金属性越
第一电离能 (注意:同周期ⅡA族与ⅢA族元 强(注意:同周期ⅤA族与ⅥA族
素例外) 元素例外)
电负性 电负性越小,元素金属性越强 电负性越大,元素非金属性越强
①单质与水或酸反应置换出H 的
2
①单质与H 化合的难易程度;
2
能力;
②最高价氧化物对应水化物的酸性
②最高价氧化物对应水化物的碱性
其他常用方法 强弱;
强弱;
③非金属单质间的置换反应;
③金属单质间的置换反应;对应金
④对应阴离子的还原性强弱等
属阳离子的氧化性强弱等
【典例精析3】氨硼烷(NH BH )含氢量高、热稳定性好,是一种具有潜力的固体储
3 3
氢材料。回答下列问题:
NH BH 分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性
3 3
(Hδ-),电负性大小顺序是________。与NH BH 原子总数相等的等电子体是________
3 3
第5页(写分子式),其熔点比NH BH________(填“高”或“低”),原因是在NH BH 分子
3 3 3 3
之间,存在________________________,也称“双氢键”。
【答案】N>H>B CHCH 低 Hδ+与Hδ-的静电引力
3 3
【解析】NH BH 分子中,与N原子相连的H呈正电性,说明N的电负性大于H;与
3 3
B原子相连的H呈负电性,说明H的电负性大于B,因此3种元素电负性由大到小的顺序
为N>H>B。NH BH 分子中有8个原子,其价电子总数为14,N和B的价电子数的平均
3 3
值为4,依据等量代换的原则,可以找到其等电子体为 CHCH 。由于NH BH 分子属于极
3 3 3 3
性分子,而CHCH 属于非极性分子,两者相对分子质量接近,但是极性分子的分子间作
3 3
用力较大,故CHCH 熔点比NH BH 低。NH BH 分子间存在“双氢键”,类比氢键的形
3 3 3 3 3 3
成原理,说明其分子间存在Hδ+与Hδ-的静电引力。
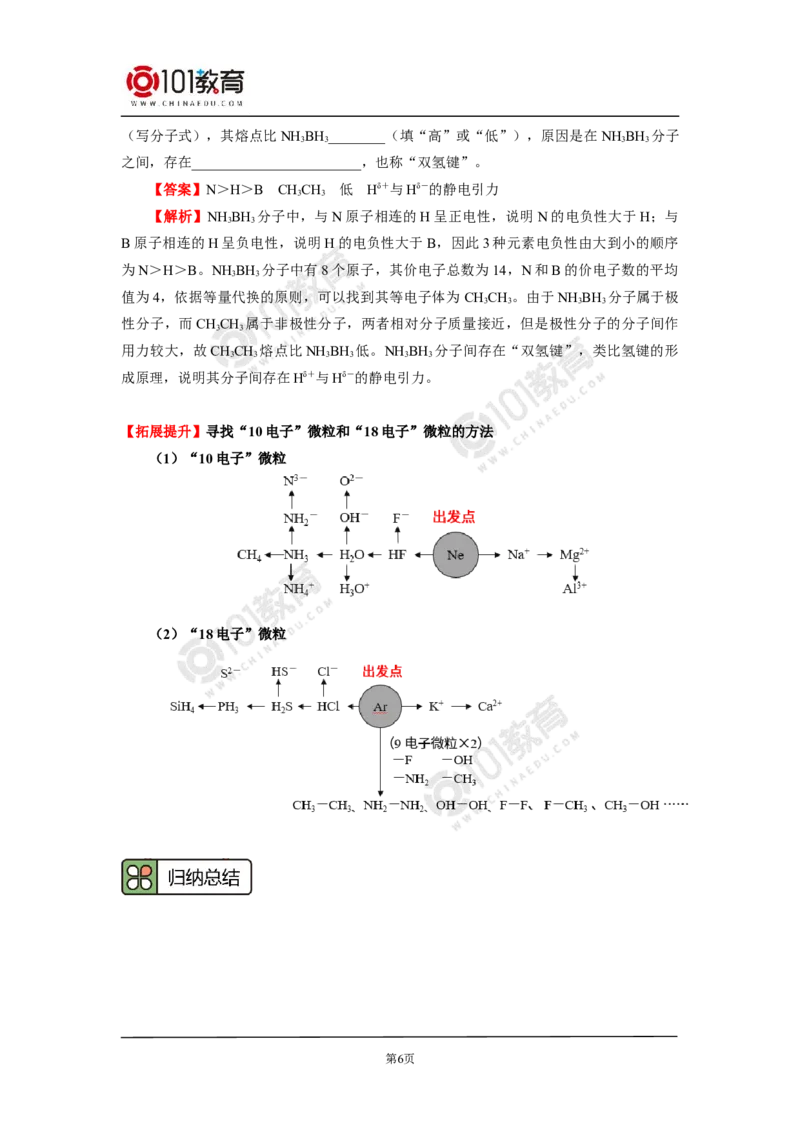
【拓展提升】寻找“10电子”微粒和“18电子”微粒的方法
(1)“10电子”微粒
(2)“18电子”微粒
第6页下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。
X Y Z
R
W
J
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1)R原子的电子排布图为________。
(2)在化合物YZ 中Y的化合价为________;Y2-与Na+的半径大小为________。
2
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是________;X与Y的第一电
离能:X________Y(填“<”“>”或“=”),其理由是________________________。
(4)在双原子分子中,最稳定单质的电子式为________;
有一种酸 HX 的酸性与醋酸相近,HX 溶液与 NaOH 溶液反应的离子方程式为
3 3
________________________。
第7页【答案】(1)
(2)+2价 O2->Na+(或Na+<O2-)
(3)F>O>N > N原子的2p轨道电子数为半充满状态,较稳定
−
(4)∶N N∶ HN +OH-===N3 +HO
3 2
【解析】由表中元素排列知6种元素位于p区二、三、四、五周期,结合问题(2)中
⋮⋮
Y2-符号知Y位于ⅥA族。六种元素分别为X:N,Y:O,Z:F,R:S,W:Br,J:
Xe。
(1)S原子的电子排布图为
(2)在化合物YZ (OF )中Y的化合价为+2价;Y2-与Na+的半径大小为O2->Na
2 2
+;
(3)在N、O、F三种元素中,电负性由大到小的顺序是F>O>N;由于N原子的2p
轨道电子数为半充满状态,较稳定,故N、O的第一电离能:N>O;
(4)在双原子分子中,最稳定单质为N ,电子式为∶N N∶;HN 溶液与NaOH溶
2 3
−
液反应的离子方程式为:HN
3
+OH-===N3 +H
2
O。
⋮⋮
(答题时间:45分钟)
一、选择题
1. 下列说法正确的是( )
A. 任何一个电子层最多只有s、p、d、f四个能级
B. 用n表示电子层数,则每一电子层最多可容纳的电子数为2n2
C. 核外电子运动的概率密度分布图就是原子轨道
D. 电子的运动状态可从电子层、能级、原子轨道三个方面进行描述
2. 铋的相关信息如图所示,下列说法正确的是( )
元素符号:Bi
原子序数:83
相对原子质量:209. 0
价电子排布式:6s26p3
A. Bi元素的质量数是209
B. Bi元素位于第六周期第ⅤA族
C. Bi原子的6p能级上有1个未成对电子
第8页D. Bi原子最外层有5个能量相同的电子
3. 对应下列叙述的微粒M和N,肯定属于同主族元素且化学性质相似的是( )
A. 原子核外电子排布式:M为1s22s2,N为1s2
B. 结构示意图:M为 ,N为
C. M原子基态2p轨道上有一对成对电子,N原子基态3p轨道上有一对成对电子
D. M原子基态2p轨道上有1个未成对电子,N原子基态3p轨道上有1个未成对电子
4. 如图是第三周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的
是( )
A. y轴表示的可能是电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是形成基态离子转移的电子数
5. 下列判断正确的是( )
A. 第一电离能:B>Al>Ga B. 电负性:F>N>O
C. 最高正化合价:F>S>Si D. 原子半径:P>N>C
6. 硒是人体必需的微量元素,它能有效提高人体免疫机能,抑制癌症和心脑血管等疾病
的发病率。下列有关说法正确的是( )
A. 硒元素位于元素周期表中第15列
B. 硒元素原子的价电子排布式为4s24p4
C. 硒的氧化物只有一种
D. 基态原子核外电子排布中共有7个能级
7. 下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中
正确的是( )
A. W元素的第一电离能小于Y元素的第一电离能
B. Y、Z的阴离子电子层结构都与R原子的相同
第9页C. p能级未成对电子最多的是Z元素
D. X元素是电负性最大的元素
8. X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层
电子总数少4,Z的最外层电子数是内层电子总数的3倍。下列有关叙述正确的是( )
A. Y的价电子排布式为3s23p5 B. 稳定性:Y的氢化物>Z的氢化物
C. 第一电离能:Y<Z D. X、Y两元素形成的化合物为离子化合物
9. 13C—NMR(核磁共振)、15N—NMR可用于测定蛋白质、核酸等生物大分子的空间结
构。下面有关13C、15N的叙述正确的是( )
A. 13C与15N有相同的中子数 B. 13C的电子排布式为1s22s22p3
C. 15N与14N互为同位素 D. 15N的电子排布式为1s22s22p4
10. 主族元素A和B可形成AB 型离子化合物,则A、B两元素原子的最外层电子排布
2
式分别为( )
A. ns2np2和ns2np4 B. ns1和ns2np4
C. ns2和ns2np5 D. ns1和ns2
11. 镁、锂在元素周期表中具有特殊的“对角线”关系,它们的性质相似。下列有关锂
的性质的叙述,不正确的是( )
A. Li SO 易溶于水 B. LiOH是受热不易分解的强碱
2 4
C. Li遇浓硫酸不产生“钝化”现象 D. Li CO 受热分解,生成LiO和CO
2 3 2 2
12. 下列元素的最高价氧化物对应的水化物酸性最强的是( )
A. L电子层p轨道只填了2个电子的元素
B. 外围电子排布式为3s23p2的元素
C. 第三周期有7个价电子的元素
D. 3p轨道电子半充满的元素
二、非选择题
13. 根据原子结构、元素周期表和元素周期律的知识回答下列问题:
1
4
(1)A元素次外层电子数是最外层电子数的 ,其外围电子排布图是_____________。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称
是________,在元素周期表中的位置是_______________________________。
(3)C元素基态原子的电子排布图是下图中的________(填序号),另一电子排布图
不能作为基态原子的电子排布图是因为它不符合________(填序号)。
第10页A. 能量最低原理 B. 泡利原理 C. 洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子
所需的最低能量叫作第一电离能(设为E)。如图所示:
①同周期内,随着原子序数的增大,E值变化的总趋势是________;
②根据图中提供的信息,可推断出E ________E (填“>”“<”或“=”,下
氧 氟
同);
③根据第一电离能的含义和元素周期律,可推断出E ________E 。
镁 钙
第11页1.【答案】B
【解析】A项,由于元素周期表未填满,以后还会有元素被发现,电子层除有s、p、
d、f四个能级外,可能还有其他能级存在,错误。C项,核外电子运动的概率密度分布图
表示电子在核外空间单位体积内出现的概率,电子在原子核外的一个空间运动状态称为一
个原子轨道,错误。D项,电子的运动状态可从电子层、能级、原子轨道、电子的自旋状
态四个方面进行描述,错误。
2.【答案】B
【解析】A项,209为铋元素的相对原子质量不是质量数,错误。C项,Bi原子的6p
能级上有3个未成对电子,错误。D项,Bi原子最外层的5个电子能量不完全相同,错误。
3.【答案】C
【解析】A项,M为Be,N为He,二者不属于同主族元素,错误;B项,前者属于原
子,后者属于离子,性质不相似,错误;C项,M为O,N为S,二者属于同主族元素,化
学性质相似,正确;D项,M可能为B或F,N可能为Al或Cl,二者可能不属于同主族元
素,错误。
4.【答案】B
【解析】对于第三周期11~17号元素,随着原子序数的增大,第一电离能呈增大趋势,
但Mg、P特殊,故A项错误;同周期元素自左到右原子半径逐渐减小,故C项错误;形成
基态离子转移的电子数依次为:Na为1,Mg为2,Al为3,Si不易形成离子,P为3,S为
2,Cl为1,故D项错误。
5.【答案】A
【解析】同主族元素的第一电离能随原子序数的增大而减小,A项正确;同周期元素
的电负性随原子序数的增大而增大,B项错误;F无正价,C项错误;同周期元素(0族元
素除外)的原子半径随原子序数的增大而减小,D项错误。
6.【答案】B
【解析】硒是34号元素,其基态原子电子排布式为 1s22s22p63s23p63d104s24p4,可确定
B正确,A错误;应含有8个能级,D错误;C中,由同主族元素硫存在两种氧化物SO 和
2
SO ,可推得硒也有两种氧化物SeO 和SeO,故C错误。
3 2 3
7.【答案】D
【解析】根据五种元素所处位置,X、W、Y、R、Z五种元素分别为:F、P、S、
Ar、Br。P元素的第一电离能比S元素的第一电离能要略大,Z的阴离子比R原子多一个
电子层,故A选项和B选项是错误的。W元素的p能级上有3个未成对的电子,故C选项
是错误的;X是所有元素中非金属性最强的元素,即D选项是正确的。
第12页8.【答案】C
【解析】Y原子应该有3个电子层,最外层电子数为6,是硫元素,价电子排布式为
3s23p4;Z元素是O,第一电离能O>S;X可能是H,也可能是Li或Na,HS是共价化合
2
物。
9.【答案】C
【解析】A项中两种原子的中子数分别为7和8;B项中碳的核外电子数为6,所以电
子排布式为1s22s22p2;C项符合同位素的概念;D项中N的电子排布式应为1s22s22p3。
10.【答案】C
【解析】A和B为主族元素,且二者能形成AB 型离子化合物,则A为第ⅡA族元素,
2
B为第ⅦA族元素,故A元素原子的最外层电子排布式为ns2,B元素原子的最外层电子排
布式为ns2np5。
11.【答案】B
【解析】运用对角线规则,可由Mg及其化合物的性质推测Li及其相应化合物的性质。
根据MgSO 易溶于水,Mg(OH) 是一种易分解的中强碱,Mg在浓硫酸中不会发生“钝
4 2
化”,MgCO 受热易分解为MgO和CO 等性质,推测出LiSO 易溶于水,LiOH是一种易
3 2 2 4
分解的中强碱,Li在浓硫酸中不会发生“钝化”,LiCO 受热易分解为LiO和CO 等。
2 3 2 2
12.【答案】C
【解析】A项中元素为C,B项中元素为Si,C项中元素为Cl,D项中元素为P。酸性:
HClO>HPO >HCO>HSiO。
4 3 4 2 3 2 3
13.【答案】(1) (2)铬 第四周期第ⅥB族 (3)② C (4)
①增大 ②< ③>
1
4
【解析】(1)次外层电子数是最外层电子数的 的元素是氖。(2)1~36号元素中,
原子核外电子排布中未成对电子数最多的元素是铬,共有 6个未成对电子。(3)由该基态
原子的电子排布图中的电子数可知,C元素是硅,根据洪特规则,当电子排布在同一能级
的不同轨道时,总是优先单独占据一个轨道,且自旋方向相同,故硅元素基态原子的电子
排布图为②。(4)同周期内,随着原子序数的增大,第一电离能变化的总趋势是增大;同
主族内,随着电子层数的增多,第一电离能变化的总趋势是减小。
第13页