文档内容
分子结构与性质
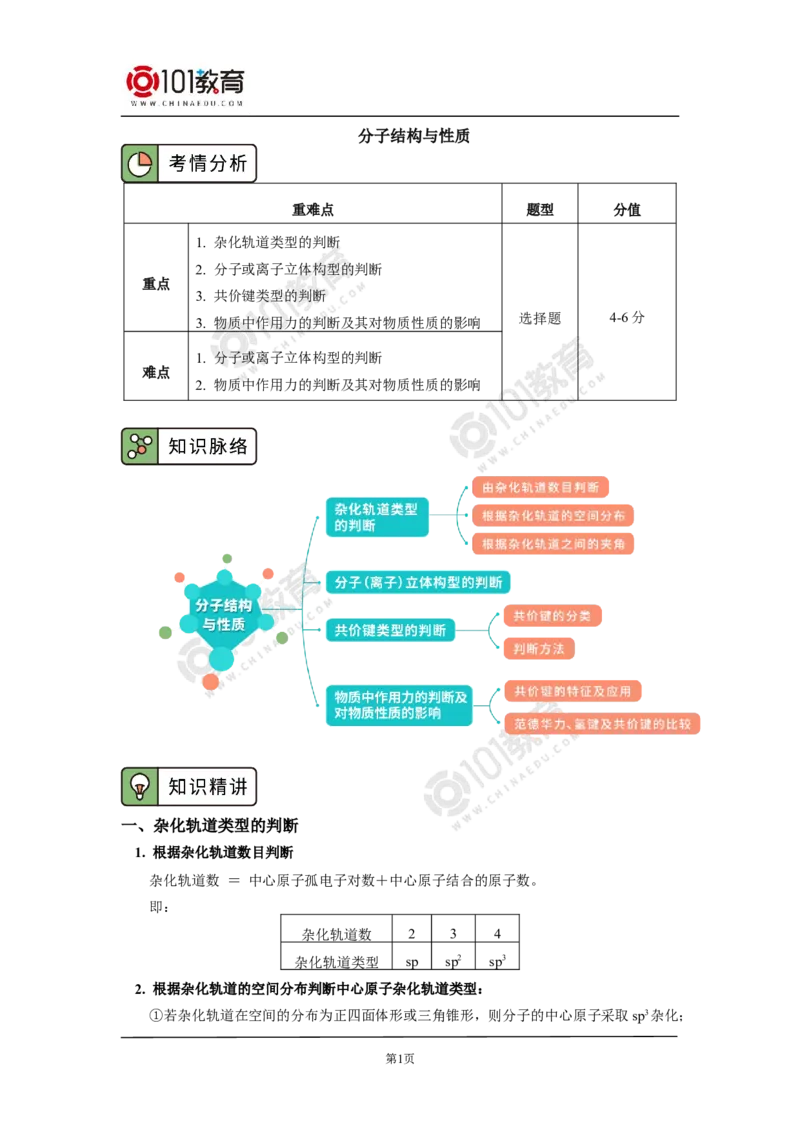
重难点 题型 分值
1. 杂化轨道类型的判断
2. 分子或离子立体构型的判断
重点
3. 共价键类型的判断
选择题 4-6分
3. 物质中作用力的判断及其对物质性质的影响
1. 分子或离子立体构型的判断
难点
2. 物质中作用力的判断及其对物质性质的影响
一、杂化轨道类型的判断
1. 根据杂化轨道数目判断
杂化轨道数 = 中心原子孤电子对数+中心原子结合的原子数。
即:
杂化轨道数 2 3 4
杂化轨道类型 sp sp2 sp3
2. 根据杂化轨道的空间分布判断中心原子杂化轨道类型:
①若杂化轨道在空间的分布为正四面体形或三角锥形,则分子的中心原子采取sp3杂化;
第1页②若杂化轨道在空间的分布为平面三角形,则分子的中心原子采取sp2杂化;
③若杂化轨道在空间的分布为直线形,则分子的中心原子采取sp杂化。
3. 根据杂化轨道之间的夹角判断中心原子杂化轨道类型:若杂化轨道之间的夹角为
109°28′,则分子的中心原子采取sp3杂化;若杂化轨道之间的夹角为120°,则分子的中心
原子采取sp2杂化;若杂化轨道之间的夹角为180°,则分子的中心原子采取sp杂化。
【典例分析1】氯化亚砜(SOCl )是一种很重要的化学试剂,可以作为氯化剂和脱水
2
剂。下列关于氯化亚砜分子的几何构型和中心原子(S)采取杂化方式的说法正确的是(
)
A. 三角锥形、sp3 B. V形、sp2
C. 平面三角形、sp2 D. 三角锥形、sp2
【答案】A
1
2
【解析】SOCl 分子中硫原子的价层电子对数=σ键电子对数+孤电子对数=3+ ×
2
(6-2×1-2)=4,故S原子采取sp3杂化,由于孤电子对占据一个杂化轨道,所以分子构
型为三角锥形。
二、分子(离子)立体构型的判断
通过分子的价层电子对数、孤电子对数确定分子的立体构型。
其中:a是中心原子的价电子数(阳离子要减去电荷数、阴离子要加上电荷数),b是
与中心原子结合的原子最多能接受的电子数,x是与中心原子结合的原子数。
σ键电子对数 中心原子上的孤电子对数 价层电子对数 立体构型
1
SnCl 2 2 2 (4-2×1)=1 3 V形
1
BeCl 2 2 2 (2-2×1)=0 2 直线形
1
CS 2 2 2 (4-2×2)=0 2 直线形
1
OF 2 2 2 (6-2×1)=2 4 V形
第2页方法规律:判断分子或离子的立体构型时,要能够正确计算价层电子对数:一是直接
根据中心原子的价电子成键情况分析;二是运用计算式推导出价层电子对数。
【总结提升】
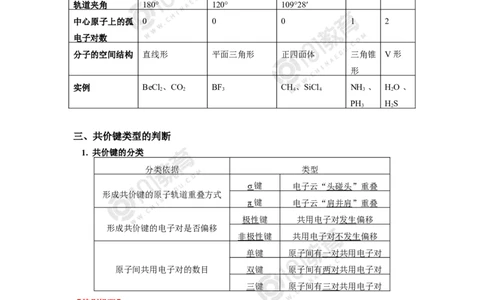
s、p 杂化轨道和简单分子的空间结构的关系
杂化类型 sp sp2 sp3 sp3不等性杂化
轨道夹角 180° 120° 109°28′
中心原子上的孤 0 0 0 1 2
电子对数
分子的空间结构 直线形 平面三角形 正四面体 三角锥 V形
形
实例 BeCl 、CO BF CH、SiCl NH 、 HO 、
2 2 3 4 4 3 2
PH HS
3 2
三、共价键类型的判断
1. 共价键的分类
分类依据 类型
σ 键 电子云“头碰头”重叠
形成共价键的原子轨道重叠方式
π 键 电子云“肩并肩”重叠
极性键 共用电子对发生偏移
形成共价键的电子对是否偏移
非极性键 共用电子对不发生偏移
单键 原子间有一对共用电子对
原子间共用电子对的数目 双键 原子间有两对共用电子对
三键 原子间有三对共用电子对
【特别提醒】
(1)只有两原子的电负性相差不大时,才能形成共用电子对,形成共价键,当两原子
的电负性相差很大(大于1.7)时,不会形成共用电子对,而形成离子键。
(2)同种非金属元素原子间形成的共价键为非极性键,不同种非金属元素原子间形成
的为极性键。
2. 共价键类型的判断方法
①根据成键元素判断:同种元素间形成的是非极性键,不同元素间形成的是极性键。
②根据原子间共用电子对数目判断单键、双键或三键。
第3页③根据共价键规律判断σ键、π键及其个数;原子间形成单键,则为σ键;形成双键,
则含有一个σ键和一个π键;形成三键,则含有一个σ键和两个π键。
【拓展提升】键的极性与分子极性的关系
1. 对于双原子分子,键的极性就是分子的极性。
①由极性键形成的双原子分子(表示为 AB型分子),一定是极性分子,如 CO、
NO、HCl等分子。
②由非极性键形成的双原子分子(表示为A 型分子),一定是非极性分子,如O 、
2 2
N、Cl 等分子。
2 2
2. 三原子及三原子以上的分子,结构有可能对称,键的极性互相抵消,有可能为非极性
分子,比如:CH、、CCl 、CO 等。
4 4 2
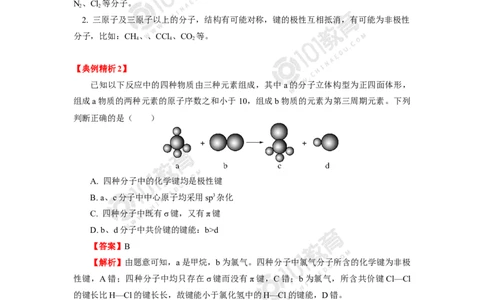
【典例精析2】
已知以下反应中的四种物质由三种元素组成,其中a的分子立体构型为正四面体形,
组成a物质的两种元素的原子序数之和小于10,组成b物质的元素为第三周期元素。下列
判断正确的是( )
A. 四种分子中的化学键均是极性键
B. a、c分子中中心原子均采用sp3杂化
C. 四种分子中既有σ键,又有π键
D. b、d分子中共价键的键能:b>d
【答案】B
【解析】由题意可知,a是甲烷,b为氯气。四种分子中氯气分子所含的化学键为非极
性键,A错;四种分子中均只存在σ键而没有π键,C错;b为氯气,所含共价键Cl—Cl
的键长比H—Cl的键长长,故键能小于氯化氢中的H—Cl的键能,D错。
四、物质中作用力的判断及对物质性质的影响
1. 共价键的特征及应用
(1)利用范德华力判断物质熔、沸点高低的前提是物质的组成和结构要相似。结构相
似的判断方法有两种:一是同一主族同一类别的物质的结构相似,如HS和HTe;二是运
2 2
用价层电子对互斥理论模型判断其分子的立体构型。
(2)比较分子沸点时,一定要注意氢键的存在。分子间氢键能使沸点升高,分子内氢
键使沸点降低。
第4页2. 范德华力、氢键及共价键的比较
范德华力 氢键 共价键
氢原子、电负性很大的
作用微粒 分子或原子(稀有气体) 原子
原子
强度比较 共价键 > 氢键 > 范德华力
①随着分子极性的增大而
成键原子半径越
增大; 对于A—H…B—,A、B
影响强度 小,键长越短,
②组成和结构相似的物 的电负性越大,B原子的
的因素 键能越大,共价
质,相对分子质量越大, 半径越小,作用力越大
键越稳定
范德华力越大
①影响物质的熔点、沸
点、溶解度等物理性质; 分子间氢键的存在,使 ①影响分子的稳
②组成和结构相似的物 物质的熔、沸点升高, 定性;
对物质性
质,随相对分子质量的增 在水中的溶解度增大, ②共价键的键能
质的影响
大,物质的熔、沸点升 如熔、沸点:HO>HS, 越大,分子稳定
2 2
高,如FHCl,NH >PH 性越强
2 2 2 2 3 3
CFBCl >PCl4>NH>H O,所以B正确。
2 3 3 2
7.【答案】D
【解析】乳酸CH—CHOH—COOH中次甲基上的碳原子连有四个不同的原子或原子
3
团,故只有1个手性碳原子,A项错误;甘油CHOH—CHOH—CH OH中没有手性碳原子,
2 2
B项错误;脱氧核糖CHOH—CHOH—CHOH—CH —CHO中次甲基上的碳原子连有四个
2 2
不同的原子或原子团,故含有2个手性碳原子,C项错误;核糖CHOH—CHOH—CHOH
2
—CHOH—CHO中次甲基上的碳原子连有四个不同的原子或原子团,故有3个手性碳原子,
D项正确。
8.【答案】B
【解析】CHCl 分子中C原子没有孤电子对,是四面体,A错误;AB 分子中A原子
3 2
如果以sp2或sp3杂化均是V形,B正确;二氧化硅中硅以sp3杂化,且是共价晶体,无分子,
+
C错误;NH4是正四面体结构,D错误。
9.【答案】(Ⅰ.(1)配位键 Fe3+提供空轨道,CN-提供孤对电子,形成配位键
(2)极性 O>N>C (3)sp3 乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢
键 (4)三角锥形 sp3
Ⅱ. (1)CD (2)+3 正四面体形 (3)CO、CS(其他合理答案也可)
2 2
第12页