文档内容
原子结构与元素周期表(1)
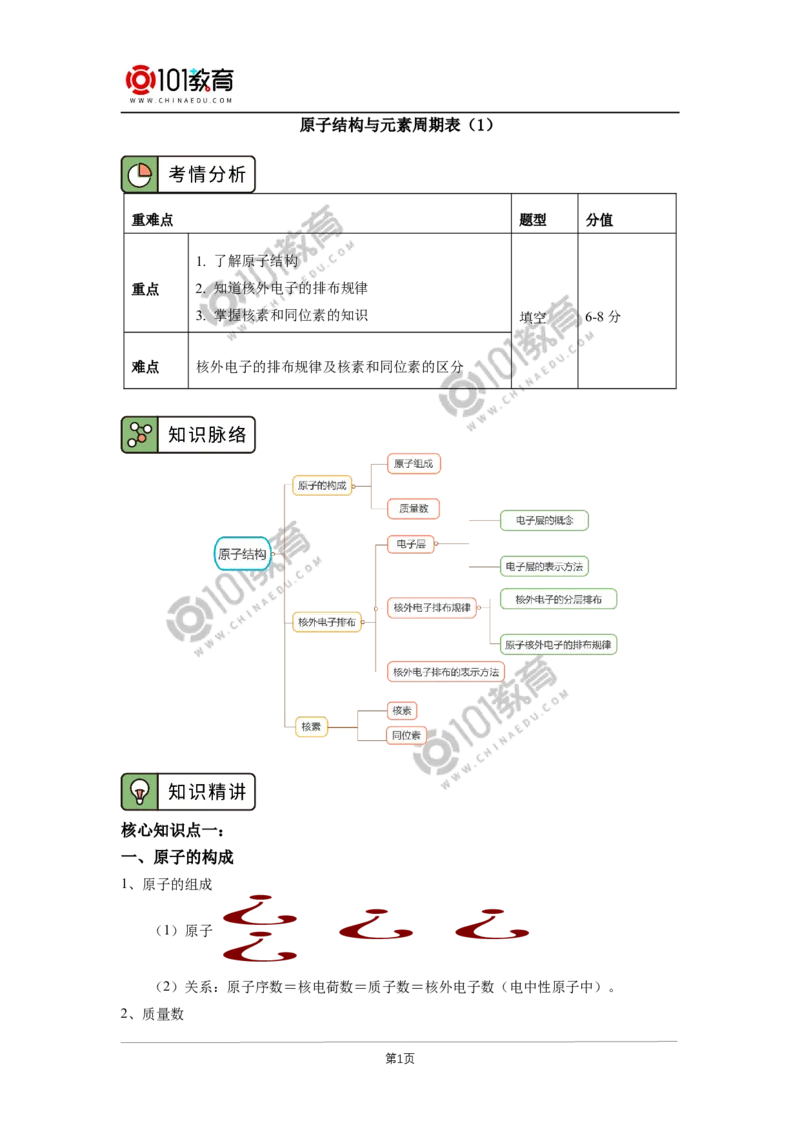
重难点 题型 分值
1. 了解原子结构
重点 2. 知道核外电子的排布规律
3. 掌握核素和同位素的知识 填空 6-8分
难点 核外电子的排布规律及核素和同位素的区分
核心知识点一:
一、原子的构成
1、原子的组成
¿
¿ ¿
(1)原子
¿
(2)关系:原子序数=核电荷数=质子数=核外电子数(电中性原子中)。
2、质量数
第1页(1)概念:质子和中子的相对质量都近似为1,忽略电子的质量,将原子核内所有质
子和中子的相对质量取近似整数值相加,所得的数值叫作质量数。
(2)关系:质量数(A)= 质子数( Z ) + 中子数( N ) 。
二、核外电子排布
1、电子层
(1)概念:在多电子原子里,把电子运动的能量不同的区域简化为不连续的壳层,称作
电子层。
(2)、电子层的表示方法
通常把能量最低、离核最近的电子层成为第一层;能量稍高、离核稍远的电子层称为第
2层;这样由内向外称为第1、2、3、4、5、6、7···层,或用符号依次表示为K、L、M、
N、O、P、Q···层。各电子层的表示符号及离核远近、能量高低关系可表示如下:
电子层数 1 2 3 4 5 6 7
字母代号 K L M N O P Q
各电子层由内到外
离核远近 由近到远
能量高低 由低到高
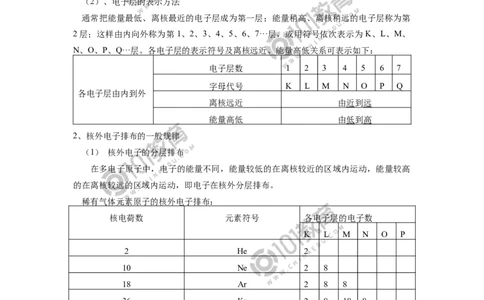
2、核外电子排布的一般规律
(1) 核外电子的分层排布
在多电子原子中,电子的能量不同,能量较低的在离核较近的区域内运动,能量较高
的在离核较远的区域内运动,即电子在核外分层排布。
稀有气体元素原子的核外电子排布:
核电荷数 元素符号 各电子层的电子数
K L M N O P
2 He 2
10 Ne 2 8
18 Ar 2 8 8
36 Kr 2 8 18 8
54 Xe 2 8 18 18 8
86 Rn 2 8 18 32 18 8
原子最外层有8个电子(最外层K层时,只有2个电子)的结构是相对比较稳定结构,
稀有气体在结构上满足这一条件。
(2)原子核外电子的排布规律
①能量规律
核外电子总是优先排布在能量最低的电子层里,然后再由里往外排布在能量逐步升高
第2页的电子层里,即按K→L→M→N……顺序排列。
②数量规律
Ⅰ、第n层最多容纳 2 n 2 个电子。如K、L、M、N层最多容纳电子数分别为 2 、 8 、
18 、 32 。
Ⅱ、最外层电子数目最多不能超过8 个(K层为最外层时不能超过2 个)。
Ⅲ、次外层最多能容纳的电子数不超过18 个。
3、核外电子排布的表示方法
(1)原子结构示意图,如下所示
(2)离子结构示意图
原子得到或失去一定数目的电子形成阴离子或阳离子,原子核不发生改变,只有核外
电子(一般是最外层电子)数目发生了改变。
原子结构示意图中,核内质子数等于核外电子数,而离子结构示意图中,二者则不相
等。如:
阳离子:核外电子数小于核电荷数。
阴离子:核外电子数大于核电荷数。
核心知识点二:
三、核素
1.原子构成及表示方法
(1)原子构成及表示方法:X,X表示元字符号,A表示原子的质量数,Z表示原子核内
的质子数为14,质子数为6,中子数为8的碳原子。
(2)构成
原子
2. 核素
把具有一定数目质子和一定数目中子的一种原子叫做核素。如12C、13C、14C就是碳元
素的三种不同核素。
第3页3. 同位素
(1)定义:质子数相同而中子数不同的同一元素的不同原子互称为同位素。即同一元
素的不同核素之间互为同位素,如三种核素均是氢元素的同位素。
(2)实例——氢元素的同位素:1H、2H、3H
氢元素的原子核 原子
原子名称
(
AX)
质子数(Z) 中子数(N) 符号 Z
1
1 0 氕 1H
2
1 1 氘 1H或D
3
1 2 氚 1H或T
(3)同位素的特征
①位置:因质子数相同,故元素符号相同,在元素周期表里占据同一位置,即同位。
②结构:质子数相同,中子数不同
③性质:同位素的原子核外电子层结构相同,因此化学性质几乎完全相同,因质量数
不同,物理性质略有差异
④存在:天然存在的同位素,相互间保持一定的比率。元素的相对原子质量,就是按
照该元素各种核素所占的一定百分比计算出来的平均值
(4)同位素的用途
14
① C在考古工作中用于测定文物的年代。
6
2 3
② H、 H用于制造氢弹。
1 1
③利用放射性同位素释放的射线育种、给金属探伤、诊断和治疗疾病等。
核心知识点一:
下列各原子结构示意图中所表示的核外电子排布正确的是( )
【答案】C
【解析】A项不符合能量最低原理,应该先排满K层再排L层;B项不符合各层最多
排2n2个电子,K层最多排2个电子;D项不符合最外层最多只能排8个电子。
【考点】原子核外电子的排布
第4页(1)A元素原子的核电荷数为8,其原子核内的质子数为______,该元素原子的二价
阴离子中,核外电子数为______。
(2)B元素原子的一价阳离子的核外有18个电子,质量数为40,该元素原子的原子
核内中子数为________。
【答案】(1)8 10 (2)21
【解析】(1)核电荷数=质子数,阴离子的核外电子数=质子数+所带电荷数=10。
(2)B元素质子数是18+1=19,质量数为40,该元素原子的中子数为40-19=21。
【考点】考查原子结构的基本知识
核心知识点二:
106
下列有关钯原子( Pd)的说法错误的是( )
46
A. 原子序数为46 B. 质子数为46
C. 电子数为46 D. 中子数为46
【答案】D
106
【解释】由 Pd可知,钯的原子序数为46,核外电子数=原子序数=质子数=46;
46
核内中子数为106-46=60,D选项错误。
【考点】考查原子结构知识点
6 14 23 24 7 14
2. 在 Li、 N、 Na、 Mg、 Li、 C中:
3 7 11 12 3 6
(1)________和________互为同位素。
(2)________和________质量数相等,但不能互称同位素。
(3)________和________的中子数相等,但质子数不相等,所以不是同一种元素。
6 7 14 14 23 24
【答案】(1) Li Li (2) N C (3) Na Mg
3 3 7 6 11 12
6 7
【解析】质子数相同,中子数不同的同一元素的不同原子互称为同位素,故 Li与 Li
3 3
14 14 23 24
互为同位素; N与 C质量数相等,但因质子数不同,不能互称同位素; Na和 Mg
7 6 11 12
的中子数均是12,但质子数不相等,所以不是同一种元素。
【考点】考查同位素相关知识
第5页(答题时间:25分钟)
一、选择题:本题包括12小题,每小题4分,共48分。
1. 下列叙述正确的是( )
A. 电子的能量越低,运动区域离核越远
B. 核外电子的分层排布即是核外电子的分层运动
C. 稀有气体元素原子的最外层都排有8个电子
D. 当M层是最外层时,最多可排布18个电子
2. 核电荷数小于或等于18的元素中,原子的最外层电子数是其余电子总数一半的元素
种类有( )
A. 1种 B. 2种 C. 3种 D. 4种
3. 下图微粒的结构示意图,正确的是( )
4. 简单原子的原子结构可用下图形象地表示:
其中 表示质子或电子, 表示中子,则下列有关①②③的叙述正确的
是 ( )
A. ①②③互为同素异形体
B. ①②③互为同位素
C. ①②③是三种化学性质不同的粒子
D. ①②③具有相同的质量数
5. 下列说法错误的是( )
1 2
A. H、 H、H+和H 是氢元素的四种不同粒子
1 1 2
40 42
B. Ca和 Ca、石墨和金刚石均为同素异形体
20 20
1 2
C. H和 H是不同的核素
1 1
12 14
D. C和 C互为同位素,物理性质不同,但化学性质几乎完全相同
20
6. Ne 是最早发现的 Ne 元素的稳定同位素,汤姆孙(J.J.Thomson)和阿斯通
10
22
(F.W.Aston)在1913年发现了 Ne。下列有关说法正确的是( )
10
22 20
A. Ne和 Ne是同素异形体
10 10
第6页22 20
B. Ne和 Ne属于不同的核素
10 10
22 20
C. Ne和 Ne的性质完全相同
10 10
22 20
D. Ne转变为 Ne为化学变化
10 10
7. (1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该
元素的原子结构示意图是________。
(2)已知某粒子的结构示意图为 ,试回答:
①当x-y=10时,该粒子为________(填“原子”“阳离子”或“阴离子”)。
②当y=8时,粒子可能为(填名称) ________、________、________、________、
________。
第7页1. B 解析:电子的能量越低,运动区域离核越近,A错误;氦最外层只有2个电子,C
错误;当M层是最外层时,最多可排布8个电子,D错误。
2. B 解析:在1号~18号元素中,符合题给要求的元素是Li和P。
3. A 解析:B中微粒结构示意图是 Cl-而不是Cl,C中Ar的原子结构示意图应为
,D中K的原子结构示意图应为 。
4. B 解析:由题图可知三个原子的质子数、核外电子数相同,而中子数不同,所以应
为同位素,同位素的化学性质相同。
5. B 解析:元素的存在形式有游离态和化合态两种,A项中的四种微粒是氢元素的四
1 2
种不同粒子,1H和1H是质子数均为1,中子数不等的不同的氢原子,它们是不同的核素;
40
12C和14C由于其质子数均为6,而中子数分别为6和8,故它们互为同位素,同理,20Ca
42
和20Ca互为同位素其物理性质不同但化学性质几乎完全相同;金刚石与石墨是由碳元素组
成的不同的单质,它们互为同素异形体。
22 20 22
6. B 解析: Ne和 Ne的质子数相同,中子数不同,互为同位素,A错误; Ne和
10 10 10
20 22 20
Ne的质子数相同,中子数不同,属于不同的核素,B正确; Ne和 Ne的化学性质完
10 10 10
22 20
全相同,物理性质不同,C错误; Ne 转变为 Ne中没有新物质生成,不是化学变化,
10 10
D错误。
7.(1) (2)①原子 ②氩原子 氯离子 硫离子 钾离子 钙离子
解析:(1)设:核电荷数=质子数=a,元素原子的电子层数为x,最外层电子数为
y,依题意:a=5x,a=3y,则5x=3y,x=3y/5。因原子的最外层电子数不超过8,即y为
1~8的正整数,故仅当y=5,x=3合理,该元素的核电荷数为15。
(2)①当x-y=10时,x=10+y,说明核电荷数等于核外电子数,所以该粒子应为
原子;②当y=8时,应有18个电子的粒子,所以可能为氩原子、氯离子、硫离子、钾离
子、钙离子。
第8页