化学反应平衡图像
重难点 题型 分值
1. 理解化学平衡常数定义、掌握化学平衡常数
的表达式的书写;
重点 2. 理解化学平衡常数和平衡移动原理的关系;
3. 理解化学平衡常数的应用和意义;
选择与填空 4-6分
4. 会应用化学平衡常数进行综合的计算
1. 理解化学平衡常数的应用和意义;
难点
2. 会应用化学平衡常数进行综合的计算
一、解答化学平衡图像题的一般步骤
任何类型的图像,分析时首先要明确纵坐标与横坐标代表的意义,观察图像中纵坐标
代表的量值随横坐标代表的量值的变化而变化的情况,然后与理论知识对照确定答案,具
第1页体步骤如下:
二、化学平衡图像的类型
类型1 “先拐先平数值大”原则的应用
1. 基本原理
同一可逆反应,若反应条件不同,达到平衡所用的时间也可能不同,反映到图像出现
“拐点”的时间也就有差异。
温度越高或压强越大,反应速率越快,达到平衡所用的时间越短,故当横坐标为时间
时,先出现拐点的曲线对应的体系先达到平衡状态。根据”温度一时间”曲线可以确定陌
生反应的吸、放热情况,根据“压强一时间”曲线可以确定陌生反应的反应前后气体分子
数的增减情况。
2. 温度和压强对平衡的影响
增大压强,平衡向气体分子数减小的方向移动;减小压强,平衡向气体分子数增大的
方向移动。
升高温度,平衡向吸热方向移动;降低温度,平衡向放热方向移动。
3. “先拐先平数值大”原则的应用举例
(1)对于可逆反应aA(g) bB(g)ΔH ,满足如下图像:
第2页分析:T 先出现拐点,故达到平衡所用的时间短,反应速率快,则T>T ;由T 到T
2 2 1 1 2
的过程为升温过程,温度升高,导致A的平衡转化率由x 减小为x ,平衡逆向移动,则逆
1 2
反应方向为吸热反应,故正反应为放热反应,ΔH <0。
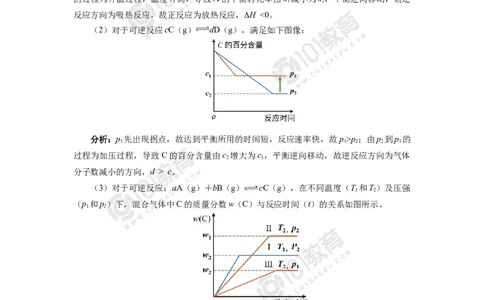
(2)对于可逆反应cC(g) dD(g),满足如下图像:
分析:p 先出现拐点,故达到平衡所用的时间短,反应速率快,故p>p;由p 到p 的
1 1 2 2 1
过程为加压过程,导致C的百分含量由c 增大为c ,平衡逆向移动,故逆反应方向为气体
2 1
分子数减小的方向,d > c。
(3)对于可逆反应:aA(g)+bB(g) cC(g),在不同温度(T 和T )及压强
1 2
(p 和p)下,混合气体中C的质量分数w(C)与反应时间(t)的关系如图所示。
1 2
分析:曲线Ⅰ先出现拐点,故达到平衡所用的时间短,所以曲线Ⅰ的反应速率快,曲
线Ⅰ、Ⅱ压强相同,那此时最先出现拐点的曲线的温度高,即 T>T ;曲线Ⅱ、Ⅲ (温度
1 2
相同时),最先出现拐点的压强大,即p>p。
2 1
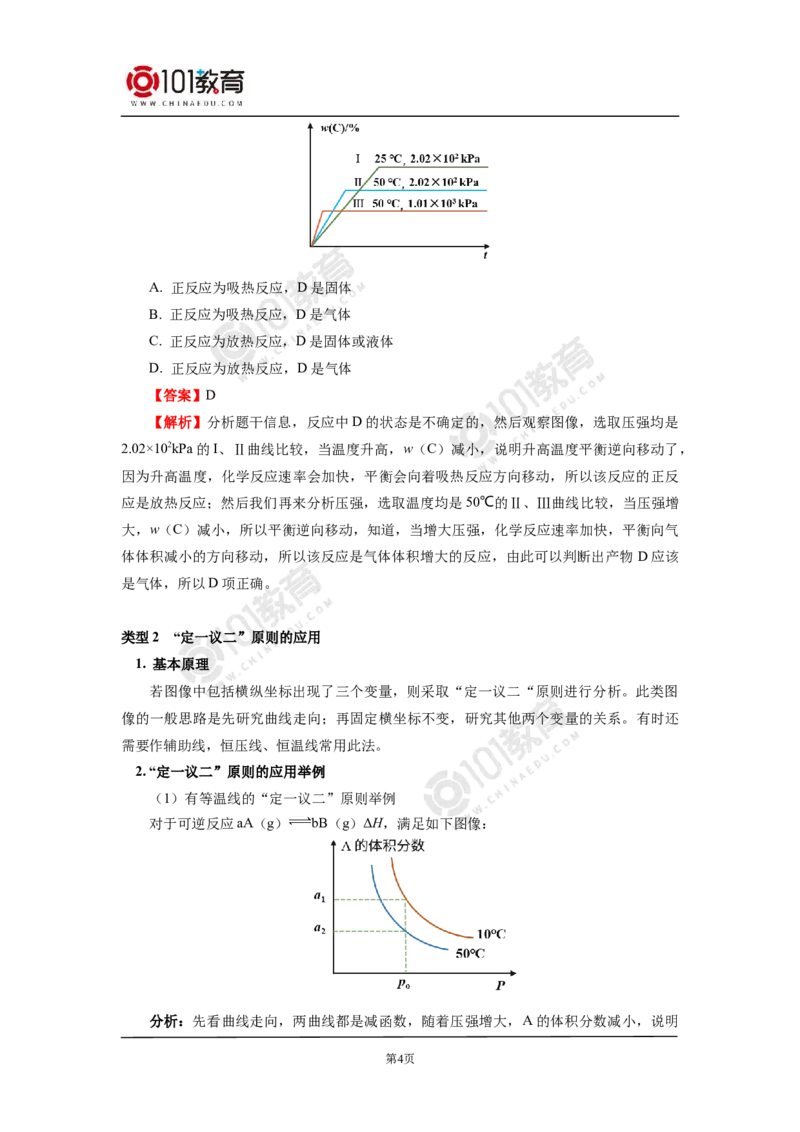
【即时练】在一密闭容器中进行如下反应:A(g) + B(g) 2C(g) + 2D (?) ,有如图所示
关系[其中 w(C) 是混合物中 C 的质量分数,t 为反应时间]。关于此反应的叙述正确的是
( )
第3页A. 正反应为吸热反应,D是固体
B. 正反应为吸热反应,D是气体
C. 正反应为放热反应,D是固体或液体
D. 正反应为放热反应,D是气体
【答案】D
【解析】分析题干信息,反应中D的状态是不确定的,然后观察图像,选取压强均是
2.02×102kPa的I、Ⅱ曲线比较,当温度升高,w(C)减小,说明升高温度平衡逆向移动了,
因为升高温度,化学反应速率会加快,平衡会向着吸热反应方向移动,所以该反应的正反
应是放热反应;然后我们再来分析压强,选取温度均是50℃的Ⅱ、Ⅲ曲线比较,当压强增
大,w(C)减小,所以平衡逆向移动,知道,当增大压强,化学反应速率加快,平衡向气
体体积减小的方向移动,所以该反应是气体体积增大的反应,由此可以判断出产物 D应该
是气体,所以D项正确。
类型2 “定一议二”原则的应用
1. 基本原理
若图像中包括横纵坐标出现了三个变量,则采取“定一议二“原则进行分析。此类图
像的一般思路是先研究曲线走向;再固定横坐标不变,研究其他两个变量的关系。有时还
需要作辅助线,恒压线、恒温线常用此法。
2. “定一议二”原则的应用举例
(1)有等温线的“定一议二”原则举例
对于可逆反应aA(g) bB(g)ΔH,满足如下图像:
分析:先看曲线走向,两曲线都是减函数,随着压强增大,A的体积分数减小,说明
第4页平衡正向移动,故正反应方向为气体分子数减小的方向,a>b;再固定某一个横坐标p 不
O
变,由10℃到50℃的过程是升温过程,温度升高,导致A的体积分数由α 减小为α ,升
1 2
温平衡正向移动,故正反应为吸热反应,ΔH>0。
(2)有等压线的“定一议二”原则举例
分析:先看曲线走向,两条曲线都是增函数,随着温度的升高,C的转化率增大,即
平衡正向移动,故正反应为吸热反应,ΔH>0;再固定某一个横坐标T 不变,由30kPa到
0
50kPa的过程是加压过程,导致C的转化率由c 减小为c ,平衡逆向移动,故逆反应方向
1 2
为气体分子数减小的方向,d>c。
【即时练】对于反应 m A(s) + n B(g) e C(g) + f D(g),当其他条件不变时,C 的百
分含量[ φ (C) ]和压强 (p) 的关系如图,下列叙述正确的是( )
A. 化学方程式中 n<e + f
B. 达到平衡后,若升温,v 减小,v 增大
正 逆
C. 达到平衡后,增加 B 的量,B 的转化率增大
D. 若 B 为有色物质,达到平衡后缩小容器容积,重新达平衡后与原平衡比较,气体
颜色变浅
【答案】C
【解析】选取一条温度曲线观察,发现随着压强增大,φ(C)逐渐增大,说明增大压
强,平衡正向移动,增大压强,化学平衡向气体体积减小的方向移动,可判断n>e+f,A项
错误;然后再固定压强不变,作垂线,我们发现升高温度,c的百分含量在减小,说明升
高温度,平衡向逆向移动,说明逆向是吸热反应,所以此反应是一个放热反应,然后我们
来看B选项,升高温度,正反应速率和逆反应速率应该均增大,所以 B项错误;因为A是
固体,所以增加B的量,相当于等比例的加入反应物,从等效平衡的角度考虑,加入反应
第5页物B后,相当于加压,增大压强平衡向气体体积减小的方句移动,即正向移动,B的转化
率增大,C项正确;若B为有色物质,达到平衡后缩小容器容积,反应体系压强会增大,
根据勒夏特列原理,增大压强,平衡会向正向移动,虽然平衡向正向移动,B的浓度在减
小,但是由于缩小了容器容积,新平衡中B的浓度还是比原平衡的大,所以气体颜色会加
深,D项错误。
例题1 已知:4NH (g)+5O (g) 4NO(g)+6H O(g) ΔH=-1 025 kJ/mol。
3 2 2
若反应起始物质的量相同,下列关于该反应的示意图不正确的是( )
【解题思路】先看拐点的高低,再分析平衡移动的方向。
【答案】C
【解析】该反应的正反应为放热反应,温度升高平衡逆向移动,NO的含量降低,故
A项正确,C项错误;该反应的正反应是气体体积增大的反应,压强减小平衡正向移动,
NO的含量增大,故B项正确;催化剂的使用只能改变反应速率,不能使平衡发生移动,
NO的含量不变,故D正确。
例题2 已知反应:2CHCOCH (l) CHCOCH COH(CH ) (l)。取等量
3 3 3 2 3 2
CHCOCH ,分别在0 ℃和20 ℃下,测得其转化分数随时间变化的关系曲线(Y-t)如下
3 3
图所示。下列说法正确的是( )
第6页A. b代表0 ℃下CHCOCH 的Y-t曲线
3 3
B. 反应进行到20 min末,CHCOCH 的 >1
3 3
C. 升高温度可缩短反应达平衡的时间并能提高平衡转化率
D. 从Y=0到Y=0. 113,CHCOCH COH(CH) 的 =1
3 2 3 2
【答案】D
【解析】A项,反应开始时b曲线所示化学反应速率快,达到平衡所需的时间短,所
以b代表20 ℃下CHCOCH 的Y-t曲线。B项,由题图可知,20 min末时CHCOCH 的
3 3 3 3
<1,所以CHCOCH 的 <1。C项,由题图可知,20 ℃时CHCOCH 的平
3 3 3 3
衡转化率一定小于0 ℃时的平衡转化率。D项,当Y=0. 113时,a曲线与b曲线相交,故
产物量相同。
例题3 在密闭容器中充入一定量NO ,发生反应2NO (g) NO (g) ΔH=
2 2 2 4
-57 kJ·mol-1。在温度为T 、T 时,平衡体系中NO 的体积分数随压强变化的曲线如图所
1 2 2
示。下列说法正确的是( )
A. a、c两点的反应速率:a>c
B. a、b两点NO 的转化率:a
0。如图所示为该反应正、
⇌
逆反应速率(v)与时间(t)的关系示意图,如果在t 时刻改变以下条件:①加入A;②加
1
入催化剂;③加压;④升温;⑤减少C。符合图示的是( )
A. ②③ B. ①② C. ③④ D. ④⑤
5. 往恒容密闭容器中通入一定量的NO ,发生反应NO (g) 2NO (g),随着温度
2 4 2 4 ⇌ 2
的升高,气体颜色变深。如图表示该反应平衡时有关物理量Y随某条件X(其他条件不
变)变化的规律。X、Y分别是( )
第9页A. 温度T,逆反应速率v
B. 温度T,气体的密度ρ
C. 压强p,平衡常数K
D. 压强p,NO 的转化率α
2 4
6. 在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应 C(s)+
2NO(g) CO (g)+N (g),平衡时c(NO)与温度t的关系如图所示,则下列说法
⇌ 2 2
正确的是( )
A. 该反应的ΔH>0
B. 若该反应在t、t ℃时的平衡常数分别为K 、K ,则K v
2 正 逆
D. 若状态B、C、D的压强分别为p(B)、p(C)、p(D),则p(C)=p(D)>p
(B)
7. 将1 mol CO和2 mol H 充入一容积为1 L的密闭容器中,分别在250 ℃、T ℃下发生
2
反应:CO(g)+2H(g) CHOH(g) ΔH=a kJ·mol-1,如右图所示。下列分析正确
2 ⇌ 3
的是( )
A. 250 ℃时,0~10 min内H 的平均反应速率为0. 015 mol·L-1·min-1
2
B. 平衡时CO的转化率:T ℃时小于250 ℃时
C. 其他条件不变,若减小容器体积,CO体积分数增大
D. a<0,平衡常数K:T ℃时大于250 ℃
二、非选择题
8. 298 K时,将20 mL 3x mol·L-1NaAsO 、20 mL 3x mol·L-1 I 和20 mL NaOH溶液混
3 3 2
第10页合,发生反应:AsO
3−
(aq)+I (aq)+2OH-(aq) AsO
3−
(aq)+2I-(aq)+HO
3 2 ⇌ 4 2
3−
(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
4
①下列可判断反应达到平衡的是________(填标号)。
3−
a. 溶液的pH不再变化 b. v(I-)=2v(AsO )
3
c(AsO3−)
4
c. 不再变化 d. c(I-)=y mol·L-1
c(AsO3−)
3
②t 时,v ________v (填“大于”“小于”或“等于”)。
m 正 逆
③t 时v ________t 时v (填“大于”“小于”或“等于”),理由是_____。
m 逆 n 逆
④若平衡时溶液的pH=14,则该反应的平衡常数K为________。
第11页一、选择题
1.【答案】A
【解析】A项正确,达平衡时,c(N )=c(O )=c mol·L-1,c(NO)=2(c -
2 2 1 0
c )mol·L-1;B项错误,因反应前后容器体积不变,且反应中无固态(或液态)物质参加
1
或生成,故混合气体的密度始终不变;C项错误,催化剂只能改变到达平衡的时间,不会
破坏平衡,即加入催化剂时氮气的平衡浓度不会改变;D项错误,对比曲线a和b到达平
衡所需时间,可知曲线b对应的条件改变是升高温度,达新平衡时c(N)减小,则平衡正
2
向移动,故该反应应为吸热反应,即ΔH>0。
2.【答案】C
【解析】依据题中图示,可看出T>T ,由T 时X的平衡浓度大于T 时X的平衡浓度,
1 2 1 2
可推出该反应为放热反应。M点与W点比较,X的转化量前者小于后者,故进行到M点
a−b
放出的热量应小于进行到W点放出的热量,A错误;2v(Y)=v(X)= mol·L-
t
1
1·min-1,B错误;T>T ,温度越高,反应速率越大,M点的正反应速率v 大于W点的正
1 2 正
反应速率v ′,而W点的正反应速率v ′等于其逆反应速率v ′大于N点的逆反应速
正 正 逆
率v ,C正确;恒容时充入X,压强增大,平衡正向移动,X的转化率增大,D错误。
逆
3.【答案】B
3×0.75mol⋅L−1
【解析】3 min时反应还没有平衡,A错误;v(H )=3v(CO )=
2 2 10min
=0. 225 mol·L-1·min-1,B正确;由于容器的体积没有变化,所以各成分的浓度没有变化,
化学反应速率不变,C错误;根据C项分析可知,平衡没有移动,CO 的转化率不变,D
2
错误。
4.【答案】A
【解析】由题图可知,在t 时刻改变条件使正、逆反应速率均增大且平衡不移动,符
1
合题意的只有加入催化剂和加压(此反应为气体体积不变的反应)。故选A。
5.【答案】D
【解析】升高温度,正、逆反应速率均增大,A错误;气体的总质量不变,容器体积
不变(恒容),则升高温度,气体的密度不变,B错误;平衡常数K仅受外界因素温度的
影响,故增大压强,K不变,C错误;增大压强,平衡向左移动,NO 的转化率降低,D
2 4
正确。
6.【答案】C
【解析】由图可知,温度越高平衡时c(NO)越大,即升高温度,平衡向逆反应方向
移动,所以正反应为放热反应,即ΔH<0,A错误;升温化学平衡常数减小,故K >K ,B
1 2
第12页错误;t 时反应处于状态D,c(NO)大于平衡浓度,故反应向正反应方向进行,则一定有
2
v >v ,C正确;达到平衡状态时,压强和温度成正比例关系,则 p(B)=p(D)v ;M点为刚达到平衡点(如图甲);M点后为平衡受温度的影响情况,即升温,
正 逆
A的百分含量增加或C的百分含量减少(如图乙),平衡左移,故正反应ΔH<0。
3. 不在曲线上的点的处理
在曲线上的点都处于平衡状态,v =v ,不在曲线上的点都在“奔向平衡的路上”,
正 逆
v ≠v 。若从正反应方向趋向平衡。则v >v ;若从逆反应方向趋向平衡,则v v ;则L线的右下方(F点),v <v 。
正 逆 正 逆
【即时练】
已知:2NO + O 2NO ΔH < 0 ,其他条件一定时,NO的转化率与温度的关系
2 2
第16页曲线如下,图中有 a、b、c、d 四点,其中表示未达平衡状态,且 v > v 的点是(
正 逆
)
A. a点 B. b点 C. c点 D. d点
【答案】C
【解析】A. a点在曲线上,处于平衡状态,v(正)= v(逆),故A错误;B、b点在
曲线上,处于平衡状态,v(正)= v(逆),故B错误;C. c点在曲线下方,未达到平衡
状态,欲达到同温度下的平衡状态,即由 c点向上引垂直线到曲线上的一点,则 NO的转
化率要增大,平衡向右移动,即v(正)>v(逆),所以C选项是正确的;D、d点在曲
线上方,未达到平衡状态,欲达到同温度下的平衡状态,即由 d点向下引垂线到曲线上的
一点,则NO的转化率要减小,平衡向左移动,即v(逆)>v(正),故D错误;所以C
选项是正确的。
例题1 下列叙述与对应的图相符的是( )
A. 图甲表示反应:4CO(g)+2NO (g) N (g)+4CO (g) ΔH<0, 在其他
2 2 2
条件不变时,改变起始物CO的物质的量对此反应平衡的影响,则有T0
2 4 2
【答案】A
【解析】A中反应的ΔH<0,升高温度,平衡逆向移动,平衡时 φ(N )减小,则有
2
Tv
M P
B. 平衡常数:K v
正 逆
【答案】D
【解析】A项,温度越高,反应速率越大,v < v ;B项,由题图可知,升温,c
M P
(I-)减小,所以平衡常数:K >K ;C项,M、N两点相比,M点温度低于N点温度,升
3 N P
温,平衡左移,所以M点的c(I-)小。
例题3 将燃煤废气中的 CO 转化为甲醚的反应原理为 2CO (g)+6H (g)
2 2 2
CHOCH (g)+3H O(g);已知在压强为a MPa下,该反应在不同温度、不同投料比时,
3 3 2
CO 的转化率如图:
2
第18页此反应____________(填“放热”或“吸热”);若温度不变,提高投料比[ n
(H)/n(CO)],则 K 将____________(填“增大”“减小”或“不变”)。
2 2
【答案】放热 不变
【解析】当投料比一定时,温度越高,CO 的转化率越低,所以升温平衡左移,正反
2
应为放热反应。平衡常数只与温度有关,不随投料比的变化而变化。
(答题时间:40分钟)
一、选择题
1. 一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合下图的是( )
A. CO (g)+2NH (g) CO(NH )(s)+HO(g) ΔH<0
2 3 2 2 2
B. CO(g)+H(g) CO(g)+HO(g) ΔH>0
2 2 2
C. CHCHOH(g) CH===CH (g)+HO(g) ΔH>0
3 2 2 2 2
D. 2C HCHCH(g)+O(g) 2C HCH===CH(g)+2HO(g) ΔH<0
6 5 2 3 2 6 5 2 2
2. 对于反应2A(g)+B(g) 2C(g) ΔH<0,下列图像正确的是( )
第19页3. 在某密闭容器中,可逆反应:A(g)+B(g) xC(g)符合图中(Ⅰ)所示
关系,φ(C)表示气体C在混合气体中的体积分数。由此判断,对图像(Ⅱ)说法不正确
的是( )
A. p>p,Y轴表示A的转化率
3 4
B. p>p,Y轴表示B的质量分数
3 4
C. p>p,Y轴表示B的转化率
3 4
D. p>p,Y轴表示混合气体的平均相对分子质量
3 4
二、非选择题
4. 能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应
用前景。工业上合成甲醇的反应为CO(g)+2H(g) CHOH(g) ΔH<0。
2 3
(1)在300 ℃,5 MPa条件下,将0. 20 mol的CO与0. 58 mol H 的混合气体充入2 L
2
密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示。
①列式计算300 ℃时该反应的平衡常数K=________。
②300 ℃时,将0. 50 mol CO、1. 00 mol H 和1. 00 mol CH OH充入容积为2 L的密闭
2 3
容器中,此时反应将________。
第20页A. 向正反应方向移动 B. 向逆反应方向移动
C. 处于平衡状态 D. 无法判断
③下列措施可提高甲醇产率的是________。
A. 压缩容器体积
B. 将CHOH(g)从体系中分离
3
C. 充入He,使体系总压强增大
D. 再充入0. 20 mol CO和0. 58 mol H
2
(2)若其他条件不变,使反应在500 ℃下进行,在图中作出甲醇的物质的量浓度随
时间的变化的示意图。
5. 已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ 700 800 830 1 000 1 200
平衡常数 1. 7 1. 1 1. 0 0. 6 0. 4
回答下列问题:
( 1 ) 该 反 应 的 平 衡 常 数 表 达 式 K = ________ , ΔH________
(填“<”、“>”或“=”)0。
(2)830 ℃时,向一个5 L的密闭容器中充入0. 20 mol A和0. 80 mol B,如反应初始
6 s内A的平均反应速率v(A)=0. 003 mol·L-1·s-1。则6 s时c(A)=________mol·L-
1,C 的物质的量为________mol;若反应经一段时间后,达到平衡时 A 的转化率为
________,如果这时向该密闭容器中再充入1 mol 氩气,平衡时A的转化率为________。
(3)判断该反应是否达到平衡的依据为________。
a. 压强不随时间改变
b. 气体的密度不随时间改变
c. c(A)不随时间改变
d. 单位时间里生成C和D的物质的量相等
(4)1 200 ℃时,反应C(g)+D(g) A(g)+B(g)的平衡常数的值为
________。
6. CH CO 催化重整不仅可以得到合成气(CO和H ),还对温室气体的减排具有重要意
4 2 2
义。回答下列问题:
(1)CHCO 催化重整反应为:CH(g)+CO(g)===2CO(g)+2H(g)。
4 2 4 2 2
已知:C(s)+2H(g)===CH (g) ΔH=-75 kJ·mol-1
2 4
C(s)+O(g)===CO (g)ΔH=-394 kJ·mol-1
2 2
1
C(s)+ O(g)===CO(g)ΔH=-111 kJ·mol-1
2 2
该催化重整反应的 ΔH=________kJ·mol-1。有利于提高 CH 平衡转化率的条件是
4
第21页________(填标号)。
A. 高温低压 B. 低温高压 C. 高温高压 D. 低温低压
某温度下,在体积为2 L的容器中加入2 mol CH 、1 mol CO 以及催化剂进行重整反应,
4 2
达到平衡时CO 的转化率是50%,其平衡常数为________mol2·L-2。
2
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。
相关数据如下表:
积碳反应 消碳反应
CH (g)=C(s)+2H (g) CO (g)+C(s)=2CO(g)
4 2 2
ΔH/(kJ⋅mol−1
) 75 172
活化能/ 催化剂X 33 91
(kJ⋅mol−1
) 催化剂Y 43 72
①由上表判断,催化剂X________Y(填“优于”或“劣于”),理由是
____________________________________。
在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的
变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率
(v)的叙述正确的是________(填标号)。
A. K 、K 均增加
积 消
B. v 减小,v 增加
积 消
C. K 减小,K 增加
积 消
D. v 增加的倍数比v 增加的倍数大
消 积
②在一定温度下,测得某催化剂上沉积碳的生成速率方程为 v=k·p(CH )·[p
4
(CO )]-0. 5(k为速率常数)。在p(CH )一定时,不同p(CO )下积碳量随时间的变
2 4 2
化趋势如下图所示,则 p (CO )、p (CO )、p (CO )从大到小的顺序为
a 2 b 2 c 2
________________。
第22页第23页1.【答案】A
【解析】四个选项中水蒸气均为生成物。依左图可知:T>T ,升温,水蒸气含量减
2 1
小,平衡左移,所以正反应为放热反应即ΔH<0,B、C错;依右图可知:p>p ,增压,水
1 2
蒸气含量增加,即正反应为气体体积减小的反应,A对,D错。
2.【答案】D
3.【答案】B
c(CH
3
OH)
0.02
4.【答案】(1)① = =4
c(CO)⋅c2 (H ) 0.8×0.25
2
②B ③A、B、D
(2)如图所示
【解析】(1)②向体系中加入0. 50 mol CO、1. 00 mol H 和1. 00 mol CH OH时,可
2 3
利用反应体系中浓度商和平衡常数的比较,判断平衡的移动方向;③压缩容器体积,压强
增大,平衡右移;将CHOH(g)从体系中分离是降低了生成物的浓度,平衡右移;恒容
3
充惰性气体,平衡不移动;再充入0. 20 mol CO和0. 58 mol H 相当于增大压强,平衡右
2
移。(2)升高温度,平衡向逆反应方向移动,甲醇的物质的量浓度减小,但温度升高,化
学反应速率加快。
c(C)⋅c(D)
5.【答案】(1) <
c(A)⋅c(B)
(2)0. 022 0. 09 80% 80%
(3)c (4)2. 5
【解析】(1)因反应中的物质都是气体,根据平衡常数的定义可知,K=
c(C)⋅c(D)
;由表中数据可知,温度升高,K值减小,故正反应为放热反应,ΔH<0。
c(A)⋅c(B)
(2)v(A)=0. 003 mol·L-1·s-1,则A减少的浓度c(A)=v(A)·t=0. 003 mol·L-
0.2mol
1·s-1×6 s=0. 018 mol·L-1,故剩余的A的浓度为 -0. 018 mol·L-1=0. 022 mol·L-
5L
1;A减少的物质的量为0. 018 mol·L-1×5 L=0. 09 mol,根据化学方程式中的化学计量关系
知,生成的C的物质的量为0. 09 mol。
设830 ℃达到化学平衡时,A的转化浓度为x mol·L-1,则
第24页A(g) + B(g) C(g)+ D(g)
起始浓度(mol·L-1) 0.04 0.16 0 0
转化浓度(mol·L-1) x x x x
平衡浓度(mol·L-1) 0.04-x 0.16-x x x
x⋅x
由 =1. 0,解得 x=0. 032,故 A 的转化率 α(A)=
(0.04−x)×(0.16−x)
0.032mol⋅L−1
×100%=80%;由于容器的容积是固定的,通入氩气后各组分的浓度不
0.04mol⋅L−1
变,反应速率不改变,化学平衡不移动。
(3)由于该反应是反应前后气体体积不变的反应,容器中压强、气体的密度都始终不
变,a、b项不符合题意;c(A)随反应的进行不再变化,c可以说明反应已达到平衡状
态;不论是否达到平衡状态,单位时间里生成C和D的物质的量都相等,d项不符合题
意。
(4)反应“C(g)+D(g) A(g)+B(g)”与“A(g)+B(g) C(g)
+D(g)”互为逆反应,平衡常数互为倒数关系,故1 200 ℃时,C(g)+D(g) A
1
(g)+B(g)的平衡常数K= =2. 5。
0.4
1
6. 【答案】(1)247 A (2)①劣于 相对于催化剂X,催化剂Y积碳反应的
3
活
化能大,积碳反应的速率小;而消碳反应活化能相对小,消碳反应速率大 AD
②p(CO)、p(CO)、p(CO)
c 2 b 2 a 2
【解析】 (1)已知:①C(s)+2H(g)===CH (g)
2 4
ΔH=-75 kJ·mol-1
②C(s)+O(g)===CO (g) ΔH=-394 kJ·mol-1
2 2
1
③C(s)+ O(g)===CO(g) ΔH=-111 kJ·mol-1
2 2
根据盖斯定律可知③×2-②-①即得到CHCO 催化重整反应CH (g)+CO (g)
4 2 4 2
===2CO(g)+2H (g)的ΔH=+247 kJ·mol-1。正反应是体积增大的吸热反应,所以有
2
利于提高CH 平衡转化率的条件是高温低压;某温度下,在体积为2 L 的容器中加入2 mol
4
CH 、1 mol CO 以及催化剂进行催化重整反应,达到平衡时CO 的转化率是50%,根据方
4 2 2
程式可知
CH(g)+CO(g)===2CO(g)+2H(g)
4 2 2
起始浓度(mol·L-1) 1 0. 5 0 0
转化浓度(mol·L-1) 0. 25 0. 25 0. 5 0. 5
第25页平衡浓度(mol·L-1) 0. 75 0. 25 0. 5 0. 5
0.52 ×0.52 1
所以平衡常数为 mol2·L-2= mol2·L-2。
0.75×0.25 3
(2)①根据表中数据可知相对于催化剂X,催化剂Y积碳反应的活化能大,积碳反应
的速率小;而消碳反应活化能相对小,消碳反应速率大,所以催化剂 X劣于Y。正反应均
是吸热反应,升高温度平衡向正反应方向进行,因此 K 、K 均增加,A正确,C错误;
积 消
升高温度反应速率均增大,B错误;积碳量达到最大值以后再升高温度积碳量降低,这说
明v 增加的倍数比v 增加的倍数大,D正确。
消 积
②根据反应速率方程式可知在p(CH )一定时,生成速率随p(CO )的升高而降低,
4 2
根据图像可知 p (CO )、p (CO )、p (CO )从大到小的顺序为 p (CO )、p
a 2 b 2 c 2 c 2 b
(CO)、p(CO)。
2 a 2
第26页