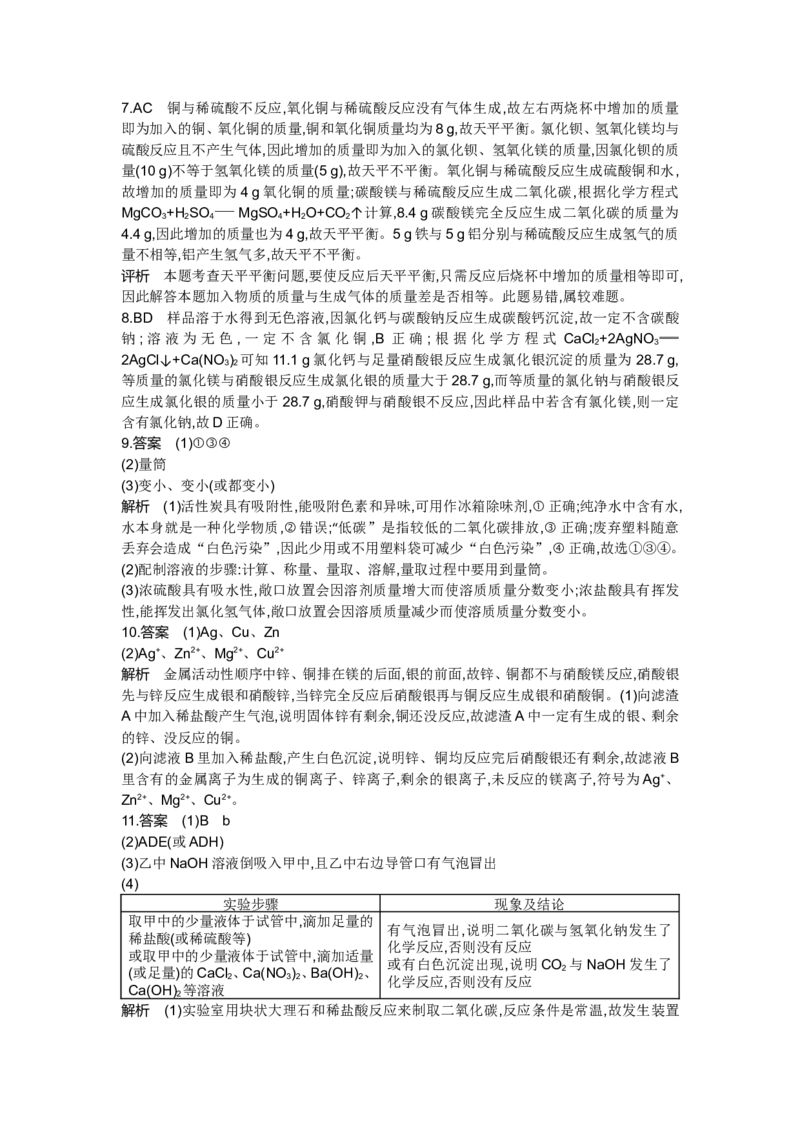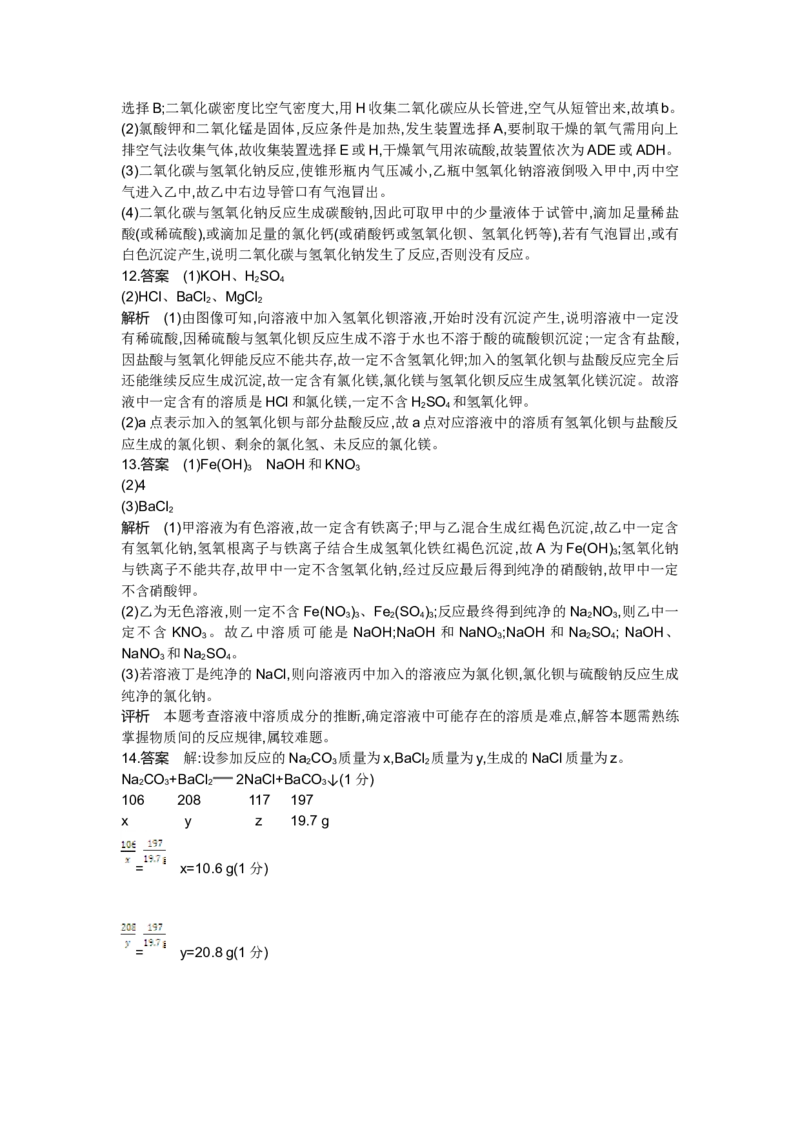文档内容
包头市 2014 年初中升学考试
化学试题(含答案全解全析)
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Mg—24 Al—27 S—32 Cl
—35.5 Ca—40 Fe—56 Cu—64 Ag—108 Ba—137
一、选择题(1~5题为单项选择题。6~8题为多项选择题,每小题有二个或三个选项符合题意,
全部选对得2分,选对但不全得1分。每题2分,共16分)
1.下列变化属于化学变化的是( )
A.干冰升华 B.葡萄酿酒
C.瓷碗破碎 D.自行车胎爆炸
2.下列按氧化物、化合物、混合物顺序排列的是( )
A.蒸馏水、碘酒、空气 B.二氧化锰、盐酸、小苏打
C.冰水混合物、熟石灰、医用酒精 D.水银、氧化铜、纯碱
3.下列说法正确的是( )
A.分子是保持物质性质的最小粒子
B.中和反应生成盐和水,有盐和水生成的反应一定是中和反应
C.任何不饱和溶液降低温度后,一定会变为饱和溶液
D.在化学反应aA+bB cC+dD(a、b、c、d为化学计量数)中,若A和B的质量都为m克,充
分反应后,生成C和D的质量总和不一定是2m克
4.下列有关物质的检验、除杂、鉴别、分离所用试剂或方法正确的是( )
选项 实验目的 所用试剂或方法
A 检验生石灰中是否含有杂质石灰石 水或稀盐酸
B 除去BaCl 溶液中的Ba(OH) 加适量的稀硫酸后过滤
2 2
C 鉴别NH Cl溶液和KCl溶液 NaOH溶液
4
D 分离C和CuO的固体混合物 加水溶解后过滤
5.下列各组溶液,不加其他试剂就能鉴别的是( )
A.K SO 、BaCl 、Na CO 、HCl B.HNO 、Na CO 、Ca(NO ) 、HCl
2 4 2 2 3 3 2 3 3 2
C.CuCl 、K SO 、NaNO 、NaOHD.AgNO 、KCl、NaCl、HNO
2 2 4 3 3 3
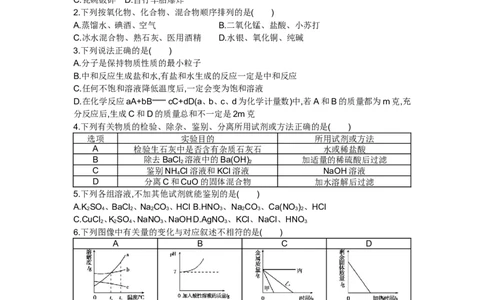
6.下列图像中有关量的变化与对应叙述不相符的是( )
A B C D
将a、b、c三种物质
向三份完全相同的
的饱和溶液分别由t
1 稀盐酸中分别加入
℃升温至t ℃时,所 向水中加入酸性溶 高温煅烧一定质量
2 甲、乙、丙三种金属,
得溶液中溶质质量 液 的石灰石
则金属活动性顺序
分 数 的 顺 序 为
为甲>乙>丙
a>b>c
7.天平两边各放质量相等的烧杯,分别盛有100克溶质质量分数为9.8%的稀硫酸,此时天平
平衡。若将下列各组的两种物质分别加入左右两烧杯中,充分反应后,天平仍平衡的是( )
A.铜8克,氧化铜8克 B.氯化钡溶液10克,氢氧化镁5克
C.氧化铜4克,碳酸镁8.4克 D.铁5克,铝5克
8.某CaCl 样品中,可能含有KNO 、CuCl 、MgCl 、NaCl和Na CO 中的某些物质,取该样品
2 3 2 2 2 311.1克溶于适量水中,得到澄清的无色溶液,然后向其中加入足量AgNO 溶液,得到28.7克
3
白色沉淀,则对该样品组成的下列推断中正确的是( )
A.只有MgCl ,没有NaCl B.肯定没有CuCl 和Na CO
2 2 2 3
C.肯定有MgCl 和KNO D.样品可能由CaCl 、NaCl、MgCl 组成
2 3 2 2
二、填空题(共5个小题,每空1分,共17分)
9.(1)有关生活常识的说法中正确的是 。(填序号)
①活性炭可用作冰箱除味剂 ②纯净水中不含任何化学物质 ③“低碳”是指较低的二氧
化碳排放 ④提倡购物时少用塑料袋或不用塑料袋,以减少“白色污染”。
(2)现有托盘天平、药匙、烧杯、玻璃棒、胶头滴管、试剂瓶,若要配制50克溶质质量分数为
6%的NaCl溶液,还需要的仪器是 。
(3)如果将浓硫酸、浓盐酸敞口放置在空气中一段时间后,它们的溶质质量分数分别将会
。
10.向硝酸银、硝酸镁的混合溶液中,加入一定量锌粉和铜粉的混合物,充分反应后过滤,得滤
渣A和滤液B。
(1)若向滤渣A中加入稀盐酸,有气泡冒出,则滤渣A中一定有 。
(2)若向滤液 B 里滴加稀盐酸,有白色沉淀产生,则滤液 B 里一定含有的金属离子是
。(填离子符号)
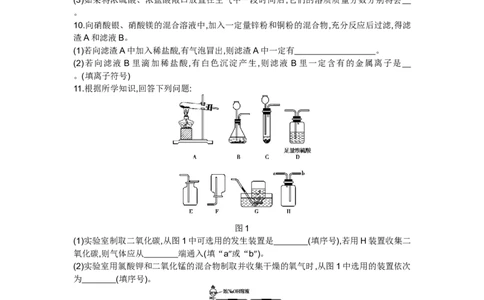
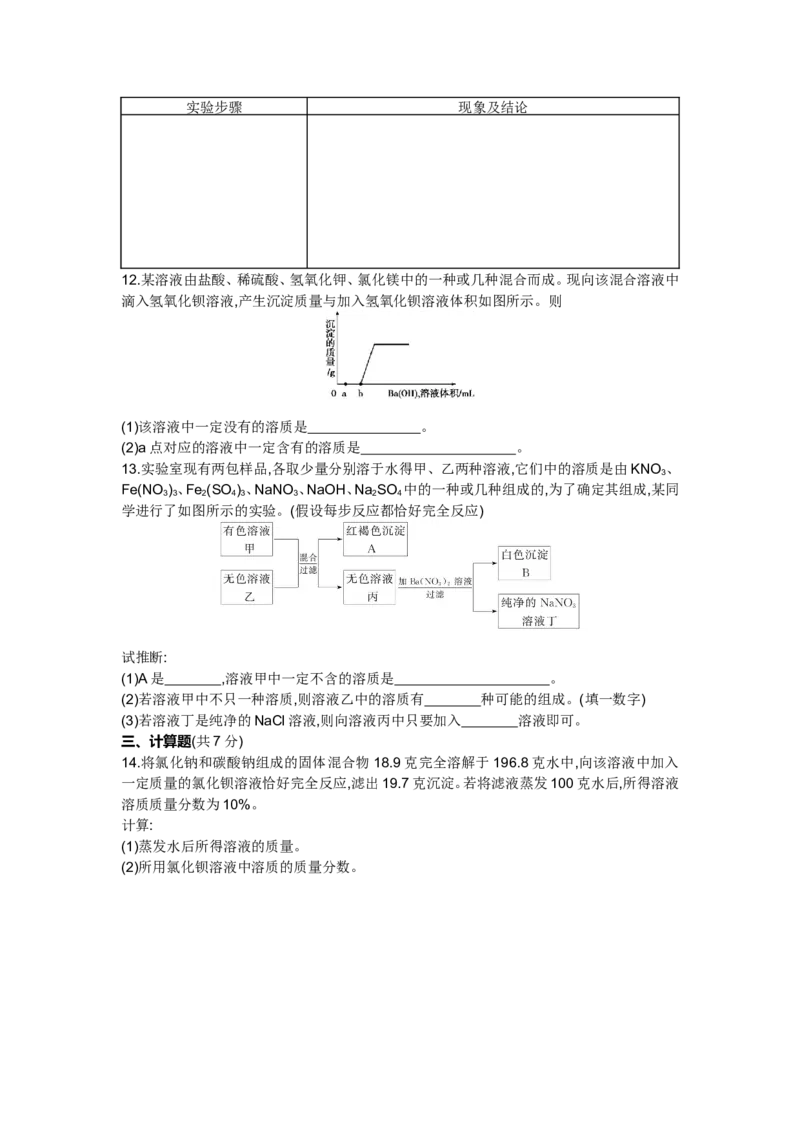
11.根据所学知识,回答下列问题:
图1
(1)实验室制取二氧化碳,从图1中可选用的发生装置是 (填序号),若用H装置收集二
氧化碳,则气体应从 端通入(填“a”或“b”)。
(2)实验室用氯酸钾和二氧化锰的混合物制取并收集干燥的氧气时,从图1中选用的装置依次
为 (填序号)。
图2
(3)为探究二氧化碳和氢氧化钠是否发生了化学反应,某同学设计了如图2所示实验,若该装
置气密性良好,将浓氢氧化钠溶液滴入锥形瓶中,可能观察到的实验现象为
。
(4)实验结束后,请你通过对锥形瓶内溶液中溶质组成的探究,来推测二氧化碳与氢氧化钠是
否发生了化学反应。实验步骤 现象及结论
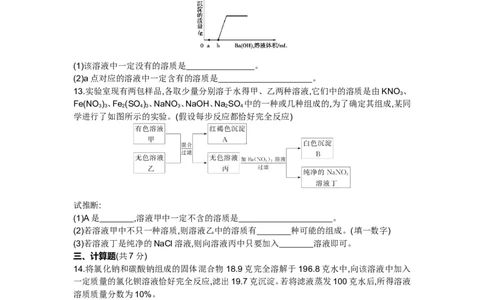
12.某溶液由盐酸、稀硫酸、氢氧化钾、氯化镁中的一种或几种混合而成。现向该混合溶液中
滴入氢氧化钡溶液,产生沉淀质量与加入氢氧化钡溶液体积如图所示。则
(1)该溶液中一定没有的溶质是 。
(2)a点对应的溶液中一定含有的溶质是 。
13.实验室现有两包样品,各取少量分别溶于水得甲、乙两种溶液,它们中的溶质是由KNO 、
3
Fe(NO ) 、Fe (SO ) 、NaNO 、NaOH、Na SO 中的一种或几种组成的,为了确定其组成,某同
3 3 2 4 3 3 2 4
学进行了如图所示的实验。(假设每步反应都恰好完全反应)
试推断:
(1)A是 ,溶液甲中一定不含的溶质是 。
(2)若溶液甲中不只一种溶质,则溶液乙中的溶质有 种可能的组成。(填一数字)
(3)若溶液丁是纯净的NaCl溶液,则向溶液丙中只要加入 溶液即可。
三、计算题(共7分)
14.将氯化钠和碳酸钠组成的固体混合物 18.9克完全溶解于196.8克水中,向该溶液中加入
一定质量的氯化钡溶液恰好完全反应,滤出19.7克沉淀。若将滤液蒸发100克水后,所得溶液
溶质质量分数为10%。
计算:
(1)蒸发水后所得溶液的质量。
(2)所用氯化钡溶液中溶质的质量分数。答案全解全析:
1.B 干冰升华时,二氧化碳由固态变为气态,没有生成新物质,是物理变化;葡萄酿酒过程中
生成了新物质酒精,是化学变化;瓷碗破碎只是形状发生改变,没有生成新物质,是物理变化,自
行车胎爆炸只是车胎的形状发生变化,没有生成新物质,是物理变化。故选B。
2.C A中碘酒中含有碘和酒精,是混合物,不符合题意。B中盐酸是氯化氢的水溶液,是混合
物,不符合题意。C中冰水混合物中只含一种物质水,水是氧化物;熟石灰是由多种元素组成的
纯净物,是化合物;医用酒精是酒精和水的混合物,C符合题意。D中水银是单质,不符合题意。
评析 本题考查物质的分类,明确物质的分类依据是解答此类题的关键,属中档题。
3.D 由分子构成的物质,分子是保持物质化学性质的最小粒子,物理性质不是由单个分子来
保持的,A错误;有盐和水生成的反应不一定是中和反应,如酸和金属氧化物的反应,中和反应
的反应物必须是酸和碱,B错误;氢氧化钙的溶解度随温度降低而增大,将不饱和石灰水降温
后仍为不饱和溶液,C错误;根据质量守恒定律,参加反应的各物质的质量总和等于生成的各
物质的质量总和,若A和B有一者剩余时,生成C和D的质量总和就小于2m g,故D正确。
4.C 生石灰与水反应生成微溶的氢氧化钙,用水不能检验生石灰中是否含有杂质石灰石,A
错误;氯化钡与稀硫酸反应生成硫酸钡沉淀,加入稀硫酸会除去原物质,故B错误;氯化铵与氢
氧化钠反应生成有刺激性气味的气体,而氯化钾与氢氧化钠不反应,故可以鉴别,C正确;碳和
氧化铜都不溶于水,用水不能分离,D错误。
[失分警示] 本题易错选B,认为稀硫酸与氢氧化钡反应生成硫酸钡和水,没有混入新杂质,忽
略了稀硫酸与原物质也反应。除杂质的题目要注意三个原则“不增、不减、易分离”。
5.A A项,四种无色溶液两两混合后观察现象,产生一种沉淀的是硫酸钾,两种沉淀的氯化钡,
一种沉淀和一种气体的是碳酸钠,一种气体的是盐酸,故A能鉴别出来;B中硝酸和盐酸都与
碳酸钠反应产生气体,现象相同,无法鉴别;C中氯化铜溶液呈蓝色,与氯化铜反应产生蓝色沉
淀的是氢氧化钠,而硫酸钾和硝酸钠与氯化铜和氢氧化钠都不反应,无法鉴别;D中氯化钾、氯
化钠都与硝酸银反应产生白色沉淀,现象相同,无法鉴别。
评析 本题考查溶液的鉴别,熟练掌握复分解反应发生的条件以及酸、碱、盐的化学性质是解
答本题的关键。解答本题一般有两种方法:一是观察借用,即利用观察法找出具有特殊颜色或
其他特殊性质的物质,借助这种物质来鉴别其他物质;二是组内溶液都是无色溶液时,可用两
两混合看现象的方法。
6.ABD t ℃时a、b的溶解度相等且大于c的溶解度,故t ℃时三种物质饱和溶液的溶质质
1 1
量分数的大小顺序是a=b>c,当升温至t ℃,a、b均变为不饱和溶液,但溶质质量分数不变;而
2
c由于溶解度随温度升高而减小,从而析出晶体,使c溶液的溶质质量分数变小,故t ℃时溶液
2
中溶质质量分数的大小顺序为a=b>c,A错误。向水中加入酸性溶液,溶液的pH应减小,B错
误。由图可知等质量的甲、乙与完全相同的稀盐酸完全反应时所用时间甲<乙,丙不反应,故三
种金属活动性顺序为甲>乙>丙,C正确。石灰石高温分解生成固体氧化钙,最终固体质量不可
能为0,故D错误。
评析 本题为图像题,属较难题,解答图像题首先要看横、纵坐标的含义,然后再看三点及变化
趋势,即“起始点、转折点、终点及曲线的走向”。7.AC 铜与稀硫酸不反应,氧化铜与稀硫酸反应没有气体生成,故左右两烧杯中增加的质量
即为加入的铜、氧化铜的质量,铜和氧化铜质量均为8 g,故天平平衡。氯化钡、氢氧化镁均与
硫酸反应且不产生气体,因此增加的质量即为加入的氯化钡、氢氧化镁的质量,因氯化钡的质
量(10 g)不等于氢氧化镁的质量(5 g),故天平不平衡。氧化铜与稀硫酸反应生成硫酸铜和水,
故增加的质量即为4 g氧化铜的质量;碳酸镁与稀硫酸反应生成二氧化碳,根据化学方程式
MgCO +H SO MgSO +H O+CO ↑计算,8.4 g碳酸镁完全反应生成二氧化碳的质量为
3 2 4 4 2 2
4.4 g,因此增加的质量也为4 g,故天平平衡。5 g铁与5 g铝分别与稀硫酸反应生成氢气的质
量不相等,铝产生氢气多,故天平不平衡。
评析 本题考查天平平衡问题,要使反应后天平平衡,只需反应后烧杯中增加的质量相等即可,
因此解答本题加入物质的质量与生成气体的质量差是否相等。此题易错,属较难题。
8.BD 样品溶于水得到无色溶液,因氯化钙与碳酸钠反应生成碳酸钙沉淀,故一定不含碳酸
钠;溶液为无色,一定不含氯化铜 ,B 正确;根据化学方程式 CaCl +2AgNO
2 3
2AgCl↓+Ca(NO ) 可知11.1 g氯化钙与足量硝酸银反应生成氯化银沉淀的质量为 28.7 g,
3 2
等质量的氯化镁与硝酸银反应生成氯化银的质量大于28.7 g,而等质量的氯化钠与硝酸银反
应生成氯化银的质量小于28.7 g,硝酸钾与硝酸银不反应,因此样品中若含有氯化镁,则一定
含有氯化钠,故D正确。
9.答案 (1)①③④
(2)量筒
(3)变小、变小(或都变小)
解析 (1)活性炭具有吸附性,能吸附色素和异味,可用作冰箱除味剂,①正确;纯净水中含有水,
水本身就是一种化学物质,②错误;“低碳”是指较低的二氧化碳排放,③正确;废弃塑料随意
丢弃会造成“白色污染”,因此少用或不用塑料袋可减少“白色污染”,④正确,故选①③④。
(2)配制溶液的步骤:计算、称量、量取、溶解,量取过程中要用到量筒。
(3)浓硫酸具有吸水性,敞口放置会因溶剂质量增大而使溶质质量分数变小;浓盐酸具有挥发
性,能挥发出氯化氢气体,敞口放置会因溶质质量减少而使溶质质量分数变小。
10.答案 (1)Ag、Cu、Zn
(2)Ag+、Zn2+、Mg2+、Cu2+
解析 金属活动性顺序中锌、铜排在镁的后面,银的前面,故锌、铜都不与硝酸镁反应,硝酸银
先与锌反应生成银和硝酸锌,当锌完全反应后硝酸银再与铜反应生成银和硝酸铜。(1)向滤渣
A中加入稀盐酸产生气泡,说明固体锌有剩余,铜还没反应,故滤渣A中一定有生成的银、剩余
的锌、没反应的铜。
(2)向滤液B里加入稀盐酸,产生白色沉淀,说明锌、铜均反应完后硝酸银还有剩余,故滤液B
里含有的金属离子为生成的铜离子、锌离子,剩余的银离子,未反应的镁离子,符号为Ag+、
Zn2+、Mg2+、Cu2+。
11.答案 (1)B b
(2)ADE(或ADH)
(3)乙中NaOH溶液倒吸入甲中,且乙中右边导管口有气泡冒出
(4)
实验步骤 现象及结论
取甲中的少量液体于试管中,滴加足量的
有气泡冒出,说明二氧化碳与氢氧化钠发生了
稀盐酸(或稀硫酸等)
化学反应,否则没有反应
或取甲中的少量液体于试管中,滴加适量
或有白色沉淀出现,说明CO 与NaOH发生了
(或足量)的CaCl 、Ca(NO ) 、Ba(OH) 、 2
2 3 2 2 化学反应,否则没有反应
Ca(OH) 等溶液
2
解析 (1)实验室用块状大理石和稀盐酸反应来制取二氧化碳,反应条件是常温,故发生装置选择B;二氧化碳密度比空气密度大,用H收集二氧化碳应从长管进,空气从短管出来,故填b。
(2)氯酸钾和二氧化锰是固体,反应条件是加热,发生装置选择A,要制取干燥的氧气需用向上
排空气法收集气体,故收集装置选择E或H,干燥氧气用浓硫酸,故装置依次为ADE或ADH。
(3)二氧化碳与氢氧化钠反应,使锥形瓶内气压减小,乙瓶中氢氧化钠溶液倒吸入甲中,丙中空
气进入乙中,故乙中右边导管口有气泡冒出。
(4)二氧化碳与氢氧化钠反应生成碳酸钠,因此可取甲中的少量液体于试管中,滴加足量稀盐
酸(或稀硫酸),或滴加足量的氯化钙(或硝酸钙或氢氧化钡、氢氧化钙等),若有气泡冒出,或有
白色沉淀产生,说明二氧化碳与氢氧化钠发生了反应,否则没有反应。
12.答案 (1)KOH、H SO
2 4
(2)HCl、BaCl 、MgCl
2 2
解析 (1)由图像可知,向溶液中加入氢氧化钡溶液,开始时没有沉淀产生,说明溶液中一定没
有稀硫酸,因稀硫酸与氢氧化钡反应生成不溶于水也不溶于酸的硫酸钡沉淀;一定含有盐酸,
因盐酸与氢氧化钾能反应不能共存,故一定不含氢氧化钾;加入的氢氧化钡与盐酸反应完全后
还能继续反应生成沉淀,故一定含有氯化镁,氯化镁与氢氧化钡反应生成氢氧化镁沉淀。故溶
液中一定含有的溶质是HCl和氯化镁,一定不含H SO 和氢氧化钾。
2 4
(2)a点表示加入的氢氧化钡与部分盐酸反应,故a点对应溶液中的溶质有氢氧化钡与盐酸反
应生成的氯化钡、剩余的氯化氢、未反应的氯化镁。
13.答案 (1)Fe(OH) NaOH和KNO
3 3
(2)4
(3)BaCl
2
解析 (1)甲溶液为有色溶液,故一定含有铁离子;甲与乙混合生成红褐色沉淀,故乙中一定含
有氢氧化钠,氢氧根离子与铁离子结合生成氢氧化铁红褐色沉淀,故A为Fe(OH) ;氢氧化钠
3
与铁离子不能共存,故甲中一定不含氢氧化钠,经过反应最后得到纯净的硝酸钠,故甲中一定
不含硝酸钾。
(2)乙为无色溶液,则一定不含Fe(NO ) 、Fe (SO ) ;反应最终得到纯净的Na NO ,则乙中一
3 3 2 4 3 2 3
定不含 KNO 。故乙中溶质可能是 NaOH;NaOH 和 NaNO ;NaOH 和 Na SO ; NaOH、
3 3 2 4
NaNO 和Na SO 。
3 2 4
(3)若溶液丁是纯净的NaCl,则向溶液丙中加入的溶液应为氯化钡,氯化钡与硫酸钠反应生成
纯净的氯化钠。
评析 本题考查溶液中溶质成分的推断,确定溶液中可能存在的溶质是难点,解答本题需熟练
掌握物质间的反应规律,属较难题。
14.答案 解:设参加反应的Na CO 质量为x,BaCl 质量为y,生成的NaCl质量为z。
2 3 2
Na CO +BaCl 2NaCl+BaCO ↓(1分)
2 3 2 3
106 208 117 197
x y z 19.7 g
= x=10.6 g(1分)
= y=20.8 g(1分)= z=11.7 g(1分)
(1)蒸发水后NaCl溶液质量 = =200 g(1分)
(2)BaCl 溶液质量 200 g+100 g+19.7 g-18.9 g-196.8 g=104 g(1分)
2
或BaCl 溶液质量 20.8 g+(200 g+100 g-20 g-196.8 g)=104 g
2
所用BaCl 溶液中溶质质量分数 ×100%=20%(1分)
2
答:(略)
其他合理答案参照给分
解析 (1)碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,反应后滤液为氯化钠溶液,溶质为
氯化钠,根据化学方程式中碳酸钡的质量可求出生成的氯化钠质量、混合物中碳酸钠的质量,
则原混合物中氯化钠的质量为样品总质量减去碳酸钠质量,则蒸发水后所得溶液中溶质
NaCl的质量为生成的氯化钠与原混合物中NaCl的质量和,根据蒸发掉100 g水后得到的氯
化钠溶液中溶质的质量分数可求出溶液的质量。(2)根据质量守恒定律可知,18.9 g+196.8
g+氯化钡溶液的质量=19.7 g+100 g+蒸发水后氯化钠溶液的质量,由此可求出氯化钡溶液的
质量,根据溶质质量分数的计算公式可求出氯化钡溶液中溶质的质量分数。
评析 本题考查化学方程式与溶质质量分数的综合计算,题目中未知量较多,属较难题。