文档内容
1.1.2 热化学方程式(分层作业)
【基础检测题】
一、单选题(共0分)
1.在298K、101kPa下,将13.2gCO 通入400mL1mol/LKOH溶液中充分反应(不考虑气体逸出),测得反应放出
2
akJ的热量,已知该条件下,将0.5molCO 通入1L1mol/LKOH溶液中充分反应放出bkJ的热量。则下列表示
2
CO 与KOH溶液反应生成KHCO 溶液的热化学方程式书写正确的是
2 3
A.CO(g)+KOH(aq)=KHCO (aq) ΔH= -(10a-b)kJ•mol-1
2 3
B.CO(g)+KOH(aq)=KHCO (aq) ΔH= -(10b-2a)kJ•mol-1
2 3
C.CO(g)+KOH(aq)=KHCO (aq) ΔH= -(5a-b)kJ•mol-1
2 3
D.CO(g)+KOH(aq)=KHCO (aq) ΔH= -(10a-2b)kJ•mol-1
2 3
2.标准状况下将1L纯净的 在空气中完全燃烧,生成 和液态水,放出39.75kJ热量,则燃烧的热化学
方程式为
A.
B.
C.
D.
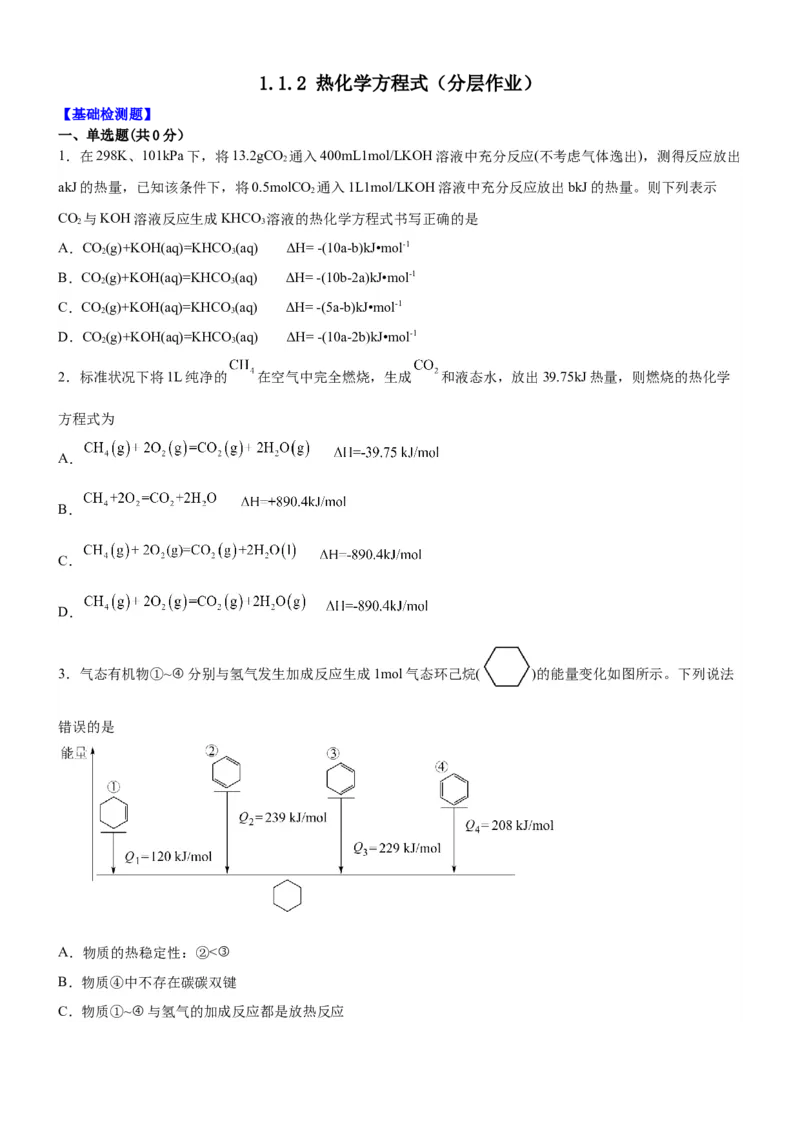
3.气态有机物①~④分别与氢气发生加成反应生成1mol气态环己烷( )的能量变化如图所示。下列说法
错误的是
A.物质的热稳定性:②<③
B.物质④中不存在碳碳双键
C.物质①~④与氢气的加成反应都是放热反应D.物质③脱氢生成④的热化学方程式为: (g) (g)+H(g)-21kJ
2
4.25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
A.2H(g)+O(g) = 2HO(1) △H=-285.8kJ/mol
2 2 2
B.2H(g)+ O (g) = 2HO(1) △H=+571.6 kJ/mol
2 2 2
C.2H(g)+O(g) = 2HO(g) △H= -571.6 kJ/mol
2 2 2
D.H(g)+ O(g) = HO(1) △H=-285.8kJ/mol
2 2 2
5.已知298K时,合成氨反应:2SO (g)+O(g) 2SO (g)△H=-196.6kJ/mol,将此温度下的2molSO 和1molO
2 2 3 2 2
放在一密闭容器中,在催化剂存在时进行反应,达到平衡时,反应放出的热量为(忽略能量损失)
A.一定大于196.6kJ B.一定小于196.6kJ
C.一定等于196.6kJ D.不能确定
6.已知高炉炼铁时发生反应Fe O(s)+3CO(g)=2Fe(s)+3CO (g)△H=-24.6kJ•mo1-1,则消耗84g CO 时,上述反应
2 3 2
的能量变化为
A.吸收8.2kJ能量 B.放出8.2kJ能量
C.吸收24.6kJ能量 D.放出24.6kJ能量
7.CO(g)与HO(g)反应过程的能量变化如图所示,有关两者反应的说法正确的是
2
A.该反应为吸热反应
B.CO(g)和HO(g)所具有的总能量大于CO(g)和H(g)具有的总能量
2 2 2
C.反应的热化学方程式为CO(g)+HO(g)=CO(g)+H(g) ΔH=+41kJ/mol
2 2 2
D.1molCO (g)和1molH (g)反应生成1molCO(g)和1molHH O(g)要放出41kJ的热量
2 2 2
8.已知:①H+(aq)+OH-(aq)=H O(1) △H;②N(g)+3H(g)⇌2NH (g) △H。其他条件不变时,增加反应物的量,
2 1 2 2 3 2
下列判断正确的是
A.△H、△H 都不变 B.△H、△H 都增大
1 2 1 2
C.△H、△H 都减小 D.△H 减小,△H 增大
1 2 1 2
9.依据事实写出下列反应的热化学方程式。
(1)在25 ℃、101 下,1 乙醇燃烧生成 和液态水时放热 。则表示乙醇燃烧热的热化学方程式为_______。
(2)若适量的 和 完全反应,每生成23 需要吸收 热量,则表示 和 反应生成 的热化学
方程式为_______。
10.完成下列问题。
(1)如图 和CO(g)反应生成 和NO(g)过程中能量变化图,该反应物的总焓___________生成物的焓
(填“小于”或“大于”)。请写出 和CO反应的热化学方程式___________;
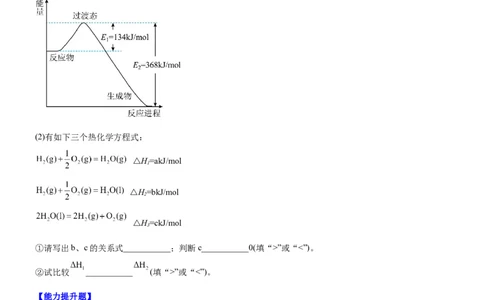
(2)有如下三个热化学方程式:
△H=akJ/mol
1
△H=bkJ/mol
2
△H=ckJ/mol
3
①请写出b、c的关系式___________;判断c___________0(填“>”或“<”)。
②试比较 ___________ (填“>”或“<”)。
【能力提升题】
11.图象可更直观地表现化学变化中的物质变化和能量变化。下列判断错误的是A.图甲所示反应为放热反应,且 H=Ea-
△
B.若已知石墨比金刚石稳定,则C(石墨,s)=C(金刚石,s)
C.图乙所示反应的热化学方程式为:
D.若 ,则物质能量高低如图丙
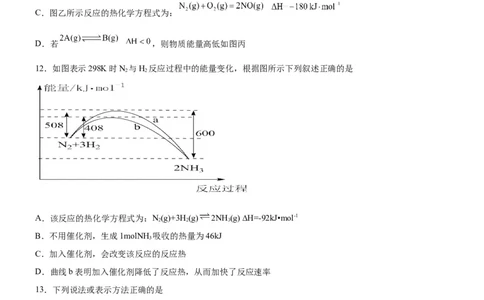
12.如图表示298K时N 与H 反应过程中的能量变化,根据图所示下列叙述正确的是
2 2
A.该反应的热化学方程式为:N(g)+3H(g) 2NH (g) ∆H=-92kJ•mol-1
2 2 3
B.不用催化剂,生成1molNH 吸收的热量为46kJ
3
C.加入催化剂,会改变该反应的反应热
D.曲线b表明加入催化剂降低了反应热,从而加快了反应速率
13.下列说法或表示方法正确的是
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(s,石墨)=C(s,金刚石)ΔH=+1.90kJ·mol-1可知金刚石比石墨坚硬
C.在101kPa时,2gH 完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H(g)
2 2
+O (g)=2HO(l) ΔH=-285.8kJ·mol-1
2 2
D.在稀溶液中,H+(aq)+OH-(aq)=H O(l) ΔH=-57.3kJ·mol-1,若将含0.5molHSO 的浓硫酸与含1molNaOH的溶
2 2 4
液混合,放出的热量大于57.3kJ
14.下列热化学方程式正确的是
A.已知1 g甲烷燃烧生成二氧化碳和液态水放出的热量为55.625 kJ:kJ⋅mol-1
B.12g碳与适量水蒸气反应生成一氧化碳和氢气,需吸收120 kJ的热量:
kJ⋅mol-1
C.通常状况下,将1g氢气在氯气中完全燃烧,放出92.4 kJ热量:
kJ⋅mol-1
D.已知充分燃烧a g乙炔气体生成1 mol二氧化碳气体和液态水,放出b kJ热量:
kJ⋅mol-1
15.在25℃和101kPa,8g 燃烧生成液态水放出445kJ的热量,则下列热化学方程式中书写正确的是
A.
B.
C.
D.
16.下列热化学方程式及有关应用的叙述中,正确的是
A.已知25℃、101kPa条件下: ,
,则 比 稳定
B.已知强酸与强碱在稀溶液里反应的中和热为 ,则
C.2mol 分解生成1mol 和2molNO,并吸收116.2kJ热量,其热化学方程式为
D. 的燃烧热为 ,则 燃烧的热化学方程式可表示为:17.在25℃和101kPa下,2gH 燃烧生成液态水放出285.8kJ的热量,则下列热化学方程式中书写正确的是
2
A.2H(g)+O(g)=2HO(l) ΔH=-142.9kJ/mol B.H(g)+ O(g)=HO(l) ΔH=-285.8kJ/mol
2 2 2 2 2 2
C.2H(g)+O(g)=2HO(g) ΔH=-571.6kJ/mol D.H(g)+ O(g)=2HO(l) ΔH=+285.8kJ/mol
2 2 2 2 2 2
18.化学反应不仅有物质的变化还伴随能量的变化,下列说法错误的是
A.已知 ,则其逆反应的 一定大于0
B.热化学方程式和化学方程式的化学计量数的意义不完全相同
C.常温常压下, 完全燃烧比 完全燃烧时的焓变大
D. ,则
19.回答下列问题:
(1)火箭发射时可用肼( ,液态)作燃料,液态肼与 反应生成 和水蒸气。有关该反应的能量变化曲线如
图所示,写出该反应的热化学方程式:_______。
(2)液态肼可与氧化剂 反应生成 和水蒸气。已知:
①
②
③
写出液态肼和 反应生成 和水蒸气的热化学方程式:_______。
20.已知红磷和Cl 发生反应生成PCl 或PCl ,反应过程中的能量变化如图所示(图中 H表示生成1mol产物的
2 3 5
数据)。 △(1)P和Cl 反应生成PCl (g)的热化学方程式为______。
2 3
(2)PCl (g)分解生成PCl (g)和Cl 的热化学方程式为______。
5 3 2
(3)白磷能自燃,红磷不能自燃。白磷转变成红磷是______(“放”或“吸”)热反应,如果用白磷代替红磷和Cl
2
反应生成1molPCl 的反应热为 H,则 H______ H(填“>”、“<”或“=”)。
5 3 3 1
(4)工业上制备PCl
5
通常分两步△进行,先△将P和Cl
2
反△应生成中间产物PCl
3
,然后降温,再和Cl
2
反应生成PCl
5
,
其原因是______。
【拔尖训练题】
21.将一块擦去氧化膜的铝片放入20mL0.5mol•L-1CuSO 溶液中,观察到实验现象为:铝表面有红色物质析出,
4
同时有少量气泡,铝片上下翻滚,溶液中出现黑色物质。下列方程式不正确的是
A.Cu2+(aq)+2H O(l) Cu(OH) (s)+2H+(aq) H>0
2 2
△
B.2Al(s)+3Cu2+(aq)=2Al3+(aq)+3Cu(s) H<0
△
C.Cu(OH) (s) CuO(s)+H O(l) H>0
2 2
△
D.2Al(s)+6H+(aq)=2Al3+(aq)+3H (g) H<0
2
22.下列说法正确的是 △
A.由 ,可知:金刚石比石墨更稳定
B.吸热反应: ,设 和 不随温度而变,则该反应任何温度下都不能自发进行
C.由 ,可知:含1mol 的溶液与含1mol 的溶液混合,放出热量等于
D.2g 完全燃烧生成液态水放出 热量,则氢气燃烧的热化学方程式为
23.H 和I 在一定条件下能发生反应:H(g)+I (g) 2HI(g),1molH 完全反应放出akJ热量.已知:
2 2 2 2 2
(a、b、c均大于零)
下列说法不正确的是
A.反应物的总能量高于生成物的总能量
B.断开 键和 键所需能量大于断开 键所需能量
C.断开 键所需能量约为
D.向密闭容器中加入 和 ,充分反应放出的热量小于
24.有关热化学方程式书写与对应表述正确的是
A.稀醋酸与 溶液反应:
B.在101kPa下 的燃烧热为 ,则水分解的热化学方程式:
C.已知 的燃烧热为 ,则有
D.已知9.6g硫粉与11.2g铁粉混合加热生成 时放出19.12kJ热量,则
25.应用过渡状态理论讨论化学反应时,可将反应过程中体系的势能变化情况表示在反应历程一势能图上。甲
烷在光照条件下发生的氯代反应历程如图所示。下列说法错误的是(1)Cl-Cl→2Cl·
(2)Cl·+CH -H→CH ·+H-Cl
3 3
(3)CH ·+Cl-Cl→CH -C1+C1·
3 3
A.反应Cl·+CH -H→CH ·+H-Cl △H=+7.5kJ·mol-1
3 3
B.反应Cl·+CH -H→CH ·+H-Cl的活化能E=+16.7kJ·mol-1
3 3 a
C.反应(2)比反应(3)更容易进行
D.CH(g)+Cl (g)=CH Cl(g)+HCl(g) H=-105.4kJ·mol-1
4 2 3
26.下列离子方程式或化学反应方程△式与所述事实相符且正确的是
A.将 气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:
B.将少量 气体通入NaClO溶液中:
C. 溶液中加入 溶液使 完全沉淀:
D.向含有 的溶液中通入 充分反应:
27.电石气是一种常见燃料,C H(g) + 5/2 O (g) = 2CO(g) + HO(l) ΔH 有关化学反应的能量变化如右图所示,
2 2 2 2 2
已知断裂1mol化学键所需的能量(kJ):O=O为500、C-H为410,则断裂1molC≡C 键所需的能量(kJ)是A.840 B.1590 C.900 D.1250
28.下列说法或表示法正确的是
A.化学反应必须发生有效碰撞,但有效碰撞不一定发生化学反应
B.由C(s,石墨)=C(s,金刚石);ΔH = +1.19 kJ· mol—1可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)= H O(l);ΔH=-57.3 kJ· mol—1,若将0.5 mol/L 的HSO 溶液与1
2 2 4
mol/L的 NaOH溶液等体积混合,放出的热量等于57.3 kJ
D.乙醇的燃烧热ΔH= -1366.8 kJ· mol—1,则在25℃、101kPa时,1kg乙醇充分燃烧后放出2.971×104kJ热量
29.I.完成下列问题。
(1) 的盐酸与 的 溶液在如下图所示的装置中进行中和反应。烧杯间填满碎
泡沫塑料的作用是___________。大烧杯上如不盖硬纸板,则求得的中和热数值___________(填“偏大”、“偏
小”或“无影响”)。
(2)向 的 溶液中分别加入稍过量的稀醋酸、稀盐酸、浓硫酸,则完全反应时的放出热量
从大到小的排序是___________。
(3)已知 ; 。现有下列反应
① ;
② ;
③ ;④ ;
⑤
其中反应热符合 的是___________(写序号)
Ⅱ.以 为催化剂的光热化学循环分解 (生成一氧化碳和氧气)反应为温室气体减排提供了一个新途径,
该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
(4)上述过程中,能量的变化形式是由___________转化为___________,上述过程的的热化学方程式为
___________。
30.回答下列问题
(1)已知C(s,石墨)=C(s,金刚石) △H>0,则稳定性:金刚石____石墨(填“>”、“=”或“<”)
(2)已知:2C(s) +2O (g)=2CO (g) △H 2C(s) +O (g)=2CO(g) △H
2 2 1 2 2
则 △H________△H (填“>”、“=”或“<”)
1 2
(3)“嫦娥五号”已于2020年11月24日在海南文昌发射中心成功发射。火箭的第一、二级发动机所用的燃料为
偏二甲肼和四氧化二氮,其中偏二甲肼可与肼(N H)来制备。用肼为燃料,四氧化二氮做氧化剂,二者反应生
2 4
成氮气和气态水。已知:
①N(g) + 2O(g) = NO(g) △H=10.7kJ/mol
2 2 2 4
②N H(g) + O(g) = N(g) + 2HO(g)△H=-543kJ/mol
2 4 2 2 2
写出气态肼和四氧化二氮反应的热化学方程式__________
(4)25℃、101kPa时,14gCO在足量的O 中充分燃烧,放出141.3kJ的热量,写出该反应的热化学方程式
2
___________
(5)0.50L 2.00mol/LH SO 溶液与2.0L 1.00mol/LKOH溶液完全反应,放出114.6kJ热量,该反应的中和热
2 4
△H=______