文档内容
第一章 物质及其变化
课标要求:
(1)能根据物质的组成和性质对物质进行分类,感受分类方法对化学学科研究和化学学习的
重要作用;
(2)知道胶体是一种常见的分散系,了解丁达尔效应;
(3)了解电解质的概念,知道酸、碱、盐在溶液中能发生电离;
(4)根据实验事实认识离子反应用及其发生的条件;
(5)通过实验事实了解氧化还原反应的本质是电子转移,能举例说明生产、生活中常见的氧
化还原反应;
(6)能正确认识氧化还原反应的价值。
第一节 物质的分类及转化
教学目标:
1.能根据物质的组成和性质对物质进行分类
2.通过查阅资料等手段,浓度按不同的方法对物质进行分类
3.感悟分类法是一种行之有效、简单易行的科学方法
4.知道胶体是一种常见的分散系
5.认识丁达尔效应
6.逐步探究胶体与浊液、溶液的区别
7.发展学生的学习兴趣,乐于探究物质变化的奥秘,感受化学世界的奇妙
教学重点、难点
重点:1.常见化学物质的分类方法;2.胶体及其主要性质
难点:1.常见化学物质的分类方法;2.丁达尔效应
教学方法与过程:
第一节 物质的分类
一、物质的分类
1.根据物质的组成和性质分类
(1)同一种可以组成不同的单质,由同一种元素组成的不同单质之间互称为同素异形体;不
同元素可以组成化合物,100多种元素可以能成种类繁多的物质。我们可以采用树状分类法
和交叉分类法来认识和研究物质的组成、性质、用途、制备等。
(2)树状分类法和交叉分类法A.树状分类法
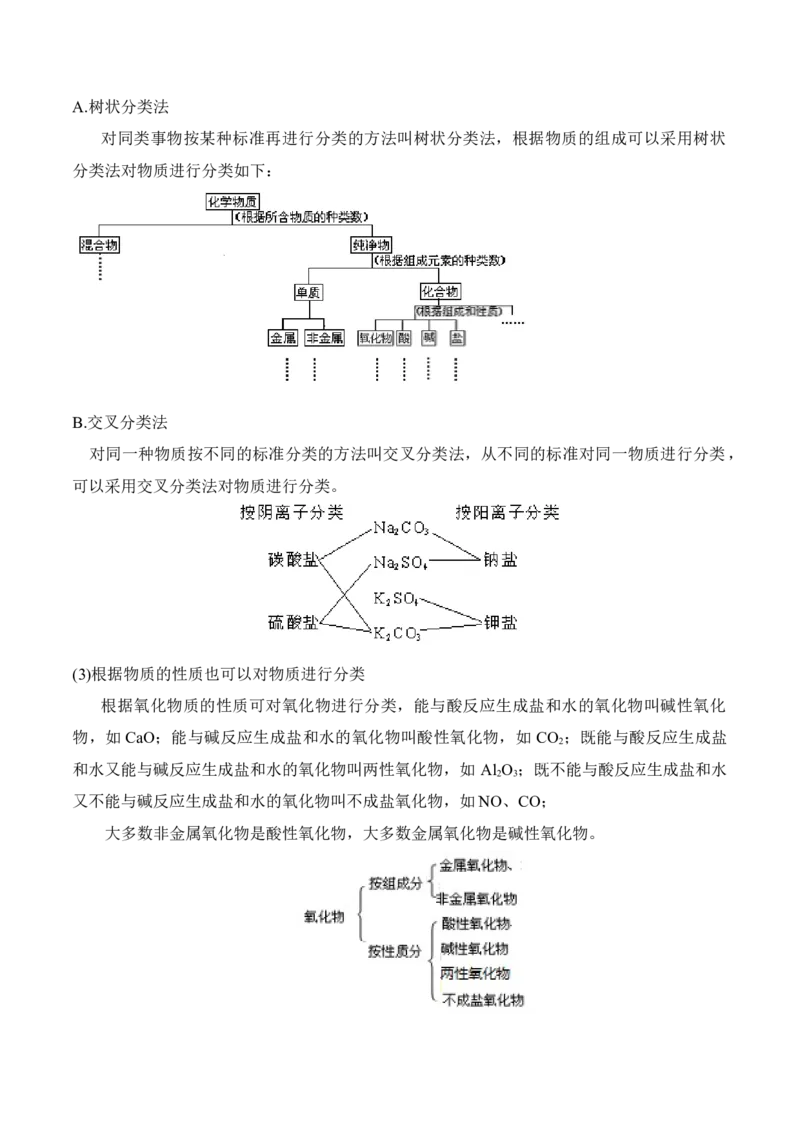
对同类事物按某种标准再进行分类的方法叫树状分类法,根据物质的组成可以采用树状
分类法对物质进行分类如下:
B.交叉分类法
对同一种物质按不同的标准分类的方法叫交叉分类法,从不同的标准对同一物质进行分类,
可以采用交叉分类法对物质进行分类。
(3)根据物质的性质也可以对物质进行分类
根据氧化物质的性质可对氧化物进行分类,能与酸反应生成盐和水的氧化物叫碱性氧化
物,如CaO;能与碱反应生成盐和水的氧化物叫酸性氧化物,如 CO ;既能与酸反应生成盐
2
和水又能与碱反应生成盐和水的氧化物叫两性氧化物,如 Al O ;既不能与酸反应生成盐和水
2 3
又不能与碱反应生成盐和水的氧化物叫不成盐氧化物,如NO、CO;
大多数非金属氧化物是酸性氧化物,大多数金属氧化物是碱性氧化物。[实践与探究]选择熟悉的物质,制作一张交叉分类图。
提示:氧化物、酸、碱、盐等还可以按照不同的标准进一步进行分类,化合物也可以分为无
机化合物和有机化合物等。
2.分散系及其分类
(1)分散系:一种(或多种物质)分散到另一种(或多种)物质中所得到的体系,叫做分散
系。被分散的物质称作分散质,容纳分散质的物质称作分散剂。
(2)根据分散质粒子的直径大小对分散系进行分类,分散质粒子直径小于 1nm的分散系是
溶液;分散质粒子直径大于100nm的分散系是悬浊液或乳浊液;分散质粒子直径在 1nm——
100nm的分散系是胶体。
(3)胶体按照分散剂所处的状态(气态、液态、固态)不同,可分为气溶胶、液溶胶和固溶
胶;
分散剂是气体的叫气溶胶,如烟、云、雾;分散剂是液体的叫液溶胶,如 Fe(OH) 胶体;
3
分散剂是固体的叫固溶胶,如有色玻璃。
(4)透明的液溶胶与溶液从外观上没有区别,可以利用丁达尔效应进行区分。
[实验与探究]
1.取2个100mL小烧杯,分别加入 40 mL 蒸馏水、40 mL CuSO 溶液和25 mL泥水。将烧
4
杯中的蒸馏水加热至沸腾,向沸水中逐滴加入 5~6滴 FeCl 饱和溶液。继续煮沸至溶液呈红
3
褐色,停止加热。观察制得的Fe(0H) 胶体,并与CuSO 溶液比较。
3 4
2.将盛有CuSO 溶液和Fe(0H) 胶体的烧杯置于暗处,分别用激光笔(或手电筒)照射烧杯
4 3
中的液体,在于光束垂直的方向进行观察,并记录实验现象。
注:Fe(OH) 胶体的制备注意要点
3
(1)实验操作中,必须选用氯化铁饱和溶液而不能用氯化铁稀溶液。原因是若氯化铁溶液浓度
过低,不利于氢氧化铁胶体的形成。
(2)向沸水中滴加FeCl 饱和溶液,而不是直接加热FeCl 饱和溶液,否则会因溶液浓度过大直
3 3
接生成Fe(OH) 沉淀而无法得到Fe(OH) 胶体。
3 3
(3)实验中必须用蒸馏水,而不能用自来水。原因是自来水中含电解质、杂质较多,易使制备
的胶体发生聚沉。
(4)往沸水中滴加氯化铁饱和溶液后,可稍微加热煮沸,但不宜长时间加热。原因是长时间加
热将导致氢氧化铁胶体聚沉。
(5)要边加热边摇动烧杯,但不能用玻璃棒搅拌,否则会使Fe(OH) 胶粒碰撞成大颗粒形成沉
3淀。
[归纳与整理]
1.当光束通过Fe(0H) 胶体时,可以看到一条光亮的“通路”。而光束通过CuSO 溶液时,
3 4
则看不到此现象。这条光亮的“通路”是由于胶体粒子对光线散射(光波偏离原来的方向而
分散传播)形成的,叫做丁达尔效应。利用丁达尔效应是区分胶体与溶液的一种常用物理方
法。
注:①丁达尔效应是由于胶粒对可见光的散射而产生的,是一种物理现象;
②丁达尔效应是胶体特有的性质,可用来鉴别胶体与溶液;
③液溶胶、气溶胶能发生丁达尔效应,大多数固溶胶无此性质;
④丁达尔效应证明了胶粒的大小范围。
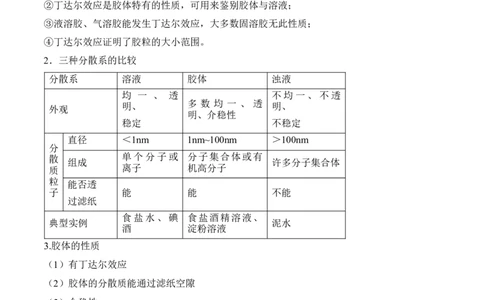
2.三种分散系的比较
分散系 溶液 胶体 浊液
均 一 、 透 不均一、不透
多 数 均 一 、 透
明、 明、
外观
明、介稳性
稳定 不稳定
直径 <1nm 1nm~100nm >100nm
分
散 单个分子或 分子集合体或有
组成 许多分子集合体
质 离子 机高分子
粒
能否透
子 能 能 不能
过滤纸
食盐水、碘 食盐酒精溶液、
典型实例 泥水
酒 淀粉溶液
3.胶体的性质
(1)有丁达尔效应
(2)胶体的分散质能通过滤纸空隙
(3)介稳性
二、物质的转化
1.酸、碱、盐的性质
同类物质的性质具有相似的性质,酸、碱、盐都各自有自己的化学通性。
(1)酸:酸溶液中都含有H+
①酸与活泼金属单质反应,生成盐和氢气: Fe+2HCl=FeCl +H ↑
2 2
②酸与金属化合物反应,生成盐和水: Fe O +6HCl=2FeCl +3H O
2 3 3 2③酸与碱反应:HCl+NaOH=NaCl+H O
2
④酸与盐反应:HCl+AgNO =AgCl↓+HNO
3 3
(2)碱:碱溶液中都含有OH-
①碱与非金属氧化物反应:2NaOH+CO =Na CO +H O
2 2 3 2
②碱与酸反应:2NaOH+H SO =Na SO +2H O
2 4 2 4 2
③碱与盐反应:2NaOH+CuSO =Cu(OH) ↓+Na SO
4 2 2 4
(3)盐:同类盐含有相同的酸根离子
①盐与某些金属单质反应:Fe+CuSO =FeSO +Cu
4 4
②盐与酸反应:BaCl +H SO =BaSO ↓+2HCl
2 2 4 4
③盐与碱反应:CuCl +2NaOH=Cu(OH) ↓+2NaCl
2 2
2、反应类型
根据反应物和生成物的类别和种类可分为化合反应、分解反应、置换反应和
复分解反应,金属与酸的反应一般属于置换反应,酸与碱、盐与酸、盐与碱、盐与盐的反应
一般属于复分解反应。
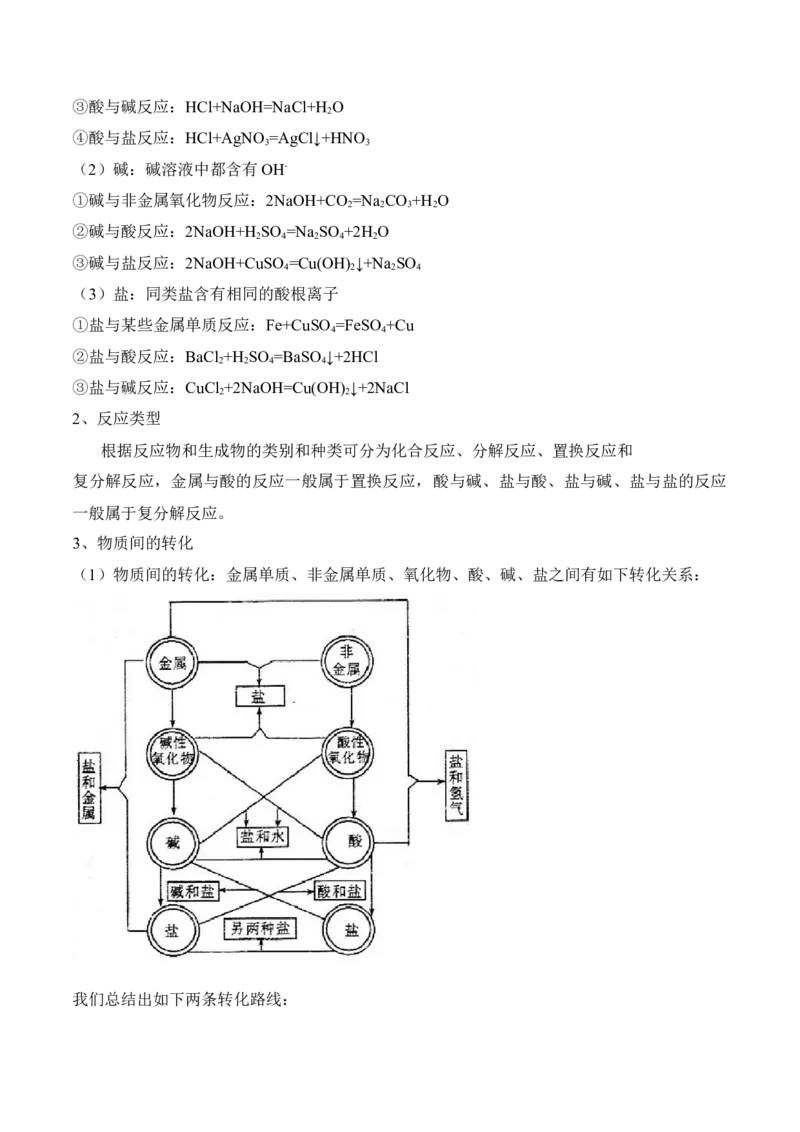
3、物质间的转化
(1)物质间的转化:金属单质、非金属单质、氧化物、酸、碱、盐之间有如下转化关系:
我们总结出如下两条转化路线:金属单质 碱性氧化物 碱 盐
非金属单质 酸性氧化物 酸 盐
(2)物质间转化的应用
1)物质的制备:从上述转化关系我们可以找到制备某种物质的可能方法。
①酸的制备:酸性氧化物与水反应、盐与另一种酸反应
②碱的制备:碱性氧化物与水反应、盐与另一种碱反应
③盐的制备:金属单质与非金属单质反应、酸性氧化物与碱性氧化物反应、盐与盐反应、酸
与盐反应、碱与盐反应
2)工业上物质的制备方法选择因素:要从反应的可能性、原料来源、成本高低、设备要求等
方面来选择物质制备的适宜方法。
补充练习:
1.由同一种元素所构成的不同单质被称为同素异形体,下列哪组物质不属于同素异形体的
是( )
A.钢和铁 B.金刚石和石墨 C.红磷和白磷 D.氧气和臭氧
答案A
解析:由同一种元素所构成的不同单质被称为同素异形体,据此判断。A.钢和铁都是铁和
碳的合金,是混合物,不是单质,不能互为同素异形体,A正确;
B.金刚石和石墨都是由碳元素形成的不同物质,都是单质,互为同素异形体,B错误;C.
红磷和白磷都是由磷元素形成的不同物质,都是单质,互为同素异形体,C错误;D.氧气与
臭氧都是由氧元素形成的不同物质,都是单质,互为同素异形体,D错误。答案选A。
2.从对化合物的分类方法出发,指出下列各组物质中与其他类型不同的一种物质是
(1)Na O CaO SO CuO ______
2 2
(2)NaCl KCl NaClO CaCl ______
3 2
(3)HClO KClO HCl NaClO ______
3 3 3
(4)NaHCO Ca(HCO ) NH HCO K CO ______
3 3 2 4 3 2 3
答案:(1)SO
2
(2)NaClO (3)HCl (4)K CO
3 2 3解析:仔细分析各物质在元素组成、化合价规律、酸、碱、盐、氧化物分类方法等找出答案。
(1)SO 是非金属氧化物,其他三种为金属氧化物;(2)NaClO 是氯的含氧酸盐,其他三种是金
2 3
属氯化物(或从氯元素的价态上找);(3)从氯元素的价态上分析,HCl中Cl为-1价,其他为
+5价;(4)前三者为酸式碳酸盐,K CO 为正盐。
2 3
3.根据物质分类的方法,请对“混合物”从几个角度进行分类。举例说明。
答案:(1)以混合物呈现的聚集状态为标准
(2)以混合物中分散质的大小为标准
(3)以混合物的组成成分为标准
4.利用交叉分类法,请你说出Na SO 可能属于的类型名称是____________。
2 4
答案:纯净物、化合物、盐、钠盐、硫酸盐、正盐或含氧酸盐。
解析:(1)从其分子组成上分类,只由一种分子组成,是纯净物;(2)从元素组成上分类,由三
种元素组成的,是化合物;(3)从化合物组成上分类,属于盐;(4)从阳离子组成上分类,属于
钠盐;(5)从阴离子组成上分类,属于硫酸盐、正盐或含氧酸盐。
5.下列说法正确的是( )
A.丁达尔效应不是胶体特有的现象,溶液与浊液也有
B.胶体与其他分散系的本质区别是有丁达尔效应,而其他分散系没有
C.胶体粒子的直径小于1 nm
D.丁达尔效应可用于鉴别胶体和溶液
答案:D解析:胶体与其他分散系的本质区别是胶体粒子的直径在 1~100 nm之间;丁达尔效应是胶
体特有的现象,故选D
6.纳米材料是粒子直径为1~100 nm的材料,其研究成果已应用于医学、化工、军事等领域。
纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,下列有关形成的物质的判断正
确的是( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会
析出黑色沉淀
A.①②③④ B.②③⑤⑥
C.②③④ D.②③④⑥
答案:C
解析:纳米碳的粒子直径在 1~100 nm。将其分散到蒸馏水中形成的分散系属于胶体,能产
生丁达尔效应;胶体的粒子不能透过半透膜,但能透过滤纸;胶体是一种“介稳体系”,虽
然不如溶液稳定,但比浊液稳定,放置较长时间不会聚沉而析出沉淀。
7.现有下列十种物质:①H O、②空气、③Mg、④H SO 、⑤CaO、⑥CuSO 、⑦碘酒、
2 2 4 4
⑧Ca(OH) 、⑨酒精、⑩NaHCO 。其中属于混合物的是______________(填序号,下同);
2 3
属于氧化物的是_____________;属于酸的是____________;属于碱的是________________;
属于盐的是_____________。
答案:②⑦ ①⑤ ④ ⑧ ⑥⑩。
解析:由两种或两种以上物质组成的是混合物,属于混合物的是空气、碘酒;由两种元素组
成,其中一种是氧元素的化合物是氧化物,属于氧化物的是H O、CaO;电离出的阳离子全
2
部是氢离子的化合物是酸,属于酸的是H SO ;电离出的阴离子全部是氢氧根的化合物是碱,
2 4
属于碱的是Ca(OH) ;由金属阳离子或铵根离子与酸根离子组成的化合物是盐,属于盐的是
2
CuSO 、NaHCO 。
4 3
8.胆矾(CuSO ·5H O)是一种蓝色晶体,用它进行以下几个实验:①取少量胆矾晶体,用
4 2
研钵研碎后,放入硬质玻璃管中,加热,可以看到固体颜色逐渐变成白色,同时试管口有水
珠生成;②冷却后,取试管内白色粉末少许,用蒸馏水溶解后得到蓝色溶液,将此溶液分置
于两支试管中;③向第一支试管中滴入NaOH溶液后,可观察到有蓝色沉淀生成;④将一枚
洁净的铁钉放入第二支试管中,过一会,取出铁钉,观察到铁钉表面附着一层红色物质。用
化学方程式表示上述变化,并指出所发生的反应的类型。
⑴加热胆矾晶体: ,( );⑵生成蓝色沉淀: ,( );
⑶生成红色物质: ,( )。
答案:⑴CuSO ·5H O CuSO +5H O↑ 分解反应
4 2 4 2
⑵CuSO +2NaOH=Cu(OH) ↓+Na SO 复分解反应
4 2 2 4
⑶CuSO +Fe=Cu+FeSO 置换反应
4 4
解析:⑴CuSO ·5H O)是一种蓝色晶体,CuSO 而是一种白色固体,所以加热胆矾晶体的化
4 2 4
学反应方程式为CuSO ·5H O CuSO +5H O↑ ,该反应属于分解反应;⑵滴入NaOH溶
4 2 4 2
液后,可观察到有蓝色沉淀生成,该蓝色沉淀为Cu(OH) ,其形成的化学方程式为CuSO +
2 4
2NaOH=Cu(OH) ↓+Na SO ,该反应属于 复分解反应;⑶铜离子可以被铁置换出来,所以
2 2 4
生成红色物质的化学反应方程式为CuSO +Fe=Cu+FeSO ,该反应属于置换反应。
4 4