文档内容
第一章 物质及其变化
第二节 离子反应 课时作业
第二课时 离子反应及离子方程式
基础达标
1.下列各组物质混合后,不能发生离子反应的是( )
A.二氧化碳气体通入硝酸钙溶液中 B.碳酸钠溶液与稀盐酸混合
C.醋酸钡溶液与稀硫酸溶液混合 D.氢氧化钠溶液中加入稀盐酸
2.NaHCO 和NaHSO 的溶液混合后,实际参加反应的离子是( )
3 4
A.H+和CO2- B.HCO -和HSO -
3 3 4
C.Na+、HCO -和H+ D.HCO -和H+
3 3
3.下列反应属于离子反应的是( )
A.H 和O 反应生成水 B.锌片投入稀硫酸中
2 2
C.双氧水(H O)分解制取O D.氨气遇到HCl气体生成白烟(NH Cl颗粒)
2 2 2 4
4. 关于离子方程式Cu2++2OH- === Cu(OH) ↓的下列说法正确的是( )
2
A. 可表示所有铜盐和强碱的反应
B. 可表示某一个具体的反应,也可以表示一类反应
C. 离子方程式中的OH-可代表所有的碱
D. 反应中可看到Cu(OH) 白色沉淀
2
5.下列反应可以用同一离子方程式表示的是( )
A.HCl溶液+NaCO 溶液 HCl溶液+NaHCO 溶液
2 3 3
B.NaOH溶液+HCl溶液 Ba(OH) 溶液+HSO 溶液
2 2 4
C.BaCl 溶液+HSO 溶液 Ba(OH) 溶液+NaSO 溶液
2 2 4 2 2 4
D.CaCO +HCl溶液 NaCO 溶液+HSO 溶液
3 2 3 2 4
6.下列反应的离子方程式书写正确的是( )
A.将鸡蛋壳在醋酸中溶解有气泡产生:CaCO +2H+=Ca2++H O+CO↑
3 2 2
B.向CuSO 溶液中加入NaOH溶液:Cu2++2OH-=Cu(OH) ↓
4 2
C.将Cu丝插入AgNO 溶液中:Cu+Ag+=Cu2++Ag
3
D.向NaHCO 溶液中逐滴加入Ba(OH) 溶液: +OH-=H O+
3 2 2
7.某同学在奥运五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质
间不能发生反应。下列说法不正确的是( )
A.NaOH溶液与CO 反应的离子方程式一定为2OH-+CO=HO+
2 2 2
B.稀盐酸与NaOH溶液反应的离子方程式为H++OH-=HO
2
C.Fe与稀盐酸反应的离子方程式为Fe+2H+=Fe2++H↑
2
D.CO 与C的反应属于化合反应
2
8.下列各项中两组物质间的反应,可以用同一个离子方程式表示的是( )
A.HSO 和NaOH;HNO 和Ba(OH)
2 4 3 2
B.HSO 和Ba(OH) ;BaCl 和NaSO
2 4 2 2 2 4
C.NaCO 溶液和少量稀盐酸;NaCO 溶液和过量稀盐酸
2 3 2 3
D.HSO 和NaOH;HSO 和Cu(OH)
2 4 2 4 2
9.能正确表示下列化学反应的离子方程式是( )
A.氢氧化钡溶液与硝酸的反应OH-+H+ HO
2
B.澄清的石灰水与稀盐酸反应Ca(OH) +2H+ Ca2++2H O
2 2
C.铜片插入硝酸银溶液中Cu+Ag+ Cu2++Ag
D.碳酸钡溶于稀盐酸中C +2H+ HO+CO↑
O2− 2 2
3
10.下列离子方程式改写成化学方程式正确的是( )
A.Cu2++2OH-==Cu(OH) ↓ CuCO+2NaOH==Cu(OH) ↓+Na CO
2 3 2 2 3
B.CO2-+2H+==CO ↑+H O BaCO +2HCl==BaCl +CO ↑+H O
3 2 2 3 2 2 2
C.Ca2++CO2-===CaCO↓ Ca(NO )+Na CO==CaCO↓+2NaNO
3 4 3 2 2 3 4 3
D.OH-+H+ HO CH COOH+KOH==CH COOK+H O
2 3 3 2
能力提升
11.下列叙述中正确的是( )
A.凡是盐在离子方程式中都要以离子形式表示
B.离子互换反应总是向着溶液中反应物离子浓度减小的方向进行
C.酸碱中和反应的实质是H+与OH-结合生成水,故所有的酸碱中和反应的离子方程
式都可写成H++OH-===H O的形式
2D.复分解反应必须同时具备离子反应发生的三个条件才能进行
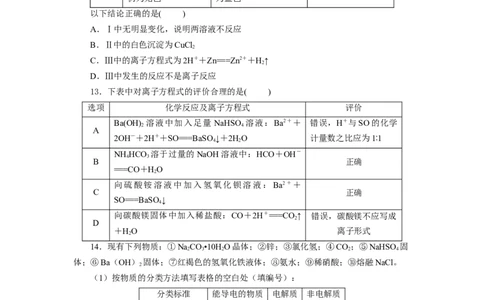
12.某同学在实验室中进行如下实验:
编号 Ⅰ Ⅱ Ⅲ
实验
没有明显变化,溶液 有白色沉淀生成,溶液
现象 有无色气体放出
仍为无色 为蓝色
以下结论正确的是( )
A.Ⅰ中无明显变化,说明两溶液不反应
B.Ⅱ中的白色沉淀为CuCl
2
C.Ⅲ中的离子方程式为2H++Zn===Zn2++H↑
2
D.Ⅲ中发生的反应不是离子反应
13.下表中对离子方程式的评价合理的是( )
选项 化学反应及离子方程式 评价
Ba(OH) 溶液中加入足量 NaHSO 溶液:Ba2++ 错误,H+与SO的化学
2 4
A
2OH-+2H++SO===BaSO ↓+2HO 计量数之比应为1∶1
4 2
NH HCO 溶于过量的NaOH溶液中:HCO+OH-
4 3
B 正确
===CO+HO
2
向硫酸铵溶液中加入氢氧化钡溶液:Ba2++
C 正确
SO===BaSO ↓
4
向碳酸镁固体中加入稀盐酸:CO+2H+===CO ↑ 错误,碳酸镁不应写成
2
D
+HO 离子形式
2
14.现有下列物质:①NaCO•10H O晶体;②锌;③氯化氢;④CO;⑤NaHSO 固
2 3 2 2 4
体;⑥Ba(OH) 固体;⑦红褐色的氢氧化铁液体;⑧氨水;⑨稀硝酸;⑩熔融NaCl。
2
(1)按物质的分类方法填写表格的空白处(填编号):
分类标准 能导电的物质 电解质 非电解质
属于该类的物
质
(2)上述物质中有物质之间在溶液中可发生离子反应:H++OH-=HO,写出一个该
2
离子反应对应的化学方程式__________________________________________。
(3)将⑨滴加到⑦中至过量的实验现象是____________________________。
(4)将③通入⑧中至恰好完全反应,则溶液导电能力的变化为______________。
(5)⑤的溶液中加入②反应的离子方程式为
___________________________________。直击高考
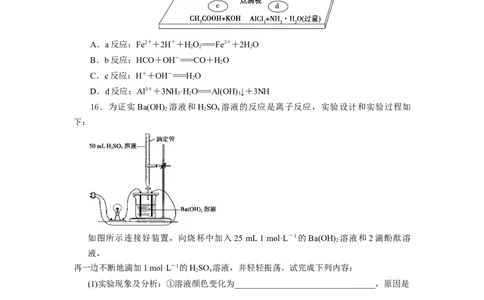
15.在下图点滴板上进行四个溶液间反应的小实验,其对应反应的离子方程式书写正
确的是( )
A.a反应:Fe2++2H++HO===Fe3++2HO
2 2 2
B.b反应:HCO+OH-===CO+HO
2
C.c反应:H++OH-===H O
2
D.d反应:Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
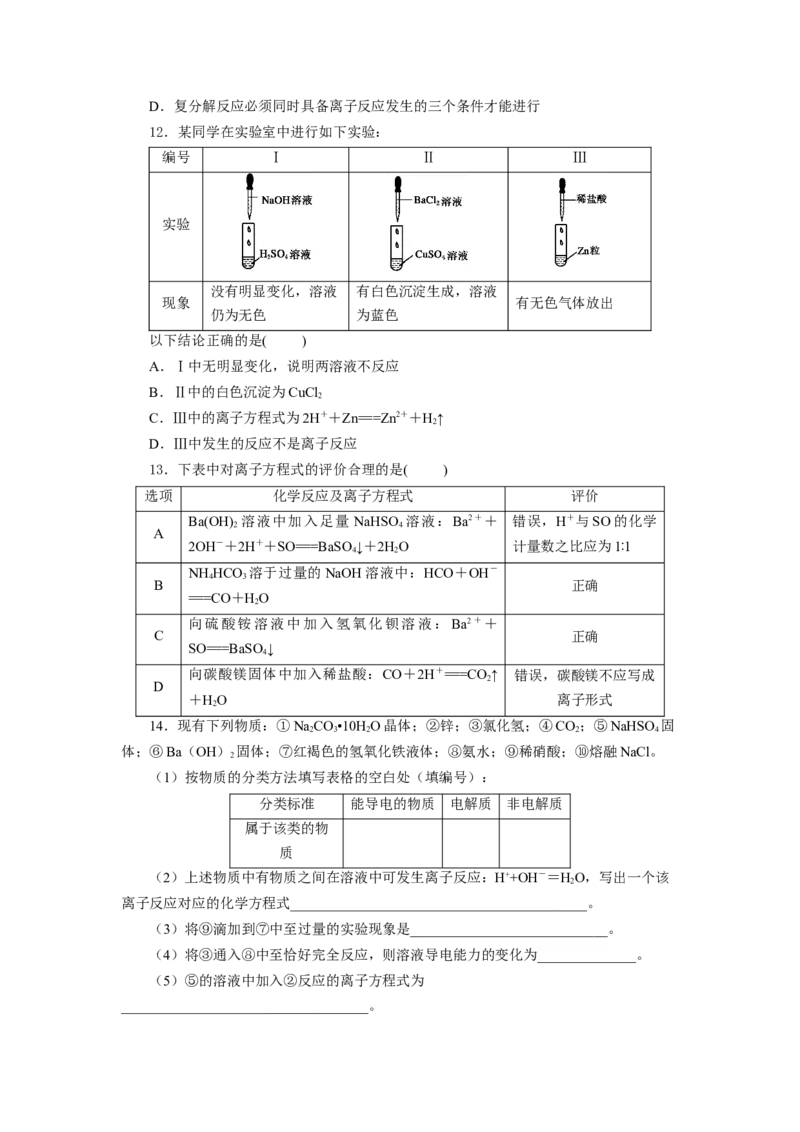
16.为证实Ba(OH) 溶液和HSO 溶液的反应是离子反应,实验设计和实验过程如
2 2 4
下:
如图所示连接好装置,向烧杯中加入 25 mL 1 mol·L-1的Ba(OH) 溶液和2滴酚酞溶
2
液,
再一边不断地滴加1 mol·L-1的HSO 溶液,并轻轻振荡。试完成下列内容:
2 4
(1)实验现象及分析:①溶液颜色变化为_________________________________,原因是
_____________________________________________。
②灯泡亮度变化:____________________________________________________,原因
是
______________________________________________________________________。
③溶液变浑浊,原因是_____________________________________________________。
(2)实验结论:稀HSO 与Ba(OH) 溶液反应的实质是_____________________________
2 4 2