文档内容
第二章 分子结构与性质
第一节 共价键
2.1.1 共价键
一.选择题
1. 下列说法中正确的是
A. 双原子分子中化学键键能越大,分子越稳定
B. 双原子分子中化学键键长越长,分子越稳定
C. 双原子分子中化学键键角越大,分子越稳定
D. 在双键中, 键的键能要小于 键的键能
【答案】A
【解析】
A.双原子分子中化学键键能越大,分子越稳定,故A正确;
B.双原子分子中化学键键长越短,分子越稳定,故B错误;
C.双原子分子中没有键角,且分子稳定性与键角无关,故C错误;
D.一般 键的重叠程度比 键的重叠程度大, 键的键能要大于 键,故D错误;
故选A。
2. 下列说法中正确的是
A. 乙烯分子中既含 键又含 键
B. 分子中的化学键为非极性键
C. p和p不能形成 键
D. HF、HCl、HBr、HI的稳定性依次增强
【答案】A
【解析】略
3. 观察下列模型并结合有关信息,判断下列说法不正确的是HCN 结构单元
结构
模型
示意图
备注 易溶于 熔点
A. HCN的结构式为 ,分子中含有2个 键和2个 键
B. 固态硫 属于原子晶体
C. 是由极性键构成的非极性分子
D. 单质硼属共价晶体,结构单元中含有30个 键
【答案】B
【解析】
A.HCN的结构式为 ,单键都是 键,三键中有1个 键、2个 键,所以分子中含有2
个 键和2个 键,故A说法正确;
B.固态硫 属于分子晶体,故B说法错误;
C. 是由极性键构成的非极性分子,故C说法正确;
D.单质硼熔点高,属原子晶体,结构单元中含有 个 键,故D说法正确。
故选B。
4. 能与过量的 反应得到一种固体M和单质H。下列说法正确的是
A. M中含离子键、共价键、配位键 B. 的电子式为
C. H中 键与 键个数比为 D. 和 都属于极性分子
【答案】A
【解析】
能与过量的 反应得到一种固体 M 是氯化铵和单质 H 是氮气,发生的反应为
,以此解答。
A.氯化铵中铵根离子和氯根离子间存在离子键,氮原子和氢原子间存在共价键,其中 中氮原
子含有孤电子对,铵根离子中其中一个氢原子含有空轨道,所以氮原子和含有空轨道的氢原子之间
存在配位键,所以氯化铵中含离子键、共价键、配位键,故A正确;B. 的电子式为 ,故B错误;
C.H是 , 分子中含氮氮三键,所以 键与 键个数比为 ,故C错误;
D. 的分子构型为三角锥形,结构不对称,正负电荷的中心不重合,属于极性分子; 分子
是非极性键构成的非极性分子,故D错误;
故选A。
5. 下列说法中错误的是
A. 键比 键重叠程度大,形成的共价键强
B. 两个原子之间形成共价键时,最多有一个 键
C. 气体单质分子中,一定有 键,可能有 键
D. HClO分子中有 键和 键
【答案】C
【解析】
A. 键是电子“头对头”重叠形成的, 键是电子“肩并肩”重叠形成的,所以 键比 键重叠程
度大,故A正确;
B. 键是头碰头形成的,两个原子之间能形成一个,原子轨道杂化的对称性很高,一个方向上只可
能有一个杂化轨道,所以最多有一个,故B正确;
C.气体单质分子中,可能只有 键,如 ;也可能既有 键又有 键,如 ;但也可能没有化学
键,如稀有气体,故C错误;
D.HClO分子中有 键和 键,故D正确。
故选C。
6. 下列关于 的说法中不正确的是
A. 1个 中有3个 键
B. 中心原子上有1对孤对电子
C. 的立体构型是三角锥形D. 键之间的夹角:
【答案】D
【解析】
对于 ,根据VSEPR理论,中心O原子的配位原子数为3,孤电子对数为 ,
则价电子对数为 ,根据杂化轨道理论,中心O原子为 杂化,
A. 中中心O为 杂化,有4个 杂化轨道,而成键是3根键,还有一对孤电子对,则1个
中有3个 键,故A正确;
B.中心O上存在一对孤电子对,占据正四面体形的一个顶点,故B正确;
C. 杂化的粒子的理论空间构型为正四面体形,由于 中存在一对孤电子对占据正四面体形
的一个顶点,因此粒子的立体构型为三角锥形,故C正确;
D. 中含有1对孤电子对, 中含有2对孤电子对,由于孤电子对斥力大于键合电子对斥力,
孤电子对数目越多,键角越小,因此 键之间的夹角: ,故D错误。
故选D。
7. 关于 键和 键的比较,下列说法不正确的是
A. 键是轴对称的, 键是镜面对称的
B. 键是“头碰头”式重叠, 键是“肩并肩”式重叠
C. 键不能断裂, 键容易断裂
D. H原子只能形成 键,O原子可以形成 键和 键
【答案】C
【解析】
A. 键是“头碰头”式重叠,是轴对称的, 键是“肩并肩”式重叠,是镜面对称的,故A正确;
B. 键是s轨道与s轨道或s轨道与p轨道“头碰头”式重叠形成的, 键是p轨道与p轨道“肩并
肩”式重叠形成的,故B正确;
C. 键较稳定,不易断裂,而不是不能断裂,故C错误;D.H原子只有s轨道电子,只能形成 键,O原子既有s轨道电子也有p轨道电子,可以形成 键和
键,故D正确。
故选C。
8. 下列说法中正确的是
A. 在气体单质分子中,一定含有 键,可能含有 键
B. 烯烃比烷烃的化学性质活泼是由于烷烃中只含 键,而烯烃含有 键
C. 等电子体结构相似,化学性质相同
D. 共价键的方向性决定了原子在形成分子时相互结合的数量关系
【答案】B
【解析】
A.在气体单质分子中,可能存在 键 如 、 、 键 如 分子中存在 键、 键 ,而稀有
气体为单原子分子,不存在化学键,故A错误;
B.烯烃中含有碳碳双键,其中一个是 键,因 键易断裂,故化学性质较活泼,故B正确;
C.等电子体结构相似,但化学性质不一定相同,故C错误;
D.共价键的方向性决定分子的立体构型,饱和性决定分子中各原子的数量关系,故D错误。
故选B
9. 化合物X是一种新型锅炉水除氧剂,其结构式为 ,设 为阿伏加德
罗常数的值。下列说法中正确的是
A. X分子中只有极性键,没有非极性键
B. 1个X分子中的共用电子对数目为11
C. 分子中所含的 键数目为
D. X是共价化合物
【答案】D
【解析】
A. X分子中有极性键,也有 非极性键,故A错误;
B. 1个X分子中的共用电子对数目为12,故B错误;
C. 分子中所含的 键数目为 ,故C错误;D. X是只含共价键的化合物,自然是共价化合物,故D正确;
故选D
10. 下列关于化学键的说法,认识错误的有几个
键与 键的对称性不同
键不能单独存在,一定要和 键共存
含有 键的化合物与只含 键的化合物的化学性质不同
两个非金属元素的原子之间形成的化学键都是共价键
分子中含有共价键,则一定含有一个 键
成键的原子间已知轨道重叠越多,共价键越牢固
个N原子最多只能与3个H原子结合形成 分子,是由共价键的饱和性决定的
A. 1 B. 2 C. 3 D. 4
【答案】B
【解析】
键是轴对称, 键也是轴对称,对称性相同,故 错误;
键不能单独存在,一定要和 键共存,故 正确;
含有 键的化合物, 键易断裂,化学性质相对活泼,与只含 键的化合物的化学性质不同,故
正确;
两个非金属元素的原子之间形成的化学键都是共价键,故 正确;
分子中含有共价键,则一定含有 键,不一定是一个,比如 ,分子中含有不止一个 键,
故 错误;
成键的原子间已知轨道重叠越多,原子间作用力越强,共价键越牢固,故 正确;
个N原子最多只能与3个H原子结合形成 分子,是由共价键的饱和性决定的,故 正确。
综上所述 错误,故B正确。
二、填空题
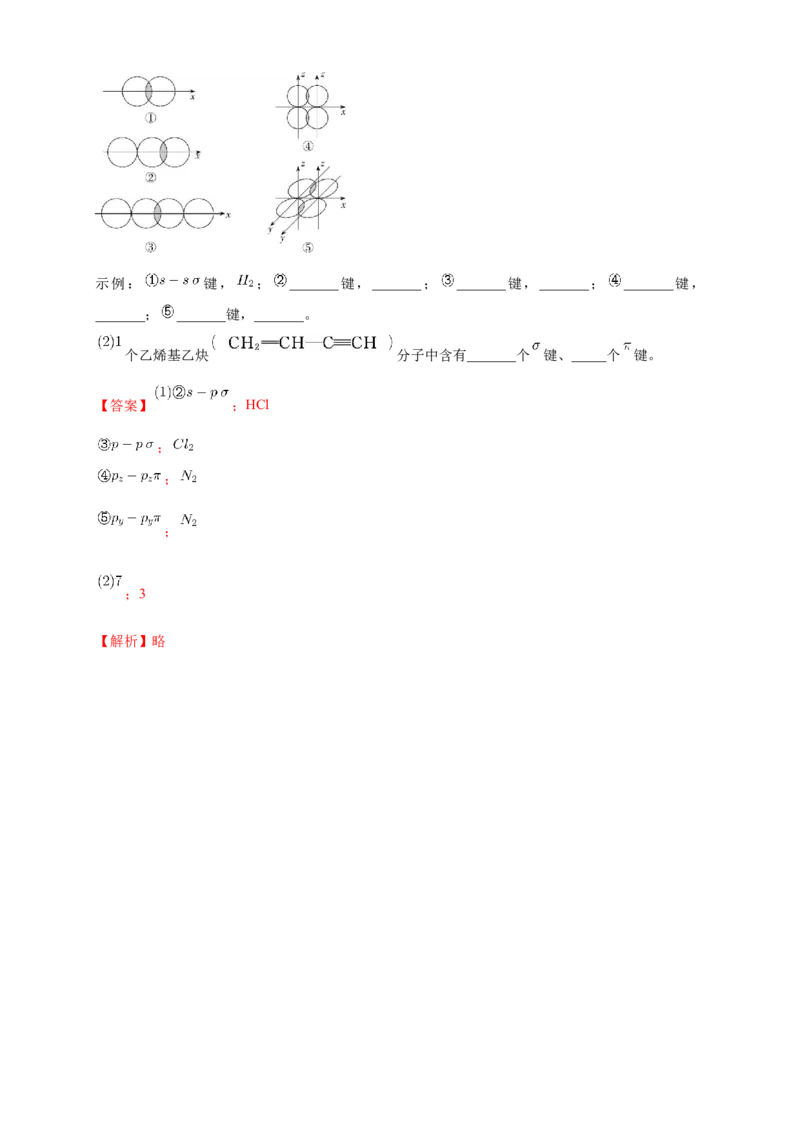
11. 写出下图所表示的共价键名称,并列举含有该共价键的一种物质,写出其分子式。示例: 键, ; _______键,_______; _______键,_______; _______键,
_______; _______键,_______。
个乙烯基乙炔 分子中含有_______个 键、_____个 键。
【答案】 ;HCl
;
;
;
;3
【解析】略