文档内容
第二章 海水中的重要元素—钠和氯
第一节 钠及其化合物 课时作业
第一课时 活泼的金属单质—钠
基础达标
1.下面关于金属钠的描述正确的是( )
A.钠的化学性质很活泼,在自然界里不能以游离态存在
B.钠离子具有较强的还原性
C.钠很软,在新材料领域没有用途
D.钠露置于空气中最后变为NaO
2
2.当钠着火时,不能用的灭火剂是( )
A.泡沫灭火剂 B.干沙
C.石粉 D.专用灭火剂
3.下列做法正确的是( )
A.钠着火时可用泡沫灭火器灭火
B.取用金属钠时,多余的钠应放回原试剂瓶中
C.进行钠在空气中燃烧实验时,为了观察仔细,可以近距离俯视坩埚
D.如果不慎将酸沾到皮肤上,应立即用大量水冲洗,然后用3%~5%的氢氧化钠溶液
冲洗
4.下列有关金属钠说法正确的是( )
A.金属钠燃烧时火焰为黄色
B.实验剩余的金属钠不能放回原瓶
C.金属钠遇水直接生成过氧化钠并放出大量热
D.金属钠的保存应避光避雨,存放于敞开容器中
5.下列有关钠的描述中错误的是( )
A.钠可以保存在煤油中,说明钠的密度比煤油的大且钠不与煤油发生反应
B.实验时钠需用镊子夹取,用后剩余的钠不能放回试剂瓶中
C.新切开的钠放置在空气中会迅速被氧化
D.钠能与氯化钠溶液发生化学反应
6.下列关于钠的叙述正确的是( )
A.钠放置在空气中表面变暗是由于钠的表面生成了NaO
2 2
B.钠与硫酸铜溶液反应生成硫酸钠和单质铜C.钠与水反应的现象说明钠的熔点低,且与水反应放出热量
D.将4.6g钠投入95.4g水中,所得溶液中溶质的质量分数为8%
7.将绿豆大的钠块投入如图所示的烧杯中,可能出现的现象是( )
A.钠块只在煤油层中游动,并放出气体
B.钠块只在水层中游动,钠块熔化,水层变红
C.钠块在 层和水层界面处游动并上下跳动,钠块熔化,水层变红
D.钠块在水层和煤油层界面处游动并上下跳动,钠块熔化,水层变红
8.将少量金属钠分别投入下列物质的水溶液中,反应后溶液质量减轻的是( )
A.HCl B.KSO
2 4
C.NaOH D.CuSO
4
9.一定温度下,向饱和NaOH溶液中加入一定量的钠块,充分反应后恢复到原来的温
度,下列说法正确的是( )
A.溶液中溶质质量增加,溶剂质量减少,溶液中溶质质量分数变大
B.溶液中溶质的质量分数不变,有氧气放出
C.溶液中Na+数目减少,有氢气放出
D.溶液中Na+数目增多,有氢气放出
10.已知,锂单质化学性质与钠类似,活泼性比钠略差。它的密度为0.534g/cm3,锂
元素的焰色为紫红色,将绿豆大的锂投入水中,下列实验现象合理的有( )
①锂沉入水中 ②锂浮在水面上 ③水中有大量气泡 ④反应后
在水中加入几滴石蕊试液,溶液变红
⑤反应剧烈,发出紫红色火焰 ⑥锂四处游动
A.②⑥ B.①③ C.②③⑤ D.②④⑤⑥
能力提升
11.下列关于钠的说法中不正确的是( )
A.金属钠和氧气反应,条件不同,产物不同
B.金属钠与Ca(HCO ) 溶液反应时,既有白色沉淀生成又有气体逸出
3 2
C.将一小块钠投入装有氯化镁溶液的试管中,钠熔成小球并在液面上游动
D.将一小块钠投入装有硫酸铜溶液的试管中,试管底部有红色物质生成12.钛合金是具有耐压耐腐蚀性质的重要金属材料,反应4Na+TiCl ====4NaCl+Ti可
4
以制取金属钛.下列说法不正确的是( )
A.TiCl 中 的化合价:+4
4
B.NaCl的电离方程式:NaCl=Na++Cl-
C.该反应也可在水中完成
D.Na原子在反应中容易得到1个电子生成Na+
13.向分别盛有100 mL水、100 mL稀盐酸、100 mL稀NaOH溶液的X、Y、Z三个
烧杯中各投入0.5 g Na。下列有关说法正确的是( )
A.三个烧杯中均先发生的离子反应为2Na+2HO=2Na++2OH-+H↑
2 2
B.三个烧杯中钠均在液面上剧烈反应,且X烧杯中的反应最剧烈
C.三个烧杯反应后,溶质的质量分数相同
D.三个烧杯反应后,生成的气体的质量一定相同
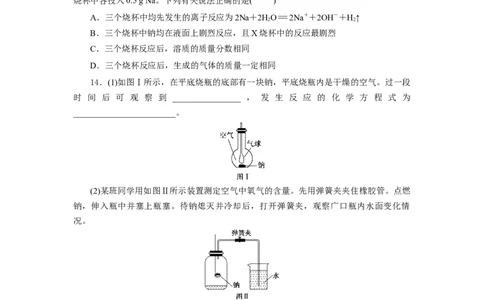
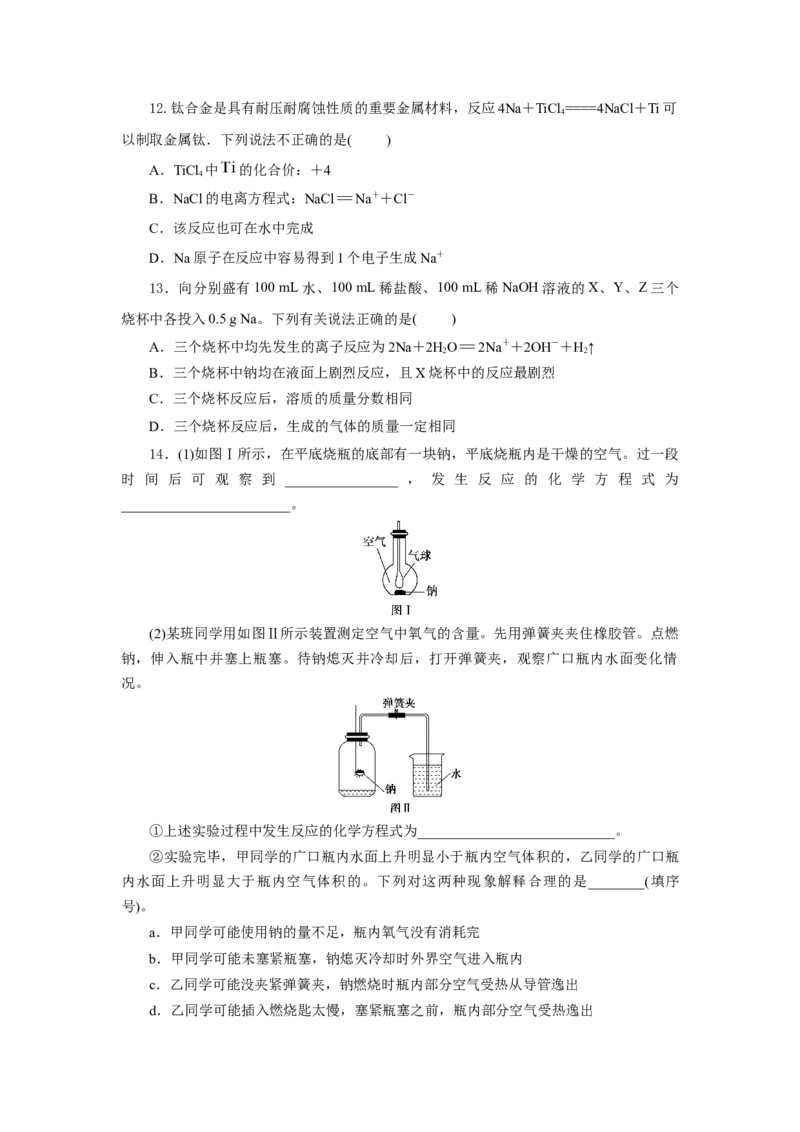
14.(1)如图Ⅰ所示,在平底烧瓶的底部有一块钠,平底烧瓶内是干燥的空气。过一段
时 间 后 可 观 察 到 ________________ , 发 生 反 应 的 化 学 方 程 式 为
________________________。
(2)某班同学用如图Ⅱ所示装置测定空气中氧气的含量。先用弹簧夹夹住橡胶管。点燃
钠,伸入瓶中并塞上瓶塞。待钠熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情
况。
①上述实验过程中发生反应的化学方程式为____________________________。
②实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的,乙同学的广口瓶
内水面上升明显大于瓶内空气体积的。下列对这两种现象解释合理的是________(填序
号)。
a.甲同学可能使用钠的量不足,瓶内氧气没有消耗完
b.甲同学可能未塞紧瓶塞,钠熄灭冷却时外界空气进入瓶内
c.乙同学可能没夹紧弹簧夹,钠燃烧时瓶内部分空气受热从导管逸出
d.乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出直击高考
15.我国“蛟龙”号载人潜水器重要部件是用钛合金材料制造的。金属钛(Ti)抗腐蚀性
能好,在高温环境下具有强还原性。以金红石(主要成分为TiO)为原料生产钛的工艺流程
2
如下,下列说法错误的是
A.①中发生的反应:TiO+2C+2Cl TiCl +2CO
2 2 4
B.钠可以与TiCl 溶液反应制备金属钛
4
C.②中氩气的作用是隔绝空气,防止金属钛被氧化
D.钛抗腐蚀性好是因为常温下钛与氧气化合生成一层极薄的致密氧化膜
16.钠、氯及其化合物在生产和生活中有广泛的应用。金属钠是在1807年通过电解氢
氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解
氯化钠制得工业方法,其反应原理: 。根据所学知识完成下列各
题。
(1)下列各项中保存金属钠的正确方法是___________。
A.石蜡封存 B.放在细沙中 C.放在水中 D.放在煤油中
(2)将金属钠放入 溶液中会产生蓝色沉淀,请用化学方程式解释这一现象
_______
__________________________________________________。
(3) 将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,其现象为
__________
_________________________________。请写出发生反应的化学方程式:
__________________。
(4)钠的一种氧化物常用于呼吸面具和潜水艇氧气的来源,用化学反应方程式表示其原
理:_______________________________________________________________。
(5)已知金属钠在二氧化碳中燃烧生成碳酸钠和一种黑色固体,请写出该反应的化学方
程式,并用双线桥表示电子的转移_______________________________________。