文档内容
2.1.1 化学反应速率 影响化学反应速率的因素(学案)
1.了解化学反应速率的概念,会定量表示化学反应速率。
2.掌握化学反应速率的简单计算,会比较化学反应速率的快慢。
1.化学反应速率的简单计算,会比较化学反应速率的快慢。
影响化学反应速率的因素有___________、__________、____________、___________。
知识点一:化学反应速率
1.化学反应速率是定量描述化学反应进行________的物理量。通常用单位时间内__________
的减少或__________的增加来表示。
其数学表达式为v=_______________________或v=_______________________。
Δc表示_________________,常用单位__________。
Δt表示_________,常用单位______________。
化学反应速率的单位是____________、___________。
二、同一反应中不同物质间反应速率的规律
同一反应用不同物质来表示反应速率时,其数值不一定相等;它们的比值等于化学方程式的
____________之比。
对于在一个容器中的一般反应 aA+bB cC+dD来说有,
v(A)∶v(B)∶v(C)∶v(D)=Δc(A)∶Δc(B)∶Δc(C)∶Δc(D)=Δn(A)∶Δn(B)∶Δn(C)∶Δn(D)=____________。【方法技巧】
反应速率大小(或快慢)比较方法
同一反应的化学反应速率用不同物质表示时数值可能不同,比较化学反应速率的快慢不能只看数值
大小,而要进行一定的转化。
(1)归一法
将同一反应中的不同物质的反应速率转化成同一单位、同一种物质的反应速率,再进行比较。
(2)比值法
用各物质的量表示的反应速率除以对应各物质的化学计量数,然后再对求出的数值进行大小排序,
数值大的反应速率快。如反应mA+nB⇌pC+qD,若v(A)/m>v(B)/n,则反应速率A>B。
(3)注意单位是否统一。
三、化学反应速率的测量方法
(1)利用能够直接观察的某些性质测定
如通过测量释放出一定体积的气体的____________来测定反应速率,或测量一定时间内气体压强的
变化来测定反应速率。
(2)利用科学仪器测量出的性质进行测定,如颜色的深浅、光的吸收、光的发射、导电能力等。
(3)在溶液中,当反应物或生成物本身有比较明显的颜色时,常常利用____________和____________
的正比关系来跟踪反应的过程和测量反应速率。
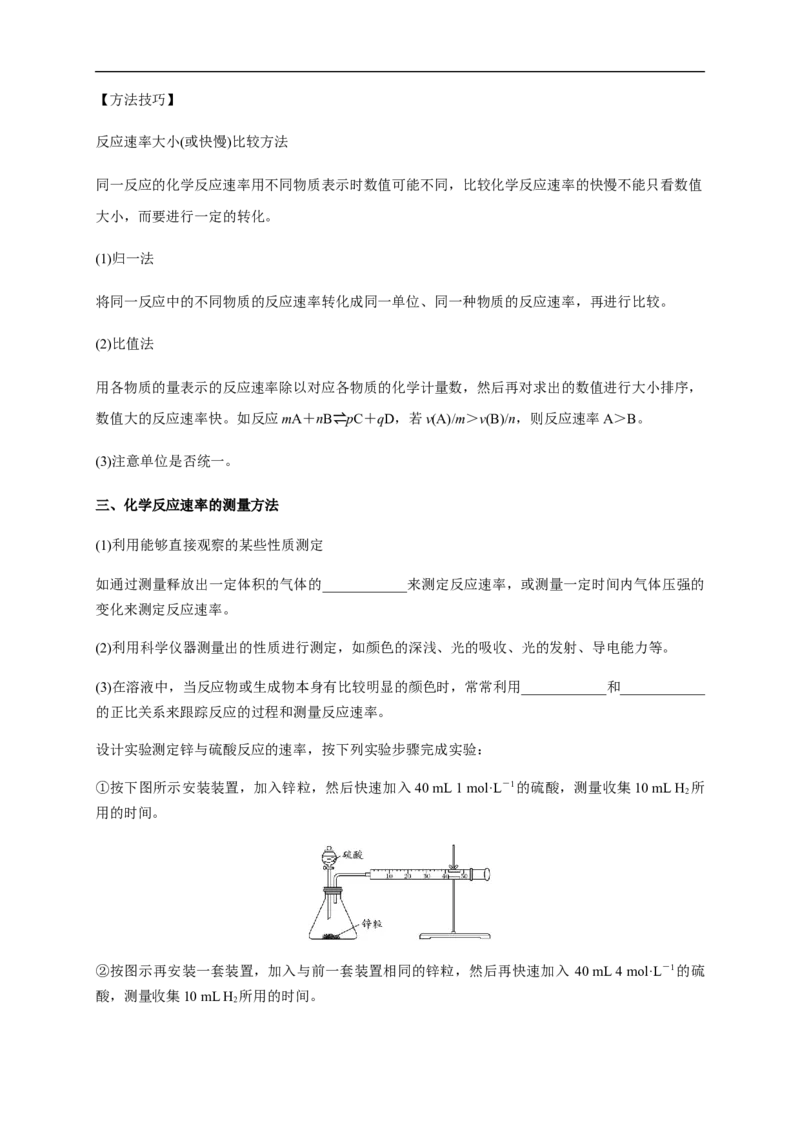
设计实验测定锌与硫酸反应的速率,按下列实验步骤完成实验:
①按下图所示安装装置,加入锌粒,然后快速加入40 mL 1 mol·L-1的硫酸,测量收集10 mL H 所
2
用的时间。
②按图示再安装一套装置,加入与前一套装置相同的锌粒,然后再快速加入 40 mL 4 mol·L-1的硫
酸,测量收集10 mL H 所用的时间。
2四、影响化学反应速率的因素
1. 决定因素(内因):________________________(决定因素)
2. 条件因素(外因):
(1)浓度对反应速率的影响(固体和纯液体除外),
①浓度越大,反应速率越____________,浓度越小,反应速率越____________。
②变化情况:对于可逆反应来说,增大反应物的浓度,正反应速率瞬间增大,逆反应速率不
变,随后,由于反应物浓度减小,生成物浓度增大,正反应速率减慢,逆反应速率增大。
(2)压强对反应速率的影响(方程式中必须要有____________),
①压强越大,反应速率越____________,压强越小,反应速率越____________。
②说明
A若参加反应的物质为固体或液体,由于压强对它们的浓度影响几乎为零,可以认为速率不
变。
B压强对反应速率影响的前提是有气体参加的反应。其实质是加压(体积减小)使物质的浓
度增大。若加压后物质的体积不变,则浓度不变,反应速率也不变(如向恒容的容器中充
入惰性气体)。
C惰性气体对反应速率的影响
⃗引起 ⃗导致
恒容:充入惰性气体, 总压增大 物质浓度不变,反应速率____________。
⃗引起 ⃗导致
充入反应气体, 总压增大 物质浓度增大,反应速率____________。
⃗引起 ⃗导致
恒压:充入惰性气体, 体积增大 物质浓度减小,反应速率____________。
⃗引起 ⃗导致
充入反应气体, 体积增大 物质浓度不变,反应速率____________。
(3)温度对反应速率的影响(提高了反应物分子的能量),升高温度,反应速率变____________,降低温度,反应速率变____________。
(4)催化剂对反应速率的影响(降低了活化能),
①加入催化剂可以改变(加快或减慢)化学反应速率。
②加入催化剂可以降低反应的活化能,但不能改变反应热。
(5)其他因素
接触面积(乳化剂)、构成原电池、光、电磁波、溶剂的性质等也能影响化学反应速率
(6)随着反应的进行,反应速率先加快后减慢,加快的原因可能是:
①________________________;②________________________;③____________。
【练习】下列表示化学反应速率的单位正确的是( )
A.mol•h﹣1 B.mol/L•s
C.mol•L﹣1•min﹣1 D.mol•L﹣1
【练习】一定条件下,将4.0mol NH 充入容积为2L的密闭容器中,5min后容器内剩余2.4mol
3
NH .该分解反应中,v(NH )应为(单位:mol•L﹣1•min﹣1)( )
3 3
A.0.32 B.0.16 C.0.8 D.0.4
【练习】一定条件下,下列表示4NH (g)+5O (g)⇌4NO(g)+6H O(g)的反应速率中,最
3 2 2
快的是( )
A.v(NH )=0.8mol•L﹣1•s﹣1
3
B.v(O )=0.9mol•L﹣1•s﹣1
2
C.v(NO)=0.6mol•L﹣1•s﹣1
D.v(H O)=1.0mol•L﹣1•s﹣1
2
【练习】在恒容密闭容器中发生反应:3CO(g)+Fe O (s) 3CO (g)+2Fe(s),下列
2 3 2
说法不正确的是( )A.增加块状Fe O 的量,反应速率增大
2 3
B.降低温度,反应速率减慢
C.使用催化剂,反应速率增大
D.充入CO,反应速率增大
【练习】下列关于影响化学反应速率的条件的说法正确的是( )
A.增大压强一定能加快化学反应速率
B.使用催化剂对化学反应速率没影响
C.增加反应物的量一定能加速化学反应速率
D.升高温度,一般能加快化学反应速率
【练习】某温度下按如图安装好实验装置,在锥形瓶内盛6.5g锌粒(颗粒大小基本相同),通过分
液漏斗加入40mL 2.5mol•L﹣1的硫酸溶液,将产生的H 收集在一个注射器中,用时10s时恰好
2
收集到气体的体积为50mL(若折合成0℃、101 kPa条件下的H 体积为44.8mL),在该温度
2
下,下列说法不正确的是( )
A.可以通过测定锌粒减少质量来测定反应速率
B.忽略锥形瓶内溶液体积的变化,用H+来表示10 s内该反应的速率为0.01 mol•L﹣1•s﹣1
C.忽略锥形瓶内溶液体积的变化,用Zn2+来表示10 s内该反应速率为0.01 mol•L﹣1•s﹣1
D.用H 来表示10 s内该反应的速率为0.000 2 mol•s﹣1
2
1.下列做法的目的与改变化学反应速率无关的是( )A.在糕点包装内放置小包除氧剂 B.在糖果制作过程中添加着色剂
C.高炉炼铁前先将铁矿石粉碎 D.牛奶在冰箱里保存
2.决定化学反应速率的主要因素是( )
A.反应温度 B.反应物的浓度
C.反应物本身的性质 D.反应物之间的接触面积
3.反应4A(s)+3B(g)═2C(g)+D(g),经2min后,B的浓度减少了0.6mol/L.下列反应
速率的表示正确的是( )
A.在这2min内用A表示的反应速率是0.4mol/(L•min)
B.在这2min内用C表示的反应速率是0.2mol/(L•min)
C.2min末时的反应速率,用B表示是0.3mol/(L•min)
D.在这2min内用B表示的反应速率的值是减小的,C表示的反应速率逐渐增大
4.在不同条件下分别测得反应2SO +O ⇌2SO 的化学反应速率,其中表示该反应进行得最快的是
2 2 3
( )
A.v(SO )=4mol/(L•min) B.v(O )=6mol/(L•min)
3 2
C.v(SO )=8mol/(L•min) D.v(O )=3mol/(L•min)
2 2
5.在恒温、恒容的密闭容器中进行反应A(g)=B(g)+C(g),若反应物的浓度由2mol•L﹣1
降到0.8mol•L﹣1需要10s,那么反应物浓度再由0.8mol•L﹣1降到0.2mol•L﹣1所需要的时间为(
)
A.5s B.小于5s C.大于5s D.无法判断
6.下列说法错误的是( )
A.升高温度可加快H O 的分解速率
2 2
B.减小H O 溶液浓度可降低其分解速率
2 2
C.加FeCl 不能加快H O 分解速率
3 2 2D.用带火星的木条可检验H O 分解产生的气体
2 2
7.下列关于影响化学反应速率的条件的说法正确的是( )
A.增大压强一定能加快化学反应速率
B.使用催化剂对化学反应速率没影响
C.增加反应物的量一定能加速化学反应速率
D.升高温度,一般能加快化学反应速率
8.下列有关化学反应速率和限度的说法中,不正确的是( )
A.实验室用H O 分解制O ,加入MnO 后,反应速率明显加快
2 2 2 2
B.2SO +O 2SO 是可逆反应,SO 不能全部转化为SO
2 2 3 2 3
⇌
C.2SO +O 2SO 反应中,增加O 用量,SO 就可以全部转化为SO
2 2 3 2 2 3
⇌
D.实验室用碳酸钙和盐酸反应制取CO ,用碳酸钙粉末比用块状碳酸钙反应要快
2
9.室温下铁块与稀盐酸反应速率较慢,下列措施不能加快反应速率的是( )
A.加适量蒸馏水稀释盐酸 B.用较浓盐酸代替稀盐酸
C.将反应液适当加热 D.将铁块换成铁粉
【课前复习填空答案】
浓度;温度;压强;催化剂;
【知识点填空答案】
快慢程度;反应物浓度;生成物浓度;Δc/Δt,Δn/(V·Δt);某物质浓度的变化;mol·L-1;时间变化;
s、min或h;mol/(L.s);mol·L-1·s-1;计量数之比;a∶b∶c∶d;时间;颜色深浅;显色物质浓度;
反应物的性质;快;慢;气体;快;慢;不变;加快;减小;不变;快;慢;反应放热,温度升高,
反应速率加快;生成物做催化剂;构成原电池。
【练习答案】CBAADC
【检测反馈答案】1-9:BCBBCCDCA