文档内容
第一节 钠及其化合物
第1课时 活泼的金属单质——钠
基础巩固
1.下列关于钠的叙述正确的是
A.钠在自然界中存在游离态 B.钠是一种灰色的固体
C.钠可以保存在煤油中 D.钠着火时可以用水扑灭
【答案】C
【解析】
A.钠的性质活泼,易与空气中的水、氧气反应,在自然界中以化合态存在,自然界中不存在游离态,故
A错误;
B.钠是银白色的金属,故B错误;
C.钠与煤油不反应,且密度比煤油大,可保存在煤油中,沉在底部,煤油隔绝了空气,故C正确;
D.钠与水剧烈反应,生成氢气,钠着火时不能用水扑灭,可以用沙子隔绝空气盖灭,故D错误;
答案为C。
2.下列关于钠的叙述中,不正确的是
A.钠燃烧时发出黄色火焰 B.钠燃烧时生成氧化钠
C.钠具有很强的还原性 D.钠原子的最外电子层上只有1个电子
【答案】B
【解析】
A.钠元素焰色试验显黄色,因此金属钠燃烧时发出黄色火焰,A正确;
B.钠在室温下被氧气氧化产生氧化钠,在加热时发生燃烧产生过氧化钠,B错误;
C.Na是11号元素,原子核外电子排布是2、8、1,由于原子最外层只有1个电子,Na原子半径比较大,
最外层电子受到的吸引力比较小,容易失去,因此钠具有很强的还原性,C正确;
D.Na是11号元素,原子核外电子排布是2、8、1,故钠原子的最外电子层上只有1个电子,D正确;
故合理选项是B。
3.将一小块金属钠投入滴有紫色石蕊试液的盛冷水的烧杯中,甲同学认为可以观察到下列实验现象,
其中正确的有
①钠投入水中,先沉入水底,后浮出水面 ②钠立即与水反应,并有气体产生 ③反应后溶液变红
色 ④钠熔化成光亮的小球 ⑤小球在水面上迅速游动 ⑥有“嘶嘶”的响声发出
A.①②③④ B.②③④⑤
C.②④⑤⑥ D.③④⑥
【答案】C
【解析】
钠投入水中,不是沉入水底,而是浮在水面上;钠与水反应生成 NaOH,溶液呈碱性,使紫色石蕊试液变
蓝。
学科网(北京)股份有限公司4.等质量的两块金属钠,第一块在足量氧气中加热,第二块在氧气中(常温下)充分反应,则下列说法正
确的是
A.第一块钠失去电子多
B.两块钠失去电子一样多
C.第二块钠的生成物质量最大
D.两块钠的生成物质量一样多
【答案】B
【解析】
A.两块钠的质量相等,则物质的量也相等,在反应中,钠显+1价,所以在反应中转移电子数是一样多的,
故A错误;
B.由A可知,B正确;
C.钠在足量氧气中加热生成的是过氧化钠,在常温下反应生成的是氧化钠。两块钠物质的量相等,生成
的Na O、Na O 的物质的量也相等,Na O 的摩尔质量比Na O大,所以生成的Na O 的质量比生成的Na O
2 2 2 2 2 2 2 2 2
大,故C错误;
D.由C可知,D错误;
故选B。
5.已知: ,用等质量的金属钠进行下列实验,其中生成氢气最多
的是
A.把钠放入足量稀盐酸中 B.将钠用铝箔包好并刺些小孔,再放入水中
C.把钠放入硫酸铜溶液中 D.把钠放入足量水中
【答案】B
【解析】
少量钠与稀盐酸、硫酸铜溶液、水反应的化学方程式分别是 、
、 。由方程式可知钠和生成氢气
的关系为 ,三者生成氢气的物质的量相同。若将钠用铝箔包好并刺些小孔,再放入水中反应,
化学方程式为 、 ,除钠和水反应生成
的氢气外,反应生成的氢氧化钠还与铝反应生成氢气,则放出的氢气要比钠与稀盐酸、硫酸铜溶液和水
反应的多,故用等质量的金属钠进行上述实验,其中生成氢气最多的是将钠用铝箔包好并刺些小孔,再
放入水中,因此合理选项是B。
6.不能正确表示下列反应离子方程式的是
A.钠与水反应:2Na+2H O=2Na++2OH-+H ↑
2 2
B.钠与硫酸铜溶液反应:2Na+Cu2+=Cu+2Na+
C.钠与盐酸反应:2Na+2H+=2Na++H ↑
2
D.钠跟氯化钾溶液反应:2Na+2H O=2Na++2OH-+H ↑
2 2
【答案】B
【解析】
学科网(北京)股份有限公司A.钠与水反应的离子反应为2Na+2H O=2Na++2OH-+H ↑,故A正确;
2 2
B.钠与硫酸铜溶液反应实质是钠与水先反应生成氢氧化钠和氢气,氢氧化钠再与硫酸铜反应产生蓝色氢
氧化铜沉淀,反应的离子反应为:2H O+Cu2++2Na=2Na++Cu(OH) ↓+H ↑,故B错误;
2 2 2
C.钠盐酸反应实质上是钠与盐酸电离的氢离子反应生成氢气:2Na+2H+=2Na++H ↑,故C正确;
2
D.钠跟氯化钾溶液反应,本质为钠与水反应:2Na+2H O=2Na++2OH-+H ↑,故D正确;
2 2
故选B。
7.将金属钠投入盛有下列溶液的小烧杯中,既有气体生成,又有白色沉淀产生的是(不考虑反应中溶液温
度的变化)
①MgSO 溶液 ②NaCl溶液 ③Na SO 溶液 ④饱和Ca(OH) 溶液 ⑤CuSO 溶液 ⑥饱和NaCl溶液
4 2 4 2 4
⑦Fe (SO ) 溶液
2 4 3
A.①②④ B.②③⑥ C.①④⑥ D.④⑤⑥
【答案】C
【解析】
将钠投入碱或盐的溶液中,钠首先和水反应生成NaOH和H ,反应方程式为2Na+2H O=2NaOH+H ↑,
2 2 2
NaOH和部分盐能发生复分解反应,根据产物的可溶性判断即可。
①中NaOH再与MgSO 发生反应产生Mg(OH) 白色沉淀,既有气体生成,又有白色沉淀产生。①符合题意;
4 2
②钠与氯化钠溶液中的水反应生成NaOH和氢气,NaOH与NaCl不反应,不能得到沉淀,②不符合题意;
③钠与硫酸钠溶液反应只生成氢气,不能达到沉淀,③不符合题意;
④钠与溶液中水反应产生NaOH和H ,由于水减少,则有Ca(OH) 不能完全溶解而析出,产生白色沉淀,
2 2
④符合题意;
⑤中NaOH与CuSO 溶液反应生成蓝色的Cu(OH) 沉淀,⑤不符合题意;
4 2
⑥中由于水减少,则有NaCl析出,⑥符合题意;
⑦中OH-与Fe3+反应生成Fe(OH) 红褐色沉淀,⑦不符合题意;
3
综上所述可知:将金属钠投入相应溶液中,既有气体生成,又有白色沉淀产生的序号是①④⑥,故合理
选项是C。
8.在蒸发皿中放入一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO 与熔化的钠接触,瞬间产生
4
耀眼的火花,同时有红色物质生成。下列说法中不正确的是
A.上述反应是置换反应
B.上述反应是放热反应
C.上述反应中无水CuSO 表现了还原性
4
D.加热且无水条件下,Na可以与CuSO 反应并生成Cu
4
【答案】C
【解析】
A.钠比铜活泼,在无水条件下,Na可以与CuSO 反应并生成Cu,属于置换反应,A正确;
4
B.根据以上分析,反应是放热反应,B正确;
C.根据以上分析,钠作还原剂,硫酸铜作氧化剂,所以CuSO 表现了氧化性, C错误;
4
D.根据以上分析,在无水、加热至熔化下,Na可以与CuSO 发生置换反应生成Cu,D正确;
4
学科网(北京)股份有限公司故答案为:C。
9.在实验室里为了研究钠的性质,做了如下实验:
(1)取用浸没在煤油中的金属钠的操作方法是_______。
(2)取一块金属钠放在燃烧匙里加热,观察到下列实验现象:①金属先熔化 ②在空气中燃烧,放出黄色
火花 ③燃烧后得白色固体 ④燃烧时火焰为黄色 ⑤燃烧后生成淡黄色固体,描述正确的是_______。
A.①② B.①②③ C.①③ D.①④⑤
(3)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中轻缓的加入一绿豆大小的金属钠,可
能观察到的现象符合图中的_______。
(4)将一小块钠投入到FeCl 溶液中,发生反应的有关化学方程式为_______。
3
【答案】 用镊子取出钠块,用滤纸吸干钠块表面的煤油,在玻璃片上用小刀切去表面的氧化层,
再切下一小粒备用,余下的钠全部放回试剂瓶中 D A 2Na+2H O=2NaOH+H ↑,
2 2
3NaOH+FeCl =Fe(OH) ↓+3NaCl
3 3
【解析】
(1)钠保存在煤油中,沉在煤油的底部,取用时需用镊子夹取一小块钠,然后用滤纸吸干表面的煤油,再
用小刀切去表面的氧化膜,切一小块内部的钠备用,剩余的钠要放回原试剂瓶中保存,故答案为:用镊
子取出钠块,用滤纸吸干钠块表面的煤油,在玻璃片上用小刀切去表面的氧化层,再切下一小粒备用,
余下的钠全部放回试剂瓶中;
(2) 金属钠放在燃烧匙里加热,因其熔点较低,受热首先会熔化成小球,继续加热钠会燃烧,火焰呈黄色,
燃烧生成淡黄色的过氧化钠固体,故答案为:D;
(3)煤油和水互不相溶,且煤油的密度小于水,两者分层,煤油在上层,加入钠后,因钠的密度比煤油大,
比水的小,因此钠处于煤油和水的交界处,与水反应生成气泡,因此正确的是A,故答案为:A。
(4) 钠投入到FeCl 溶液中,首先发生与水的反应生成氢氧化钠和氢气,反应为:2Na+2H O=2NaOH+H ↑,
3 2 2
生成的氢氧化钠再与氯化铁反应生成氢氧化铁,反应为:3NaOH+FeCl =Fe(OH) ↓+3NaCl,故答案为:
3 3
2Na+2H O=2NaOH+H ↑,3NaOH+FeCl =Fe(OH) ↓+3NaCl;
2 2 3 3
10.如图是有关钠与水反应及产物检验的实验装置。实验开始时先向管内加入滴有酚酞试液的水,使水
位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时Na掉入水中。回答下列问题:
学科网(北京)股份有限公司(1)钠与水反应的化学方程式为_____________。
(2)钠与水反应的现象有很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是_________。
②能证明钠的熔点低的现象是_________。
③能证明有氢氧化钠生成的现象是__________。
④能证明有气体产生的现象是A端液面________(填“上升”“下降”或“不变”,下同),B端液面
________。
【答案】 2Na+2H O=2NaOH+H ↑ 钠浮在水面上 钠熔化为光亮的小球 溶液
2 2
呈红色 上升 下降
【解析】
本题主要考查金属钠和水的反应,该反应的现象为“浮”、“响”、“游”、“熔”、“红”。“浮”
指钠块浮在水面上;“响”是因为反应放热,且不断有H 生成;“游”是产生的H 不断推动钠块来回移
2 2
动;“熔”是因为钠块的熔点很低,反应放热使钠块熔化;“红”是因为反应生成了NaOH,使事先加入
的酚酞变红。
(1)钠与水反应生成NaOH和H ,其化学方程式为:2Na+2H O=2NaOH+H ↑;
2 2 2
(2)①钠浮在水面上,证明钠的密度比水小;
②钠熔化为光亮的小球,证明钠的熔点低;
③反应后溶液呈红色,证明有氢氧化钠生成;
④B端压强增大,液面下降,A端液面上升,证明有气体生成。
能力提升
11.将钠和碳分别置于如图所示的两个盛满足量氧气的集气瓶中燃烧完毕后,恢复到起始温度,再同时
打开装置中的两个止水夹,这时观察到
A.水进入左瓶 B.水进入右瓶
C.水同时进入两瓶 D.水不进入任何一瓶
【答案】A
【解析】
钠与氧气反应生成过氧化钠固体,化学反应为2Na+O Na O ,燃烧后左瓶内气体体积减少,压强减小;
2 2 2
学科网(北京)股份有限公司碳与氧气反应生成二氧化碳气体,化学反应为C+O CO ,右瓶内气体体积变化不大,压强变化不大;
2 2
故燃烧完毕后同时打开装置中的两个活塞,水只会进入左瓶中,答案选A。
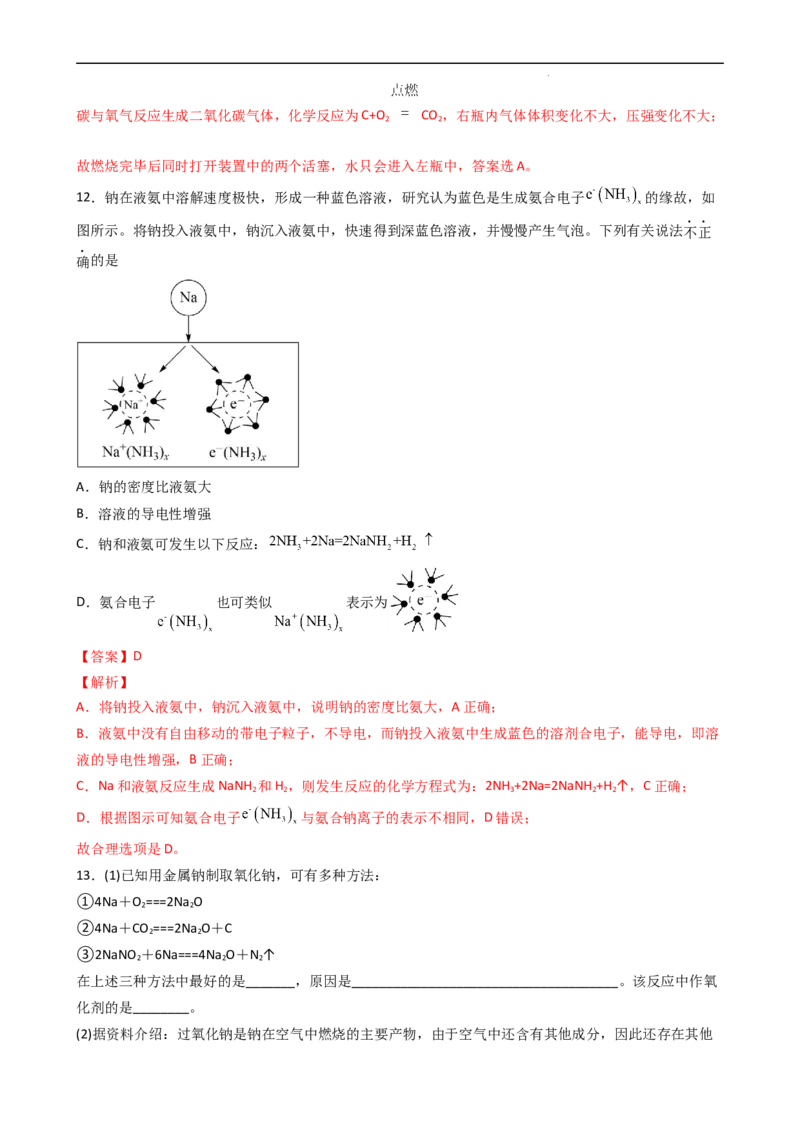
12.钠在液氨中溶解速度极快,形成一种蓝色溶液,研究认为蓝色是生成氨合电子 的缘故,如
图所示。将钠投入液氨中,钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列有关说法不正
确的是
A.钠的密度比液氨大
B.溶液的导电性增强
C.钠和液氨可发生以下反应:
D.氨合电子 也可类似 表示为
【答案】D
【解析】
A.将钠投入液氨中,钠沉入液氨中,说明钠的密度比氨大,A正确;
B.液氨中没有自由移动的带电子粒子,不导电,而钠投入液氨中生成蓝色的溶剂合电子,能导电,即溶
液的导电性增强,B正确;
C.Na和液氨反应生成NaNH 和H ,则发生反应的化学方程式为:2NH +2Na=2NaNH +H ↑,C正确;
2 2 3 2 2
D.根据图示可知氨合电子 与氨合钠离子的表示不相同,D错误;
故合理选项是D。
13.(1)已知用金属钠制取氧化钠,可有多种方法:
①4Na+O ===2Na O
2 2
②4Na+CO ===2Na O+C
2 2
③2NaNO +6Na===4Na O+N ↑
2 2 2
在上述三种方法中最好的是_______,原因是______________________________________。该反应中作氧
化剂的是________。
(2)据资料介绍:过氧化钠是钠在空气中燃烧的主要产物,由于空气中还含有其他成分,因此还存在其他
学科网(北京)股份有限公司产物,如氮化钠。已知氮化钠与水反应能生成氢氧化钠和氨气,则氮化钠与水反应的化学方程式为
____________________________。
【答案】 ③ 此反应中产物只有Na O是固体,而另一产物N 可以把周围环境中的氧气
2 2
排干净,使得Na O不能继续被氧化成Na O NaNO Na N+3H O===3NaOH+NH ↑
2 2 2 2 3 2 3
【解析】
(1)方法①钠与氧气反应时,总会伴随有2Na+O =2Na O ,引入Na O 杂质,故不适合方法①。
2 2 2 2 2
方法②首先是产物中混有碳杂质,且生成的Na O会与CO 反应生成Na CO ,故此方法也不好。
2 2 2 3
方法③,此反应中产物只有Na O是固体,而另一产物N 可以把周围环境中的氧气排干净,使得Na O不
2 2 2
能继续被氧化成Na O 。
2 2
故方法③最好
方法③反应中Na的化合价升高,NaNO 中N的化合价降低,所以NaNO 为氧化剂。
2 2
故答案分别是③ ; 此反应中产物只有Na O是固体,而另一产物N 可以把周围环境中的氧气排干净,使
2 2
得Na O不能继续被氧化成Na O ; NaNO 。
2 2 2 2
(2)由提示可知反应方程式为Na N+3H O===3NaOH+NH ↑
3 2 3
14.现用金属钠和空气制备纯度较高的NaO ,可利用的装置如图所示。回答下列问题[已知NaO 易与
2 2 2 2
空气中CO、HO(g)反应]:
2 2
(1) 装 置 Ⅳ 中 盛 放 的 试 剂 是 ____________ , 其 作 用 是
___________________________________________________________________________________________
_______________。
(2)若规定气体的气流方向从左到右,则组合实验装置时各件仪器的正确连接顺序为(按从左到右顺
序写明仪器的编号Ⅰ、Ⅱ……)________________,各仪器接口的标号字母(a、b……)顺序是空气进入
________,________接________,________接________,________接________。
(3)装置Ⅱ的作用是_____________________。
(4)操作中通空气和加热的顺序为________。
【答案】(1)氢氧化钠溶液 吸收导入空气中的二氧化碳
(2)Ⅳ、Ⅲ、Ⅰ、Ⅱ h g f e a(或b) b(或a) c
(3)防止空气中的水分和二氧化碳进入装置Ⅰ
(4)先通一段时间的空气,再加热Ⅰ装置
【解析】 用金属钠和空气制备纯度较高的NaO ,要避免生成的NaO 与空气中的水分和二氧化碳发
2 2 2 2
生反应,在制取过程中要除去这两种杂质,且要防止外界空气中的水分和二氧化碳倒吸进入装置。
(1)由上述分析可知,应该除去空气中的CO,故Ⅳ中的试剂为氢氧化钠溶液。
2
(2)由上述分析可知,实验的顺序为除CO→除水蒸气→与钠反应→避免CO 、水蒸气进入反应装置,
2 2
故装置顺序为Ⅳ→Ⅲ→Ⅰ→Ⅱ,接口顺序为hgfeabc或hgfebac。
(3)装置Ⅱ的作用是避免空气中的CO、水蒸气进入反应装置Ⅰ。
2
(4)为防止NaO 与CO、水蒸气反应,应先排尽空气,再加热金属钠。
2 2 2
学科网(北京)股份有限公司学科网(北京)股份有限公司