文档内容
第二章 烃
第二节 烷烃
2.1.1 烷烃的结构和性质
1. 了解烷烃物理性质的变化与分子中碳原子数目的关系
2. 认识烷烃的结构特征,以典型物为例,理解烷烃的化学性质,
教学重点:依据甲烷的结构和性质认识烷烃的结构和性质
教学难点:依据甲烷的结构和性质认识烷烃的结构和性质
【复习回顾】
1. 烃:仅含 两种元素的有机化合物。
2. 根据其结构不同,烃可分为 等。
3. 烃中 ,是预测化学反应中烃分子可能的断键
部位与相应反应类型的依据。
【学生活动一】
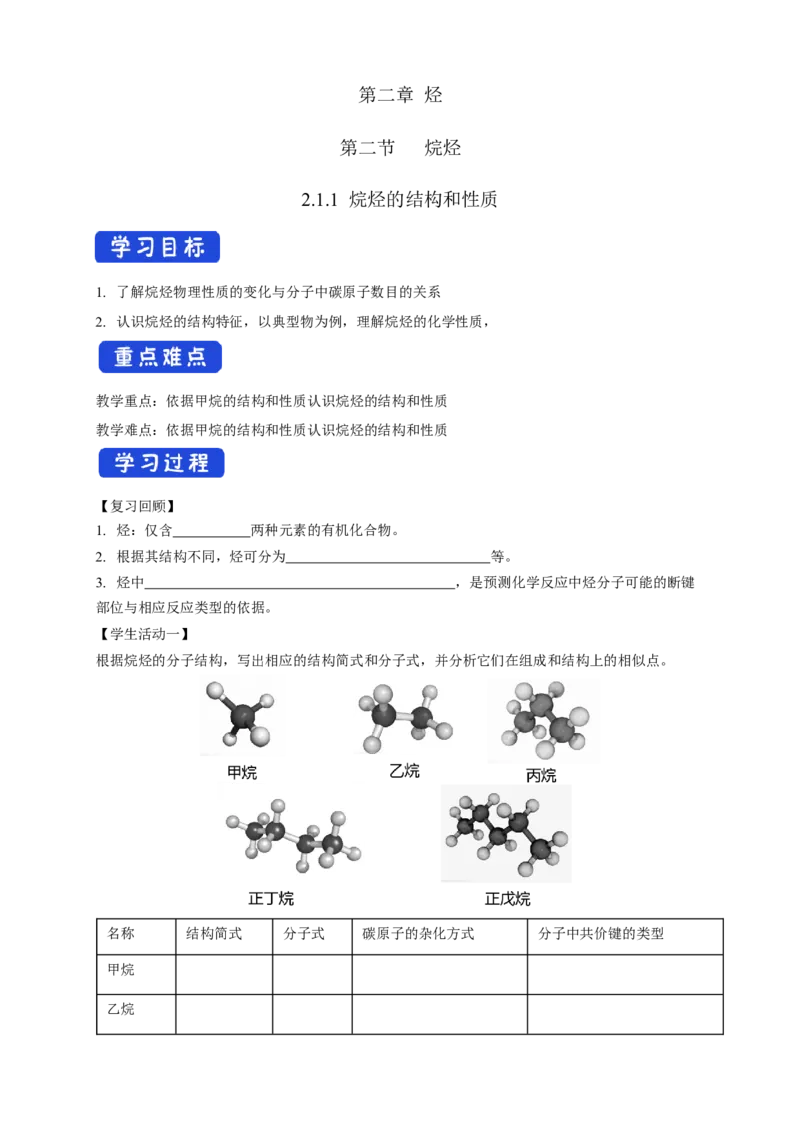
根据烷烃的分子结构,写出相应的结构简式和分子式,并分析它们在组成和结构上的相似点。
名称 结构简式 分子式 碳原子的杂化方式 分子中共价键的类型
甲烷
乙烷丙烷
正丁烷
正戊烷
总结:
1. 烷烃的结构与甲烷的相似,其分子中的碳原子都采取 杂化,以伸向四面体四个顶点
方向的sp3杂化轨道与其他碳原子或氢原子结合,形成 。烷烃分子中的共价键全部是
。
2. 同系物:像甲烷、乙烷、丙烷这些结构相似、分子组成上相差 的化合物
互称为同系物,烷烃同系物的通式: 。
【复习回顾】
1. 甲烷
(1) 物理性质:纯净的甲烷是 、 的气体, 溶于水,密度比空气的
。
(2) 化学性质:
①化学性质比较 ,常温下 被酸性高锰酸钾溶液氧化,也 与强酸强碱及溴的
四氯化碳溶液反应。
②能在空气中 。
③能在光照下与氯气发生 。
【学生活动二】
阅读教材表2-1几种烷烃的熔点、沸点和密度。分析烷烃的密度、熔点和沸点等物理性质变化的基
本规律。
总结:
1. 烷烃同系物的某些物理性质随着 的增大而发生规律性变化,随烷烃碳原子的
增多,烷烃的熔点和沸点逐渐 ,密度逐渐 ,常温下的存在状态也由气态逐渐过渡
到液态、固态。
2. 所有烷烃均 溶于水,密度均 1。
【学生活动三】
1.根据甲烷的性质推测烷烃可能具有的性质,填写下表。
与酸性高锰 与溴的四氯化 与强酸、 与氯气(在
颜色 溶解性 可燃性
酸钾溶液 碳溶液 强碱溶液 光照下)
2.根据甲烷的燃烧反应,写出汽油的成分之一辛烷(C H )完全燃烧的化学方程式。
8 18
3.根据甲烷与氯气的反应,写出乙烷与氯气反应生成一氯乙烷的化学方程式。指出该反应的反应类
型,并从化学键和官能团的角度分析反应中有机化合物。
4.乙烷与氯气在光照下反应,可能生成哪些产物?请写出它们的结构简式。总结:
烷烃的化学性质
(1)稳定性
常温下烷烃很不活泼,与强酸、强碱、强氧化剂等都 发生反应,只有在特殊条件(如光照或
高温)下才能发生某些反应。
(2)特征反应——取代反应
烷烃可与卤素单质在光照下发生 生成卤代烃和卤化氢。
(3)氧化反应——可燃性
烷烃可在空气或氧气中完全燃烧生成CO 和HO,燃烧的通式为:
2 2
(4)分解反应——高温裂化或裂解
烷烃受热时会分解,生成含碳原子数较少的烷烃和烯烃,如:
C H C H +C H 。
16 34 8 16 8 18
1. 下列有关烷烃的叙述中,正确的是
在烷烃分子中,所有的化学键都是单键
烷烃中除甲烷外,很多都能使酸性 溶液的紫色褪去
分子通式为 的烃不一定是烷烃
所有的烷烃在光照条件下都能与氯气发生取代反应
光照条件下,乙烷通入溴水中,可使溴水褪色
所有的烷烃都可以在空气中燃烧
A. B. C. D.
2. 用氯气取代相对分子质量为44的烃分子上的一个氢原子,所得的化合物可能有
A. 3种 B. 4种 C. 5种 D. 6种
3. 下列有关烷烃的叙述中,不正确的是( )
A. 在烷烃分子中,所有的化学键都为单键
B. 所有的烷烃在光照条件下都能与氯气发生取代反应
C. 烷烃分子的通式为 ,符合该通式的烃不一定是烷烃
D. 随着碳原子的增加,烷烃的熔、沸点逐渐升高4. 下列说法正确的是
符合分子通式 的烃一定都是烷烃,分子中均只含单键
苯能使溴水褪色,说明苯环结构中含有碳碳双键
与 一定不是同系物
乙烯使溴水褪色属于取代反应
与 是同分异构体
相同质量的烃完全燃烧,耗氧量最大的是
乙烯能使溴水和酸性 溶液褪色,且反应类型相同
A. B. C. D.
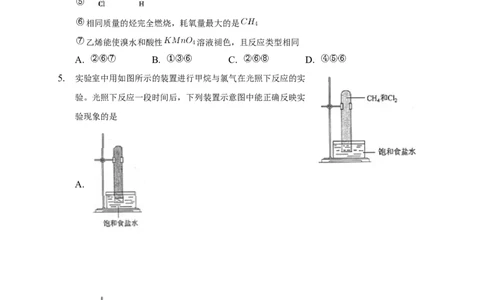
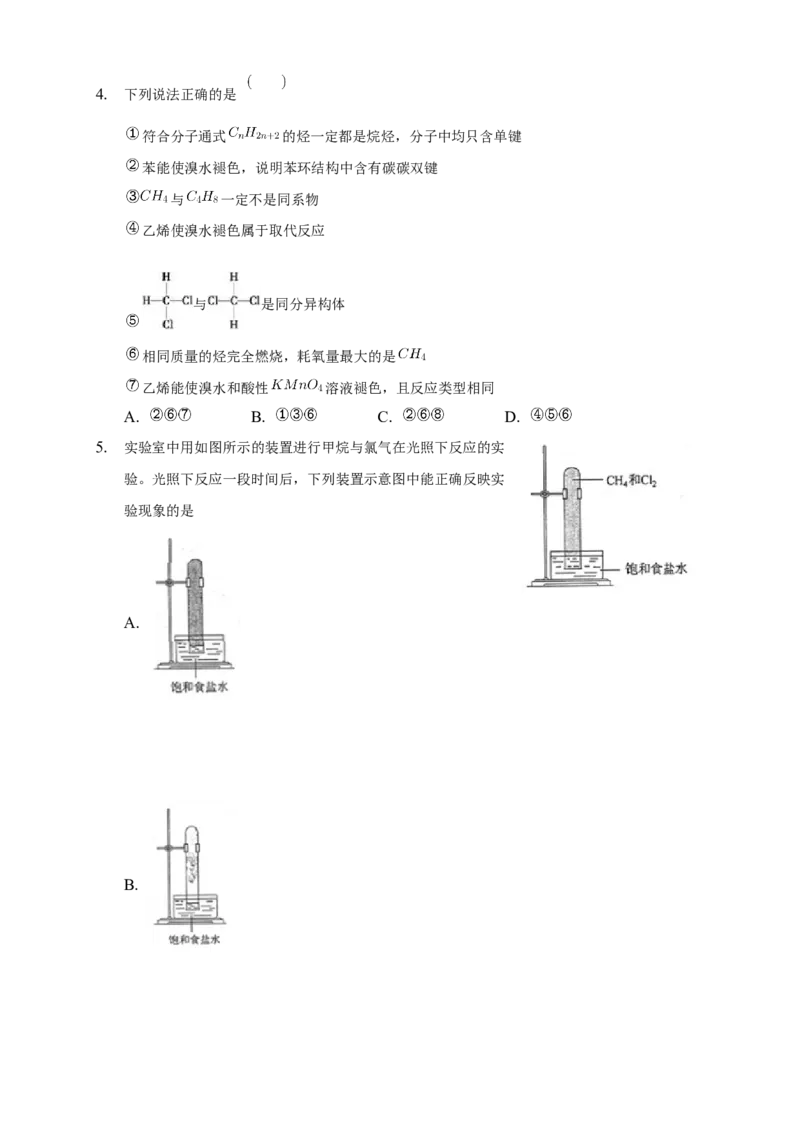
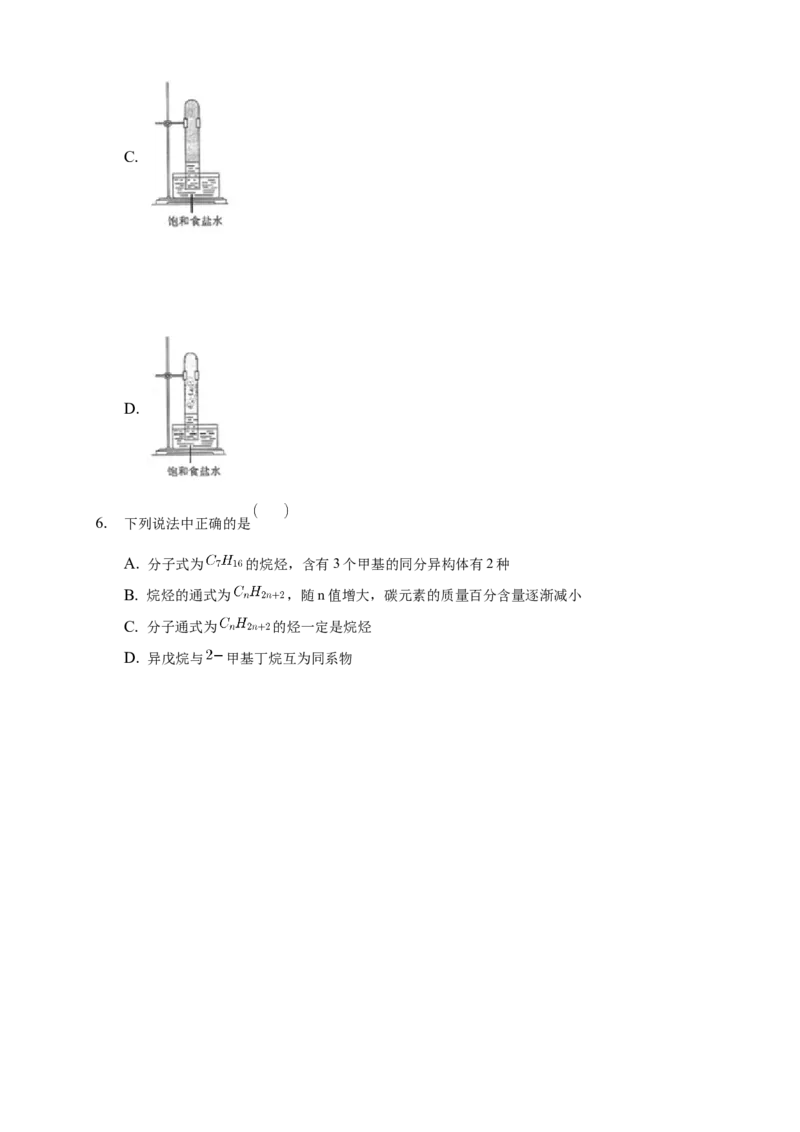
5. 实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实
验。光照下反应一段时间后,下列装置示意图中能正确反映实
验现象的是
A.
B.C.
D.
6. 下列说法中正确的是
A. 分子式为 的烷烃,含有3个甲基的同分异构体有2种
B. 烷烃的通式为 ,随n值增大,碳元素的质量百分含量逐渐减小
C. 分子通式为 的烃一定是烷烃
D. 异戊烷与 甲基丁烷互为同系物