文档内容
第一节 钠及其化合物
第2课时 氧化钠和过氧化钠
基础巩固
1.下列物质和水或二氧化碳反应均能生成氧气的是
A.Na B.NaO C.NaO D.NaHCO
2 2 2 3
【答案】C
【详解】
A.Na和水剧烈反应产生氢氧化钠和氢气,不生成氧气,A项不选;
B.NaO和水反应生成氢氧化钠,不生成氧气,B项不选;
2
C.NaO 和水反应生成氢氧化钠和氧气,和二氧化碳反应生成碳酸钠和氧气,C项选;
2 2
D.NaHCO 不能和水或二氧化碳反应,D项不选;
3
答案选C。
2.为了使宇航员在飞船中得到一个稳定的,良好的生存环境,一般在飞船内安装盛有Na O 或K O 颗粒
2 2 2 2
的装置,它的用途是产生氧气。下列关于Na O 的叙述不正确的是。
2 2
A.Na O 中正负离子的个数比为2:1
2 2
B.Na O 与SO 反应生成Na SO 时,Na O 作氧化剂
2 2 2 2 4 2 2
C.Na O 与CO 反应产生1个 O ,转移电子的个数为4
2 2 2 2
D.Na O 分别与水及CO 反应产生相同量的O 时,需要水和CO 的数目相等
2 2 2 2 2
【答案】C
【解析】
A.Na O 由Na+和 构成,Na O 中正负离子的个数比为2:1,故A正确;
2 2 2 2
B.Na O 与SO 发生反应 ,反应过程中,Na O 中的O元素的化合价由-1价降低到-2
2 2 2 2 2
价,Na O 作氧化剂,故B正确;
2 2
C.Na O 与CO 反应的化学方程式为 , 根据反应的方程式可知,生成1个
2 2 2
O 转移电子数目为2,故C错误;
2
D.Na O 与CO 反应的化学方程式为 ,Na O 分别与水反应的化学方程式为
2 2 2 2 2
,根据反应的方程式可知,产生相同量的O 时,需要水和CO 的数目相等,
2 2
故D正确;
答案选C。
3.下列关于NaO和NaO 的叙述正确的是( )
2 2 2
A.NaO与NaO 均可与盐酸反应,故二者均为碱性氧化物
2 2 2
B.NaO在一定条件下可以转化为NaO
2 2 2
C.NaO与HO的反应属于化合反应,而NaO 与HO的反应属于氧化还原反应,其中NaO 是氧化剂,HO
2 2 2 2 2 2 2 2
是还原剂
学科网(北京)股份有限公司D.在呼吸面具中,NaO常作供氧剂
2
【答案】B
【解析】
A.能与盐酸反应的氧化物不一定是碱性氧化物,还必须考虑生成物是否仅为盐和 HO:NaO+
2 2
2HCl===2NaCl+HO、2NaO+4HCl===4NaCl+2HO+O↑,A项错误;
2 2 2 2 2
B.NaO在一定条件下可以转化为NaO:2NaO+O=====2NaO,B项正确;
2 2 2 2 2 2 2
C.NaO+HO===2NaOH是化合反应(非氧化还原反应),2NaO +2HO===4NaOH+O↑是氧化还原反应,其中
2 2 2 2 2 2
NaO 既是氧化剂又是还原剂,C项错误;
2 2
D.NaO 常作供氧剂,D项错误。
2 2
4.下列有关Na O和Na O 的叙述中,正确的是
2 2 2
A.Na O比Na O 稳定
2 2 2
B.只用水来确定某Na O粉末中是否含有Na O
2 2 2
C.Na O、Na O 分别与CO 反应,产物相同
2 2 2 2
D.将足量的Na O 比Na O分别加到酚酞溶液中,最终溶液均为红色
2 2 2
【答案】B
【解析】
A.Na O在空气中加热时会转化为Na O ,所以Na O 比Na O稳定,故A错误;
2 2 2 2 2 2
B.Na O 与水反应会放出氧气,产生气泡,有明显的现象,所以可用水来确定某Na O粉末中是否含有
2 2 2
Na O ,故B正确;
2 2
C.Na O与CO 反应生成碳酸钠,Na O 与CO 反应生成碳酸钠和氧气,产物不同,故C错误;
2 2 2 2 2
D.Na O、Na O 加到酚酞溶液中,二者均先与溶液中的水反应生成碱而使溶液变为红色,但Na O 具有漂
2 2 2 2 2
白性,溶液最终褪色,故D错误;
选B。
5.下列表示对应化学反应的离子方程式正确的是
A. 溶于水产生 :
B.钠和水反应:
C.氯化镁溶液中加入澄清石灰水:
D.碳酸钙加入过量盐酸中:
【答案】D
【解析】
A. 不能拆写为离子形式,正确的离子方程式为 ,故A错误;;
B.电荷和元素均不守恒,正确的离子方程式为 ,故B错误;
C.澄清石灰水要拆写为离子形式,正确的离子方程式为 ,故C错误;
D.碳酸钙加入过量盐酸生成氯化钙和二氧化碳、水,离子方程式正确,故D正确;
故选D。
学科网(北京)股份有限公司6.下列关于钠及其化合物的说法正确的是
A. 与 都具有强还原性
B. 和 长期露置于空气中最终产物不相同
C.将足量的 、 和 分别加入含有酚酞的水中,最终溶液均变为红色
D.将少量 和 分别投入 溶液中,均既有沉淀生成又有气体放出
【答案】D
【解析】
A.钠具有强还原性,钠失去电子生成钠离子,钠离子没有还原性,只有微弱的氧化性,性质较稳定,A
项错误;
B. 和 长期置于空气中,最终都生成相同的产物: ,B项错误 ;
C. 具有漂白性,故 加入含有酚酞的水中,溶液先变红,最终红色褪去,C项错误;
D.将少量 和 分别投入 溶液中均先和水反应生成氢氧化钠和气体,然后再和硫酸铜生成
氢氧化铜沉淀,D项正确。
故选D。
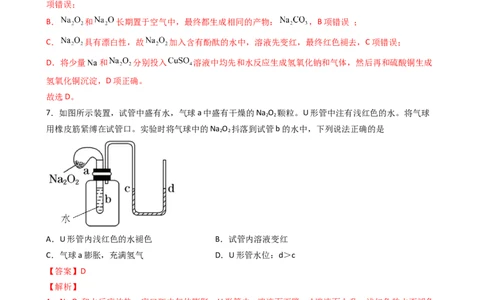
7.如图所示装置,试管中盛有水,气球a中盛有干燥的Na O 颗粒。U形管中注有浅红色的水。将气球
2 2
用橡皮筋紧缚在试管口。实验时将气球中的Na O 抖落到试管b的水中,下列说法正确的是
2 2
A.U形管内浅红色的水褪色 B.试管内溶液变红
C.气球a膨胀,充满氢气 D.U形管水位:d>c
【答案】D
【解析】
A.Na O 和水反应放热,广口瓶内气体膨胀,U形管内c端液面下降、d端液面上升,浅红色的水不褪色,
2 2
故A错误;
B.Na O 和水反应生成氢氧化钠和氧气,试管内溶液不变色,故B错误;,
2 2
C.Na O 和水反应生成氢氧化钠和氧气,气球a膨胀,充满氧气,故C错误;
2 2
D.Na O 和水反应放热,广口瓶内气体膨胀,U形管内c端液面下降、d端液面上升,U形管水位:d>
2 2
c,故D正确;
选D。
8.10.现有2.3 g纯净的金属钠在干燥的空气中被氧化后得到3.5 g固体,由此判断其产物是 ( )
A.只有氧化钠 B.只有过氧化钠
学科网(北京)股份有限公司C.氧化钠和过氧化钠 D.无法确定
【答案】C
【解析】若2.3 g钠全部生成氧化钠,质量为3.1 g;若2.3 g钠全部生成过氧化钠,质量为3.9 g,因为3.1 g<3.5
g<3.9 g,氧化产物应为氧化钠和过氧化钠的混合物。
9.小明在课堂上进行了化学魔术小实验“滴水生火”“吹气生火”,如图所示:
(1)脱脂棉 (用化学方法处理的棉花)易着火燃烧。用脱脂棉包裹的过氧化钠“滴水生火”,其原理是什么?
___________
(2)用脱脂棉包裹的过氧化钠“吹气生火”,其原理是什么?___________
【答案】(1)Na O 与水反应生成NaOH和O ,同时放出大量的热,使脱脂棉达到着火点而着火燃烧。
2 2 2
(2)人呼出的气体中含有CO 、H O(g),二者均与Na O 反应生成O ,并放出大量的热促使脱脂棉着火燃烧。
2 2 2 2 2
【解析】
过氧化钠可与水或二氧化碳发生反应产生氧气,且反应放热。物质燃烧需满足:可燃物、助燃剂如氧气
还有温度达到物质着火点以上三个条件,据悉结合过氧化钠的化学性质分析。
(1)Na O 与水反应生成NaOH和O ,同时放出大量的热,使脱脂棉达到着火点而着火燃烧,可解释“滴水
2 2 2
生火”的原理。
(2)人呼出的气体中含有CO 、H O(g),二者均与Na O 反应生成O ,并放出大量的热促使脱脂棉着火燃烧,
2 2 2 2 2
这就是过氧化钠“吹气生火”的原理。
10.金属钠是一种性质活泼的银白色金属,学习小组观察到金属钠在表面皿上发生的一系列变化为:银
白色断面→断面变暗→断面变白色→出现小液滴伴有气泡→白色固体→白色粉末
回答下列问题:
(1)实验室少量的钠保存在___________中。
(2)“断面变暗”发生反应的化学方程式是___________。
(3)“出现小液滴”的过程属于___________(填“物理变化”或“化学变化”),“伴有气泡”反应的离子方
程式为___________。
(4)最终白色粉末为___________(填化学式),该物质溶于水的电离方程式为___________。
【答案】(1)煤油 (2) (3) 物理变化
(4)
【解析】
(1)实验室少量的钠保存在煤油中;
(2)“断面变暗”是Na和氧气反应生成Na O,化学方程式为 ;
2
(3)Na O可以和空气中的水蒸气反应,出现小液滴是空气中的水蒸气液化,是物理变化;Na和空气中的水
2
学科网(北京)股份有限公司反应生成NaOH和H ,离子方程式为 ;
2
(4)Na O、Na和水反应生成NaOH,白色固体为NaOH,NaOH可以和空气中的水、二氧化碳反应生成
2
NaHCO ,NaHCO 和CO 反应生成Na CO ,则最终白色粉末为 ; 是强电解质,溶于水的电
3 3 2 2 3
离方程式为 。
能力提升
11.向NaO 与HO反应后所得溶液中滴加酚酞溶液,酚酞先变红后褪色。某小组欲探究其原因,进行如
2 2 2
图所示实验:①取反应后的溶液加入MnO 后迅速产生大量气体且该气体能使带火星的木条复燃;实验
2
②③中红色均不褪去。下列分析错误的是( )
A.NaO 与HO反应产生的气体为O
2 2 2 2
B.NaO 与HO反应需要MnO 作催化剂
2 2 2 2
C.实验②③证明使酚酞褪色的不是NaOH和O
2
D.NaO 与HO反应可能生成了具有强氧化性的HO
2 2 2 2 2
【答案】B
【解析】
NaO 与HO反应产生的气体为O,A项正确;
2 2 2 2
NaO 与HO反应不需要催化剂,双氧水分解需要MnO 作催化剂,B项错误;
2 2 2 2
实验②③作为对照实验,能证明使酚酞褪色的不是NaOH和O,C项正确;
2
根据向反应后所得溶液中加入MnO 后迅速产生大量气体且该气体能使带火星的木条复燃,可判断NaO 与
2 2 2
HO反应可能生成了具有强氧化性的HO,D项正确。]
2 2 2
12.将CO 和O 的混合气体7.6g通入Na O ,充分反应后,气体质量变为4.8g,原混合气体中O 的质量
2 2 2 2 2
是( )
A.6.4g B.3.2g C.1.6g D.0.8g
【答案】B
【解析】将CO 和O 的混合气体7.6g通入Na O ,发生下列反应: ,消
2 2 2 2
耗2mol(即88g)二氧化碳,气体质量减少2 44g- 32g=56g,则参与反应的二氧化碳质量为(7.6g-4.8g)
× =4.4g,原混合气体中O 的质量是7.6g-4.4g=3.2g,答案选B。
2
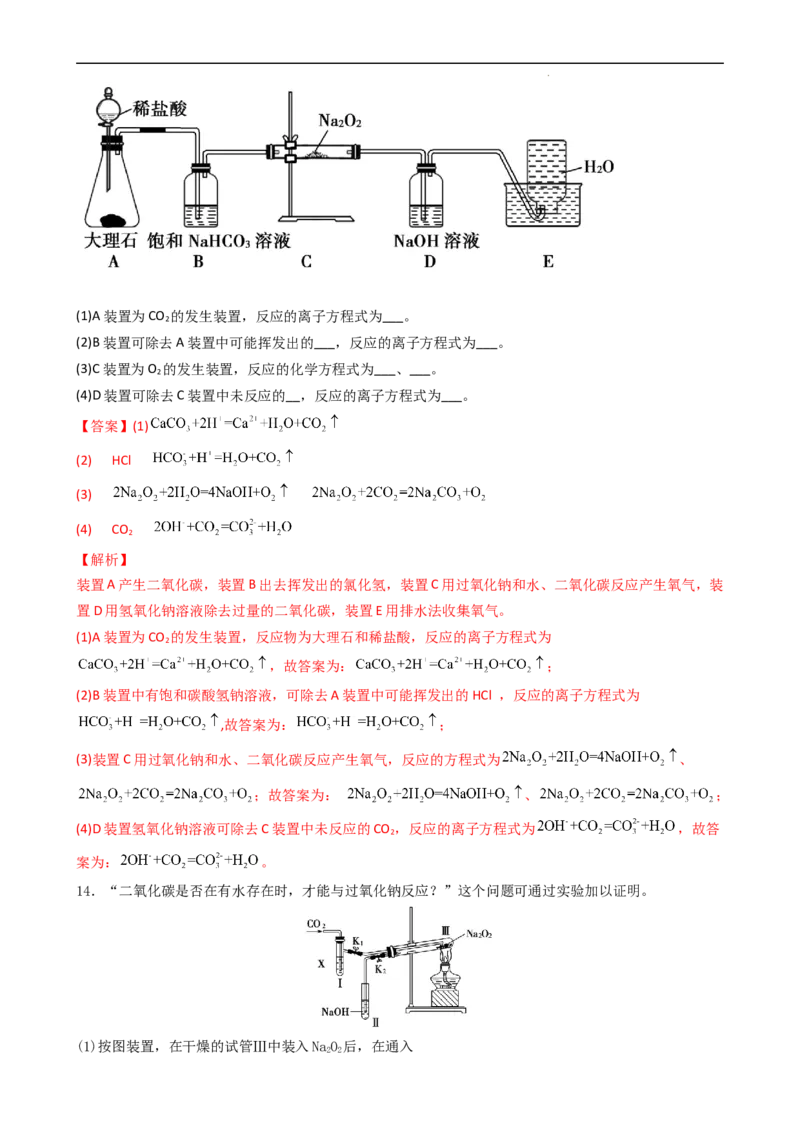
13.19.如图是实验室研究潜水艇中供氧体系反应机理的装置图(夹持仪器略)。
学科网(北京)股份有限公司(1)A装置为CO 的发生装置,反应的离子方程式为___。
2
(2)B装置可除去A装置中可能挥发出的___,反应的离子方程式为___。
(3)C装置为O 的发生装置,反应的化学方程式为___、___。
2
(4)D装置可除去C装置中未反应的__,反应的离子方程式为___。
【答案】(1)
(2) HCl
(3)
(4) CO
2
【解析】
装置A产生二氧化碳,装置B出去挥发出的氯化氢,装置C用过氧化钠和水、二氧化碳反应产生氧气,装
置D用氢氧化钠溶液除去过量的二氧化碳,装置E用排水法收集氧气。
(1)A装置为CO 的发生装置,反应物为大理石和稀盐酸,反应的离子方程式为
2
,故答案为: ;
(2)B装置中有饱和碳酸氢钠溶液,可除去A装置中可能挥发出的HCl ,反应的离子方程式为
,故答案为: ;
(3)装置C用过氧化钠和水、二氧化碳反应产生氧气,反应的方程式为 、
;故答案为: 、 ;
(4)D装置氢氧化钠溶液可除去C装置中未反应的CO ,反应的离子方程式为 ,故答
2
案为: 。
14.“二氧化碳是否在有水存在时,才能与过氧化钠反应?”这个问题可通过实验加以证明。
(1)按图装置,在干燥的试管Ⅲ中装入NaO 后,在通入
2 2
学科网(北京)股份有限公司CO 之前,应事先用弹簧夹(K、K)夹持好,目的是_______。
2 1 2
(2)试管Ⅰ内的试剂X是________时,打开弹簧夹K 、K ,加热试管Ⅲ约5分钟后,将带火星的小木条插
1 2
入试管Ⅱ的液面上,可观察到带火星的小木条不能复燃,且Ⅲ内淡黄色粉末未发生变化。则所得的结论
是________________________________________。
(3) 试 管 Ⅰ 内 试 剂 为 CO 饱 和 水 溶 液 时 , 其 他 操 作 同 (2) , 通 过
2
___________________________________________________________________________________________
_______________的现象,可以证明NaO 与潮湿的CO 能反应且放出O。
2 2 2 2
[答案] (1)防止试管Ⅲ内的过氧化钠和外界相通时发生吸潮现象
(2)浓硫酸 过氧化钠与干燥的CO 不反应
2
(3)带火星的小木条在试管Ⅱ的液面上复燃且剧烈燃烧,同时,Ⅲ内固体由淡黄色变为白色
[解析] (1)本题旨在利用对比实验,探究NaO 与CO 反应的环境,故实验步骤中,首先让NaO 与干燥
2 2 2 2 2
CO 反应,必须保证整个环境中不能有HO进入。(2)根据题意可看出此时应当提供干燥二氧化碳,故试管
2 2
Ⅰ内的试剂X是浓硫酸。
学科网(北京)股份有限公司学科网(北京)股份有限公司