文档内容
第二节 氯及其化合物
第1课时 氯气的性质
基础巩固
1.下列说法不正确的是( )
A.氯原子的最外层电子数为7,易得电子,表现氧化性
B.Cl 在化学反应中只能作氧化剂
2
C.Cl 与Fe、H 反应时均表现氧化性
2 2
D.Cl 与HO反应生成两种酸
2 2
【答案】B
【解析】Cl 在化学反应时可以作氧化剂也可以作还原剂,B不正确。
2
2.下列有关氯气的叙述中,不正确的是( )
A.氯气是一种黄绿色、有刺激性气味的气体
B.氯气、液氯是同一种物质
C.氯气不能溶于水
D.氯气是一种有毒的气体
【答案】C
【解析】Cl 能溶于水,1体积水大约能溶解2体积Cl。
2 2
3.下列关于氯气的叙述正确的是
A.燃烧不一定有氧气参加
B.红热的铜丝可以在氯气中燃烧,产生棕黄色烟雾
C.H 在Cl 中安静燃烧,产生苍白色火焰,形成白色烟雾
2 2
D.通常状况下氯气能和Fe反应,氯气的储存不能用铁质容器
【答案】A
【解析】
A.燃烧是剧烈的发光发热的氧化反应,不一定有氧气参加,比如氢气在氯气中燃烧,故A正确;
B.CuCl 为固体小颗粒,产生棕黄色的烟,没有雾,故B错误;
2
C.生成的HCl极易溶于水,与空气中的水蒸气形成盐酸小液滴,是白色的雾,故C错误;
D.铁和氯气在点燃的条件下发生反应,常温条件下不反应,故常温下可以用钢瓶来储存氯气,故D错误。
故选A。
4.下列关于氯水的叙述中,正确的是
A.新制氯水中只含Cl 和HO分子
2 2
B.液氯与氯水都是纯净物
C.新制氯水的颜色为浅黄绿色
D.氯水经光照有气泡逸出,该气体为HCl
【答案】 C
【解析】 A.新制的氯水因其含Cl 而呈淡绿色,其中还含有HClO和HO分子,故A错误;
2 2
B.液氯是纯净物,氯水是混合物,故B错误;
C.新制的氯水因其含Cl 而呈淡绿色,故C正确;
2
学科网(北京)股份有限公司D.氯水由于其中的HClO见光易分解:2HClO 2HCl+O↑,所以氯水经光照有O 气泡逸出,故D错误。
2 2
故选C。
5.下列对新制氯水与久置氯水性质的叙述正确的是( )
A.都为黄绿色 B.都具有漂白性
C.都能与硝酸银溶液产生白色沉淀 D.都能使紫色石蕊试液呈红色
【答案】C
【解析】
新制氯水中存在氯气分子、HCl和HClO;久置氯水由于次氯酸见光分解,实际都转化为HCl,所以久置氯
水就是稀盐酸,应该为无色,选项A错误。久置氯水就是稀盐酸,不含有次氯酸,所以没有漂白性,选
项B错误。新制氯水和久置氯水都有氯离子,都可以和硝酸银溶液反应生成氯化银沉淀,选项C正确。新
制氯水中有次氯酸所以具有漂白性,可以漂白石蕊溶液,最后为无色,选项D错误。
点睛:新制氯水中的离子有:氯离子、氢离子、次氯酸根离子、氢氧根离子(微量),分子有:水分子、
氯气分子、次氯酸分子,所以新制氯水具有:酸性、强氧化性和漂白性。久置氯水实际就是稀盐酸,所
以只有酸性和弱氧化性。
6.下列各项中不属于HClO的化学性质的是
A.氧化性 B.漂白性 C.酸性 D.稳定性
【答案】D
【解析】
HClO具有强氧化性、漂白性,可以电离产生氢离子,具有酸性,但其不稳定,光照条件下易分解产生
HCl和O;
2
故答案为D。
7.将一盛满Cl 的试管倒立在水槽中,当日光照射相当长一段时间后,试管中剩余气体的体积约占试管
2
容积的(假设反应前后体系温度相同) ( )
A. B. C. D.
【答案】 C
【解析】 氯气和水发生反应Cl +HO===HCl+HClO,当氯水受日光照射时发生反应2HClO=====2HCl+
2 2
O↑。由上述两个化学反应方程式可得关系式2Cl ~O ,由此可知产生的O 体积约为Cl 体积的。O 不易
2 2 2 2 2 2
溶于水,故试管中剩余气体的体积约占试管容积的。
8.下列实验过程中,不会产生气体的是( )(已知氧化性Cl>Br)
2 2
【答案】 C
【解析】 A项,新制氯水中的HClO见光分解生成氧气;B项,新制氯水中的H+与发酵粉中的NaHCO 反
3
应生成CO ;C项,新制氯水中的Cl 与NaBr反应生成Br 和NaCl,没有气体产生;D项,HO与NaO 反应
2 2 2 2 2 2
生成O。
2
学科网(北京)股份有限公司9.有X、Y、Z三种元素,已知:①X、Y、Z的单质在常温下均为气体;②X的单质可在Z的单质中燃烧,
生成XZ,火焰为苍白色;③XZ极易溶于水,电离出X+和Z-,其水溶液可使蓝色石蕊试纸变红;④每2个
X 分子可与1个Y 分子化合生成2个XY分子,XY在常温下为液体;⑤Z单质溶于XY中,所得溶液具有
2 2 2 2 2
漂白作用。
(1)推断X、Y、Z三种元素的名称为:X___________,Y___________,Z___________。
(2)化合物的化学式XZ为___________,XY为___________。Z的单质的化学式___________。
2
(3)五个过程中涉及的化学反应的方程式及电离方程式为
②___________
③___________
④___________
⑤___________
【答案】氢 氧 氯 HCl HO Cl H+Cl 2HCl HCl=H++Cl- 2H+O 2HO
2 2 2 2 2 2 2
Cl+ HO=HCl +HClO
2 2
【解析】X、Y、Z的单质在常温下均为气体;X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色,
则X是H,Z是Cl,氢气在氯气中燃烧生成氯化氢;氯化氢溶于水得到盐酸,其水溶液能使蓝色石蕊试纸
变红;每2个X 分子能与1个Y 分子化合成2个XY分子,XY常温下为液体,所以Y是O,氢气在氧气中
2 2 2 2
燃烧生成水;氯气溶于水生成次氯酸,所得溶液具有漂白性。
根据以上分析,X是氢元素,Y是氧元素、Z是氯元素。
(1)X、Y、Z三种元素的名称为:氢、氧、氯;
(2)根据上述分析,化合物的化学式XZ为HCl;XY为HO;Z的单质的化学式为Cl;
2 2 2
(3)反应②为氢气与氯气燃烧反应生成氯化氢,反应方程式为:H+Cl 2HCl;
2 2
过程③为盐酸完全电离生成氢离子和氯离子,电离方程式为:HCl=H++Cl-;
反应④为氢气与氧气化合反应生成水,反应方程式为:2H+O 2HO;
2 2 2
反应⑤为氯气与水反应生成盐酸和次氯酸,反应方程式为:Cl+ HO=HCl +HClO
2 2
10.氯水中含有多种成分,因而具有多种性质。根据氯水分别与如图四种物质发生的反应填空(a、b、
c、d重合部分代表物质间反应,且氯水足量)。(已知氧化性Cl>Fe3+)
2
(1)能证明氯水具有漂白性的是________(填“a”“b”“c”或“d”)。
(2)c过程中的现象是_____________________,
b过程中反应的离子方程式为_____________________________________________。
学科网(北京)股份有限公司(3)a过程中反应的化学方程式为__________________________________________。
【答案】 (1)d
(2)溶液中产生白色沉淀
CO+2H+===HO+CO↑
2 2
(3)2FeCl+Cl===2FeCl
2 2 3
【解析】 (1)含有HClO分子,有漂白性,可使变红的石蕊试液褪色。
(2)含有Cl-,可与AgNO 反应生成AgCl白色沉淀;含H+,可与CO反应,放出CO:
3 2
CO+2H+===HO+CO↑。
2 2
(3)含Cl 分子,可将FeCl 氧化:2FeCl+Cl===2FeCl。
2 2 2 2 3
能力提升
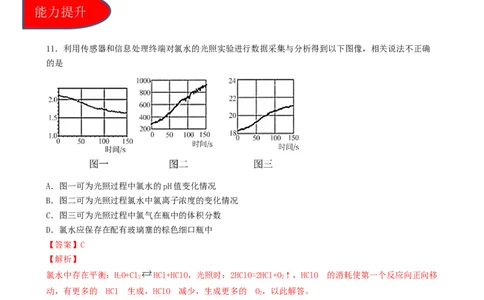
11.利用传感器和信息处理终端对氯水的光照实验进行数据采集与分析得到以下图像,相关说法不正确
的是
A.图一可为光照过程中氯水的pH值变化情况
B.图二可为光照过程氯水中氯离子浓度的变化情况
C.图三可为光照过程中氯气在瓶中的体积分数
D.氯水应保存在配有玻璃塞的棕色细口瓶中
【答案】C
【解析】
氯水中存在平衡:HO+Cl HCl+HClO,光照时:2HClO=2HCl+O↑,HClO 的消耗使第一个反应向正向移
2 2 2
动,有更多的 HCl 生成,HClO 减少,生成更多的 O,以此解答。
2
A.由分析,光照会有更多的 HCl 生成,HCl为强酸,则溶液的 pH 下降,A选项正确;
B.光照过程中,HClO 分解生成 HCl,增加 H+ 的同时也增加 Cl−,Cl− 浓度应提高,B选项正确;
C.光照使反应HO+Cl HCl+HClO向正反应进行的程度更大,消耗更多的 Cl,Cl 的浓度降低,C选
2 2 2 2
项错误;
D.光照能够使氯水中的 HClO 分解,因此氯水应保存在玻璃塞的棕色瓶中,避免阳光直射, D选项正
确;
故选C。
12.氯元素的化合价与其形成的常见物质种类的关系如图所示。
学科网(北京)股份有限公司下列说法不正确的是( )
A.b只有还原性 B.c没有漂白性,d具有漂白性
C.一定条件下e和f均属于较强氧化剂 D.g的化学式为
【答案】A
【解析】:b为HCl,其中+1 价的H化合价能降低,具有氧化性,A项错误;c为 没有漂白性,d为
HClO具有漂白性,B项正确;e为 ,f含 ,一定条件下二者均属于较强氧化剂,C项正确;g的
化学式为 ,D项正确。
13.(2021·哈密市第十五中学高一期末)BrCl是一种工业消毒剂,其结构和性质与氯气相似,下列有
关BrCl的预测正确的是
A.是一种有毒、有色的单质
B.Br、Cl元素的化合价都为0价
C.具有强氧化性,能使Fe2+转化为Fe3+
D.与HO反应的化学方程式:BrCl+HO=HClO+HBr
2 2
【答案】C
【解析】A. BrCl是一种有毒、有色的化合物,故A错误;
B. 氯元素的非金属性强于溴,Br元素的化合价为+1价,Cl元素的化合价为-1价,故B错误;
C. +1价的Br元素具有强氧化性,能使Fe2+转化为Fe3+,故C正确;
D. 与HO反应的化学方程式:BrCl+HO=HCl+HBrO,故D错误;
2 2
故选C。
14.氯气(Cl)是黄绿色气体,其水溶液叫氯水。把品红试纸(染有品红的纸)仲入氯水中,品红褪色。
2
发现问题:氯水中的哪些成分能使品红褪色呢?
查阅资料:氯气溶于水,部分与水反应,化学方程式为Cl+HO=HCl+HClO。其中,HClO名为次氯酸,
2 2
是一种弱酸,具有强氧化。
猜想:
猜想1:是氯水中的水使品红褪色的;
猜想2:是氯水中的_______(填化学式)使品红褪色的;
猜想3:是氯水中的盐酸使品红褪色的;
猜想4:是氯水中的次氯酸使品红褪色的。
实验探究:
学科网(北京)股份有限公司实验操作 实验现象 过程分析
①把品红试纸伸入水中 没有褪色 猜想1不成立
②把品红试纸伸入干燥的氯气中 没有褪色 猜想2不成立
③_______ 没有褪色 猜想3不成立
结论:
综合分析:氯水中的_______(填化学式)使品红褪色,具有漂白作用(能使品红等有色物质褪色)。
反思:
(1)HCO中氯元素的化合价为_______价。
(2)氯水中加入AgNO 溶液有白色沉淀生成,化学方程式为_______。
3
(3)向氯水中滴加紫色石蕊溶液,观察到的现象是_______。
【答案】Cl 把品红试纸伸入到盐酸中 HClO +1 HCl+AgNO=AgCl↓+HNO 先变红色后褪
2 3 3
色
【解析】猜想2:氯水是指氯气溶于水,既发生一个物理变化(氯气和水),又发生一个化学变化(生成
盐酸和次氯酸),因此一共有四个猜想;答案为:Cl。
2
要证明猜想3不成立,只要把品红试纸伸入到盐酸中,现象是无变化就可以了,因此能使品红变色的是
次氯酸;答案为:把品红试纸伸入到盐酸中。
综合分析判断:氯水中的HClO使品红褪色,具有漂白作用(能使品红等有色物质褪色);答案
为:HClO。
反思:(1)设HClO中氯元素的化合价为x,可以根据:+1+x+(-2)=0,解得x=+1;答案为:+1。
(2)AgNO 溶液和盐酸发生反应生成氯化银白色沉淀和稀硝酸,即HCl+AgNO=AgCl↓+HNO;答案为
3 3 3
HCl+AgNO=AgCl↓+HNO 。
3 3
(3)因为氯水中有HCl和HClO,向氯水中滴加紫色石蕊试液,观察到的现象是:先变红色后褪色,因为
酸能使紫色石蕊试液变红色,次氯酸具有漂白性,又能使颜色褪去;答案为先变红色后褪色。
学科网(北京)股份有限公司学科网(北京)股份有限公司