文档内容
第二章 海水中的重要元素—钠和氯
第二节 氯及其化合物 课时作业
第一课时 氯气的性质
基础达标
1.下列说法错误的是( )
A.钠和铁一样都能在氯气中燃烧生成金属氯化物
B.液氯是氯气的水溶液,它能使干燥的有色布条褪色
C.氯气是一种黄绿色、有刺激性气味的气体
D.氯水具有杀菌、漂白作用是因为氯水中含有强氧化性的次氯酸
2.制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反
应制得。用以上两种方法都可制得的氯化物是( )
A.AlCl B.FeCl
3 3
C.FeCl D.CuCl
2 2
3.下列关于氯气的叙述不正确的是( )
A.氯气是一种黄绿色、有刺激性气味、有毒的气体
B.氯气溶于水得到浅黄绿色的氯水,该过程涉及化学变化
C.氯气化学性质活泼,因此自然界中不存在游离态的氯元素
D.氢气在盛有氯气的集气瓶中燃烧,产生苍白色火焰和白烟
4.下列关于氯水的叙述中正确的是( )
A.新制氯水中只含Cl 和HO分子
2 2
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照新制氯水有气泡逸出,该气体是Cl
2
D.新制氯水在密闭无色玻璃瓶中放置数天后酸性将减弱
5.下列有关氯气实验现象的记录正确的是( )
A.纯净的氢气在氯气中安静燃烧,发出苍白色火焰
B.钠可以在氯气中燃烧,发出黄色火焰,生成黄色固体
C.用pH试纸检验干燥的氯气,试纸先变红后褪色
D.新制的氯水是由氯气溶于水形成的无色透明溶液
6.下列关于氯及其化合物的说法正确的是( )杨sir化学,侵权必究A.氯气和液氯是两种不同的物质
B.Cl 通入到含有酚酞的NaOH溶液中红色褪去,因为氯气有漂白性
2
C.Cl 在化学反应中既能作氧化剂,又能作还原剂
2
D.新制的氯水呈酸性,向其中滴加几滴紫色石蕊试液并振荡,溶液呈红色
7.下列关于氯及其化合物的叙述正确的是( )
A.氢气在氯气中燃烧产生淡蓝色火焰,在瓶口出现白烟
B.向氯水中加入NaHCO 粉末,有气泡产生,说明氯水中含有H+
3
C.工业上将氯气通入澄清石灰水中制取漂白粉
D.为了准确地了解氯水的酸性,可以用pH试纸准确测定其pH
8.下列说法正确的是( )
A.向久置的氯水中滴入紫色石蕊溶液,溶液将先变红后褪色
B.欲除去Cl 中少量的HCl气体,可将此混合气体通过盛有饱和食盐水的洗气瓶
2
C.漂白粉的有效成分是CaCl 和Ca(ClO)
2 2
D.氯水的成分为Cl 和Ca(ClO) ,应密封保存
2 2
9.氯气是一种很活泼的非金属单质,它具有较强的氧化性,下列叙述不正确的是(
)
A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟
B.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸
C.纯净的H 在Cl 中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照H 和
2 2 2
Cl 的混合气体时,因迅速化合而爆炸
2
D.通常状况下氯气能和Fe反应,氯气的储存不能用铁质容器
10.下列有关化学反应过程或实验现象的叙述中,正确的是( )
A.氯气的水溶液可以导电,说明氯气是电解质
B.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的
C.氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气
D.为证明氯水中含Cl-,可先加入盐酸酸化,再加入AgNO 溶液
3
能力提升
11.下列关于氯及其化合物的叙述正确的是( )
①纯净的氢气在氯气中燃烧发出苍白色的火焰
②实验室制氯气时,为了防止环境污染,多余氯气用石灰乳吸收
③向久置的氯水中滴入紫色石蕊溶液,溶液将先变红后褪色
④检验Cl 中是否混有HCl气体的方法是将气体通入硝酸银溶液
2
⑤除去Cl 中的HCl,可使气体通过饱和碳酸氢钠溶液
2A.① B.③④⑤
C.②⑤ D.①⑤
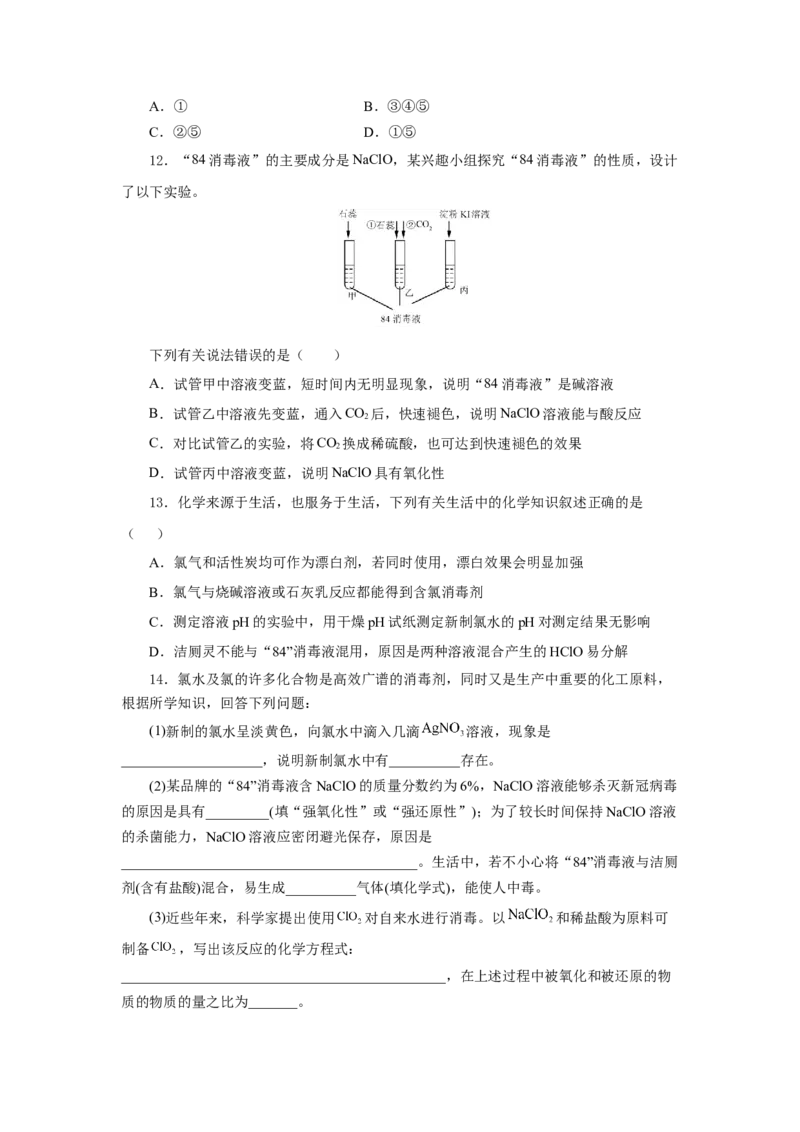
12.“84消毒液”的主要成分是NaClO,某兴趣小组探究“84消毒液”的性质,设计
了以下实验。
下列有关说法错误的是( )
A.试管甲中溶液变蓝,短时间内无明显现象,说明“84消毒液”是碱溶液
B.试管乙中溶液先变蓝,通入CO 后,快速褪色,说明NaClO溶液能与酸反应
2
C.对比试管乙的实验,将CO 换成稀硫酸,也可达到快速褪色的效果
2
D.试管丙中溶液变蓝,说明NaClO具有氧化性
13.化学来源于生活,也服务于生活,下列有关生活中的化学知识叙述正确的是
( )
A.氯气和活性炭均可作为漂白剂,若同时使用,漂白效果会明显加强
B.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
C.测定溶液pH的实验中,用干燥pH试纸测定新制氯水的pH对测定结果无影响
D.洁厕灵不能与“84”消毒液混用,原因是两种溶液混合产生的HClO易分解
14.氯水及氯的许多化合物是高效广谱的消毒剂,同时又是生产中重要的化工原料,
根据所学知识,回答下列问题:
(1)新制的氯水呈淡黄色,向氯水中滴入几滴 溶液,现象是
____________________,说明新制氯水中有__________存在。
(2)某品牌的“84”消毒液含NaClO的质量分数约为6%,NaClO溶液能够杀灭新冠病毒
的原因是具有_________(填“强氧化性”或“强还原性”);为了较长时间保持NaClO溶液
的杀菌能力,NaClO溶液应密闭避光保存,原因是
__________________________________________。生活中,若不小心将“84”消毒液与洁厕
剂(含有盐酸)混合,易生成__________气体(填化学式),能使人中毒。
(3)近些年来,科学家提出使用 对自来水进行消毒。以 和稀盐酸为原料可
制备 ,写出该反应的化学方程式:
______________________________________________,在上述过程中被氧化和被还原的物
质的物质的量之比为_______。直击高考
15.BrCl的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,也可以
与水发生如下反应:BrCl+HO=HCl+HBrO,下列说法正确的是( )
2
A.BrCl与Ca(OH) 溶液反应,产物有CaBr 、Ca(ClO) 和HO
2 2 2 2
B.BrCl与水反应时,水既是氧化剂又是还原剂
C.BrCl与钠反应,化学方程式是2Na+BrCl=NaCl+NaBr
D.BrCl与铁反应,化学方程式是2Fe+2BrCl=FeCl +FeBr
2 2
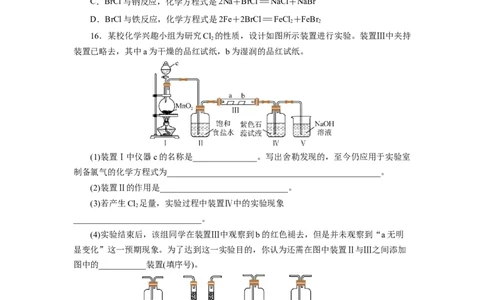
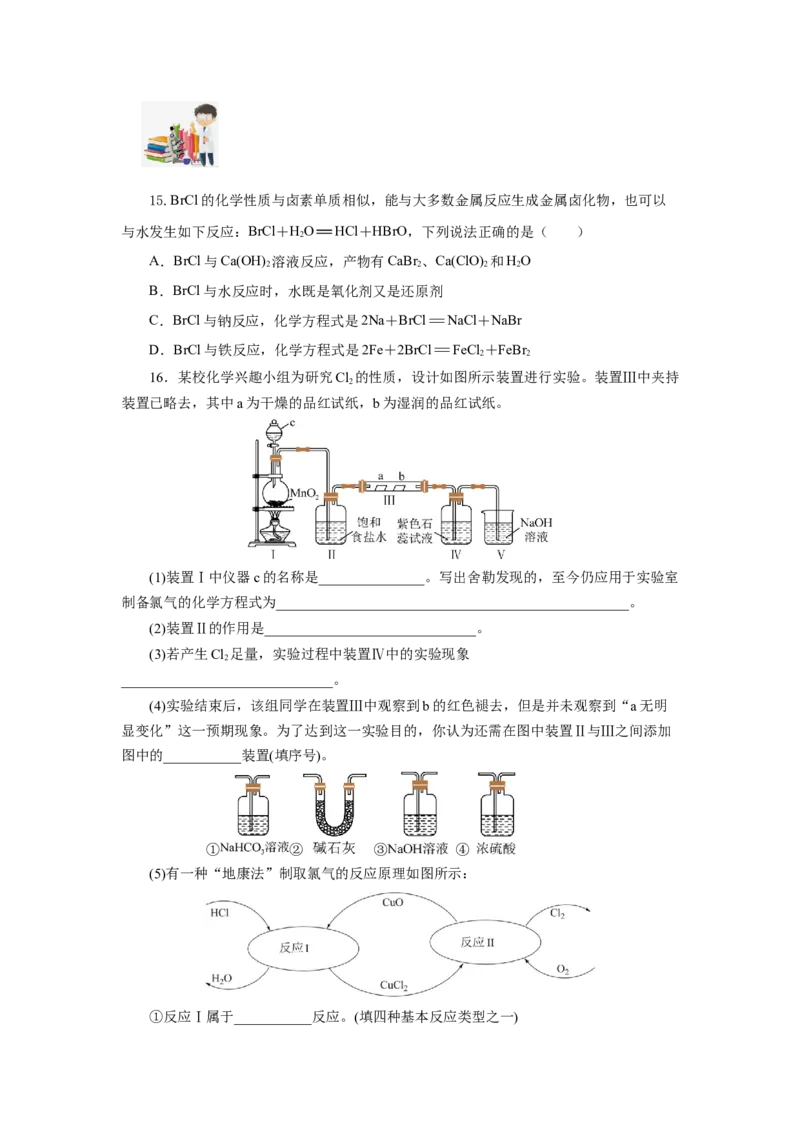
16.某校化学兴趣小组为研究Cl 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持
2
装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)装置Ⅰ中仪器c的名称是_______________。写出舍勒发现的,至今仍应用于实验室
制备氯气的化学方程式为__________________________________________________。
(2)装置Ⅱ的作用是______________________________。
(3)若产生Cl 足量,实验过程中装置Ⅳ中的实验现象
2
______________________________。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明
显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加
图中的___________装置(填序号)。
① ② ③ ④
(5)有一种“地康法”制取氯气的反应原理如图所示:
①反应Ⅰ属于___________反应。(填四种基本反应类型之一)②在450℃条件下,反应Ⅱ的化学方程式为
____________________________________。