文档内容
第二章 海水中的重要元素—钠和氯
第二节 氯及其化合物
第一课时 氯气的性质
【学习目标】1.通过观看视频、阅读教材、实验探究,认识氯是一种重要的“成盐元素”,了解氯气
的物理性质,掌握氯气的化学性质,体会实验对认识和研究物质性质的重要作用,培养证据推理意识。
2.通过分析氯原子的原子结构特点,利用离子反应、氧化还原反应的观点预测氯气的化学性质,并能
根据预测的结果,设计、实施实验方案,书写相关反应的化学方程式或离子方程式。
3.通过了解氯气的发现史, 学习科学家的研究精神及勤于钻研、严谨求实的科学态度。
【学习重点】重点:氯气的化学性质。
【学习难点】氯气分别与水、氢氧化钠的反应。
【课前预习】
旧知回顾:1.金属钠与水反应的离子方程式为 2Na+2H O == = 2Na + +2OH - +H ↑ ,与Cl 反应的化学方程
2 2 2
式: 2Na+Cl 2NaCl 。
2
2.Na O 中氧为 -1 价,具有 强氧化 性,与水反应时,氧化剂是 N aO ,还原剂是 N aO ,反应的
2 2 2 2 2 2
的离子方程式为 : 2N aO +2H O == = 4Na + +4OH - +O ↑ 。
2 2 2 2
新知预习: 1.氯气与铜、铁、氢气反应的化学方程式分别为:
Cu+Cl CuCl 、 2Fe+3Cl 2FeCl 、 H +Cl 2HCl 。
2 2 2 3 2 2
2.氯气溶于水形成的溶液叫 氯水 ,反应的化学方程式: C l + H O HCl + HClO ,其中HCl是
2 2
强 酸,HClO是 弱 酸。氯气溶于NaOH溶液反应的离子方程式为: C l + 2OH - == = Cl - + ClO - + H O
2 2
。
【课中探究】
情景导入:1915年4月22日,德军在比利时的伊普尔战役中首次大规模使用毒气。当时战场出现了
有利于德军的风向,德军打开了早已在前沿阵地屯集的装满氯气的钢瓶,一人多高的黄绿色烟云被每秒 2
-3米的微风吹向英法联军阵地。面对扑面而来的刺鼻的怪味,英法守军一阵大乱,阵线迅速崩溃,部分
士兵用湿毛巾捂住嘴巴,甚至有的士兵用自己尿液浸湿的毛巾捂住嘴巴,他们逃往地势更高的地方,幸免遇
难。这次攻击,英法守军共中毒15000人,5000多人死亡,德军亦有数千人中毒和死亡。这是战争史上的
第一次化学战,从此,化学战作为最邪恶的战争被写入了战争的史册.(见PPT视频)
一、氯元素的存在及氯气的物理性质
活动一、氯元素的存在
任务一、阅读教材P82~83第一、二段,思考氯元素在自然界存在形式及来源是什么?
【答案要点】①氯是一种重要的“成盐元素”,在自然界中除了以NaCl、MgCl 、 CaCl 等形式大量
2 2
存在于海水中,致使海水既咸又苦,不能直接饮用。还存在于陆地的盐湖和盐矿中。②人体体液中的Na+和Cl-对于调节体液的物理和化学特性有着重要的作用,它们除了来自食物外,还
要通过食盐来补充,以 NaCl为主要成分的食盐是重要的调味剂。
③氯在自然界中以化合态存在。
任务二、查阅资料,结合教材P44页“资料卡片”及有关数据,简述氯气的发现过程是什么?
【答案要点】①18世纪70年代,瑞典化学家舍勒(C.W.Scheele,1742—1786) 将软锰矿(主要成分是
MnO )与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。受当时流行学说的影响,舍勒未能
2
确认这种气体。
②1810年(36年后),英国化学家戴维( S.H.Davy,1778----1829)才确认这种气体是一种新元素组成
的单质。并将这种元素命名为chlorine,此名称来自希腊文,有“绿色”的意思,我国早年将其译成“绿
气”,后改为氯气。
活动二、氯气的物理性质
任务一、观察氯气样品、观看视频,结合上述材料和事件,思考氯气具有哪些物理性质?并填写下
表。若遇氯气泄漏你认为人该往何处逃离?(见PPT视频)
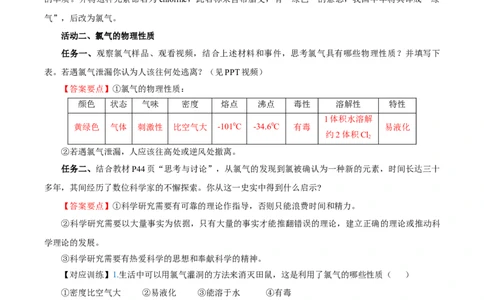
【答案要点】①氯气的物理性质:
颜色 状态 气味 密度 熔点 沸点 毒性 溶解性 特性
1体积水溶解
黄绿色 气体 刺激性 比空气大 -1010C -34.60C 有毒 易液化
约2体积Cl
2
②若遇氯气泄漏,人应该往高处或逆风处撤离。
任务二、结合教材P44页“思考与讨论”,从氯气的发现到氯被确认为一种新的元素,时间长达三十
多年,其间经历了数位科学家的不懈探索。你从这一史实中得到什么启示?
【答案要点】①科学研究需要有可靠的理论作指导,否则只能浪费时间和精力。
②科学研究需要以大量事实为依据,只有大量的事实才能推翻错误的理论,建立正确的理论或推动科
学理论的发展。
③科学研究需要有热爱科学的思想和奉献科学的精神。
【对应训练】1.生活中可以用氯气灌洞的方法来消灭田鼠,这是利用了氯气的哪些性质( )
①密度比空气大 ②易液化 ③能溶于水 ④有毒
A.①② B.③④ C.④ D.①④
【答案】D
【解析】氯气对动物具有毒性,能致死;氯气的密度比空气大,沉在空气底部;用氯气灌洞使氯气沉
在洞底,洞内田鼠吸入后中毒而亡;故选D。
2.一家大型化工厂发生爆炸,有大量的Cl 扩散,下列应急措施不正确的是( )
2
A.向逆风方向的高处跑
B.用浸有烧碱液的毛巾捂住口鼻迅速逃离
C.用浸有纯碱液的毛巾捂住口鼻迅速逃离D.来不及逃离的可用浸湿的棉被堵好门窗,并及时请求救援
【答案】 A
【解析】 氯气有毒且密度比空气大,如果发生氯气泄漏,氯气向顺风方向和低洼处扩散较快,应将
人群逆风向高处疏散,A项正确;氯气虽能和烧碱或纯碱反应生成盐,但烧碱有强腐蚀性,B项错误,C
项正确;氯气能和水反应,来不及逃离的可用浸湿的棉被堵好门窗,并及时请求救援,D项正确。
二、氯气的化学性质
活动一、与金属、非金属反应
任务一、请从原子结构的观点分析氯元素在自然界以化合态存在的原因事什么?
【答案要点】氯原子结构示意图为 ,氯原子容易得到1个电子而形成Cl-,表现出典型的非金
属性。Cl 是由Cl原子构成的双原子分子,所以较活泼,具有强氧化性,与具有还原性物质反应生成氯的
2
化合物。
任务二、观看视频,写出氯气与金属钠、铁、铜三种单质反应的化学方程式,并指明主要反应现象。
有何规律?工业上为什么可以用钢瓶储运液氯?
【答案要点】①与钠反应2Na+Cl====2NaCl,剧烈燃烧,黄色火焰 ,产生大量白烟;
2
与铁反应2Fe+3Cl====2FeCl ,剧烈燃烧,产生大量棕褐色烟;
2 3
与铜反应Cu+Cl====CuCl ,剧烈燃烧,产生大量棕黄色烟,溶于水后,溶液呈蓝绿色。
2 2
②氯气与铁在加热条件下才能反应,所以,可将液氯保存在钢瓶中。
③规律:Cl 与变价金属反应时生成高价态的金属氯化物,即Cl 与Fe、Cu反应,不论Cl 是否过量均
2 2 2
生成FeCl 和CuCl。
3 2
注意:液氯即液态的氯气,常温下干燥的氯气(或液氯)与金属铁不能反应,因此工业上可以用钢瓶
储运液氯。
任务三、完成教材P45实验2-7(或视频实验),对比两种不同条件下氯气与氢气的反应有何不同?
填写小表内容。
【答案要点】①氢气在氯气燃烧:
操作 H 在Cl 中燃烧 H 和Cl 的混合气体光照
2 2 2 2
H 在盛有Cl 的集气瓶中安静地燃烧,发
2 2
现象 发生爆炸
出苍白色火焰,集气瓶口有白雾产生。
反应原理 H+Cl====2HCl(工业制盐酸)
2 2
②氯气和氢气的混合气体在强光照射:会发生爆炸。产生此现象的原因是H 和Cl 混合后光照,反应
2 2
瞬间完成,放出的热量使气体急剧膨胀而发生爆炸。
任务四、结合教材P45“思考与讨论”,联系氧化还原反应的原理分析,谈谈你对燃烧的概念有哪些新
的认识?
【答案要点】①燃烧是指所有发光、发热的剧烈的化学反应。
②燃烧不一定要有氧气参加,物质并不是只有在氧气中才可以燃烧。
③燃烧的实质是剧烈的氧化还原反应。
【对应训练】1.下列实验现象的描述正确的是( )A.氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白色烟雾
B.铁丝在氯气中燃烧,产生棕红色的浓烟,产物溶于水,溶液呈浅绿色
C.铜在氯气中燃烧,产生棕黄色烟,产物溶于水,溶液呈蓝绿色
D.钠在空气中燃烧,发出黄色的火焰,生成白色固体
【答案】C
【解析】A项,氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白雾,错误;B项,铁丝在氯气中
燃烧,产生棕褐色的浓烟,产物FeCl 溶于水,溶液呈黄色,错误;C项,铜在氯气中燃烧,产生棕黄色
3
烟,产物CuCl 溶于水,溶液呈蓝绿色,正确;D项,钠在空气中燃烧,发出黄色的火焰,生成淡黄色固
2
体,错误。
2.下列关于氯气的叙述不正确的是( )
A.氯气可以用于自来水的杀菌、消毒。
B.红热的铜丝在氯气中燃烧生成CuCl
2
C.纯净的氢气可以在氯气中安静地燃烧,发出黄色火焰
D.向田鼠洞里通入氯气杀灭田鼠,利用了氯气有毒和密度比空气大的性质
【答案】C
【解析】A. 氯气溶于水发生化学变化,生成盐酸和次氯酸,故氯气可以用于自来水的杀菌、消毒,
故A项叙述是正确的;B. 红热的铜丝在氯气中燃烧生成CuCl ,故B项叙述是正确的;C. 纯净的氢气在
2
氯气中燃烧发出苍白色火焰,故C项叙述是不正确的;D. 氯气有毒,密度比空气的大,可杀灭田鼠,故
D项叙述是正确的;综上所述,本题的答案是C
活动二、氯气与水的反应
任务一、氯气在水中的溶解度大约为1:2,那么氯气溶于水时是否和水发生了化学反应呢?结合教材
P46页【实验2-8】完成实验探究(或观看实验视频),并将实验现象及有关结论填入表中。
【答案要点】
实验操作 实验现象 实验结论
取干燥的和湿润的有色布条,分别 ①干燥的有色布条不褪
①干燥的氯气不具有漂白性,
放入两个盛有干燥氯气的集气瓶 色;
湿润的氯气才具有漂白性;②
中,盖上玻璃片,观察现象。 ②湿润的有色布条褪色;
氯气溶于水时,氯气要与水反
将有色鲜花放入盛有干燥氯气的集 鲜花变色(见教材P43图 应生成生成新物质,具有有漂
气瓶中,盖上玻璃片,观察现象。 2-4) 白性。
任务二、根据氧化还原反应原理、质量守恒定律及已掌握的Cl 的性质预测Cl 与HO反应的生成物
2 2 2
可能是什么?
【答案要点】①氯气溶于水与水发生反应,所得的水溶液称为氯水,氯水是混合物。
②根据氯原子的结构可知,氯元素常见的化合价有-1、0、+1、+3、+5、+7等,氯气化合价为0价处
于氯元素的中间价态,因此,氯气应既有氧化性,又具有还原性。③氯气作氧化剂,还原产物为-1价的氯离子,作还原剂,氧化产物可能为为大于或等于+1价的微粒。
④根据质量守恒定律,氯气与水可能发生的反应为:Cl+HO HCl+HClO。
2 2
任务三、已知次氯酸(HClO)是一元弱酸,具有漂白性(强氧化性),见光易分解,观察氯水样品,
思考如何设计简单实验验证氯气与水发生了上述反应?说明氯水中含有哪些物质?
【答案要点】①观察氯水样品呈淡黄绿色,说明有氯气的分子存在。
②试管中加入一定量的氯水,向氯水中滴加硝酸银溶液观察到有白色沉淀,这说明氯水有一定量的氯
离子,即有HCl生成。
③根据湿润的氯气才具有漂白性或向氯水中滴加紫色的石蕊试液,观察到溶液先变红后褪色,证明产
物有HClO生成。
④结论:新制氯水中含有Cl 、HCl、HClO、HO四种物质。但由于氯气与水的反应是可逆反应,且
2 2
HClO不稳定,见光易分解:2HClO=====2HCl+O↑。因此,久置的氯水则只有HCl和HO两种物质,即
2 2
久置的氯水为稀盐酸,不再具有强氧化性或漂白性。
⑤应用:目前,很多自来水厂用氯气来杀菌、消毒,我们偶尔闻到的自来水散发出来的刺激性气味就
是余氯的气味。使用氯气对自来水消毒时,氯气会与水中的有机物发生反应,生成的有机氯化物可能对人
体有害。所以,国家规定了饮用水中余氯含量的标准,而且已开始使用新的自来水消毒剂,如二氧化氯
(ClO )、臭氧等。
2
【对应训练】1.下列关于氯水的叙述中,正确的是( )
A.新制氯水中只含Cl 和HO分子 B.液氯与氯水都是纯净物
2 2
C.新制氯水的颜色为浅黄绿色 D.氯水经光照有气泡逸出,该气体为HCl
【答案】C
【解析】A.新制的氯水因其含Cl 而呈淡绿色,其中还含有HClO和HO分子,故A错误;B.液氯
2 2
是纯净物,氯水是混合物,故B错误;C.新制的氯水因其含Cl 而呈淡绿色,故C正确;D.氯水由于其
2
中的HClO见光易分解:2HClO=====2HCl+O↑,所以氯水经光照有O 气泡逸出,故D错误。故选C。
2 2
2.下列实验现象与新制氯水中的某些成分(括号内物质)没有关系的是( )
A.将NaCO 固体加入新制氯水中,有无色气泡产生(H+)
2 3
B.新制氯水使红色布条褪色(HCl)
C.向FeCl 溶液中滴加新制氯水,再滴加KSCN溶液,溶液呈红色(Cl )
2 2
D.向新制氯水中滴加AgNO 溶液有白色沉淀产生(Cl-)
3
【答案】B
【解析】由于新制氯水中存在HCl,则将NaCO 加入新制氯水中发生反应NaCO +2HCl===2NaCl+
2 3 2 3
HO+CO↑,表现出HCl的酸性,即H+的性质,A项正确;新制氯水使红色布条褪色是次氯酸的漂白作
2 2
用,B项错误;Cl 具有强氧化性,能把Fe2+氧化为Fe3+,Fe3+遇KSCN溶液呈红色,C项正确;向新制氯
2
水中滴加AgNO 溶液,能发生反应HCl+AgNO===AgCl↓+HNO,表现出Cl-的性质,D项正确。
3 3 3
活动三、氯气与碱的反应
任务一、问题探究:市面上销售的漂白粉或消毒剂的有效成分为Ca(ClO) 或NaCIO(又名84消毒
2液),为什么不直接用次氯酸作漂白剂或消毒剂?
【答案要点】①氯气在水中的溶解度不大,而且生成的HClO不稳定,难以保存,使用起来很不方
便,效果也不理想。
②次氯酸盐比次氯酸的稳定性强很多。比如NaClO虽然也会分解,但它的水溶液在低温下存放三年才
分解一半左右,比HClO稳定得多。
③次氯酸盐可以在溶液中转化为次氯酸,从而具有一定的漂白和消毒能力,所以漂白液、漂白粉、漂
粉精都是常用的消毒剂和漂白剂。
任务二、阅读教材P47页内容,思考如何制取漂白液和漂泊粉?漂白液和漂白粉的主要成分及有效成
分分别是什么?
【答案要点】①制取漂白液—氯气与NaOH反应:Cl +2NaOH===NaCl+NaClO+HO或Cl +2OH-
2 2 2
===Cl-+ClO-+HO。漂白液的有效成分是次氯酸钠。
2
②制取漂白粉—氯气与石灰乳反应:2Ca(OH) +2Cl===CaCl +Ca(ClO) +2HO。将氯气通入冷的石
2 2 2 2 2
灰乳中会得到以次氯酸钙为有效成分的漂白粉。若充分反应使次氯酸钙成为主要成分,就得到了漂粉精。
漂白粉的主要成分是CaCl 、Ca(ClO) ,有效成分是Ca(ClO) ,漂粉精的主要成分是Ca(ClO) 。
2 2 2 2
③漂白液、漂白粉和漂粉精既可作漂白棉、麻、纸张的漂白剂,又可用作游泳池等场所的消毒剂。
任务三、应用探究:你是如何理解漂泊液、漂白粉的漂白原理?并归纳氯的用途。
【答案要点】①利用复分解反应原理,漂白粉中的次氯酸钙与酸(如盐酸或碳酸等)反应生成具有漂白
性的次氯酸,说明HClO的酸性比碳酸弱。
②漂白液、漂白粉的漂白、消毒原理相同,都是在酸性条件下生成具有漂白、消毒作用的次氯酸
(HClO)。
③反应方程式:Ca(ClO) +CO+HO===CaCO ↓+2HClO(家用漂白、消毒)
2 2 2 3
Ca(ClO) +2HCl===CaCl ↓+2HClO(工业漂白)
2 2
④氯气的用途:用于自来水的杀菌、消毒;制取漂白粉、漂白液、消毒液等;化工原料用于工业制盐
酸、有机溶剂、农药、染料等。
【 对应训练】1.在抗震救灾中要用大量漂白粉和漂白液杀菌消毒。下列说法中正确的是( )
A.漂白粉是纯净物,漂白液是混合物
B.漂白粉的有效成分是Ca(ClO)
2
C.工业上将氯气通入澄清石灰水制取漂白粉
D.漂白液的有效成分是NaO
2 2
【答案】B
【解析】漂白粉的主要成分是氯化钙和次氯酸钙,有效成分是次氯酸钙,是混合物;漂白液的主要成
分是氯化钠和次氯酸钠,有效成分是次氯酸钠,是混合物。
2.下列有关氯及其化合物的说法正确的是( )
A.Cl 和变价金属反应生成较高价态的金属氯化物
2
B.将氯气通入澄清石灰水中,即可制得漂白粉C.向新制的氯水中放入有色布条会褪色说明Cl 有漂白性
2
D.Cl―→NaCl必须加入还原剂才能实现
2
【答案】A
【解析】A项,Cl 氧化性很强,Cl 和变价金属反应生成较高价态的金属氯化物,正确;B项,应将
2 2
氯气通入石灰乳中,才可制得漂白粉,错误;C项,向新制的氯水中放入有色布条会褪色说明HClO有漂
白性,Cl 本身没有漂白性,错误;D项,Cl―→NaCl可以通过氯气与氢氧化钠反应实现,Cl +2NaOH
2 2 2
=NaCl+NaClO+HO不是必须加入还原剂才能实现,错误。
2
【课后巩固】1.(易)教材作业:P51页练习1、2、3
2.(易)下列关于氯气的叙述正确的是( )
A.钠在氯气中燃烧产生白色烟雾
B.红热的铜丝可以在氯气中燃烧,产生棕黄色烟雾
C.纯净的氢气可以在氯气中安静地燃烧,发出苍白色火焰
D.氯气可用于漂白,这是氯气的漂白作用
【答案】C
【解析】A.钠在氯气中燃烧,生成NaCl小颗粒,形成白烟,没有雾的出现,故A错误;B.CuCl
2
为鼓励提小颗粒,产生棕黄色的烟,没有雾,故B错误;C.纯净的氢气可以在氯气中安静地燃烧,发出
苍白色火焰,说法完全符合实验事实,故C正确;D.氯气用于漂泊,这是对的,但是起漂白作用的不是
氯气本身,而是次氯酸,故D错误。故选C。
3.(中)下列关于氯气的说法不正确的是( )
A.尽管氯气的化学性质很活泼,但是干燥的液氯能用钢瓶贮存
B.氯气和液氯是两种不同的物质
C.可以用浓硫酸除去氯气中的水蒸气
D.Cl 跟变价金属反应生成高价金属氯化物
2
【答案】B
【解析】氯气和液氯是同一种物质的不同状态,B项不正确。
4.(易)下列关于氯气的叙述正确的是( )
A.燃烧不一定有氧气参加
B.红热的铜丝可以在氯气中燃烧,产生棕黄色烟雾
C.H 在Cl 中安静燃烧,产生苍白色火焰,形成白色烟雾
2 2
D.通常状况下氯气能和Fe反应,氯气的储存不能用铁质容器
【答案】A
【解析】A.燃烧是剧烈的发光发热的氧化反应,不一定有氧气参加,比如氢气在氯气中燃烧,故A正确;B.CuCl 为固体小颗粒,产生棕黄色的烟,没有雾,故B错误;C.生成的HCl极易溶于水,与空
2
气中的水蒸气形成盐酸小液滴,是白色的雾,故C错误;D.铁和氯气在点燃的条件下发生反应,常温条
件下不反应,故常温下可以用钢瓶来储存氯气,故D错误。故选A。
5.(易)下列说法中不正确的是( )
A.Cl 在与金属反应时表现强氧化性
2
B.任何物质的燃烧必须有O 参与
2
C.Cl 与HO反应的离子方程式为Cl+HO=HClO+H++Cl-
2 2 2 2
D.漂白粉的主要成分是Ca(ClO) 和CaCl
2 2
【答案】B
【解析】A项,Cl 能与大多数金属化合,生成金属氯化物,表现强氧化性,正确;B项,燃烧不一定
2
有氧气参加,如氢气在氯气中燃烧,错误;C项,Cl 与HO反应生成HCl与HClO,离子方程式为Cl+
2 2 2
HO=HClO+H++Cl-,正确;D项,漂白粉的主要成分为CaCl 和Ca(ClO) ,有效成分是Ca(ClO) ,正
2 2 2 2
确。
6.(难)某校化学兴趣小组在探究新制饱和氯水成分的实验中,根据实验现象推测的有关结论中错误
的是( )
A.向氯水中滴入紫色石蕊溶液看到其先变红后褪色,推测氯水中含有Cl 分子
2
B.向氯水中滴加硝酸酸化的AgNO 溶液,产生白色沉淀,推测氯水中可能含有Cl-
3
C.向氯水中加入碳酸钠粉末,有气泡产生,推测氯水中含有H+
D.氯水放置一周后pH将变大,说明氯水中含有ClO-
【答案】AD
【解析】氯气溶于水得到的溶液为氯水,氯水中,氯气大部分以分子形式存在,少量氯气与水反应生
成氯化氢和次氯酸,氯化氢为强电解质完全电离生成氢离子和氯离子,次氯酸为弱电解质部分电离,据此
分析解答。A.氯水中含有盐酸和次氯酸,向氯水中滴入紫色石蕊溶液看到,溶液变红,次氯酸具有漂白
性,然后溶液又褪色,不能证明氯水中含有Cl 分子,故A错误;B.氯气与水反应生成氯化氢和次氯酸,
2
氯化氢为强电解质完全电离生成氢离子和氯离子,氯离子与银离子反应生成氯化银沉淀,故B正确;C.
向氯水中加入NaCO 粉末,有气泡产生,是因为碳酸根离子与氯水中的氢离子发生反应生成水和二氧化
2 3
碳,故C正确;D.次氯酸不稳定,2HClO =====2HCl+O ↑,氯水放置一周后,溶液中的盐酸浓度增大,
2
pH减小,故D错误;故选AD。
7.(中)下列生活中的物质与其有效成分的化学式、用途的对应关系中,不正确的是( )
选项 A B C D
生活中的物质 食盐 小苏打 复方氢氧化铝片 漂白粉有效成分的化学式 NaCl NaCO Al(OH) Ca(ClO)
2 3 3 2
用途 做调味品 做发酵粉 做抗酸药 做消毒剂
【答案】B
【解析】A.食盐的主要成分是氯化钠,有咸味,可做调味品,故A正确;B.小苏打的主要成分为
碳酸氢钠,不是碳酸钠,故B错误;C.氢氧化铝难溶于水,能够和盐酸反应,可以做抗酸药,故C正
确;D.漂白粉的有效成分为Ca(ClO) ,具有强氧化性,可做消毒剂,故D正确;故选B。
2
8.(中)(1)在某防空防灾演习现场,模拟一起大客车与一辆装有氯气的槽罐车发生追尾事故,造成槽
罐翻落、氯气泄露。人防办立即指挥专业救援队在事发地点,测定风向,进行事故处置。引导大客车上的
乘客_____________(填序号)
a.顺风向高处转移 b.顺风向低处转移杨sir化学,侵权必究
c.逆风向高处转移 d.逆风向低处转移
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的
现象是 _________________________________________。
(3)为防止氯气尾气污染空气,根据氯气的性质,可用NaOH溶液吸收多余的氯气,原理是(用离子方
程式表示) ______________________________________________。根据这一原理,工业上常用廉价的石灰
乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是________________(填化学式),长期露置于空气中
的漂白粉会失效的原因,用化学反应方程式可表示为
_________________________________________________。
【答案】(1)c (2)干燥的有色布条无明显变化,湿润的有色布条褪色
(3)Cl+2OH-=ClO-+Cl-+HO Ca(ClO)
2 2 2
Ca(ClO) +CO +HO=CaCO ↓+2HClO,2HClO====2HCl+O ↑
2 2 2 3 2
【解析】(1)氯气有毒,且氯气的密度大于空气的密度,因此引导大客车上的乘客逆风高处转移,选项
c正确;故答案为c;
(2)氯气本身不具有漂白性,干燥的氯气不能使干燥的有色布条褪色,氯气遇到水产生次氯酸,次氯酸
具有强氧化性,具有漂白性,氯气能使湿润有色布条褪色;故答案为干燥的有色布条无明显变化,湿润的
有色布条褪色;
(3)Cl 能与NaOH发生歧化反应,其离子方程式为Cl+2OH-=Cl-+ClO-+HO;漂白粉的成分是
2 2 2CaCl 和Ca(ClO) ,其有效成分是Ca(ClO) ;碳酸的酸性强于次氯酸,漂白粉长期露置于空气中发生
2 2 2
Ca(ClO) +CO +HO=CaCO ↓+2HClO,2HClO====2HCl+O ↑;故答案为Cl+2OH-=Cl-+ClO-+
2 2 2 3 2 2
HO;Ca(ClO) ;Ca(ClO) +CO +HO=CaCO ↓+2HClO,2HClO====2HCl+O ↑。
2 2 2 2 2 3 2