文档内容
2.2.2化学平衡常数(分层作业)
1.在恒温恒容的密闭容器中发生 ,T℃时,该反应
的化学平衡常数为K,下列说法正确的是
A.其他条件相同,升高温度降低正反应速率、提高逆反应速率
B.T℃时,若 时,则
C.若容器内气体压强保持不变,该可逆反应达到化学平衡状态
D.一定条件下, 能完全转化为
2.周期表中ⅥA族元素及其化合物应用广泛。 是常见的氧化剂和助燃剂。 催化氧化是工业制硫酸的重
要反应之一(中和热为 )。Se(硒)是重要的工业原材料与动物体必须营养素。提取Se的主要原材料为
电解铜产生的阳极泥。可通过阳极泥硫酸化焙烧提取Se,硫酸化焙烧提取Se的步骤主要分为两步:第一步焙
烧,硫酸将单质Se氧化为 。第二步还原吸收,在水中 将 转化为单质Se。对于反应
,下列有关说法不正确的是
A.该反应为放热反应 B.上述反应的平衡常数
C.使用催化剂能缩短该反应到达平衡的时间 D.增大体系的压强能提高 的反应速率
3.有催化剂的合成塔中发生的反应为 ,
。298K下合成氨反应的平衡常数K=4.1×106,下列说法错误的是
A.合成氨反应在298K时进行得比较完全
B.合成氨反应在298K时反应速率较快
C.仅从K的值无法得知该反应的平衡转化率
D.改变温度,K的值也会变化
4. 是工业提纯硅的原理之一、下列有关化学反应速率及其平衡的说法正确的是
A.恒温恒容条件下,增加Si(s)的用量,反应速率加快
B.恒温恒压条件下,向反应容器中通入氦气使容器体积增大,平衡正向移动
C.恒温恒容条件下,当反应体系气体密度不再发生改变,反应达到平衡状态
D.一定条件下反应达平衡后,对反应体系进行升温后重新达平衡,平衡常数增大
5.某温度下气体反应体系达到化学平衡,平衡常数K= ,下列说法正确的是
A.该反应的化学方程式为2E(g)+F(g) A(g)+2B(g)
B.降低温度,正反应速率增大
C.该温度时,v(F)=v(A)则反应达到平衡状态
D.增大c(A)、c(B),K增大
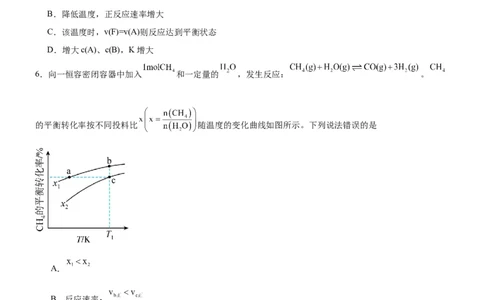
6.向一恒容密闭容器中加入 和一定量的 ,发生反应: 。
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法错误的是
A.
B.反应速率:
C.点a、b、c对应的平衡常数:
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
7.在一容积恒定的密闭容器中发生反应: ,该反应达到平衡后,测
得相关数据如下:实验序
温度/ 初始 浓度/ 初始 浓度/ 的平衡转化率
号
1 110 1 1
2 100 1 1
3 110 0.8 Y
(1)实验1中, 后达到平衡, 的平均反应速率为 。在此实验的平衡体系中再加入
和 ,平衡 移动(填“正向”“逆向”或“不”)。
(2)实验2中 的值___________(填序号)。
A.等于 B.大于 C.小于 D.无法确定
(3)实验3中 的值为 。
(4)在一恒温绝热容器中,下列选项中能说明反应 ,达到平衡状态的
是 (填序号)。
A.压强不再变化
B.生成HO的速率和消耗 的速率相等
2
C.混合气体的密度不变
D. 的质量不再变化
E.化学平衡常数 不变
F.单位时间内生成 的分子数与生成 的分子数相等
(5)某温度下,各物质的平衡浓度符合下式: ,试判此时的温度为 。
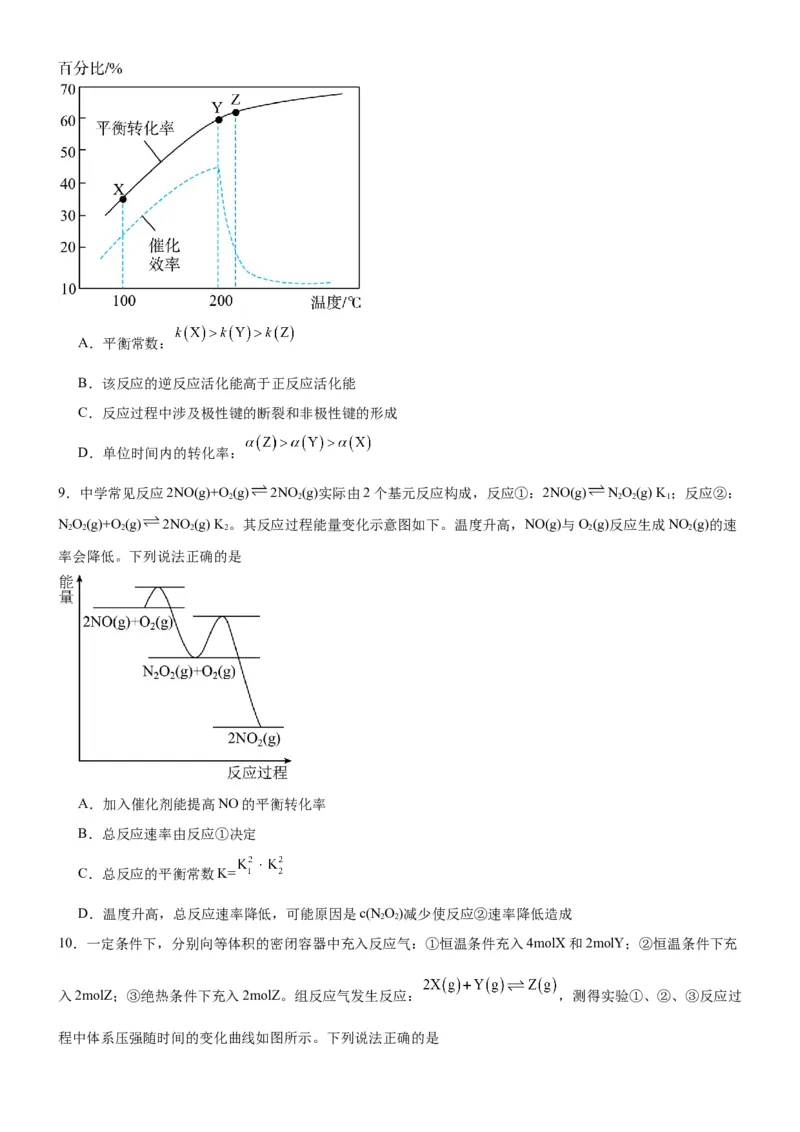
8.工业上广泛采用二氟一氯甲烷 热解制四氟乙烯: ,其他条件不变
时,温度对 的平衡转化率、催化剂的催化效率的影响如图所示,下列说法正确的是A.平衡常数:
B.该反应的逆反应活化能高于正反应活化能
C.反应过程中涉及极性键的断裂和非极性键的形成
D.单位时间内的转化率:
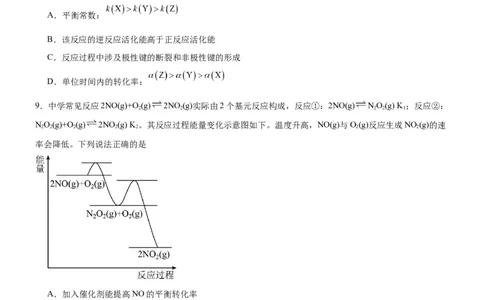
9.中学常见反应2NO(g)+O (g) 2NO (g)实际由2个基元反应构成,反应①:2NO(g) NO(g) K ;反应②:
2 2 2 2 1
NO(g)+O(g) 2NO (g) K 。其反应过程能量变化示意图如下。温度升高,NO(g)与O(g)反应生成NO (g)的速
2 2 2 2 2 2 2
率会降低。下列说法正确的是
A.加入催化剂能提高NO的平衡转化率
B.总反应速率由反应①决定
C.总反应的平衡常数K=
D.温度升高,总反应速率降低,可能原因是c(NO)减少使反应②速率降低造成
2 2
10.一定条件下,分别向等体积的密闭容器中充入反应气:①恒温条件充入4molX和2molY;②恒温条件下充
入2molZ;③绝热条件下充入2molZ。组反应气发生反应: ,测得实验①、②、③反应过
程中体系压强随时间的变化曲线如图所示。下列说法正确的是A.曲Ⅱ对应实验① B.正反应为吸热反应
C.气体的总物质的量: D.c点平衡常数比b点平衡常数大
11.一定温度下,向含一定量 恒容密闭容器中充入 发生反应 ,改变起始
的物质的量,测得 的平衡体积分数变化如图所示,下列说法正确的是
A.a、b、c三点中,b点时 的转化率最大
B. 平衡逆向移动, 平衡体积分数减小
C.d点对应体系,v(正)>v(逆)
D. 三点的平衡常数:
12.某温度下,某气相反应达到化学平衡,平衡常数 ,且正反应为吸热反应。下
列说法正确的是
A.增大 ,则 和 增大
B.减小压强,平衡向生成 的方向移动
C.降低温度,平衡向生成 的方向移动,逆反应速率增大
D.该反应的化学方程式为
13.五氯化磷(PCl )是有机合成中重要的氯化剂,可以由三氯化磷(PCl )氯化得到:PCl (g)
5 3 3+Cl(g)⇌PCl (g)△H=-93.0kJ/mol。某温度下,在2.0L密闭容器中充入1.0molPCl 和0.5molCl ,一段时间后反应
2 5 3 2
达平衡状态,实验数据如下表所示,下列说法不正确的是
t/s 0 50 150 250 350
n(PCl )/mol 0 0.21 0.36 0.40 0.40
5
A.0~150s内,PCl 的反应速率为0.0012mol(L•s)
3
B.反应至250s,该反应放出的热量为37.2kJ
C.该温度下,此反应的化学平衡常数数值为40/3
D.在此温度下,该密闭容器中若初始充入1.0molPCl 、1molCl 、2.0molPCl ,则此时反应向逆反应方向进
3 2 5
行
14.硫、氮物质的研究具有深远意义。回答下列问题:
Ⅰ.硫黄分解磷石膏工艺涉及的主要反应为:
①
②
(1)反应 的 。
(2)在恒温恒容密闭容器中只进行反应①,能说明该反应达到平衡状态的标志是 (填字母)。
A.
B.气体中含硫原子总数不随时间变化
C. 容器内混合气体的密度不再随时间变化
D.容器内混合气体的平均摩尔质量不再随时间变化
(3)在恒温恒容密闭容器中进行反应②,达到平衡时,向容器中( 、 、 均足量)再充入少量 ,
达到新平衡后,与原平衡相比, (填“增大”、“减小”或“不变”),原因是 。
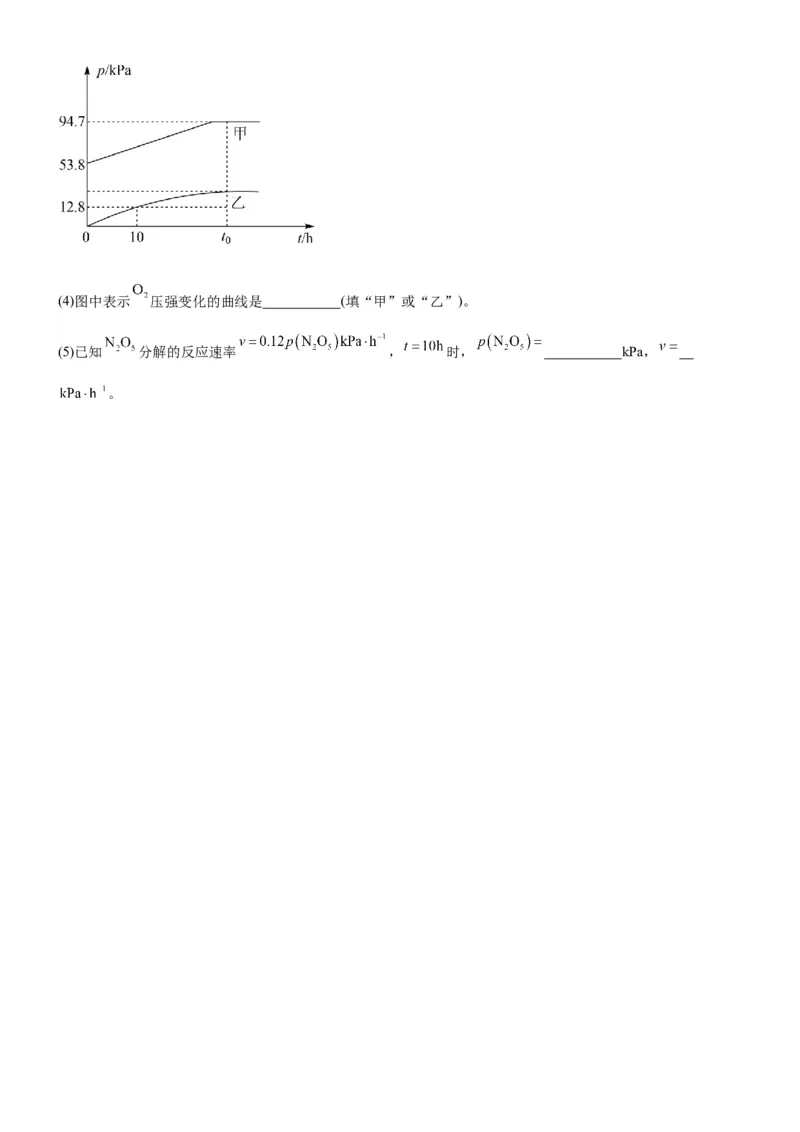
Ⅱ.某温度下, 气体在一体积固定的容器中发生如下反应:
① (慢反应)
② (快反应)
体系的总压强 和 随时间的变化如图所示,已知: 时 完全分解。(4)图中表示 压强变化的曲线是 (填“甲”或“乙”)。
(5)已知 分解的反应速率 , 时, kPa,
。