文档内容
《分子的空间结构》第二课时 教学设计
课题 《分子的空间结 单元 2 学科 化学 年级 高二
构》
本章内容比较系统地介绍了分子的结构与性质,内容比较丰富。首先,在第一章有关
电子云和原子轨道等概念的基础上,介绍了共价键的主要类型δ键和π键,以及键参数
——键能、键长、键角;接着,在共价键概念的基础上,介绍了分子的立体结构,并根据价层
电子对互斥理论和杂化轨道理论对简单共价分子结构的多样性和复杂性进行了解释;最
后,介绍了极性分子和非极性分子、分子间作用力、氢键等概念,以及它们对物质性质的影
响,并从分子结构的角度说明了“相似相溶“规则、无机含氧酸分子的酸性等。本节教学内
容是人教版高中化学选择性必修第二册第二章《分子结构与性质》第二节《分子的空间结
教材 构》第二课时。这一课时的教学内容主要是价层电子对互斥理论。
本节安排了“价层电子对互斥理论”这部分内容。学生通过学习这部分知
分析
识,认识微观结构对分子立体构型的影响,了解共价分子结构的多样性和复杂
性。通过对价层电子对互斥模型的探究,建立解决复杂分子结构判断的思维模
型。
学生能够在分子水平上,从分子结构的视角认识物质的性质,进一步形成
有关物质结构的基本观念;学生的学习兴趣能得到有效保持,学生的科学素养
能得到进一步提高。
教学 宏观辨识与微观探析:通过对典型分子空间结构的学习,认识微观结构对分子空间结
目标 构的影响,了解共价分子结构的多样性和复杂性。
与核 证据推理与模型认知:通过对价层电子对互斥模型的探究,建立解决复杂
心素 分子结构判断的思维模型。
养
重点 价层电子对互斥理论
难点
教学过程
教学环节 教师活动 学生 设计意图
活动
导入新课 【思考】 思考 通过问
1.CO 和H O都是三原子分子,为什么 CO 呈直线 问题 题,引发
2 2 2
形而H O呈V形? 学生思
2
2. CH O和NH 都是四原子分子,为什么CH O呈 考,提高
2 3 2
学生学习
平面三角形而NH 呈三角锥形?
3
积极性。讲授新课 第二节 分子的空间结构
第二课时 价层电子对互斥理论
一、价层电子对互斥理论
价层电子对互斥模型认为,分子的空间结构是中心
原子周围的“价层电子对”相互排斥的结果。 通过对价
VSEPR的“价层电子对”:是指分子中的中心原子 层电子对
与结合原子间的σ键电子对和中心原子上的孤电子对。 互斥模型
多重键只计其中的σ键电子对,不计π电子对。 的探究,
建立解决
价层电子对数目的计算:
复杂分子
价层电子对数目= σ键电子对数+中心原子上的孤
结构判断
电子对数
的思维模
1. σ键电子对数——可由化学式确定
型。
2.中心原子上的孤电子对数
中心原子孤电子对数=
a——表示中心原子的价电子数
对主族元素:a= 最外层电子数;
对于阳离子:a=价电子数-电荷数;
对于阴离子:a=价电子数+电荷数。
x为与中心原子结合的 原子数 。 思考讨
b为与中心原子结合的原子最多能接受的电子数, 论,应用
H为1,其他原子= 8﹣ 该原子的价电子数 。 模型。
【思考与讨论】
认真
(1)以S和P为例,说明如何根据主族元素在周期
思考
表中的位置确定它的价电子数。
S的价电子数是6,P的价电子数是5
(2)以N和Cl为例,说明如何根据主族元素在周
期表中的位置确定它最多能接受的电子数。
N最多能接受的电子数是3,Cl最多能接受的电子
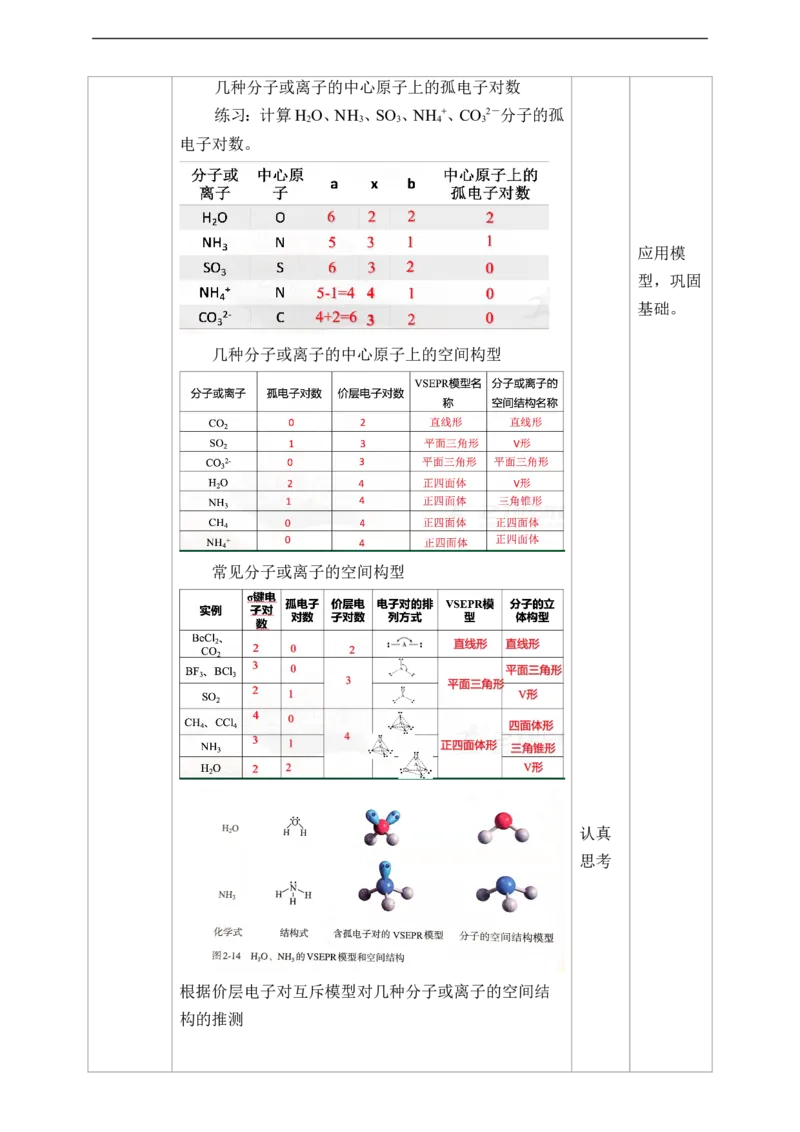
数1几种分子或离子的中心原子上的孤电子对数
练习:计算H O、NH 、SO 、NH +、CO 2-分子的孤
2 3 3 4 3
电子对数。
应用模
型,巩固
基础。
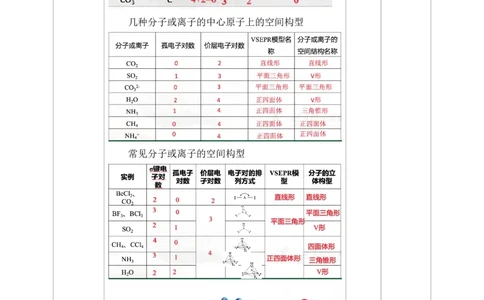
几种分子或离子的中心原子上的空间构型
常见分子或离子的空间构型
认真
思考
根据价层电子对互斥模型对几种分子或离子的空间结
构的推测根据价层电子对互斥模型判断分子的空间构型
对于ABn型分子,利用VSEPR模型预测分子空间结构
的思路:
【思考与讨论】
1. H O、NH 的键角分别是105°、107°,请解释原
2 3
因。
H O、NH 的价层电子对均为4,H O、NH 的的孤电子对
2 3 2 3
分别为2、1,分子中电子对之间的斥力大小顺序:孤电
子对-孤电子对>孤电子对-成键电子对 >成键电子-成
思考交
键电子,故 H O、NH 的键角分别是105°、107°。
2 3 流,认识
价层电子对之间的斥力:
价层电子
①电子对之间的夹角越小,斥力越大。
对之间的
②分子中电子对之间的斥力大小顺序:
斥力。
孤电子对-孤电子对>孤电子对-成键电子对>成键电
子-成键电子。③由于三键、双键比单键包含的电子多,
主动
所以斥力大小顺序:三键>双键>单键 。
探究
2. 确定BF 、NH +、 SO 2- VSEPR模型和它们的空
3 4 3
间结构,并与同学讨论。
BF 的价层电子对均为3, NH +的价层电子对为4,两者
3 4
孤电子对数为0,因此, VSEPR模型和它们的空间结构
相同, BF 为平面三角形, NH +为正四面体。SO 2-的价
3 4 3层电子对为4,孤电子对数为1, VSEPR模型为四面体
形,空间结构为三角锥形。
【课堂练习】
1.以下分子或离子的结构为正四面体形且键与键夹角
为109°28′的是( )
①CH ②GeCl ③CH Cl ④P ⑤SO 2-
4 4 3 4 4
A.①②④ B.①②③④⑤
C.①② D.①②⑤
答案: D
2.下列各组分子的立体构型名称相同的是( )
A.SCl 、BeCl B.BF 、NF
2 2 3 3
C.CF 、SiCl D.CO 、SF
4 4 2 2
答案: C
3.硫化羰(分子式为COS)是一种有臭鸡蛋气味的无色
气体,可视为由一个硫原子取代了CO 分子中的一个氧
2
原子后形成的,下列有关硫化羰的说法正确的是( )
A.硫化羰的结构式为C===O===S
B.分子中三个原子位于同一直线上
C.中心原子价层电子对数为4
D.分子是V形结构
答案: B
4.六氟化硫分子呈正八面体形(如图所示),在高电压下
仍有良好的绝缘性,在电器工业方面有着广泛的用途,
但逸散到空气中会引起温室效应。下列有关六氟化硫的
推测正确的是( )
A.六氟化硫易燃烧生成二氧化硫
B.六氟化硫中各原子均达到8电子稳定结构
C.六氟化硫分子中的S—F键都是σ键,且键长、键能都
相等
D.若将六氟化硫分子中的2个F原子换成Cl原子,可
检测
以得到3种可能结构
反馈答案: C
5.X、Y、Z、W、R是元素周期表前四周期元素中的五种
常见元素,其原子序数依次增大。X的基态原子的最外
层电子排布式为nsnnpn+1。Y、Z同主族且ZY 是导致酸
2
雨的主要物质之一。R位于ds区且原子最外层只有一个
电子。W原子次外层电子数为最外层电子数的7倍。回
答下列问题:
(1)W位于元素周期表第________周期________族,其
基态原子的核外电子排布式为________。
(2)Y的气态氢化物稳定性比Z的气态氢化物的稳定性
________(填“强”或“弱”)。Y的第一电离能比X的
________(填“大”或“小”)。
(3)X的最常见的气体氢化物分子的VSEPR模型为
________,分子的空间构型是________。
(4)原子总数相同、价电子总数相同的分子或离子称为等
电子体。分别写出一种与XO互为等电子体的单质和化
合物的化学式________、________。
答案:(1)四 Ⅷ [Ar]3d64s2 (2)强 小
(3)四面体形 三角锥形 (4)O SO
3 2
课堂小结 一、价层电子对互斥模型(VSEPR模型)板书 一、价层电子对互斥模型(VSEPR模型)