文档内容
2.2.2化学平衡常数(分层作业)
1.在恒温恒容的密闭容器中发生 ,T℃时,该反应
的化学平衡常数为K,下列说法正确的是
A.其他条件相同,升高温度降低正反应速率、提高逆反应速率
B.T℃时,若 时,则
C.若容器内气体压强保持不变,该可逆反应达到化学平衡状态
D.一定条件下, 能完全转化为
【答案】C
【解析】A.升高温度,正逆反应速率都加快,故A错误;
c(H O) c(H O)
2 2
B.T℃时,平衡时的平衡常数K= ,故若 V ,故B错误;
逆
C.反应前后的气体系数和在变化,故恒容时,压强在变化,故压强保持不变时,该可逆反应达到化学平衡状
态,故C正确;
D.可逆反应反应物的转化率不能达到100%,故D错误;
故选C。
2.周期表中ⅥA族元素及其化合物应用广泛。 是常见的氧化剂和助燃剂。 催化氧化是工业制硫酸的重
要反应之一(中和热为 )。Se(硒)是重要的工业原材料与动物体必须营养素。提取Se的主要原材料为
电解铜产生的阳极泥。可通过阳极泥硫酸化焙烧提取Se,硫酸化焙烧提取Se的步骤主要分为两步:第一步焙
烧,硫酸将单质Se氧化为 。第二步还原吸收,在水中 将 转化为单质Se。对于反应
,下列有关说法不正确的是
A.该反应为放热反应 B.上述反应的平衡常数
C.使用催化剂能缩短该反应到达平衡的时间 D.增大体系的压强能提高 的反应速率【答案】B
【解析】A.大多数的化合反应和氧化还原反应为放热反应,该反应既属于化合反应又属于氧化还原反应,所
以该反应为烦热反应,故A正确;
B.平衡常数:各生成物浓度的化学计量数次幂的乘积与各反应物浓度的化学计量数次幂的乘积的比值是个常
C2 (SO )
3
数,则反应2SO (g)+O(g)f 2SO (g)的平衡常数K= ,故B错误;
2 2 3 C2 (SO )·c(O )
2 2
C.催化剂可降低反应的活化能,加快化学反应速率,从而缩短平衡所需的时间,故C正确;
D.反应2SO (g)+O(g)f 2SO (g)为气体参加的反应,增大压强使SO 浓度增大,反应速率加快,故D正确;
2 2 3 2
答案选B。
3.有催化剂的合成塔中发生的反应为 ,
。298K下合成氨反应的平衡常数K=4.1×106,下列说法错误的是
A.合成氨反应在298K时进行得比较完全
B.合成氨反应在298K时反应速率较快
C.仅从K的值无法得知该反应的平衡转化率
D.改变温度,K的值也会变化
【答案】B
【解析】A.一般K>105就认为反应进行得较完全,298K下合成氨反应的平衡常数K=4.1×106>105,因此合成氨
反应在298K时进行得比较完全,A正确;
B.K较大,不能说明速率较快,B错误;
C.没有具体反应数据,仅从K的值无法得知该反应的平衡转化率,C正确;
D.K只和温度有关,改变温度,K的值也会变化 ,D正确;
故选B。
4. 是工业提纯硅的原理之一、下列有关化学反应速率
及其平衡的说法正确的是
A.恒温恒容条件下,增加Si(s)的用量,反应速率加快
B.恒温恒压条件下,向反应容器中通入氦气使容器体积增大,平衡正向移动
C.恒温恒容条件下,当反应体系气体密度不再发生改变,反应达到平衡状态
D.一定条件下反应达平衡后,对反应体系进行升温后重新达平衡,平衡常数增大
【答案】C
【解析】A.Si是固体,增加硅的用量,不影响化学反应速率,故A错误;B.该反应是气体体积减小的反应,恒温恒压条件下,向反应容器中通入氦气使容器体积增大,相当于降低压
强,平衡逆向移动,故B错误;
C.气体密度等于气体总质量除以容器体积,由于有固体参加反应,所以气体总质量在未平衡前是变化的,容
器体积恒定,所以气体密度在未平衡前是变量,当气体密度不再变化时反应达到了平衡状态,所以恒温恒容条
件下,当反应体系气体密度不再发生改变,反应达到平衡状态,故C正确;
D.该反应的正反应是放热反应,达平衡后升高温度,平衡逆向移动,平衡常数减小,故D错误;
故选C。
5.某温度下气体反应体系达到化学平衡,平衡常数K= ,下列说法正确的是
A.该反应的化学方程式为2E(g)+F(g) A(g)+2B(g)
B.降低温度,正反应速率增大
C.该温度时,v(F)=v(A)则反应达到平衡状态
D.增大c(A)、c(B),K增大
【答案】A
【解析】A.化学平衡常数是生成物浓度的系数次方的乘积与反应物浓度系数次方的乘积的比值,根据该反应
c(A)·c2 (B)
的平衡常数表达式K= 可知,该反应的化学方程式为2E(g)+F(g)f A(g)+2B(g),故A正确;
c2 (E)·c(F)
B.降低温度,活化分子百分数减小,有效碰撞几率减小,正逆反应速率都减慢,故B错误;
C.未说明F、A是正反应速率还是逆反应速率,不能判断反应是否达到平衡状态,反应不一定达到平衡状态,
故C错误;
D.平衡常数只与温度有关,若温度不变,c(A)、c(B),K不变,故D错误;
选A。
6.向一恒容密闭容器中加入 和一定量的 ,发生反应: 。
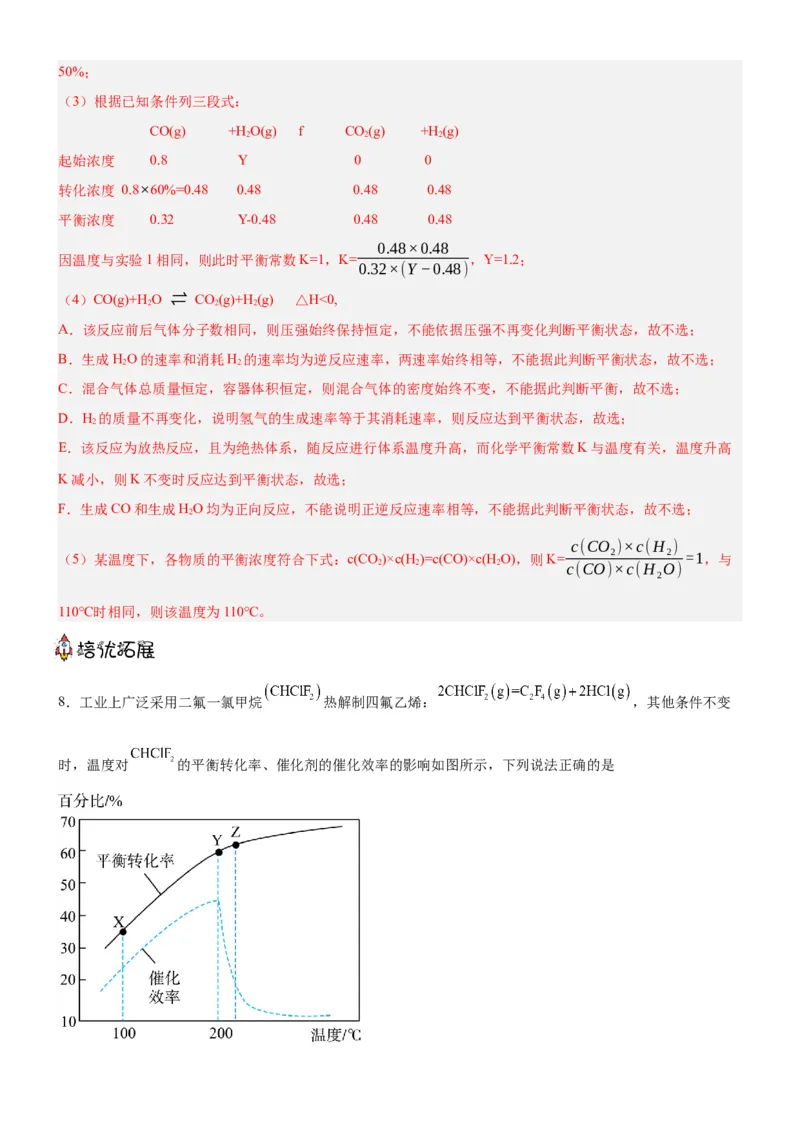
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法错误的是A.
B.反应速率:
C.点a、b、c对应的平衡常数:
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
【答案】B
【解析】A.一定条件下,增大水的浓度,能提高CH 的转化率,即x值越小,CH 的转化率越大,则XV ,故B错误;
b正 c正
C.由图像可知,x一定时,温度升高CH 的平衡转化率增大,说明正反应为吸热反应,温度升高平衡正向移动,
4
K增大;温度相同,K不变,则点a、b、c对应的平衡常数:Kα(X)>α(Z),故D错误。
答案为:C。
9.中学常见反应2NO(g)+O (g) 2NO (g)实际由2个基元反应构成,反应①:2NO(g) NO(g) K ;反应②:
2 2 2 2 1
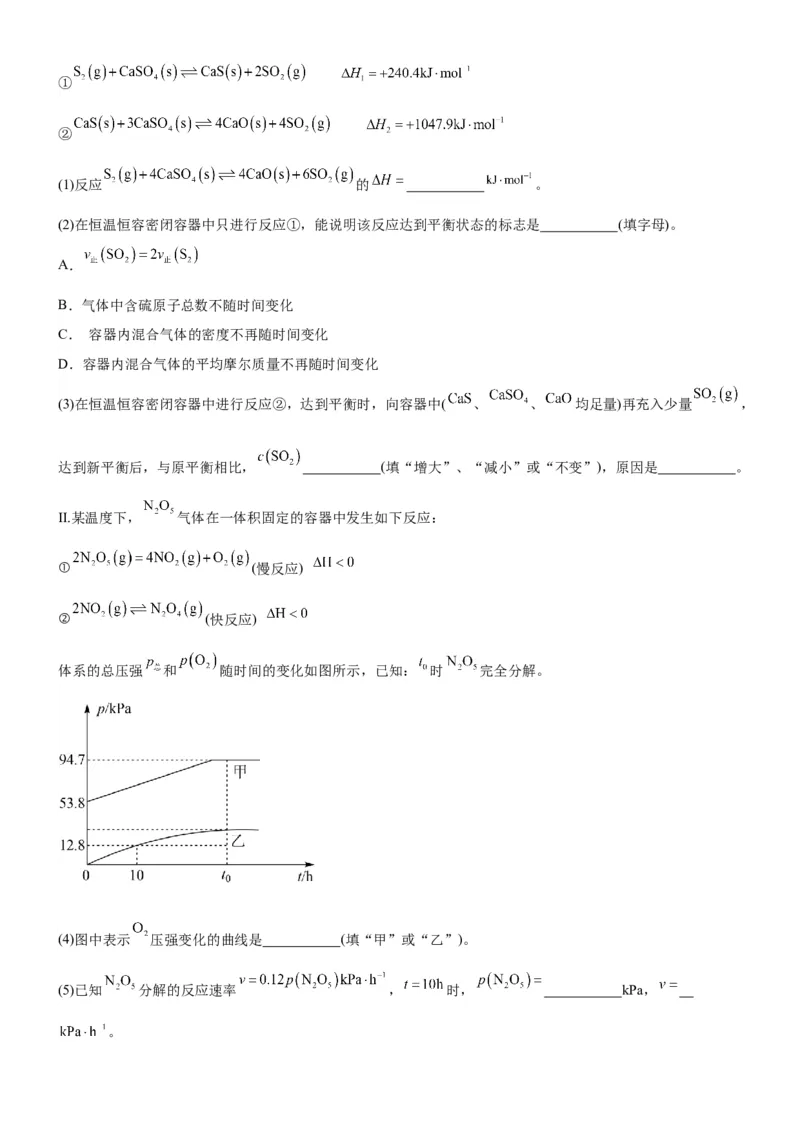
NO(g)+O(g) 2NO (g) K 。其反应过程能量变化示意图如下。温度升高,NO(g)与O(g)反应生成NO (g)的速
2 2 2 2 2 2 2
率会降低。下列说法正确的是
A.加入催化剂能提高NO的平衡转化率
B.总反应速率由反应①决定
C.总反应的平衡常数K=
D.温度升高,总反应速率降低,可能原因是c(NO)减少使反应②速率降低造成
2 2
【答案】D
【解析】A.催化剂只影响反应速率,对平衡无影响,不能改变平衡转化率,故A错误;
B.由图可知反应②的活化能较大,则反应②速率较慢,慢反应决定总反应速率快慢,故B错误;
C.总反应=反应①+反应②,则总反应的平衡常数K=K·K ,故C错误;
1 2
D.由图像可知上述两步反应均为放热反应,则温度升高会使平衡逆向移动,而反应①为快反应,导致c(NO)
2 2减少对速率的影响大于温度对速率的影响,从而使决速步速率降低,则总反应速率降低,故D正确;
故选:D。
10.一定条件下,分别向等体积的密闭容器中充入反应气:①恒温条件充入4molX和2molY;②恒温条件下充
入2molZ;③绝热条件下充入2molZ。组反应气发生反应: ,测得实验①、②、③反应过
程中体系压强随时间的变化曲线如图所示。下列说法正确的是
A.曲Ⅱ对应实验① B.正反应为吸热反应
C.气体的总物质的量: D.c点平衡常数比b点平衡常数大
【答案】D
【分析】实验①正向进行达到平衡过程中压强减小,则曲线Ⅰ对应反应①;实验②逆向建立平衡,且与实验①
最终建立的平衡等效,则曲线Ⅱ对应反应②;曲线Ⅲ对应反应③,据此解答。
【解析】A.实验①正向建立平衡状态,随反应进行体系内压强逐渐减小,曲线Ⅰ符合,故A错误;
B.由曲线Ⅲ变化,反应③逆向进行气体分子数增加,但体系内压强减小,可知是温度降低导致,则正反应为
放热反应,故B错误;
C.由以上分析知该反应为放热反应,而反应③为绝热体系,则随反应逆向进行,反应③对应体系内温度降低,
c、d两点压强相同,但c点温度低于d点,则c点气体物质的量比d点大, 故C错误;
D.c点温度低,反应为放热反应,则c点平衡常数大于b,故D正确;
故选:D。
11.一定温度下,向含一定量 恒容密闭容器中充入 发生反应 ,改变起始
的物质的量,测得 的平衡体积分数变化如图所示,下列说法正确的是A.a、b、c三点中,b点时 的转化率最大
B. 平衡逆向移动, 平衡体积分数减小
C.d点对应体系,v(正)>v(逆)
D. 三点的平衡常数:
【答案】C
【分析】向含一定量O 恒容密闭容器中充入SO 发生反应2SO (g)+O(g) f 2SO (g),改变起始SO 的物质的
2 2 2 2 3 2
量,随着SO 物质的量的增大,平衡正向移动,生成更多的三氧化硫,当SO 与O 的物质的量之比等于化学方
2 2 2
程式中计量系数之比时,三氧化硫的平衡体积分数最大,据此回答。
【解析】A. SO 与O 两种反应物反应,当SO 少,氧气充足时,SO 转化率最大,故a、b、c三点中,a点时
2 2 2 2
SO 的转化率最大,A错误;
2
B.b→c表示继续通入过量二氧化硫,根据勒夏特列原理知平衡正向移动,体系中总的物质的量在增加,故产
物三氧化硫的平衡体积分数在减小, B错误;
C.d点在c点之下说明d点还未达到该条件下的平衡,会继续从正反应方向建立平衡,故v(正)>v(逆),C正确;
D.温度不变,平衡常数不变,故K=K=K,D错误;
b c a
故选C。
12.某温度下,某气相反应达到化学平衡,平衡常数 ,且正反应为吸热反应。下
列说法正确的是
A.增大 ,则 和 增大
B.减小压强,平衡向生成 的方向移动
C.降低温度,平衡向生成 的方向移动,逆反应速率增大
D.该反应的化学方程式为
【答案】D
【分析】根据平衡常数表达式K=c(X)·c2(Y)/[c2(E)·c(F)],该反应的化学方程式为2E(g)+F(g) f X(g)+2Y(g),据
此作答。【解析】A.增大c(X),平衡往逆向移动,c(Y)减小,K只受温度影响,不变,故A错误;
B.该反应左右两边气体分子数相等,减小压强,平衡不移动,故B错误;
C.该反应为吸热反应,降低温度,平衡往逆向移动,即生成F的方向移动,但是正逆反应速率均减小,故C
错误;
D.根据分析,该反应的化学方程式为2E(g)+F(g) f X(g)+2Y(g),故D正确;
故选D。
13.五氯化磷(PCl )是有机合成中重要的氯化剂,可以由三氯化磷(PCl )氯化得到:PCl (g)
5 3 3
+Cl(g)⇌PCl (g)△H=-93.0kJ/mol。某温度下,在2.0L密闭容器中充入1.0molPCl 和0.5molCl ,一段时间后反应
2 5 3 2
达平衡状态,实验数据如下表所示,下列说法不正确的是
t/s 0 50 150 250 350
n(PCl )/mol 0 0.21 0.36 0.40 0.40
5
A.0~150s内,PCl 的反应速率为0.0012mol(L•s)
3
B.反应至250s,该反应放出的热量为37.2kJ
C.该温度下,此反应的化学平衡常数数值为40/3
D.在此温度下,该密闭容器中若初始充入1.0molPCl 、1molCl 、2.0molPCl ,则此时反应向逆反应方向进
3 2 5
行
【答案】D
0.36mol
【解析】A.0~150s内,消耗PCl 的物质的量为0.36mol,反应速率为 =0.0012 0.0012mol(L•s),
3 2L×150s
故A正确;
B.反应至250s,生成0.4mol PCl ,该反应放出的热量为93.0kJ/mol×0.4mol=37.2kJ,故B正确;
5
C.该温度下,此反应达到平衡,生成0.4mol PCl ,反应消耗0.4molPCl 、0.4molCl ,则平衡时PCl 的物质的
5 3 2 3
0.4mol
2L 40
量为0.6mol、Cl 的物质的量为0.1mol,化学平衡常数数值为 = ,故C正确;
2 0.6mol 0.1mol 3
×
2L 2L
2mol
2L
D.在此温度下,该密闭容器中若初始充入1.0molPCl 、1molCl 、2.0molPCl ,Q= =4