文档内容
第二章 海水中的重要元素—钠和氯
第三节 物质的量 课时作业
第三课时 物质的量浓度
基础达标
1.用21.2g的NaCO 固体配成溶液100ml,所得溶液的物质的量浓度为( )
2 3
A.0.4mol/L B.0.2mol/L
C.4mol/L D.2mol/L
2.下列关于0.1mol•L-1Ba(NO ) 溶液的说法中正确的是( )
3 2
A.1L该溶液中含有Ba2+的质量为1.37g
B.1L该溶液中c(NO )=0.05mol•L-1
C.1L该溶液中含有0.1molBa2+
D.该溶液就是将26.1g的Ba(NO ) 溶于1L水中所得到的溶液
3 2
3.下列说法不正确的是( )
A.HO的摩尔质量为18g/mol
2
B.标准状况下,1molN 的体积是22.4L
2
C.44gCO 中含有的氧原子数约为6.02×1023
2
D.0.5mol·L-1NaCO 溶液中c(Na+)是1mol·L-1
2 3
4.从100 mL0.5 mol·L-1NaOH 溶液中取出1mL,并加水稀释到50mL,关于稀释后的溶
液下列叙述正确的是( )
A.含NaOH的质量为2 g B.含NaOH的物质的量为0.005 mol
C.浓度为 0.01 mol • L-1 D.浓度为 0.5 mol • L-1
5.下列溶液含有的氯离子的物质的量浓度最大的是( )
A.1mL 0.2mol/L 溶液 B.1mL 0.5mol/L 溶液
C.2mL 0.3mo/L NaCl溶液 D.4mL 0.1mol/L 溶液
6.下列关于2 mol/LBa(NO ) 溶液的说法正确的是( )
3 2
A.100 mL溶液中NO -浓度是0.4 mol/L
3
B.500 mL溶液中NO -的物质的量是2 mol
3
C.500 mL溶液中含有 的质量是137 gD.100 mL溶液中所含Ba2+、NO -总数为0.4N
3 A
7.设N 为阿伏加德罗常数的值,下列对0.3 mol·L-1 KSO 溶液的叙述正确的是(
A 2 4
)
A.1 L该溶液中含有0.3N 个K+
A
B.1 L该溶液中含有K+和SO 2-的总数为0.9N
4 A
C.2 L该溶液中K+的浓度为1.2 mol·L-1
D.将0.3 mol硫酸钾溶于1 L水中,所得硫酸钾溶液的浓度为0.3 mol·L-1
8.某试剂瓶上贴有如下标签“100mL 1.0mol•L﹣1MgCl 溶液”,对该试剂理解正确的
2
是( )
A.该溶液中含有的微粒主要有:MgCl 、Mg2+、Cl﹣、HO
2 2
B.若取 50mL 溶液,其中的 c(Cl﹣)=1 mol•L﹣1
C.取该溶液 5.0 mL 恰好与 0.1 mol•L﹣1 AgNO100 mL 溶液完全反应
3
D.该溶液与 100mL 1.0 mol•L﹣1 NaCl 溶液中的 c(Cl﹣)相等
9.把100 g密度为1.22 g·mL-1的NaOH溶液蒸发浓缩,当余下溶液50 mL时,其物
质的量浓度为8 mol·L-1,(蒸发时无固体析出),则原溶液浓度为( )
①2.44 mol·L-1 ②4% ③4.88 mol·L-1 ④16%
A.③④ B.②③ C.①② D.①④
10.实验室为确定一瓶稀硫酸的浓度,用0.20 mol·L-1 NaOH溶液中和50.00 mL该稀
硫酸,当酸与碱恰好完全反应时,消耗NaOH溶液50.00 mL,下列说法正确的是( )
A.该硫酸的物质的量浓度为0.10 mol·L-1
B.该硫酸的物质的量浓度为0.20 mol·L-1
C.在最终得到的溶液中,SO 2-的物质的量为0.01 mol
4
D.在最终得到的溶液中,Na+的物质的量浓度仍为0.20 mol·L-1
能力提升
11.现有浓度为1mol·L-1的盐酸1L,欲使其浓度增大1倍,采取的措施合理的是(
)
A.通入标准状况下的HCl气体22.4L
B.将溶液加热浓缩到0.5L
C.加入10.00mol·L-1的盐酸0.2L,再稀释至1.5L
D.加入1L3mol·L-1的盐酸混合均匀12.T ℃时,有硫酸镁溶液500 mL,它的密度是1.20 g·cm-3,其中镁离子的质量分数
是4.8%,则有关该溶液的说法不正确的是( )
A.溶质的质量分数是24.0%
B.溶液的物质的量浓度是2.4 mol·L-1
C.溶质和溶剂的物质的量之比是1∶21
D.若此溶液为饱和溶液,则硫酸镁在该温度下的溶解度是 g=24 g
13.将标准状况下的a L氨气溶于1000 g水中,得到氨水的密度为b g·cm-3,则该氨
水的物质的量浓度为( )
ab ab
A.
22400
mol·L-1 B.
22400+17a
mol·L-1
1000ab 1000ab
C.
22400+17a
mol·L-1 D.
22400+35a
mol·L-1
14.标准状况下11.2 L HCl气体溶于水形成500 mL溶液。
(1)所得盐酸的物质的量浓度为 。
(2)向其中加入 g NaOH才能中和完全。
(3)若不考虑加入NaOH对体积造成的影响,所得NaCl的物质的量浓度为 。
(4)再向其中加入 mL密度为1.7 g·cm-3、质量分数为25%的AgNO 溶液可使
3
Cl-完全沉淀。
直击高考
15.4 ℃下,把摩尔质量为M g·mol-1的可溶性盐RCl A g溶解在V mL水中,恰好形
n
成该温度下的饱和溶液,密度为ρ g·cm-3,下列关系式错误的是( )
A.溶质的质量分数w=×100%
B.溶质的物质的量浓度c= mol·L-1
C.1 mL该溶液中n(Cl-)= mol(RCl 在溶液中完全电离)
n
D.该温度下此盐的溶解度S= g
16.硫酸铜在水产养殖业中可用于防治多种鱼病,不同鱼类对硫酸铜浓度的适应性不
同,在使用时需注意掌控用量。为测定某CuSO 溶液的浓度,研究性学习小组设计了以下
4
两个实验方案。
【方案Ⅰ】实验步骤:
(1)步骤②中检验固体是否洗涤干净选用的试剂为___________。(2)步骤③灼烧时盛放药品的仪器是___________。
(3)步骤④称得固体质量为2.33g,则c(CuSO)___________ 。
4
(4)若步骤①将烧杯中的固液混合物转移入过滤器时未洗涤烧杯,则导致c(CuSO)的测
4
定值___________(填“偏高”、“偏低”或“无影响”)。
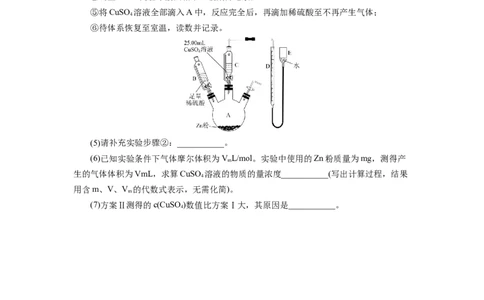
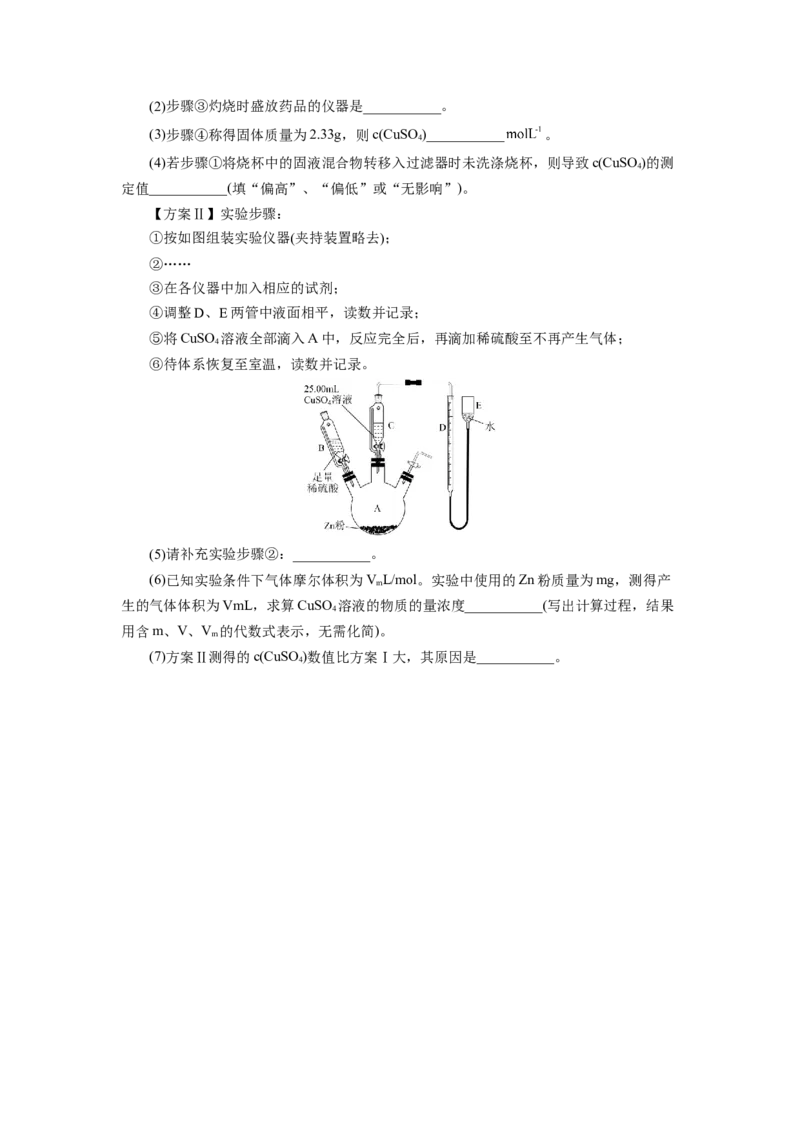
【方案Ⅱ】实验步骤:
①按如图组装实验仪器(夹持装置略去);
②……
③在各仪器中加入相应的试剂;
④调整D、E两管中液面相平,读数并记录;
⑤将CuSO 溶液全部滴入A中,反应完全后,再滴加稀硫酸至不再产生气体;
4
⑥待体系恢复至室温,读数并记录。
(5)请补充实验步骤②:___________。
(6)已知实验条件下气体摩尔体积为V L/mol。实验中使用的Zn粉质量为mg,测得产
m
生的气体体积为VmL,求算CuSO 溶液的物质的量浓度___________(写出计算过程,结果
4
用含m、V、V 的代数式表示,无需化简)。
m
(7)方案Ⅱ测得的c(CuSO)数值比方案Ⅰ大,其原因是___________。
4