文档内容
第三节 物质的量
第3课时 物质的量浓度
基础巩固
1.下列关于0.1 mol·L-1NaCO 溶液的叙述错误的是( )
2 3
A.该溶液中含有NaCO 的质量为10.6 g
2 3
B.1 L该溶液中Na+的物质的量浓度为0.2 mol·L-1
C.从1 L该溶液中取出100 mL,则取出溶液中NaCO 的物质的量浓度为0.1 mol·L-1
2 3
D.取该溶液10 mL,加水稀释至100 mL后所得溶液中NaCO 的物质的量浓度为0.01 mol·L-1
2 3
【答案】A
【解析】A项,题中没有给出溶液的体积,故不可能求出溶质的质量,A项错误;B项,c(Na+)与溶液的
体积没有关系,c(Na+)=2c(Na CO)=0.2 mol·L-1,B项正确;C项,溶液是均一、稳定的,从1 L该溶
2 3
液中取出100 mL,c(Na CO)不变,仍为0.1 mol·L-1,C项正确;D项,溶液进行稀释时,根据溶质的物
2 3
质的量守恒cV=cV,可以求出稀释后溶液的浓度为0.01 mol·L-1,D项正确;故选A。
1 1 2 2
2.下列说法中正确的是
A.将322gNaSO ·10H O溶于1L水中,所得溶液的物质的量浓度为1mol·L-1
2 4 2
B.将1L2mol·L-1硫酸溶液加水稀释到2L,所得溶液的物质的量浓度为1mol·L-1
C.将1L18.4mol·L-1硫酸溶液加入到1L水中,所得溶液物质的量浓度为9.2mol·L-1
D.将336mL氯化氢溶于水,配成300mL溶液,所得溶液物质的量浓度为0.05mol·L-1
【答案】B
【解析】A.322 g Na SO •10H O物质的量为1mol,溶于1 L水中、则溶液体积不等于1L,所得溶液的物
2 4 2
质的量浓度不等于1 mol/L,故A错误;
B.依据稀释溶液后溶质物质的量不变计算,将1 L 2 mol/L H SO 溶液加水稀释到2 L,所得溶液的物质
2 4
的量浓度为1 mol/L,故B正确;
C.18.4 mol/L的HSO 溶液加入到1L水中、则溶液体积不等于1L,所得溶液物质的量浓度不等于
2 4
9.2mol·L-1,故C错误;
D.未指明气体是否处于标准状况,溶质不一定是0.015mol,配成300mL溶液,所得溶液物质的量浓度
不一定为0.05mol·L-1,故D错误;
故答案为B。
3.下列所得溶液的物质的量浓度为0.1mol/L的是( )
A.将0.1mol氨充分溶解在1L水中
B.将10g质量分数为98%的硫酸与990g水混合
C.将25.0g胆矾溶于水配成1L溶液
D.将10mL1mol/L的盐酸与90mL水充分混合
【答案】C
【解析】A. 将0.1mol氨充分溶解在1L水中,所得溶液的体积不是1L,故不能得到0.1mol/L的溶液,A
错误;
学科网(北京)股份有限公司B. 将10g质量分数为98%的硫酸与990g水混合,不知所配溶液的密度,无法求算其物质的量浓度,B错
误;
C. 将25.0g胆矾的物质的量为0.1mol,将其溶于水配成1L溶液,所得溶液的物质的量浓度为0.1mol/L,
C正确;
D. 将10mL1mol/L的盐酸与90mL水充分混合,不同液体混合后的体积,不等于两液体体积在数值上的
简单加和,D错误;
故答案选C。
4.下列溶液中的Cl-物质的量与100mL1mol·L-1AlCl 溶液中Cl-物质的量相等的是( )
3
A.150mL1mol·L-1KCl溶液 B.100mL3mol·L-1KClO 溶液
3
C.75mL2mol·L-1CaCl 溶液 D.50mL1mol·L-1FeCl 溶液
2 3
【答案】C
【解析】A项,150mL 1mol•L-1氯化钠溶液中c(Cl-)=1 mol•L-1×1=1mol/L,Cl-物质的量
为1mol/L×0.15L=0.15mol,A错误;B项,100mL 3mol•L-1KClO 溶液中不含有氯离子,故Cl-物质的量为
3
0,B错误;C项,75mL 2 mol•L-1CaCl 溶液中c(Cl-)=2 mol•L-1×2=4mol/L,Cl-物质的量
2
为4mol/L×0.075L=0.3mol,C正确;D项,50mL 1 mol•L-1FeCl 溶液中c(Cl-)=1 mol•L-1×3=3mol/L,Cl-物质
3
的量为3mol/L×0.05L=0.15mol,D错误;故选C。
5.设 为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下, 水中约含 分子数目为
B. 的 溶液中含 的数目为
C. 与足量盐酸完全反应时,失去电子的数目为
D.将 固体溶于 中,得到 的 溶液
【答案】C
【解析】A.标准状况下,水是液体,不能用气体摩尔体积计算物质的量,故A错误;
B.溶液体积未知,无法计算 的 溶液中含 的数目,故B错误;
C. 的物质的量为0.1mol,每个钠原子失去一个电子,所以 与足量盐酸完全反应时,失
去电子的数目为0.1N ,故C正确;
A
D.40gNaOH的物质的量为1mol,将 固体溶于 中,溶液的体积不是1L,所以得到的
溶液浓度不是1mol/L,故D错误;
答案选C。
6.V mL Al (SO ) 溶液中含有Al3+m g,取 mL该溶液用水稀释至4V mL,则SO 物质的量浓度为
2 4 3
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
【答案】 A
学科网(北京)股份有限公司【解析】 mL溶液中Al3+的物质的量为 = mol,稀释后溶液中Al3+的物质的量浓度为
c(Al3+)= = mol·L-1,c(SO )= c(Al3+)= × mol·L-1= mol·L-1。
7.1L浓度为1 mol·L-1的盐酸,欲使其浓度增大1倍,采取的措施合理的是( )
A.通入标准状况下的HCl气体22.4 L
B.将溶液加热浓缩到0.5 L
C.加入10.00mol·L-1的盐酸0.2 L,再稀释至1.5 L
D.加入2 L 1mol·L-1的盐酸混合均匀
【答案】C
【解析】A项、标准状况下的HCl气体22.4L,物质的量是1mol,1L浓度为1mol•L-1的盐酸中HCl的物质的
量为1mol,但无法计算通入氯化氢后溶液的体积,故A错误;
B项、加热浓缩盐酸时,导致盐酸挥发,溶质的物质的量偏小,故B错误;
C项、VL浓度为0.5mol•L-1的盐酸的物质的量是0.5Vmol,10mol•L-1的盐酸0.1VL的物质的量是Vmol,再
稀释至1.5VL,所以C=(0.5Vmol+Vmol)/1.5VL=2 mol•L-1,故C正确;
D项、浓稀盐酸混合后,溶液的体积不是直接加和,所以混合后溶液的物质的量浓度不是原来的2倍,故
D错误。
8.在 2L 由 NaCl、MgCl 、BaCl 组成的混合液中,部分离子浓度大小如图所示,则此 溶液中 Ba2+的物
2 2
质的量是( )
A.3.0mol B.2.0mol C.1.0mol D.0.5 mol
【答案】D
【解析】依据图示可知钠离子浓度为1.0mol/L,镁离子浓度为0.5mol/L,氯离子浓度为3.0mol/L,则依据
电荷守恒可知:1.0mol/L×1+0.5mol/L×2+c(Ba2+)×2=3.0mol/L×1,解得c(Ba2+)=0.5mol/L,故答案为D。
9.将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.22 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为________。
(2)该溶液中NaOH的质量分数为________。
(3)从上述溶液中取出10 mL,其中NaOH的物质的量浓度为________,NaOH的质量分数为________,溶
液的密度为________,含NaOH的质量为________,含NaOH的物质的量为________。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为________。
【答案】 (1)6.1 mol·L-1
(2)20%
学科网(北京)股份有限公司(3)6.1 mol·L-1 20% 1.22 g·mL-1 2.44 g 0.061 mol
(4)0.61 mol·L-1
【解析】 (1)n(NaOH)=m(NaOH)/M(NaOH)==0.61 mol,c(NaOH)===6.1 mol·L-1。
(2)100 mL NaOH溶液的质量为100 mL×1.22 g·mL-1=122 g。w(NaOH)=24.4 g÷122 g×100%=20%。
(3)从原溶液中取出10 mL溶液,其中溶质的物质的量浓度、溶质质量分数、溶液的密度均不会改变,但
所含NaOH的质量、物质的量均变为原来的。
(4)取出的10 mL NaOH溶液中溶质的物质的量浓度为6.1 mol·L-1,稀释到100 mL后,NaOH的物质的量
浓度减小,为6.1 mol·L-1÷10=0.61 mol·L-1。
10.常温下,在27.5g水中溶解12.5g CuSO ·5H O,溶液恰好达到饱和,该溶液的密度为2.0g/mL。则
4 2
(1)该溶液中溶质的阴、阳离子的总物质的量为__________mol。
(2)该溶液中CuSO 的物质的量浓度为__________ 。
4
(3)取出20.0mL该溶液,配成物质的量浓度为1.0mol/L的稀溶液,则稀释后溶液的体积是____mL。
【答案】0.1 2.5 50.0
【解析】 (1)n(CuSO )= n(CuSO ·5H O)= ,所以溶质的阴、阳离子的总物质的量为
4 4 2
0.05mol2=0.1mol。
(2)溶液体积V= =20mL=0.02L,故c(CuSO )= =2.5mol/L。
4
(3)取出溶液中含溶质硫酸铜的物质的量为:2.5mol/L×0.02L=0.05mol,故稀释后溶液的体积为
=0.05L=50.0mL。
能力提升
11.学校购买了批消毒用的84消毒液,包装如图:
请根据以上信息和相关知识判断,下列分析不正确的是( )
A.该84消毒液中NaClO的浓度约为40mol/L
B.一瓶该84消毒液能吸收空气中89.6L的CO (标准状况下)而变质
2
C.取100mL该84消毒液稀释100倍后用于消毒,稀释后的溶液中c(Na+)约为0.04mol/L
D.参阅该84消毒液的配方,欲用NaClO固体配制含25%NaClO的消毒液480mL,需要称量NaClO固体的质
量为143.0g
【答案】D
【解析】 A项,根据 得,该84消毒液中 ;B
学科网(北京)股份有限公司项 , 一 瓶 该 84 消 毒 液 中 , 根 据 反 应
,可知 ,吸收的 在标准状况下的体积为 ;C
项溶液稀释时,溶液中溶质的物质的量不变, ,则稀释后的溶
液中 ;D项,配制480mL的溶液应选取500mL规格的容量瓶,所以需
要NaClO的质量为 ;故选D。
12.36.5 g HCl溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为
w,物质的量浓度为c mol·L-1,N 表示阿伏加德罗常数,则下列叙述中正确的是( )
A
A.所得溶液的物质的量浓度为1 mol·L-1
B.所得溶液中含有N 个HCl分子
A
C.36.5 g HCl气体占有的体积为22.4 L
D.所得溶液的质量分数:w=
【答案】D
【解析】A项,1 L水溶解了溶质后体积不再是1 L,故无法计算浓度,A错误;B项,HCl是强电解质,
溶于水完全电离为H+和Cl-,不存在HCl分子,B错误;C项,36.5 g HCl气体所处的温度和压强未知,
不能用标准状况下的气体摩尔体积计算其体积,C错误;D项,根据基本公式c= 变形可得w=
= ,D正确;故选D。
13.(2021·前郭尔罗斯蒙古族自治县蒙古族中学)体积为VmL,密度为的ρg/cm3含有相对分子质量为M的
某种物质的溶液,其中溶质为mg,其物质的量浓度为cmol/L,溶质的质量分数为w%,则下列表示正确
的是( )
A. B. C.c= D.
【答案】A
【解析】A项, ,A项正确;B项, ,
B项错误;C项, ,C项错误;D项,
,则 ,D项错误;故选A。
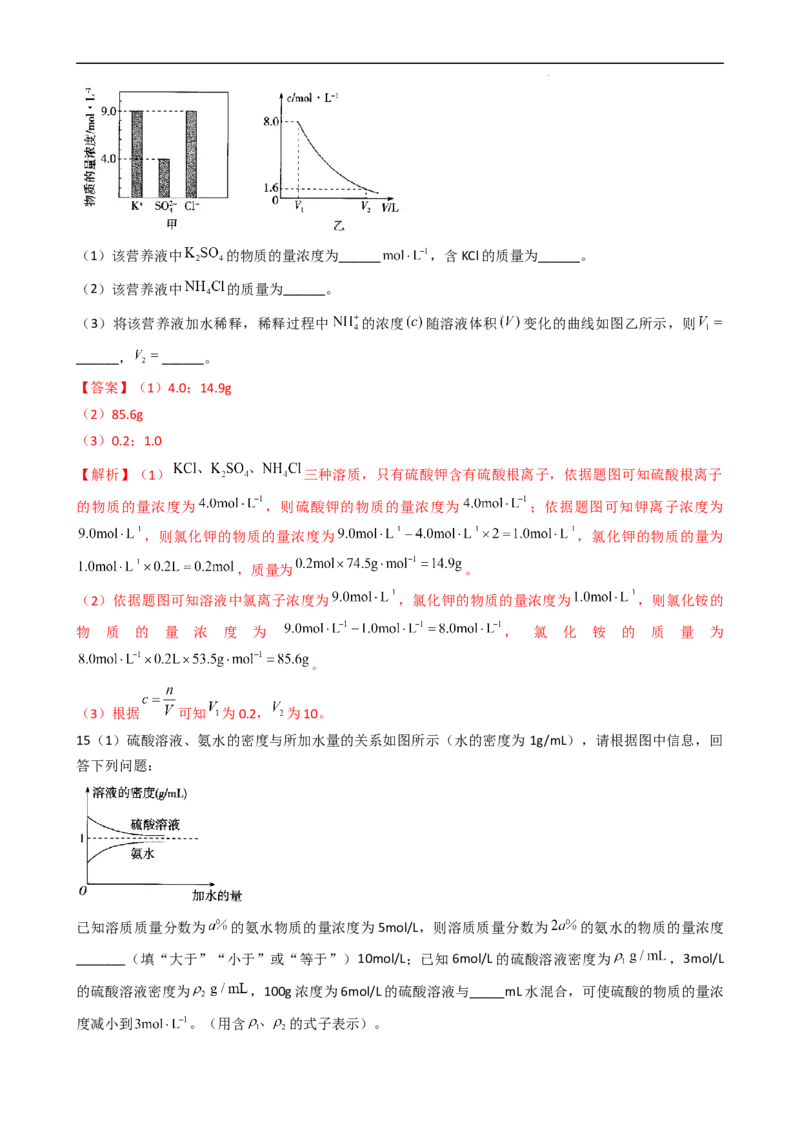
14.某0.2L无土栽培用的营养液中含有 三种溶质,测得该营养液中部分离子的浓度柱
状图如图甲所示:
学科网(北京)股份有限公司(1)该营养液中 的物质的量浓度为______ ,含KCl的质量为______。
(2)该营养液中 的质量为______。
(3)将该营养液加水稀释,稀释过程中 的浓度 随溶液体积 变化的曲线如图乙所示,则
______, ______。
【答案】(1)4.0;14.9g
(2)85.6g
(3)0.2;1.0
【解析】(1) 三种溶质,只有硫酸钾含有硫酸根离子,依据题图可知硫酸根离子
的物质的量浓度为 ,则硫酸钾的物质的量浓度为 ;依据题图可知钾离子浓度为
,则氯化钾的物质的量浓度为 ,氯化钾的物质的量为
,质量为 。
(2)依据题图可知溶液中氯离子浓度为 ,氯化钾的物质的量浓度为 ,则氯化铵的
物 质 的 量 浓 度 为 , 氯 化 铵 的 质 量 为
。
(3)根据 可知 为0.2, 为10。
15(1)硫酸溶液、氨水的密度与所加水量的关系如图所示(水的密度为 1g/mL),请根据图中信息,回
答下列问题:
已知溶质质量分数为 的氨水物质的量浓度为5mol/L,则溶质质量分数为 的氨水的物质的量浓度
_______(填“大于”“小于”或“等于”)10mol/L;已知6mol/L的硫酸溶液密度为 ,3mol/L
的硫酸溶液密度为 ,100g浓度为6mol/L的硫酸溶液与_____mL水混合,可使硫酸的物质的量浓
度减小到 。(用含 的式子表示)。
学科网(北京)股份有限公司(2)有一硫酸和硝酸的混合溶液,取出其中的 10mL,加入足量 溶液可得白色沉淀9.32g;另取
10mL该混合溶液,与 25mL4mol/L的NaOH溶液恰好完全中和。则混合溶液中 =________,
=_______。
答案】(1)小于; (2)4mol/L 2mol/L
【
【解析】:(1)设溶质质量分数为 的氨水的密度为 ,由氨水的物质的量浓度为5mol/L可得
,设溶质质量分数为 的氨水的密度为 、物质的量浓度为
,可得 ,两式相比可得 ,由氨水浓度越大密度越小可
知 ,则 ;设需要水的体积为 ,由题意可知混合后所得的 3mol/L硫酸溶液的质量为
,由稀释定律可得: ,解得 。
(2)由加入足量 溶液可得硫酸钡白色沉淀 9.32g 可知,10mL 混合溶液中硫酸的物质的量为
,则硫酸的浓度为 ;由10mL该混合溶液与25mL4mo/L的NaOH
溶液恰好完全中和可知,硝酸的物质的量为(4mol/L×0.025L-004mol×2)=0.02mol,则硝酸的浓度为
。
学科网(北京)股份有限公司学科网(北京)股份有限公司