文档内容
3.1.1 强电解质和弱电解质 弱电解质的电离平衡(学案)
重点理解弱电离平衡平衡常数。
弱电离平衡平衡常数
六大强酸是_____________________________________________________。
四大强碱是_____________________________________________________。
一、电离平衡常数(K)、电离度(α)
1.电离常数
(1)表示方法
AB A++B- K=________________
弱电解质的电离常数表达式中的c(A+)、c(B-)和c(AB)均为达到电离平衡后各粒子在溶液中的浓度
值,并不是直接指溶质的物质的量浓度值,并且在温度一定时,其电离常数就是一个定值。
①一元弱酸、一元弱碱的电离常数。例如:
CHCOOH CHCOO-+H+,K=________________
3 3
NH ·H O NH+OH-,K=________________
3 2
②多元弱酸、多元弱碱的电离常数。
多元弱酸的电离是分步进行的,每步都有相应的电离常数,通常用K ,K ,K 等来分别表示。
a1 a2 a3
例如:H PO H++H PO -,K =________________
3 4 2 4 a1
H PO - H++HPO 2-,K =________________
2 4 4 a2
HPO 2- H++PO 3-,K =________________
4 4 a3
多元弱酸各步的电离常数大小的比较为K K K ,因此多元弱酸的酸性主要由第一步电离
a1 a2 a3
决定。
≫ ≫
多元弱碱的电离与多元弱酸的电离情况相类似,但多元弱碱的电离可写成一步。
(2)影响因素
电离常数只与_________有关,_________,K值增大。
(3)电离常数的意义
①表示多元弱酸溶液中离子浓度的关系。
HPO 分三步电离,第一步最强(K =7.5×10-3),第二步弱(K =6.2×10-8),第三步最弱(K =
3 4 a1 a2 a3
2.2×10-13),c(H+)>c(HPO)>c(HPO)>c(PO)>c(OH-)。
2HS分两步电离,第一步强(K =9.1×10-8),第二步弱(K =1.1×10-12),c(H+)>c(HS-)>c(S2-)>
2 a1 a2
c(OH-)
②根据电离常数的大小,可以估算弱电解质电离的程度。例如,在相同条件下,K值越大,弱
酸的电离程度越大,酸性越强。在相同条件下,常见弱酸的酸性强弱关系为
HPO >HF>CHCOOH>HCO>HS>HClO。
3 4 3 2 3 2
2.电离度
(1)弱电解质的电离度用α表示
则____________________________________
或____________________________________
或____________________________________
【练习】1.已知25℃时,一元弱碱XOH和二元弱酸H Y的电离平衡常数如下表,下列说法错误
2
的是( )
弱电解质 XOH H Y
2
电离常数 K =1.0×10﹣5 K =1.0×10﹣3
b a1
K =1.0×10﹣8
a2
A.浓度均为0.1mol•L﹣1的XOH与XCl等体积混合,溶液中离子浓度:c(Cl﹣)>c(X+)
B.0.1mol•L﹣1的NaHY溶液中部分微粒浓度大小:c(Na+)>c(HY﹣)>c(Y2﹣)>c
(H Y)
2
C.用XOH滴定H Y生成XHY时,选用甲基橙作为指示剂比选用酚酞好
2
D.浓度均为0.1mol•L﹣1的XOH、H Y溶液中水电离出的c(H+):前者大于后者
2
【练习】2.室温时,1mol•L﹣1的HA溶液和1mol•L﹣1的HB溶液,起始时的体积均为V ,分别向
0
两溶液中加水进行稀释,所得曲线如图所示。下列说法中正确的是( )
A.M点溶液中c(A﹣)大于N点溶液中c(B﹣)
B.HA的电离常数约为10﹣6
C.浓度均为0.1mol•L﹣1的NaA和HA混合溶液的pH>7
D.M、P两点的溶液分别用等浓度的NaOH溶液中和,消耗的NaOH溶液体积:P=M
【练习】3.常温下,草酸H C O 的K =5.9×10﹣2,K =6.4×10﹣5;碳酸H CO 的K =4.3×10﹣
2 2 4 a1 a2 2 3 a1
7,K =5.6×10﹣11.下列说法正确的是( )
a2
A.NaHCO 、NaHC O 都属于酸式盐且它们对应的水溶液都呈碱性
3 2 4B.0.010mol•L﹣1NaHCO 溶液中:c(HCO ﹣)>c(H+)>c(H CO )>c(CO 2﹣)
3 3 2 3 3
C.Na CO 溶液中滴入少量H C O 溶液时,反应生成NaHCO 和NaHC O
2 3 2 2 4 3 2 4
D.10.0mL 0.10mol•L﹣1H C O 溶液与等体积NaOH溶液混合,溶液恰好呈中性:n(Na+)+n
2 2 4
(H C O )﹣n(C O 2﹣)=0.001mol
2 2 4 2 4
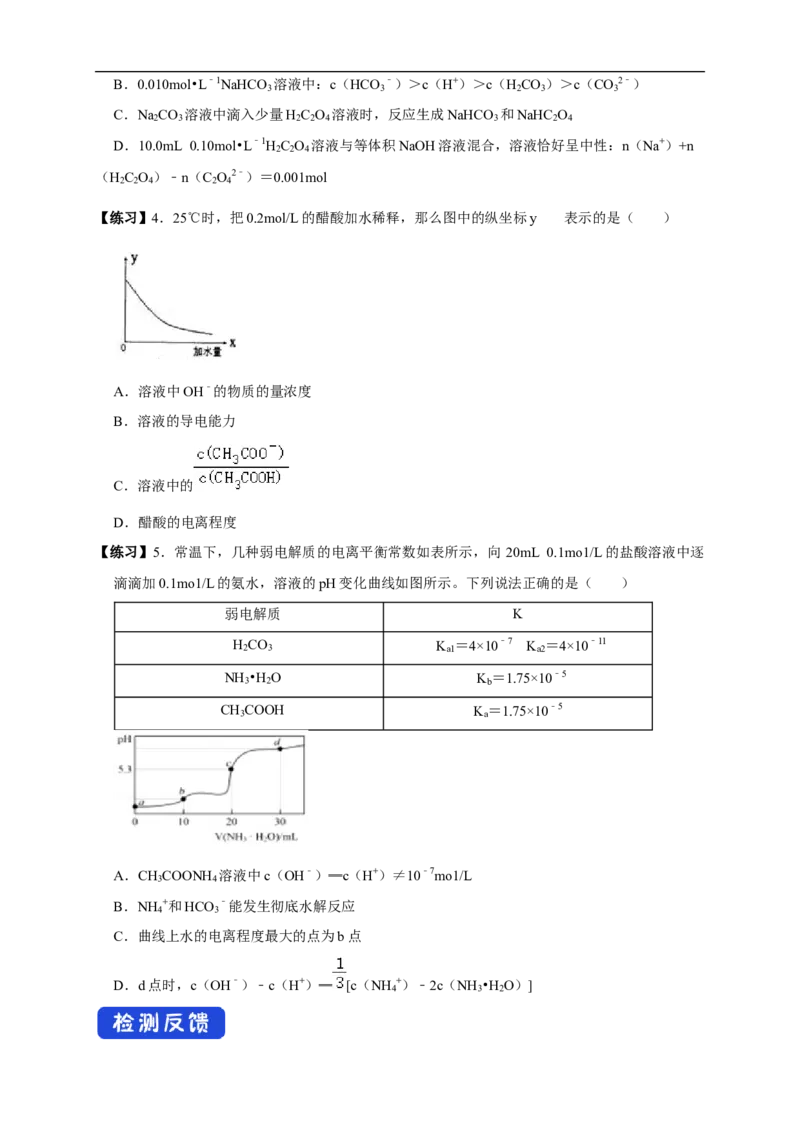
【练习】4.25℃时,把0.2mol/L的醋酸加水稀释,那么图中的纵坐标y 表示的是( )
A.溶液中OH﹣的物质的量浓度
B.溶液的导电能力
C.溶液中的
D.醋酸的电离程度
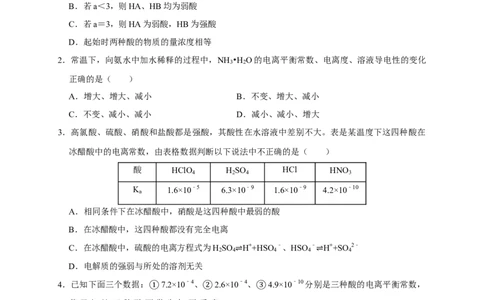
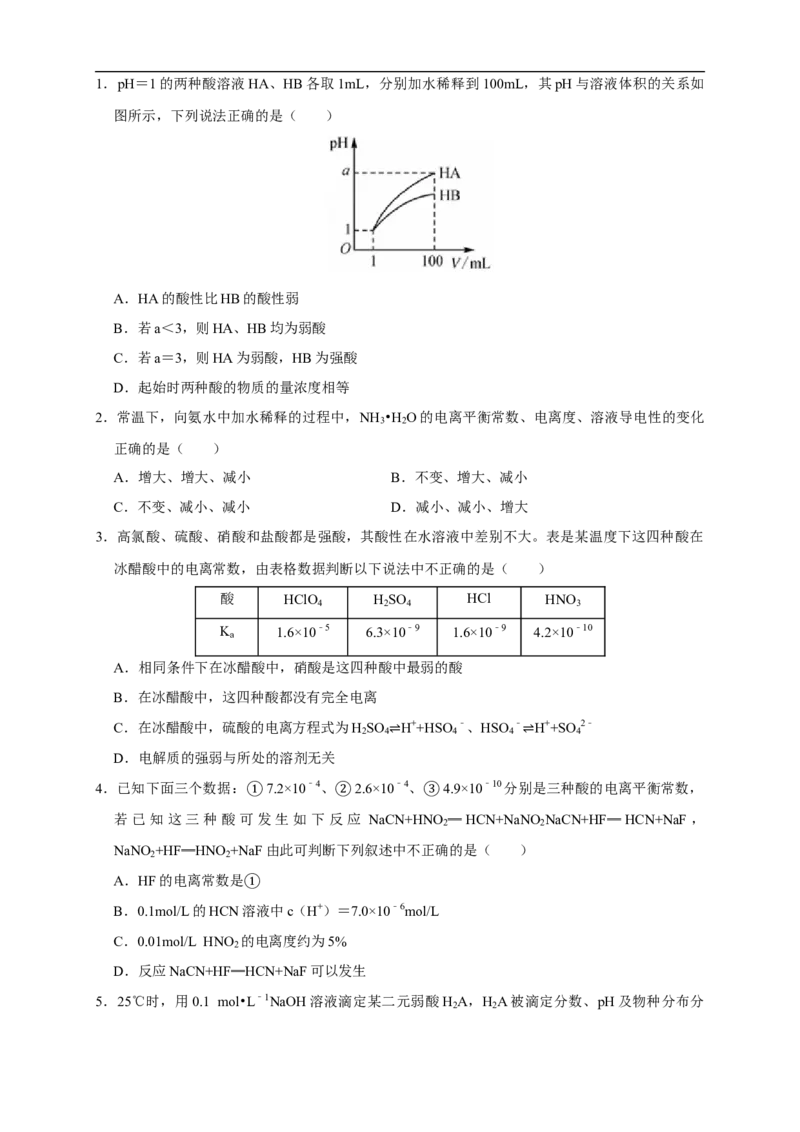
【练习】5.常温下,几种弱电解质的电离平衡常数如表所示,向 20mL 0.1mo1/L的盐酸溶液中逐
滴滴加0.1mo1/L的氨水,溶液的pH变化曲线如图所示。下列说法正确的是( )
弱电解质 K
H CO K =4×10﹣7 K =4×10﹣11
2 3 a1 a2
NH •H O K =1.75×10﹣5
3 2 b
CH COOH K =1.75×10﹣5
3 a
A.CH COONH 溶液中c(OH﹣)═c(H+)≠10﹣7mo1/L
3 4
B.NH +和HCO ﹣能发生彻底水解反应
4 3
C.曲线上水的电离程度最大的点为b点
D.d点时,c(OH﹣)﹣c(H+)═ [c(NH +)﹣2c(NH •H O)]
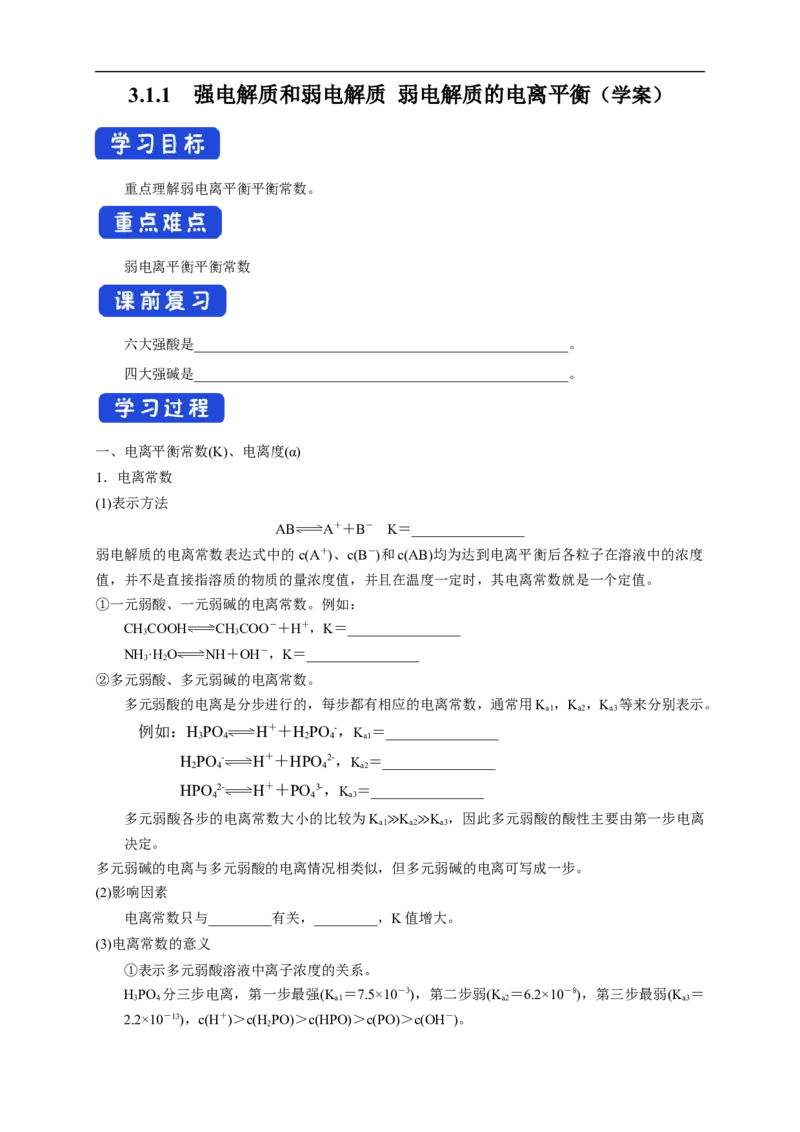
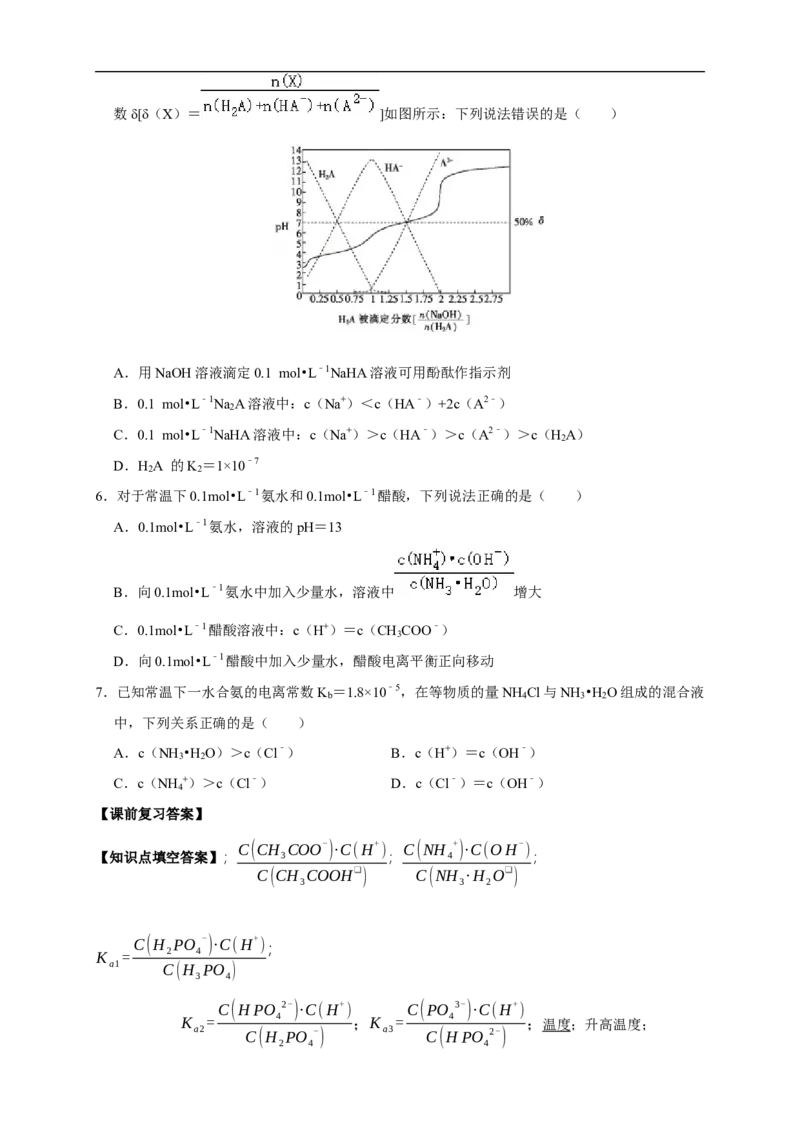
4 3 21.pH=1的两种酸溶液HA、HB各取1mL,分别加水稀释到100mL,其pH与溶液体积的关系如
图所示,下列说法正确的是( )
A.HA的酸性比HB的酸性弱
B.若a<3,则HA、HB均为弱酸
C.若a=3,则HA为弱酸,HB为强酸
D.起始时两种酸的物质的量浓度相等
2.常温下,向氨水中加水稀释的过程中,NH •H O的电离平衡常数、电离度、溶液导电性的变化
3 2
正确的是( )
A.增大、增大、减小 B.不变、增大、减小
C.不变、减小、减小 D.减小、减小、增大
3.高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。表是某温度下这四种酸在
冰醋酸中的电离常数,由表格数据判断以下说法中不正确的是( )
酸 HClO H SO HCl HNO
4 2 4 3
K 1.6×10﹣5 6.3×10﹣9 1.6×10﹣9 4.2×10﹣10
a
A.相同条件下在冰醋酸中,硝酸是这四种酸中最弱的酸
B.在冰醋酸中,这四种酸都没有完全电离
C.在冰醋酸中,硫酸的电离方程式为H SO H++HSO ﹣、HSO ﹣ H++SO 2﹣
2 4 4 4 4
D.电解质的强弱与所处的溶剂无关 ⇌ ⇌
4.已知下面三个数据: 7.2×10﹣4、 2.6×10﹣4、 4.9×10﹣10分别是三种酸的电离平衡常数,
若已知这三种酸可①发生如下反②应 NaCN+HN③O ═HCN+NaNO NaCN+HF═HCN+NaF,
2 2
NaNO +HF═HNO +NaF由此可判断下列叙述中不正确的是( )
2 2
A.HF的电离常数是
B.0.1mol/L的HCN溶①液中c(H+)=7.0×10﹣6mol/L
C.0.01mol/L HNO 的电离度约为5%
2
D.反应NaCN+HF═HCN+NaF可以发生
5.25℃时,用0.1 mol•L﹣1NaOH溶液滴定某二元弱酸H A,H A被滴定分数、pH及物种分布分
2 2数δ[δ(X)= ]如图所示:下列说法错误的是( )
A.用NaOH溶液滴定0.1 mol•L﹣1NaHA溶液可用酚酞作指示剂
B.0.1 mol•L﹣1Na A溶液中:c(Na+)<c(HA﹣)+2c(A2﹣)
2
C.0.1 mol•L﹣1NaHA溶液中:c(Na+)>c(HA﹣)>c(A2﹣)>c(H A)
2
D.H A 的K =1×10﹣7
2 2
6.对于常温下0.1mol•L﹣1氨水和0.1mol•L﹣1醋酸,下列说法正确的是( )
A.0.1mol•L﹣1氨水,溶液的pH=13
B.向0.1mol•L﹣1氨水中加入少量水,溶液中 增大
C.0.1mol•L﹣1醋酸溶液中:c(H+)=c(CH COO﹣)
3
D.向0.1mol•L﹣1醋酸中加入少量水,醋酸电离平衡正向移动
7.已知常温下一水合氨的电离常数K =1.8×10﹣5,在等物质的量NH Cl与NH •H O组成的混合液
b 4 3 2
中,下列关系正确的是( )
A.c(NH •H O)>c(Cl﹣) B.c(H+)=c(OH﹣)
3 2
C.c(NH +)>c(Cl﹣) D.c(Cl﹣)=c(OH﹣)
4
【课前复习答案】
C(CH COO-)∙C(H+ ) C(NH +)∙C(OH- )
【知识点填空答案】; 3 ; 4 ;
C(CH COOH❑) C(NH ∙H O❑)
3 3 2
K =
C(H
2
PO
4
-)∙C(H+ );
a1 C(H PO )
3 4
C(H PO 2-)∙C(H+ ) C(PO 3-)∙C(H+ )
K = 4 ;K = 4 ;温度;升高温度;
a2 C(H PO -) a3 C(H PO 2-)
2 4 4α=×100%;α=×100%;
α=×100%。
【练习答案】ADDBD
【检测反馈答案】BBDCBDC