文档内容
3.1.2电离平衡常数(分层作业)
c(SO2−
)
3
1.常温下,下列操作(忽略过程中温度变化)可以使亚硫酸稀溶液中的 增大的是
c(HSO−
)
3
A.通入HCl气体 B.通入SO 气体
2
C.加入NaOH固体 D.加入NaHSO 固体
4
【答案】C
【解析】A.向亚硫酸稀溶液中通入氯化氢气体,氯化氢在溶液中电离出氢离子,溶液中的氢离子浓度增
K c(SO2− )
a2 3
大,则 和 的值减小,故A错误;
c(H+ ) c(HSO− )
3
K
a2
B.向亚硫酸稀溶液中通入二氧化硫气体,亚硫酸的浓度增大,溶液中的氢离子浓度增大,则 和
c(H+
)
c(SO2−
)
3
的值减小,故B错误;
c(HSO−
)
3
C.向亚硫酸稀溶液中加入氢氧化钠固体,氢氧根离子与溶液中的氢离子反应,溶液中氢离子浓度减小,
K c(SO2− )
a2 3
则 和 的值增大,故C正确;
c(H+ ) c(HSO− )
3
D.向亚硫酸稀溶液中加入硫酸氢钠固体,硫酸氢钠在溶液中电离出氢离子,溶液中的氢离子浓度增大,
K c(SO2− )
a2 3
则 和 的值减小,故D错误;
c(H+ ) c(HSO− )
3
故选C。
2. 醋酸溶液中存在电离平衡CHCOOH ⇌ H++CH COO- ,下列叙述不正确的是
3 3
A.升高温度,平衡正向移动,醋酸的电离常数 增大
B.0.10mol·L-1的CHCOOH溶液中加水稀释,溶液的pH变大
3C.CHCOOH溶液中加少量的CHCOONa固体,该电离平衡逆向移动
3 3
D. 时,欲使醋酸溶液pH、电离常数K 和电离程度都减小,可加入少量冰醋酸
a
【答案】D
【解析】A.电离是一个吸热过程,升高温度,醋酸的电离常数增大,平衡正向移动,A正确;
B.醋酸溶液加水稀释,电离程度增大,但溶液体积也在增大,氢离子浓度减小,溶液的pH增大,B正确;
C.增大生成物的浓度,平衡逆向移动,C正确;
D.加入冰醋酸,电离常数不变,D错误;
故选D。
3.已知25℃时,CHCOOH 的K 为1.75×10-5,HCN的K 为6.2×10-10,HCO 的K 为4.5×10-7,K 为
3 a a 2 3 a1 a2
4.7×10-11。下列相关说法正确的是
A.CHCOOH =CH COO-+H+
3 3
B.HCO ⇌ 2H++CO2-
2 3 3
C.2CN-+H O+CO=2HCN+CO2-
2 2 3
D.25℃时,反应CHCOOH+CN- ⇌ HCN+CH COO-的化学平衡常数数量级为104
3 3
【答案】D
【分析】已知Ka越大,说明该酸电离程度越大,即其对应的酸性就越强,据此分析解题。
【解析】A.由题干信息可知,CHCOOH为一元弱酸,故其电离方程式为:
3
CHCOOH f CHCOO- + H+,A错误;
3 3
B.由题干信息可知,HCO 为二元弱酸,故其电离方程式为:HCO ⇌ H++HCO- 、HCO-⇌ H++CO2- ,
2 3 2 3 3 3 3
B错误;
C.由题干信息可知,酸性HCO>HCN>HCO- ,故离子方程式应该为:CN-+H O+CO=HCN+HCO- ,C
2 3 3 2 2 3
错误;
c(HCN)c(CH COO− )
D.25℃时,反应CHCOOH+CN- ⇌ HCN+CH COO-的化学平衡常数:K= 3 =
3 3 c(CH COOH)c(CN− )
3
c(HCN)c(CH COO− ) c(H+ ) K (CH COOH) 1.75×10−5
3 × = a 3 = ≈2.8×104,即该数量级为104,D正确;
c(CH COOH)c(CN− ) c(H+ ) K (HCN) 6.2×10−10
3 a
故答案为:D。
4.已知常温下,2mol/L的一元酸HA溶液中c(H+)为:2×10-4mol/L,下列说法错误的是
A.常温下,HA的电离常数约为2×10-8
B.NaA可以和盐酸发生反应:HCl+NaA=NaCl+HAC.该条件下,体系中HA的电离度是1%
D.向2mol/L的HA溶液中加入少量2mol/L的NaA溶液,HA的电离程度减小
【答案】C
【解析】A.已知常温下,2mol/L的一元酸HA溶液中c(H+)为2×10-4mol/L,则平衡时c(A-)=2×10-4mol/L,
c(H+ )·c(A− ) 2×10−4×2×10−4
c(HA)≈2mol/L,则电离常数Ka= = =2×10-8,A正确;
c(HA) 2
B.根据强酸制弱酸,NaA可以和盐酸发生反应:HCl+NaA=NaCl+HA,B正确;
2×10−4mol/L
C.该条件下,体系中HA的电离度是 =0.01%,C错误;
2mol/L
D.HA溶液中存在电离平衡,HA f H++ A-,加入少量2mol/L的NaA溶液,A-浓度增大,平衡逆向移动,
HA的电离程度减小,D正确;
故选C。
5.高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋
酸中的电离常数:
酸 HClO HSO HCl HNO
4 2 4 3
1.6× 6.3× 1.6× 4.2×
K
a
10-5mol·L-1 10-9mol·L-1 10-9mol·L-1 10-10mol·L-1
由以上表格中数据判断以下说法不正确的是
A.在冰醋酸中这四种酸都没有完全电离
B.在冰醋酸中高氯酸是这四种酸中酸性最强的酸
C.在冰醋酸中硫酸的电离方程式为HSO =2H++SO
2 4
D.水对这四种酸的强弱没有区分能力,但冰醋酸可以区分这四种酸的强弱
【答案】C
【解析】A.由电离常数可知,在冰醋酸中这四种酸都没有完全电离,A正确;
B.由电离常数可知,在冰醋酸中高氯酸的电离常数最大,是这四种酸中酸性最强的酸,B正确;
C.在冰醋酸中硫酸没有完全电离,应该为HSO f H++HSO2- ,C错误;
2 4 4
D.在水溶液中四种酸均为强酸,水对这四种酸的强弱没有区分能力,但冰醋酸可以区分这四种酸的强弱,
D正确;
故选C。6.常温下4种酸的电离平衡常数如下:
化学式 HF
电离平衡常数
(1)次氯酸的电离方程式为 。
(2)物质的量浓度相同的 HF 、CHCOOH、HCO、HClO中,酸性由小到大的顺序为 。
3 2 3
(3)保持温度不变,向 的醋酸溶液中加入或通入下列物质, 的电离度减小、溶液中
的c(H+)增大的是___________(填标号)。
A.醋酸钠固体 B.冰醋酸 C.水 D.氯化氢气体
(4)下列实验事实不能证明醋酸是弱酸的是________
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H 的起始速率相等
2
B.常温下,测得0.1 mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4
D.在相同条件下,醋酸溶液的导电性比盐酸的弱
(5)电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。下图
是用KOH溶液分别滴定HCl溶液和CHCOOH溶液的滴定曲线示意图。下列示意图中,能正确表示用
3
NH ·H O溶液滴定HCl和CHCOOH混合溶液的滴定曲线的是__________
3 2 3
A. B.
C. D.
(6)常温下,物质的量浓度为 的醋酸溶液中,达到电离平衡时c(H+)约为 ,此时醋
酸的电离度约为 (已知 )。【答案】(1)HClO f H++ClO-
(2)HClO20.00
【答案】C【分析】一元强酸能完全电离,一元弱酸部分电离,则等物质的量浓度的甲和乙,弱酸的pH较大,因此
曲线Ⅰ表示弱酸乙和NaOH溶液的滴定曲线,曲线Ⅱ表示强酸甲和NaOH溶液的滴定曲线;
【解析】A.根据分析可知取代II代表一元强酸,从b点看nmol/L一元强酸甲时溶液pH=1,氢离子浓度
为0.1mol/L,则n=0.1,故A错误;
B.由分析可知曲线Ⅱ为NaOH溶液滴定一元强酸甲,故B错误;
C.0.1000mol/L弱酸乙溶液的pH=3,该溶液中c(乙酸根离子)≈c(H+)=10-3mol/L,c(乙)=(0.1000-10-3)mol/L,
10−3×10−3
电离平衡常数K(乙)= =1.01×10-5,故C正确;
a 0.1000−10−3
D.甲为强酸,甲的钠盐溶液呈中性,酸碱都是一元的且酸碱的物质的量浓度相等,要使酸碱恰好完全反
应,则酸碱溶液的体积相等,所以x=20.00,故D错误;
故选:C。
5.已知常温下,几种物质的电离平衡常数,下列说法正确的是
弱酸 HCOOH(甲酸) HCO HClO HSO
2 3 2 3
K(25℃) K=1.77×10-5 K=4.3×10-7 k=5.6×10-11 K=2.98×10-8 K=1.54×10-2 K=1.02×10-7
1 2 1 2
A.向NaClO溶液中通入足量SO 能提高次氯酸的浓度
2
B.向HCOONa(甲酸钠)溶液中滴加过量CO:
2
C.向NaCO 溶液中通入过量Cl:
2 3 2
D.向NaClO溶液中通入少量CO:
2
【答案】D
【解析】A.由于HClO具有强氧化性,能够被SO 还原,故向NaClO溶液中通入足量SO 将生成NaCl和
2 2
HSO ,故不能能提高次氯酸的浓度,A错误;
2 4
B.由题干表中数据可知, Ka(HCOOH)>Ka(H CO)>Ka(H CO),故向HCOONa(甲酸钠)溶液中滴加过
1 2 3 2 2 3
量CO 不反应,B错误;
2
C.由题干表中数据可知,Ka(H CO)>Ka(HClO)>Ka(H CO),向NaCO 溶液中通入过量Cl,结合
1 2 3 2 2 3 2 3 2
Cl+H O=HCl+HClO,故该过程的总的离子方程式为:2Cl+H O+CO2- =CO ↑+2Cl-+2HClO,C错误;
2 2 2 2 3 2
D.由题干表中数据可知,Ka(H CO)>Ka(HClO)>Ka(H CO),则向NaClO溶液中通入少量CO 生成
1 2 3 2 2 3 2
NaHCO 和HClO,故该反应的离子方程式为:ClO-+CO +H O=HCO- =HClO,D正确;
3 2 2 3故答案为:D。
6.部分弱电解质的电离常数如下表:
弱电解质 HCOOH HCN HCO
2 3
电离常数(25℃) K=1.8×10-4 K=4.9×10-10 K =4.3×10-7 K =5.6×10-11
a a a1 a2
下列说法错误的是
A.根据电离常数,可判断酸性HCOOH>H CO>HCN
2 3
B.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
C.2CN-+H O+CO=2HCN+CO2-
2 2 3
D.25℃时,反应HCOOH+CN- f HCN+HCOO-的化学平衡常数为3.67×105
【答案】C
【解析】A.由电离常数可知,三种酸的酸性强弱顺序为HCOOH>HCO>HCN,故A正确;
2 3
B.由电离常数可知,甲酸和氢氰酸的酸性强弱顺序为HCOOH>HCN,则等体积、等pH的氢氰酸的浓度
大于甲酸,中和能力强于甲酸,消耗氢氧化钠的量大于甲酸,故B正确;
C.由分析可知,酸的电离程度的大小顺序为HCO>HCN>HCO- ,由强酸制弱酸的原理可知,溶液中氰
2 3 3
酸根离子与二氧化碳反应生成氢氰酸和碳酸氢根离子,反应的离子方程式为CN-+H O+CO=HCN+HCO- ,
2 2 3
故C错误;
c(HCOO− )c(HCN) c(HCOO− )c(HCN)c(H+ )
D.由方程式可知,25℃时反应的化学平衡常数K= =
c(HCOOH)c(CN−
)
c(HCOOH)c(CN− )c(H+
)
K (HCOOH) 1.8' 10−4
a
= =
K (HCN) 4.9' 10−10
a
=3.67×105,故D正确;
故选C。
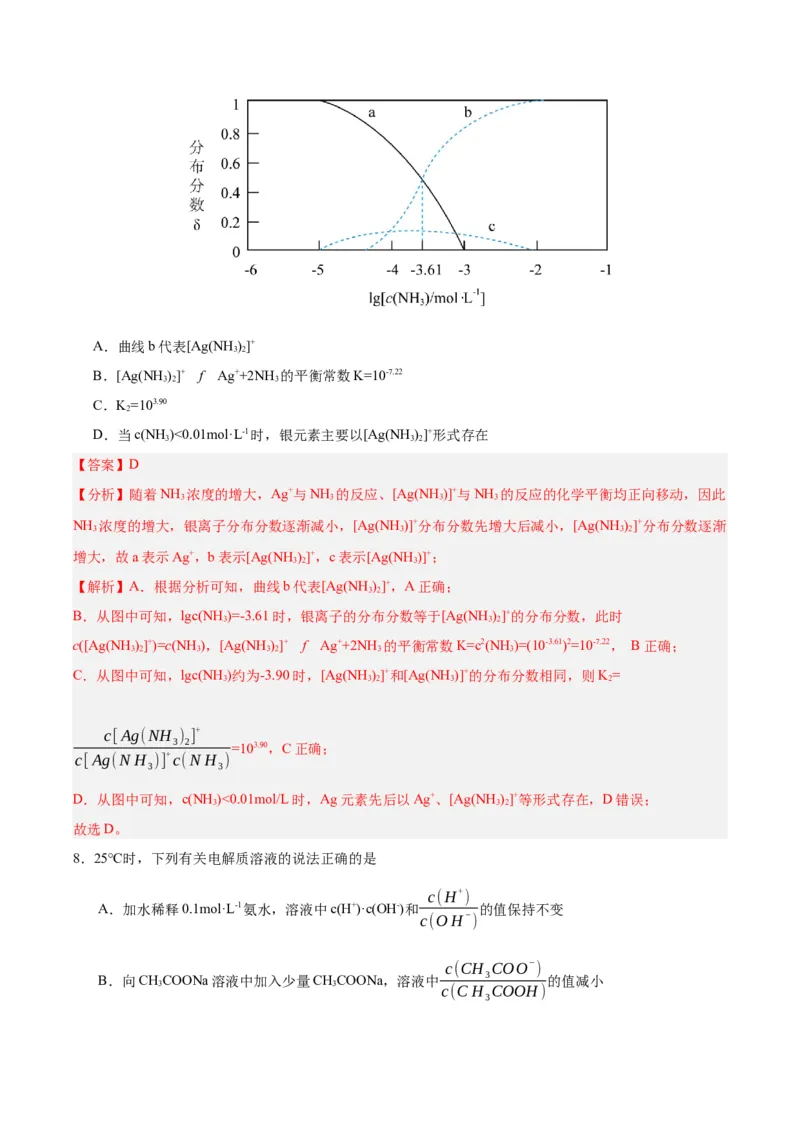
7.已知:Ag++2NH=[Ag(NH)]+ K=103.32、[Ag(NH)]++NH ⇌ [Ag(NH)]+ K Ag+、[Ag(NH)]+、
3 3 1 3 3 3 2 2. 3
[Ag(NH)]的分布系数δ与lg[c(NH)/(mol·L-1)]关系如图所示,
3 2 3
。下列说法错误的是A.曲线b代表[Ag(NH)]+
3 2
B.[Ag(NH)]+ f Ag++2NH 的平衡常数K=10-7.22
3 2 3
C.K=103.90
2
D.当c(NH )<0.01mol·L-1时,银元素主要以[Ag(NH)]+形式存在
3 3 2
【答案】D
【分析】随着NH 浓度的增大,Ag+与NH 的反应、[Ag(NH)]+与NH 的反应的化学平衡均正向移动,因此
3 3 3 3
NH 浓度的增大,银离子分布分数逐渐减小,[Ag(NH)]+分布分数先增大后减小,[Ag(NH)]+分布分数逐渐
3 3 3 2
增大,故a表示Ag+,b表示[Ag(NH)]+,c表示[Ag(NH)]+;
3 2 3
【解析】A.根据分析可知,曲线b代表[Ag(NH)]+,A正确;
3 2
B.从图中可知,lgc(NH)=-3.61时,银离子的分布分数等于[Ag(NH)]+的分布分数,此时
3 3 2
c([Ag(NH)]+)=c(NH ),[Ag(NH)]+ f Ag++2NH 的平衡常数K=c2(NH )=(10-3.61)2=10-7.22, B正确;
3 2 3 3 2 3 3
C.从图中可知,lgc(NH)约为-3.90时,[Ag(NH)]+和[Ag(NH)]+的分布分数相同,则K=
3 3 2 3 2
c[Ag(NH ) ] +
3 2 =103.90,C正确;
c[Ag(N H )] +c(N H )
3 3
D.从图中可知,c(NH )<0.01mol/L时,Ag元素先后以Ag+、[Ag(NH)]+等形式存在,D错误;
3 3 2
故选D。
8.25℃时,下列有关电解质溶液的说法正确的是
c(H+
)
A.加水稀释0.1mol·L-1氨水,溶液中c(H+)·c(OH-)和 的值保持不变
c(OH−
)
c(CH COO− )
B.向CHCOONa溶液中加入少量CHCOONa,溶液中 3 的值减小
3 3
c(CH COOH)
3c(HCO− ) c(CO2− )
C.等体积、等物质的量浓度的NaCO 和NaHCO 溶液混合: 3 > 3
2 3 3 c(H CO ) c(HCO− )
2 3 3
c(F−
)
D.将浓度为0.1mol·L-1HF溶液加水不断稀释过程中,电离平衡常数K(HF)保持不变, 始终增
a c(H+
)
大
【答案】C
c(H+
)
【解析】A.0.1mol·L-1氨水稀释过程中c(H+)增大,c(OH-)减小,因而 变大,温度不变,
c(OH−
)
c(H+)·c(OH-)=K 不变,A项错误;
w
c(CH COO− ) K c(CH COO− )
B. 3 = a ,加入CHCOONa,溶液碱性增强,则c(H+)降低,所以 3 的
c(CH COOH) c(H+ ) 3 c(CH COOH)
3 3
值增大,B项错误;
c(H+ )c(HCO−
)
C.等体积、等物质的量浓度的NaCO 和NaHCO 溶液混合,根据电离常数有K = 3 、K
2 3 3 a1 a2
c(H CO )
2 3
c(H+ )c(CO2−
)
3
=
c(HCO−
)
3
c(H CO ) c(HCO− ) c(HCO− )
,同一溶液中c(H+)相等,则c(H+)= K · 2 3 = K · 3 ,而K > K ,则 3 >
a1 c(HCO− ) a2 c(CO2− ) a1 a2 c(H CO )
3 3 2 3
c(CO2−
)
3
,C项正确;
c(HCO−
)
3
D.0.1mol·L-1的HF加水稀释,c(F-)趋近于0,而c(H+)趋于不变(10-7mol·L-1),故比值变小,D项错误;
故选C。
9. 时,草酸(H C O)的K =5.4×10-2、K =5.4×10-5,硒化氢(H Se)的K =1.3×10-4、K =1.0×10-11。回答
2 2 4 a1 a2 2 a1 a2
下列问题:
(1)写出HC O 在水中的第一步电离方程式: ;草酸水溶液中含有的离子有 种。
2 2 4
(2)草酸具有较强的还原性,将100mL 0.1mol·L-1HC O 溶液加入少量酸性KMnO 溶液中。
2 2 4 4①反应过程中的现象为 ,反应的离子方程式为 。
②忽略二者混合之后的温度变化,在反应过程中,下列物理量始终增大的是 (填标号)。
c(H+ )·c(HC O− ) c(HC O− )
A. 2 4 B.c(Mn2+) C. 2 4 D.
c(H C O ) c(H C O )
2 2 4 2 2 4
c(H+)
(3)25℃时,10mL 0.1mol·L-1的HSe溶液中,c(H+) (填“ ”、“ ”或“ ”)c(HSe-);往该
2
溶液中加入5mL 0.1mol·L-1NaC O 溶液,反应的化学方程式为 ,该过程中 的电离程度
2 2 4
(填“增大”或“减小”)。
【答案】(1)HC O f H++HC O- 4
2 2 4 2 4
(2)溶液中有气泡产生,溶液的紫红色逐渐褪去直至无色 5HC O+2MnO- +6H+=10CO ↑+2Mn2++8H O
2 2 4 4 2 2
BC
(3)> HSe+Na C O=NaHSe+NaHC O 增大
2 2 2 4 2 4
【解析】(1)HC O 为二元弱酸,在水中的第一步电离方程式:HC O f H++HC O- ;草酸水溶液中第
2 2 4 2 2 4 2 4
一步电离生成H+、HC O- ,HC O- 继续电离生成H+、C O2- ,同时存在水电离出的OH-,共存在4种离子;
2 4 2 4 2 4
(2)①HC O 具有还原性,能被高锰酸钾氧化发生反应5HC O+2MnO- +6H+=10CO ↑+2Mn2++8H O,可
2 2 4 2 2 4 4 2 2
观察到溶液中有气泡产生,溶液的紫红色逐渐褪去直至无色;
c(H+ )·c(HC O− )
②A. 2 4 =K ,温度不变,K 不变,故A不选;
a1 a1
c(H C O )
2 2 4
B.反应生成锰离子,c(Mn2+)增大,故B选;
c(HC O− ) K
C. 2 4 = a1 ,随反应进行,K 不变,c(H+)减小,则比值增大,故C选;
c(H C O ) c(H+ ) a1
2 2 4
D.反应过程中消耗氢离子,c(H+)减小,故D不选;