文档内容
3.1.2电离平衡常数(分层作业)
c(SO2−
)
3
1.常温下,下列操作(忽略过程中温度变化)可以使亚硫酸稀溶液中的 增大的是
c(HSO−
)
3
A.通入HCl气体 B.通入SO 气体
2
C.加入NaOH固体 D.加入NaHSO 固体
4
2. 醋酸溶液中存在电离平衡CHCOOH ⇌ H++CH COO- ,下列叙述不正确的是
3 3
A.升高温度,平衡正向移动,醋酸的电离常数 增大
B.0.10mol·L-1的CHCOOH溶液中加水稀释,溶液的pH变大
3
C.CHCOOH溶液中加少量的CHCOONa固体,该电离平衡逆向移动
3 3
D. 时,欲使醋酸溶液pH、电离常数K 和电离程度都减小,可加入少量冰醋酸
a
3.已知25℃时,CHCOOH 的K 为1.75×10-5,HCN的K 为6.2×10-10,HCO 的K 为4.5×10-7,K 为
3 a a 2 3 a1 a2
4.7×10-11。下列相关说法正确的是
A.CHCOOH =CH COO-+H+
3 3
B.HCO ⇌ 2H++CO2-
2 3 3
C.2CN-+H O+CO=2HCN+CO2-
2 2 3
D.25℃时,反应CHCOOH+CN- ⇌ HCN+CH COO-的化学平衡常数数量级为104
3 3
4.已知常温下,2mol/L的一元酸HA溶液中c(H+)为:2×10-4mol/L,下列说法错误的是
A.常温下,HA的电离常数约为2×10-8
B.NaA可以和盐酸发生反应:HCl+NaA=NaCl+HA
C.该条件下,体系中HA的电离度是1%
D.向2mol/L的HA溶液中加入少量2mol/L的NaA溶液,HA的电离程度减小
5.高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋
酸中的电离常数:
酸 HClO HSO HCl HNO
4 2 4 3
1.6× 6.3× 1.6× 4.2×
K
a
10-5mol·L-1 10-9mol·L-1 10-9mol·L-1 10-10mol·L-1
由以上表格中数据判断以下说法不正确的是
A.在冰醋酸中这四种酸都没有完全电离B.在冰醋酸中高氯酸是这四种酸中酸性最强的酸
C.在冰醋酸中硫酸的电离方程式为HSO =2H++SO
2 4
D.水对这四种酸的强弱没有区分能力,但冰醋酸可以区分这四种酸的强弱
6.常温下4种酸的电离平衡常数如下:
化学式 HF
电离平衡常数
(1)次氯酸的电离方程式为 。
(2)物质的量浓度相同的 HF 、CHCOOH、HCO、HClO中,酸性由小到大的顺序为 。
3 2 3
(3)保持温度不变,向 的醋酸溶液中加入或通入下列物质, 的电离度减小、溶液中
的c(H+)增大的是___________(填标号)。
A.醋酸钠固体 B.冰醋酸 C.水 D.氯化氢气体
(4)下列实验事实不能证明醋酸是弱酸的是________
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H 的起始速率相等
2
B.常温下,测得0.1 mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4
D.在相同条件下,醋酸溶液的导电性比盐酸的弱
(5)电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。下图
是用KOH溶液分别滴定HCl溶液和CHCOOH溶液的滴定曲线示意图。下列示意图中,能正确表示用
3
NH ·H O溶液滴定HCl和CHCOOH混合溶液的滴定曲线的是__________
3 2 3
A. B.
C. D.(6)常温下,物质的量浓度为 的醋酸溶液中,达到电离平衡时c(H+)约为 ,此时醋
酸的电离度约为 (已知 )。
7.常温下,部分弱电解质的电离平衡常数如表:
弱电解质 HCN HCO NH ·H O NH OH
2 3 3 2 2
电离平衡常
数
下列说法错误的是
A.往NaCN溶液中通入少量CO,反应的离子方程式为2CN-+CO +H O=2HCN+CO2-
2 2 2 3
B.等浓度的NH ·H O与NH OH的混合溶液中:
3 2 2
C.0.1mol·L-1的 溶液中,
D.适度升高温度,0.1mol·L-1的NH ·H O溶液的导电能力会增强
3 2
8.二元弱酸HX的电离过程是吸热过程,某温度下,其电离常数K =2.5×10-4、K =2×10-8。下列说法错误
2 a1 a2
的是
A.升高温度后,K 、K 均增大
a1 a2
B.向HX溶液中加入少量KHX固体,c(H+)减小
2
C.该温度下0.1mol·L-1的HX溶液中c(H+)≈5×10-3mol·L-1
2
c(H X− )
D.向HX溶液中加水稀释过程中, 减小
2 c(H X)
2
4.25℃时,用0.1000mol·L-1的NaOH溶液滴定20.00mL nmol·L-1的一元强酸甲和一元弱酸乙,滴定曲线
如图所示。下列有关说法正确的是
A.n=1B.曲线Ⅱ为NaOH溶液滴定一元弱酸乙
C.电离常数K(乙)=1.01×10-5
a
D.图像中的x>20.00
5.已知常温下,几种物质的电离平衡常数,下列说法正确的是
弱酸 HCOOH(甲酸) HCO HClO HSO
2 3 2 3
K(25℃) K=1.77×10-5 K=4.3×10-7 k=5.6×10-11 K=2.98×10-8 K=1.54×10-2 K=1.02×10-7
1 2 1 2
A.向NaClO溶液中通入足量SO 能提高次氯酸的浓度
2
B.向HCOONa(甲酸钠)溶液中滴加过量CO:
2
C.向NaCO 溶液中通入过量Cl:
2 3 2
D.向NaClO溶液中通入少量CO:
2
6.部分弱电解质的电离常数如下表:
弱电解质 HCOOH HCN HCO
2 3
电离常数(25℃) K=1.8×10-4 K=4.9×10-10 K =4.3×10-7 K =5.6×10-11
a a a1 a2
下列说法错误的是
A.根据电离常数,可判断酸性HCOOH>H CO>HCN
2 3
B.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
C.2CN-+H O+CO=2HCN+CO2-
2 2 3
D.25℃时,反应HCOOH+CN- f HCN+HCOO-的化学平衡常数为3.67×105
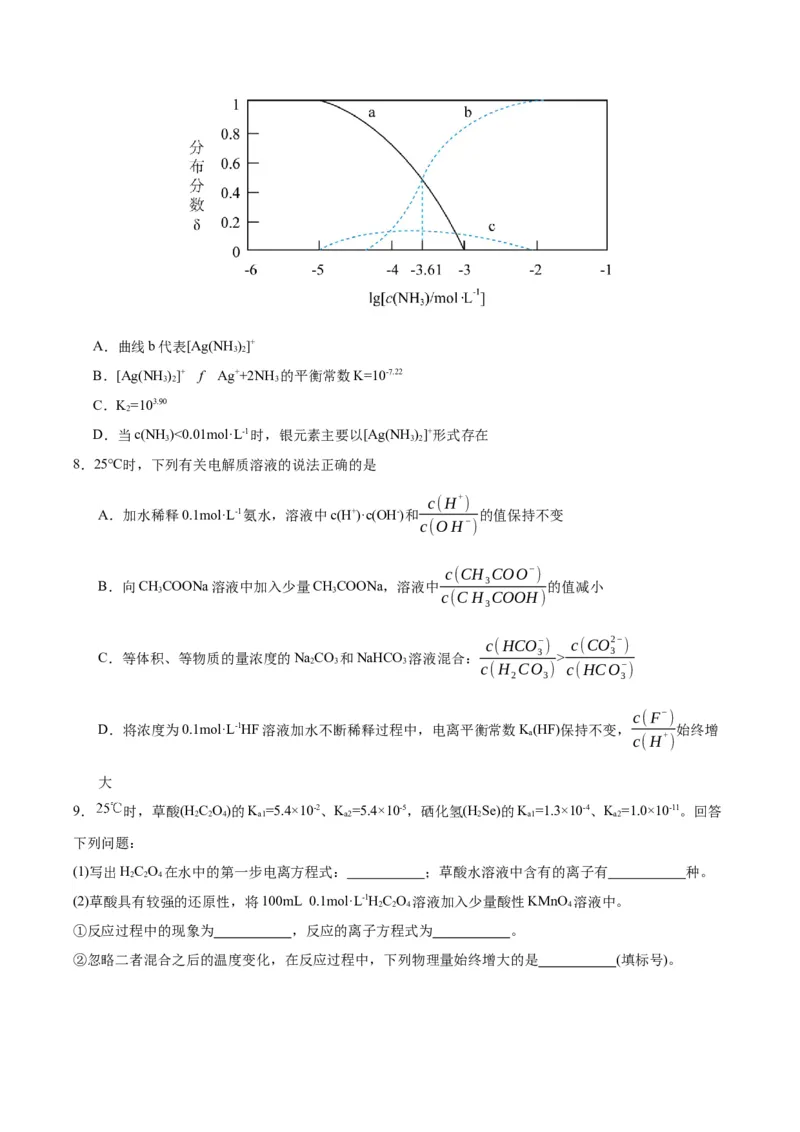
7.已知:Ag++2NH=[Ag(NH)]+ K=103.32、[Ag(NH)]++NH ⇌ [Ag(NH)]+ K Ag+、[Ag(NH)]+、
3 3 1 3 3 3 2 2. 3
[Ag(NH)]的分布系数δ与lg[c(NH)/(mol·L-1)]关系如图所示,
3 2 3
。下列说法错误的是A.曲线b代表[Ag(NH)]+
3 2
B.[Ag(NH)]+ f Ag++2NH 的平衡常数K=10-7.22
3 2 3
C.K=103.90
2
D.当c(NH )<0.01mol·L-1时,银元素主要以[Ag(NH)]+形式存在
3 3 2
8.25℃时,下列有关电解质溶液的说法正确的是
c(H+
)
A.加水稀释0.1mol·L-1氨水,溶液中c(H+)·c(OH-)和 的值保持不变
c(OH−
)
c(CH COO− )
B.向CHCOONa溶液中加入少量CHCOONa,溶液中 3 的值减小
3 3
c(CH COOH)
3
c(HCO− ) c(CO2− )
C.等体积、等物质的量浓度的NaCO 和NaHCO 溶液混合: 3 > 3
2 3 3 c(H CO ) c(HCO− )
2 3 3
c(F−
)
D.将浓度为0.1mol·L-1HF溶液加水不断稀释过程中,电离平衡常数K(HF)保持不变, 始终增
a c(H+
)
大
9. 时,草酸(H C O)的K =5.4×10-2、K =5.4×10-5,硒化氢(H Se)的K =1.3×10-4、K =1.0×10-11。回答
2 2 4 a1 a2 2 a1 a2
下列问题:
(1)写出HC O 在水中的第一步电离方程式: ;草酸水溶液中含有的离子有 种。
2 2 4
(2)草酸具有较强的还原性,将100mL 0.1mol·L-1HC O 溶液加入少量酸性KMnO 溶液中。
2 2 4 4
①反应过程中的现象为 ,反应的离子方程式为 。
②忽略二者混合之后的温度变化,在反应过程中,下列物理量始终增大的是 (填标号)。c(H+ )·c(HC O− ) c(HC O− )
A. 2 4 B.c(Mn2+) C. 2 4 D.
c(H C O ) c(H C O )
2 2 4 2 2 4
c(H+)