文档内容
第 01 讲 反应热 焓变
知识导航
课前引入
热量的释放或吸收是化学反应中能量变化的常见形式。
例如,燃料的燃烧、酸与碱的中和反应等会放出热量,
属于放热反应。而有些反应,如工业上煅烧石灰石的反应等
会吸收热量,属于吸热反应。化学反应过程中释放或吸收的
热量在生活、生产和科学研究中具有广泛的应用。
那么,在实际应用中,人们如何定量地描述化学反应过
程中释放或吸收的热量呢?
杨sir化学,侵权必究
模块一 反应热及其测定
杨sir化学,侵权必究
知识精讲
一、体系与环境
以盐酸与NaOH溶液的反应为例
在热学中体系是与周围其他部分区分开来的根据需要所研究的对象。如我们可将盐
体系
酸、NaOH溶液及发生的反应等看作一个反应体系,简称体系(又称系统)。
环境 与体系相互影响的其他部分,如盛有溶液的试管和溶液之外的空气等看作环境。
体系与环境之间存在_______交换或_______交换。
关联
杨sir化学,侵权必究二、反应热的定义
1.定义:在等温条件下①,化学反应体系向环境_______或从环境_______的_______,称为化学反应的热
效应,简称反应热。用ΔH表示。
杨sir化学,侵权必究
①注:等温条件下,指化学反应发生后,使反应后体系的温度恢复到反应前体系的温度,即反应前后体系的温度相等。
2.说明:许多反应热可以通过量热计直接测定。例如,盐酸与NaOH溶液反应的过程中会放出热量,导
致体系与环境之间的温度产生差异。在反应前后,如果环境的温度没有变化,则反应放出的热量就会使体
系的温度升高,这时可根据测得的体系的温度变化和有关物质的比热容等来计算反应热。
杨sir化学,侵权必究
三、反应热的测定实验
实验探究——中和反应反应热的测定
思考与交流:在测定中和反应的反应热时,应该测量哪些数据?如何根据测得的数据计算反应热?为
了提高测定的准确度,应该采取哪些措施?
杨sir化学,侵权必究
【实验操作】
(1)反应物温度的测量。
①用量筒量取50mL 0.50mol/L盐酸, 打开杯盖, 倒入量热计的内筒,盖上杯
盖,插入温度计,测量并记录盐酸的温度(数据填入下表)。用水把温度计上的酸
冲洗干净,擦干备用。
②用另一个量筒量取 50mL 0.55mol/L NaOH溶液, 用温度计测量并记录 NaOH
溶液的温度(数据填入下表)。
(2)反应后体系温度的测量。
打开杯盖, 将量筒中的NaOH溶液迅速倒入量热计的内筒, 立即盖上杯盖, 插入温度计,用搅拌器匀
速搅拌。密切关注温度变化,将________温度记为反应后体系的温度(t)。
2
(3)重复上述步骤(1)至步骤(2)两次。
杨sir化学,侵权必究
【数据处理】
(1)取盐酸温度和NaOH溶液温度的__________记为反应前体系的温度(t ) 。计算温度差(t - t ),
1 2 1
将数据填入下表。
反应物的温度/℃ 反应前体系的温度 反应后体系的温度 温度差
实验次数
盐酸 NaOH溶液 t / ℃ t / ℃ (t - t )/ ℃
1 1 2 1
1
2
3
(2)取三次测量所得温度差的平均值作为计算依据。
(3)根据温度差和比热容等计算反应热。
杨sir化学,侵权必究(4)实验数据处理
为了计算简便,盐酸、氢氧化钠稀溶液的密度近似地认为都是1 g·cm-3,反应后生成的溶液的比热容c=
4.18 J/(g·℃)。该实验中盐酸和NaOH溶液反应放出的热量是_______________,生成1mol HO时放出的
2
热量为___________________。
杨sir化学,侵权必究
酸碱中和反应测定实验的注意事项
(1)为了保证0.50mol· L-1的盐酸完全被NaOH中和,采用0.55mol·L-1NaOH溶液,使碱稍稍过量,
因为过量的碱并不参加中和反应。(酸稍微过量也可以)
杨sir化学,侵权必究
(2)先后测量酸、碱及混合液的温度时,测定一种溶液后必须用水冲洗干净并用滤纸擦干。温度计的
水银球部分要完全浸入溶液中,且要稳定一段时间再记下读数。
(3)实验中所用的盐酸和氢氧化钠溶液配好后要充分冷却至室温,才能使用。
(4)操作时动作要快,尽量减少热量的散失。
杨sir化学,侵权必究
(5)实验时亦可选用浓度体积都不相同的酸碱溶液进行中和热的测定,但在计算时,应取二者中量少
的一种,因为过量的酸/碱并不参加中和反应。
(6)多次试验求平均值时,若有某一组的实验数据有明显偏差,应直接舍去。
(7)隔热层的作用是保温隔热,减少热量损失。
杨sir化学,侵权必究
四、中和热的定义
大量实验测得,在25℃和101kPa下,强酸的稀溶液与强碱的稀溶液在稀溶液发生中和反应生成1 mol
HO时,放出57.3 kJ的热量。ΔH =-57.3 kJ/mol。
2 杨sir化学,侵权必究
对点训练
题型一:化学反应中的能量变化
【例1】(2019·黑龙江高二月考)下列有关能量转化的认识不正确的是
A.燃料燃烧,只是将化学能转化为了热能
B.人类使用照明设备,将电能转化为光能
C.生物体内的化学变化过程在能量转化上比在体外发生的一些能量转化更为合理有效
D.通过植物的光合作用,太阳能转化为化学能
【变1】(2020·河北高二月考)关于能量转化,下列说法不正确的是
A.燃气灶具中的能量转化:化学能主要转化为光能
B.太阳能电池的能量转化:光能(太阳能)→电能C.生物光合作用中的能量转化:光能(太阳能)→生物质能(化学能)
杨sir化学,侵权必究
D.化学反应过程中,除了物质变化外,一定伴有能量变化
题型二:中和热的测定实验
【例2】(2021·陕西咸阳市·高二期末)关于中和热的测定实验,下列说法正确的是
A.在实验中,温度计只使用2次
B.为了使反应进行的更完全,可以使酸或碱适当过量
C.向盛装酸的烧杯中加碱时要小心缓慢以免洒出
D.用铁丝代替玻璃棒搅拌,会使测得的中和热数值偏大
【变2】(2020·福建省福州第十一中学高二期中)在测定中和热的实验中,下列说法正确的是
A.使用环形玻璃搅拌器是为了加快反应速率,减小实验误差
B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触
C.用 0.5mol·L-1NaOH 溶液分别与 0.5mol·L-1 的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测
得的中和热数值相同
杨sir化学,侵权必究
D.在测定中和热实验中需要使用的仪器有量筒、烧杯、酒精灯、温度计等
【例3】(2020·原阳县第三高级中学高二月考)50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在
如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热。回答下列问
题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是_____________。
(2)如果不盖杯盖,所求得的中和反应反应热的绝对值将会__________(填“偏大”“偏小”或“无影响” )。
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,调整反应物用量后所放出的热量与原实验________________(填“相等”或“不相等”,下同);所求中和反应反应热与原实验
_____________,简述理由:_______________________。
杨sir化学,侵权必究
【例4】(2021·黑龙江大庆市·铁人中学高一期中)某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶
液进行中和热的测定。
Ⅰ.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体_______g。
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):___。
名称 托盘天平(带砝码) 小烧杯 坩埚钳 玻璃棒 药匙 量筒
仪器
序号 a b c d e f
Ⅱ.中和热的测定:
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
(3)仪器a的名称为___,实验中还需要用到的玻璃仪器是___。
杨sir化学,侵权必究
(4)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
起始温度t/℃
温度 1 温度差平均值
终止温度t/℃
实验次数 2 (t-t)/℃
HSO NaOH 平均值 2 1
2 4
1 26.2 26.0 26.1 30.1
2 27.0 27.4 27.2 33.3
___
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4
②近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容
c=4.18J/(g·℃)。则中和热△H=___________(取小数点后一位)。③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是_____(填字母)。
a.实验装置保温、隔热效果差
b.配制0.50mol/LNaOH溶液时俯视刻度线读数
杨sir化学,侵权必究
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
e.用量筒量取NaOH溶液的体积时仰视读数
(5)实验中改用30mL0.50mol/L的硫酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,所
放出的热量_________(填“相等”或“不相等”),所求中和热的数值会_____________(填“相等”或“不相等”)。
模块二 反应热与焓变
知识预习
一、内能、焓、焓变
1.内能(符号为U):体系内物质的各种能量的总和,受________、________和________等的影响。
2.焓(符号为H):与内能有关的物理量。
3.焓变:在_______条件下进行的化学反应(严格地说,对反应体系做功有限定,中学阶段一般不考虑),
其反应热等于反应的焓变,符号:________,单位:________ (或________)。
杨sir化学,侵权必究
二、焓变的意义
1.当反应体系放热时其焓减小,ΔH为________,即ΔH_______。
2.当反应体系吸热时其焓减小,ΔH为________,即ΔH_______。
三、常见的放热反应与吸热反应
放热反应 吸热反应
①所有燃烧反应;
②大多数化合反应;
①大多数分解反应;
③酸碱中和反应;
②Ba(OH) ·8HO与NH Cl反应;
2 2 4
④金属与酸或水的置换反
③高温条件下C、H 、CO作还原剂的反
应; 2
应。
⑤物质的缓慢氧化;
⑥铝热反应。
思考与交流:①所有分解反应都是吸热反应吗?②需要加热才能发生的反应一定是吸热反应吗?
四、从反应物与生成物总能量相对大小分析焓变
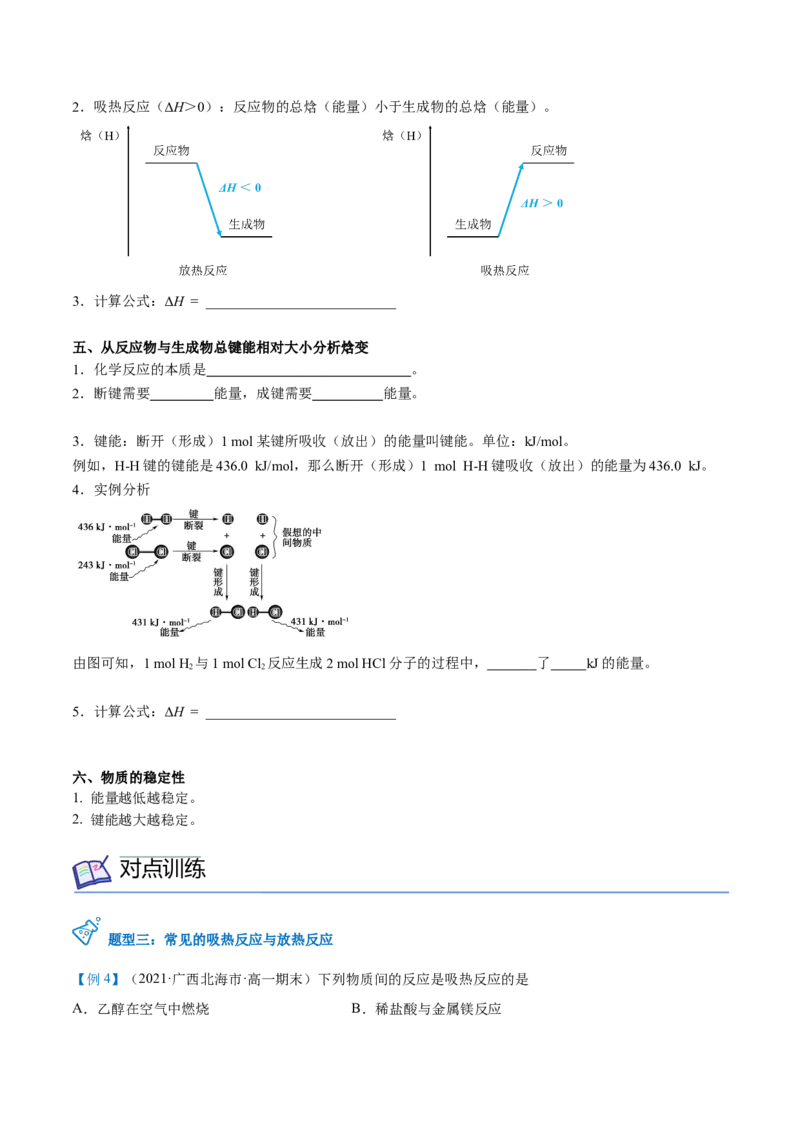
1.放热反应(ΔH<0):反应物的总焓(能量)大于生成物的总焓(能量)。2.吸热反应(ΔH>0):反应物的总焓(能量)小于生成物的总焓(能量)。
杨sir化学,侵权必究
3.计算公式:ΔH = ___________________________
五、从反应物与生成物总键能相对大小分析焓变
1.化学反应的本质是 。
2.断键需要 能量,成键需要 能量。
3.键能:断开(形成)1 mol某键所吸收(放出)的能量叫键能。单位:kJ/mol。
例如,H-H键的键能是436.0 kJ/mol,那么断开(形成)1 mol H-H键吸收(放出)的能量为436.0 kJ。
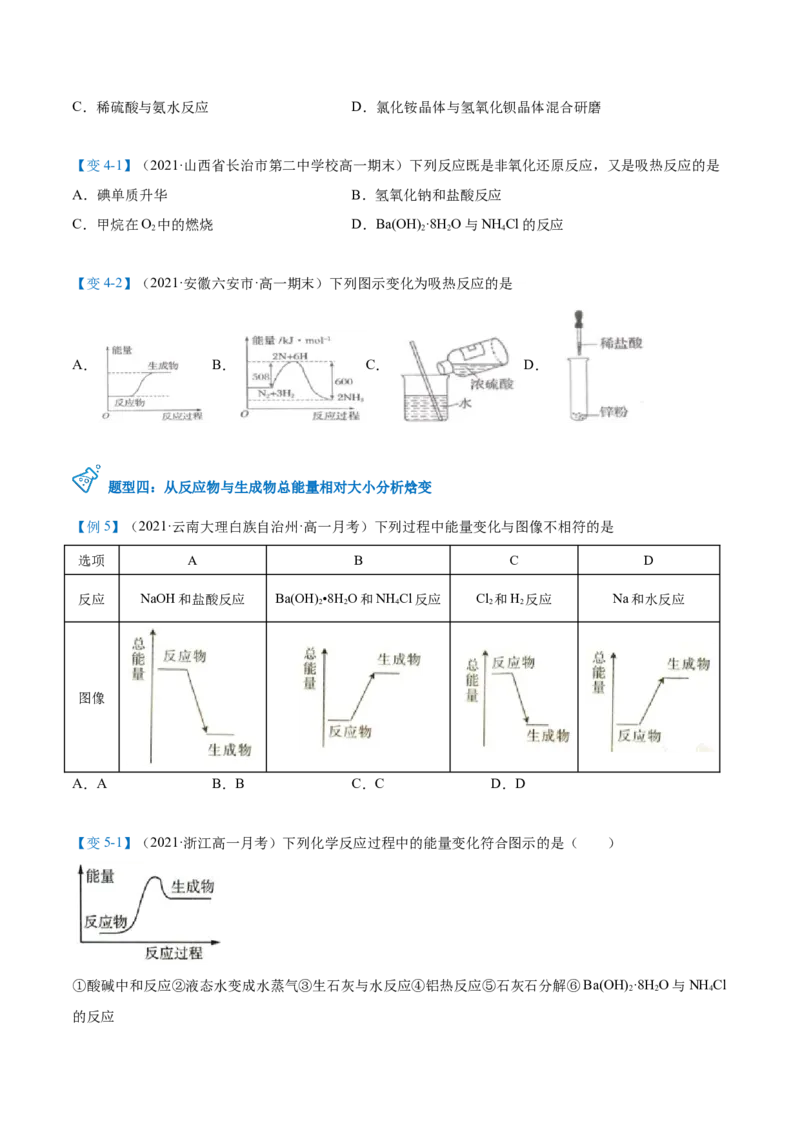
4.实例分析
由图可知,1 mol H 与1 mol Cl 反应生成2 mol HCl分子的过程中, 了 kJ的能量。
2 2 杨sir化学,侵权必究
5.计算公式:ΔH = ___________________________
六、物质的稳定性
1. 能量越低越稳定。
2. 键能越大越稳定。
对点训练
题型三:常见的吸热反应与放热反应
【例4】(2021·广西北海市·高一期末)下列物质间的反应是吸热反应的是
A.乙醇在空气中燃烧 B.稀盐酸与金属镁反应C.稀硫酸与氨水反应 D.氯化铵晶体与氢氧化钡晶体混合研磨
杨sir化学,侵权必究
【变4-1】(2021·山西省长治市第二中学校高一期末)下列反应既是非氧化还原反应,又是吸热反应的是
A.碘单质升华 B.氢氧化钠和盐酸反应
C.甲烷在O 中的燃烧 D.Ba(OH) ·8H O与NH Cl的反应
2 2 2 4
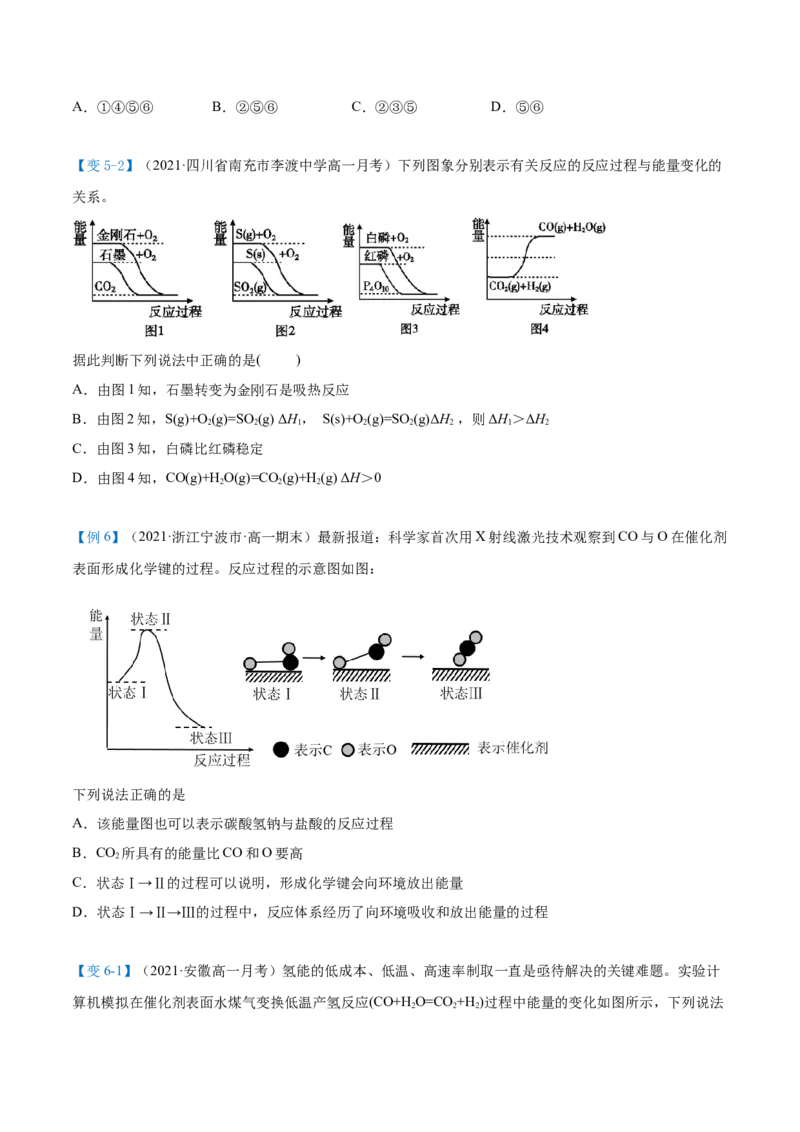
【变4-2】(2021·安徽六安市·高一期末)下列图示变化为吸热反应的是
杨sir化学,侵权必究
A. B. C. D.
题型四:从反应物与生成物总能量相对大小分析焓变
【例5】(2021·云南大理白族自治州·高一月考)下列过程中能量变化与图像不相符的是
选项 A B C D
反应 NaOH和盐酸反应 Ba(OH)•8HO和NHCl反应 Cl 和H 反应 Na和水反应
2 2 4 2 2
图像
A.A B.B C.C D.D
【变5-1】(2021·浙江高一月考)下列化学反应过程中的能量变化符合图示的是( )
杨sir化学,侵权必究
①酸碱中和反应②液态水变成水蒸气③生石灰与水反应④铝热反应⑤石灰石分解⑥Ba(OH) ·8H O与NH Cl
2 2 4
的反应A.①④⑤⑥ B.②⑤⑥ C.②③⑤ D.⑤⑥
【变5-2】(2021·四川省南充市李渡中学高一月考)下列图象分别表示有关反应的反应过程与能量变化的
关系。
据此判断下列说法中正确的是( )
A.由图1知,石墨转变为金刚石是吸热反应
B.由图2知,S(g)+O(g)=SO(g) ΔH, S(s)+O (g)=SO(g)ΔH ,则ΔH>ΔH
2 2 1 2 2 2 1 2
C.由图3知,白磷比红磷稳定
D.由图4知,CO(g)+HO(g)=CO(g)+H(g) ΔH>0
2 2 2
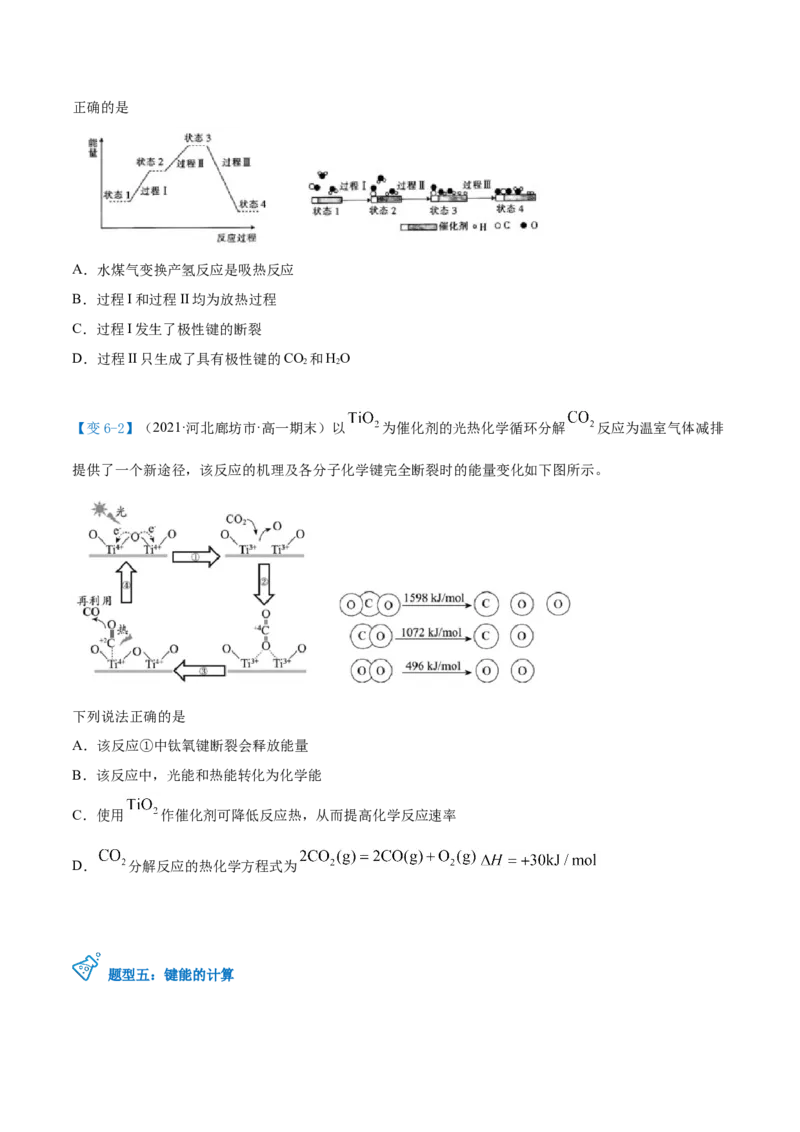
【例6】(2021·浙江宁波市·高一期末)最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂
表面形成化学键的过程。反应过程的示意图如图:
下列说法正确的是
A.该能量图也可以表示碳酸氢钠与盐酸的反应过程
B.CO 所具有的能量比CO和O要高
2
C.状态Ⅰ→Ⅱ的过程可以说明,形成化学键会向环境放出能量
D.状态Ⅰ→Ⅱ→Ⅲ的过程中,反应体系经历了向环境吸收和放出能量的过程
杨sir化学,侵权必究
【变6-1】(2021·安徽高一月考)氢能的低成本、低温、高速率制取一直是亟待解决的关键难题。实验计
算机模拟在催化剂表面水煤气变换低温产氢反应(CO+HO=CO+H )过程中能量的变化如图所示,下列说法
2 2 2正确的是
A.水煤气变换产氢反应是吸热反应
B.过程I和过程II均为放热过程
C.过程I发生了极性键的断裂
D.过程II只生成了具有极性键的CO 和HO
2 2
【变6-2】(2021·河北廊坊市·高一期末)以 为催化剂的光热化学循环分解 反应为温室气体减排
提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如下图所示。
杨sir化学,侵权必究
下列说法正确的是
A.该反应①中钛氧键断裂会释放能量
B.该反应中,光能和热能转化为化学能
C.使用 作催化剂可降低反应热,从而提高化学反应速率
D. 分解反应的热化学方程式为
题型五:键能的计算【例6】(2021·银川市·宁夏大学附属中学高二月考)已知H(g)+ O(g)=HO(g) ΔH=-242kJ·mol-1,断开
2 2 2
1molO=O键和1mol H—O键所吸收的能量分别为496kJ和463kJ,则断开1molH—H键所吸收的能量为
杨sir化学,侵权必究
( )
A.920kJ B.557kJ C.436kJ D.188kJ
【变6】(2021·河北石家庄二中高一期中)已知:N(g) +3H (g) 2NH (g) △H=-92.4 kJ/mo1.若断裂1
2 2 3
mol H-H、1 molN≡N需要吸收的能量分别为akJ、b kJ。则生成1 mol N-H放出能量的数值为
A. B.
C. D.
题型六:从反应物与生成物总键能相对大小分析焓变
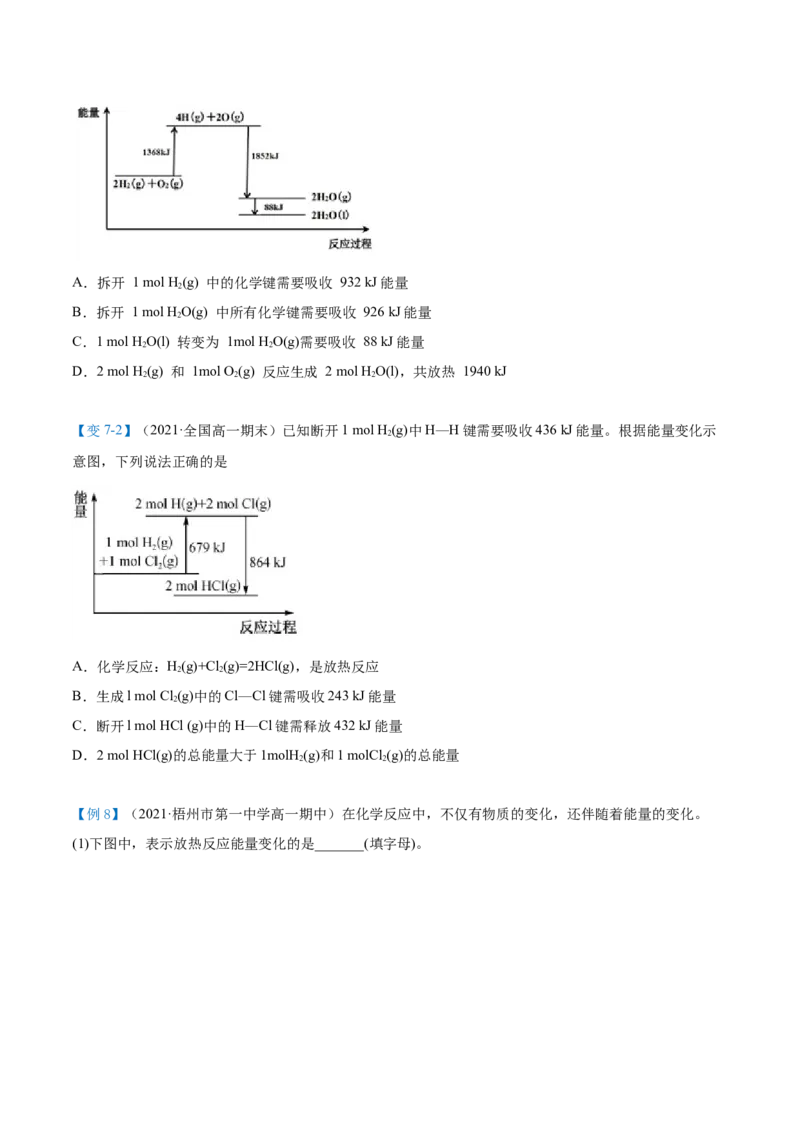
【例7】(2021·北京师范大学万宁附属中学高一期中)如图所示N(g)和O(g)反应生成NO(g)过程中能
2 2
量变化,判断下列说法错误的是( )
A.直观看,该反应中反应物断键吸收的总能量高于生成物形成键放出的总能量
B.2mol气态氧原子结合生成O(g)时,能放出498kJ能量
2
C.断裂1mol NO分子中的化学键,需要吸收632kJ能量
D.1molN 和1molO 的反应热ΔH=-180kJ·mol-1
2 2
【变7-1】(2021·浙江高二期中)已知 2O(g)=O (g) ∆H = - 496 kJ ∙mol -1,结合能量变化示意图。下列说法
2
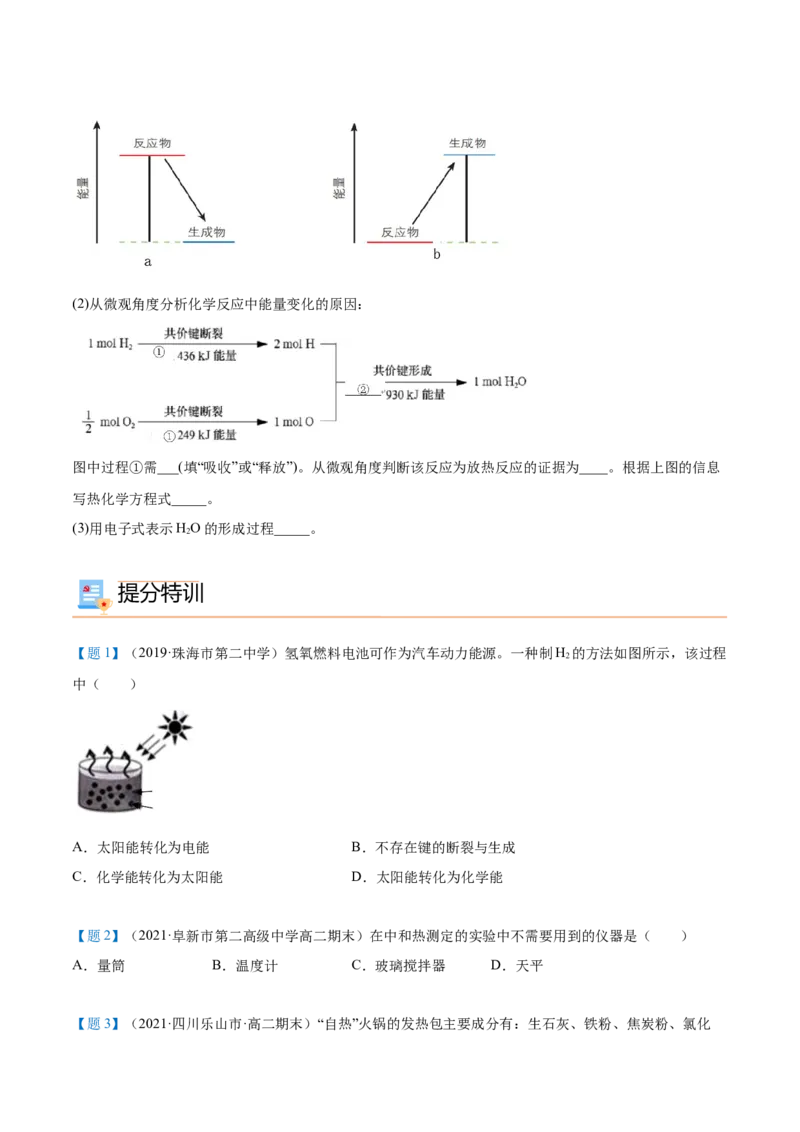
正确的是( )A.拆开 1 mol H (g) 中的化学键需要吸收 932 kJ能量
2
B.拆开 1 mol H O(g) 中所有化学键需要吸收 926 kJ能量
2 杨sir化学,侵权必究
C.1 mol H O(l) 转变为 1mol HO(g)需要吸收 88 kJ能量
2 2
D.2 mol H (g) 和 1mol O(g) 反应生成 2 mol H O(l),共放热 1940 kJ
2 2 2
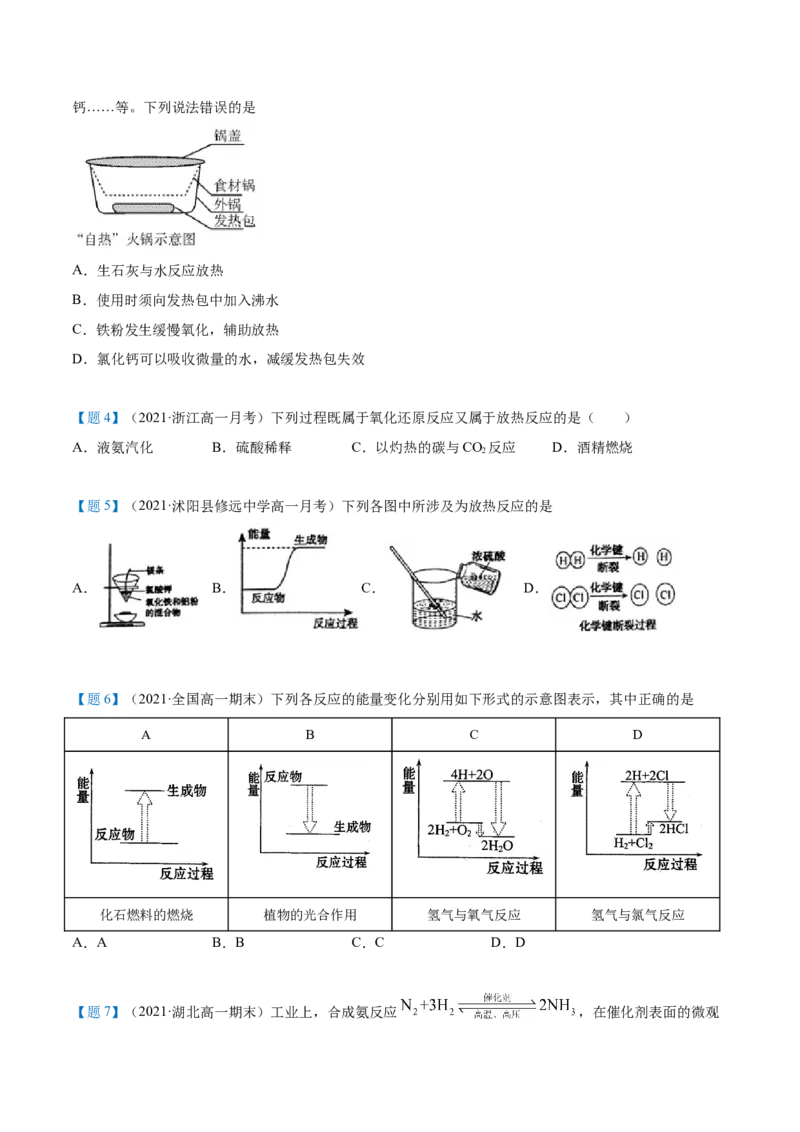
【变7-2】(2021·全国高一期末)已知断开1 mol H (g)中H—H键需要吸收436 kJ能量。根据能量变化示
2
意图,下列说法正确的是
A.化学反应:H(g)+Cl (g)=2HCl(g),是放热反应
2 2
B.生成l mol Cl (g)中的Cl—Cl键需吸收243 kJ能量
2
C.断开l mol HCl (g)中的H—Cl键需释放432 kJ能量
D.2 mol HCl(g)的总能量大于1molH (g)和1 molCl (g)的总能量
2 2
【例8】(2021·梧州市第一中学高一期中)在化学反应中,不仅有物质的变化,还伴随着能量的变化。
(1)下图中,表示放热反应能量变化的是_______(填字母)。(2)从微观角度分析化学反应中能量变化的原因:
图中过程①需___(填“吸收”或“释放”)。从微观角度判断该反应为放热反应的证据为____。根据上图的信息
写热化学方程式_____。
(3)用电子式表示HO的形成过程_____。
2
提分特训
【题1】(2019·珠海市第二中学)氢氧燃料电池可作为汽车动力能源。一种制H 的方法如图所示,该过程
2
中( )
杨sir化学,侵权必究
A.太阳能转化为电能 B.不存在键的断裂与生成
C.化学能转化为太阳能 D.太阳能转化为化学能
【题2】(2021·阜新市第二高级中学高二期末)在中和热测定的实验中不需要用到的仪器是( )
A.量筒 B.温度计 C.玻璃搅拌器 D.天平
【题3】(2021·四川乐山市·高二期末)“自热”火锅的发热包主要成分有:生石灰、铁粉、焦炭粉、氯化钙……等。下列说法错误的是
A.生石灰与水反应放热
B.使用时须向发热包中加入沸水
C.铁粉发生缓慢氧化,辅助放热
D.氯化钙可以吸收微量的水,减缓发热包失效
【题4】(2021·浙江高一月考)下列过程既属于氧化还原反应又属于放热反应的是( )
A.液氨汽化 B.硫酸稀释 C.以灼热的碳与CO 反应 D.酒精燃烧
2
【题5】(2021·沭阳县修远中学高一月考)下列各图中所涉及为放热反应的是
杨sir化学,侵权必究
A. B. C. D.
【题6】(2021·全国高一期末)下列各反应的能量变化分别用如下形式的示意图表示,其中正确的是
A B C D
化石燃料的燃烧 植物的光合作用 氢气与氧气反应 氢气与氯气反应
A.A B.B C.C D.D
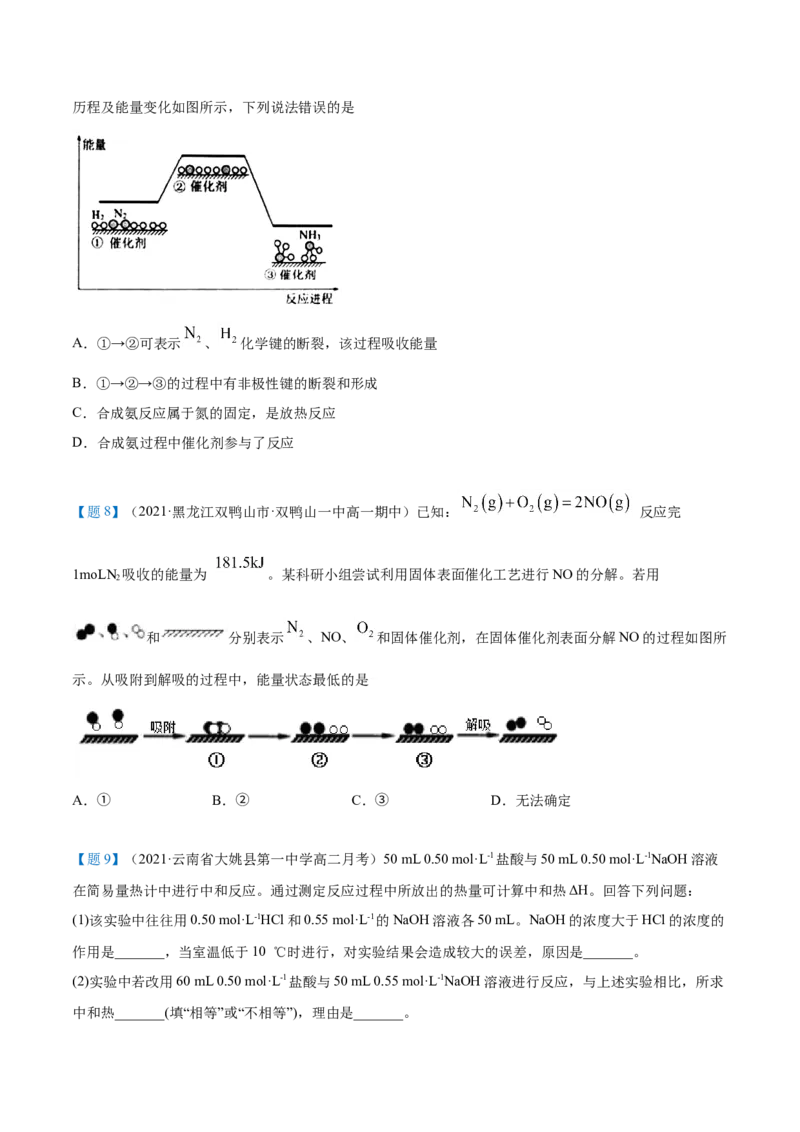
【题7】(2021·湖北高一期末)工业上,合成氨反应 ,在催化剂表面的微观历程及能量变化如图所示,下列说法错误的是
A.①→②可表示 、 化学键的断裂,该过程吸收能量
B.①→②→③的过程中有非极性键的断裂和形成
C.合成氨反应属于氮的固定,是放热反应
D.合成氨过程中催化剂参与了反应
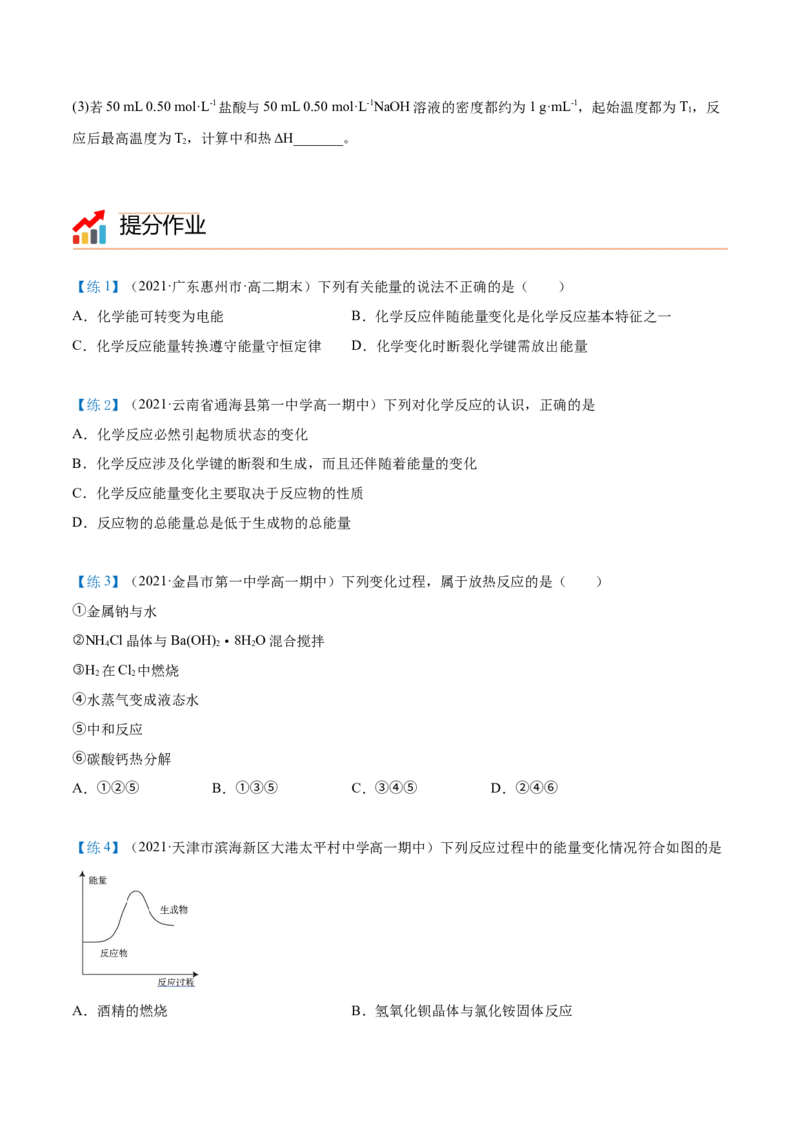
【题8】(2021·黑龙江双鸭山市·双鸭山一中高一期中)已知: 反应完
1moLN 吸收的能量为 。某科研小组尝试利用固体表面催化工艺进行NO的分解。若用
2
和 分别表示 、NO、 和固体催化剂,在固体催化剂表面分解NO的过程如图所
示。从吸附到解吸的过程中,能量状态最低的是
杨sir化学,侵权必究
A.① B.② C.③ D.无法确定
【题9】(2021·云南省大姚县第一中学高二月考)50 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1NaOH溶液
在简易量热计中进行中和反应。通过测定反应过程中所放出的热量可计算中和热ΔH。回答下列问题:
(1)该实验中往往用0.50 mol·L-1HCl和0.55 mol·L-1的NaOH溶液各50 mL。NaOH的浓度大于HCl的浓度的
作用是_______,当室温低于10 ℃时进行,对实验结果会造成较大的误差,原因是_______。
(2)实验中若改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所求
中和热_______(填“相等”或“不相等”),理由是_______。(3)若50 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1NaOH溶液的密度都约为1 g·mL-1,起始温度都为T,反
1
应后最高温度为T,计算中和热ΔH_______。
2
提分作业
【练1】(2021·广东惠州市·高二期末)下列有关能量的说法不正确的是( )
A.化学能可转变为电能 B.化学反应伴随能量变化是化学反应基本特征之一
C.化学反应能量转换遵守能量守恒定律 D.化学变化时断裂化学键需放出能量
杨sir化学,侵权必究
【练2】(2021·云南省通海县第一中学高一期中)下列对化学反应的认识,正确的是
A.化学反应必然引起物质状态的变化
B.化学反应涉及化学键的断裂和生成,而且还伴随着能量的变化
C.化学反应能量变化主要取决于反应物的性质
D.反应物的总能量总是低于生成物的总能量
【练3】(2021·金昌市第一中学高一期中)下列变化过程,属于放热反应的是( )
①金属钠与水
②NH Cl晶体与Ba(OH) ·8HO混合搅拌
4 2 2
③H 在Cl 中燃烧
2 2
④水蒸气变成液态水
⑤中和反应
⑥碳酸钙热分解
A.①②⑤ B.①③⑤ C.③④⑤ D.②④⑥
【练4】(2021·天津市滨海新区大港太平村中学高一期中)下列反应过程中的能量变化情况符合如图的是
A.酒精的燃烧 B.氢氧化钡晶体与氯化铵固体反应C.镁和稀硫酸的反应 D.酸和碱的中和反应
杨sir化学,侵权必究
【练5】(2021·北京大兴区·高一期末)氢气和氧气发生反应的过程,可用如下模型表示(“-”表示化学键),
下列说法不正确的是
A.过程I是吸热过程
B.该反应为放热反应
C.状态a的总能量大于状态d的总能量
D.该反应的能量转化形式只能以热能的形式进行
【练6】(2021·北京高一学业考试)已知:Mg+2HCl=MgCl +H ↑,测得反应过程中溶液温度升高。下列关
2 2
于该反应的说法中,不正确的是
A.属于吸热反应
B.属于氧化还原反应
C.反应物的总能量高于生成物的总能量
D.化学键的断裂与形成是化学反应中能量变化的主要原因
【练7】(2021·湖北高二月考)工业上可采用 CHOH CO+2H 的方法来制取高纯度的 CO 和
3 2
H。我国科研人员通过计算机模拟,研究了在钯基催化剂表面甲醇制氢的反应历程如图所示,其中吸附在
2
钯催化剂表面上的物种用*标注。下列说法正确的是
已知:甲醇(CHOH)脱氢反应的第一步历程,有两种可能的方式:
3
方式I:CHOH*→CH O*+H* E=+103.1 kJ·mol-1
3 3 a方式II:CHOH*→CH*+OH E =+249.3 kJ·mol-1
3 b
A.CHOH*→CO*+2H (g)的ΔH<0
3 2
B.①②都为 O—H 键的断裂过程
C.由活化能 E 值推测,甲醇裂解过程主要历经的方式应为II
杨sir化学,侵权必究
D.放热最多阶段的化学方程式为 CHO*+3H*→CO*+4H*
【练8】(2021·广西钦州市·高二期末)已知:① 2NO (g)⇌N O(g) △H<0;② 2NO (g)⇌N O(l)
2 2 4 1 2 2 4
△H<0;下列能量变化示意图中,正确的是
2
A. B. C. D.
【练9】(2020·浙江省东阳中学高二期中)已知H(g)+Br (g)=2HBr(g) ΔH =-102kJ·mol-1,1molHBr分子中
2 2
的化学键断裂时需要吸收369kJ的能量,1molBr 分子中的化学键断裂时需要吸收的能量为200kJ,则
2
1molH 分子中的化学键断裂时需要吸收的能量为( )
2
A.436kJ B.218 kJ C.169kJ D.569kJ
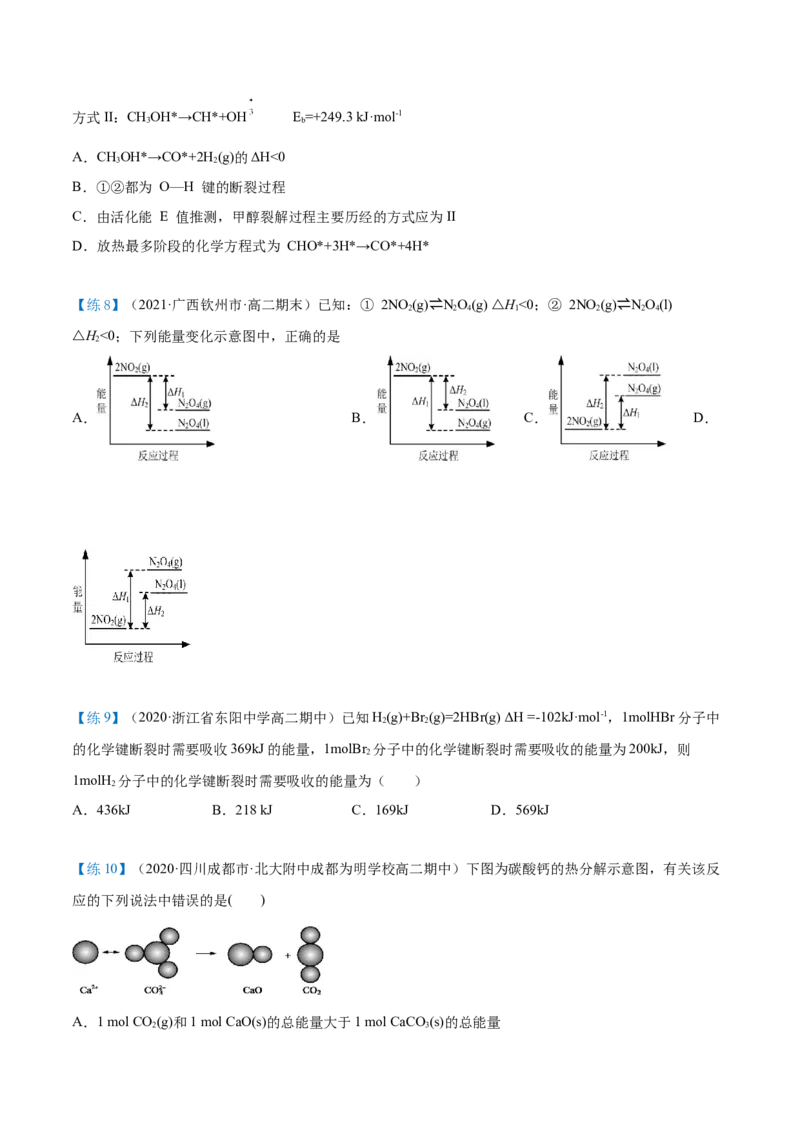
【练10】(2020·四川成都市·北大附中成都为明学校高二期中)下图为碳酸钙的热分解示意图,有关该反
应的下列说法中错误的是( )
A.1 mol CO (g)和1 mol CaO(s)的总能量大于1 mol CaCO(s)的总能量
2 3B.该反应的ΔH>0
C.该反应中有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键形成放出能量
D.由该反应可推出凡是需要加热才发生的反应均为吸热反应
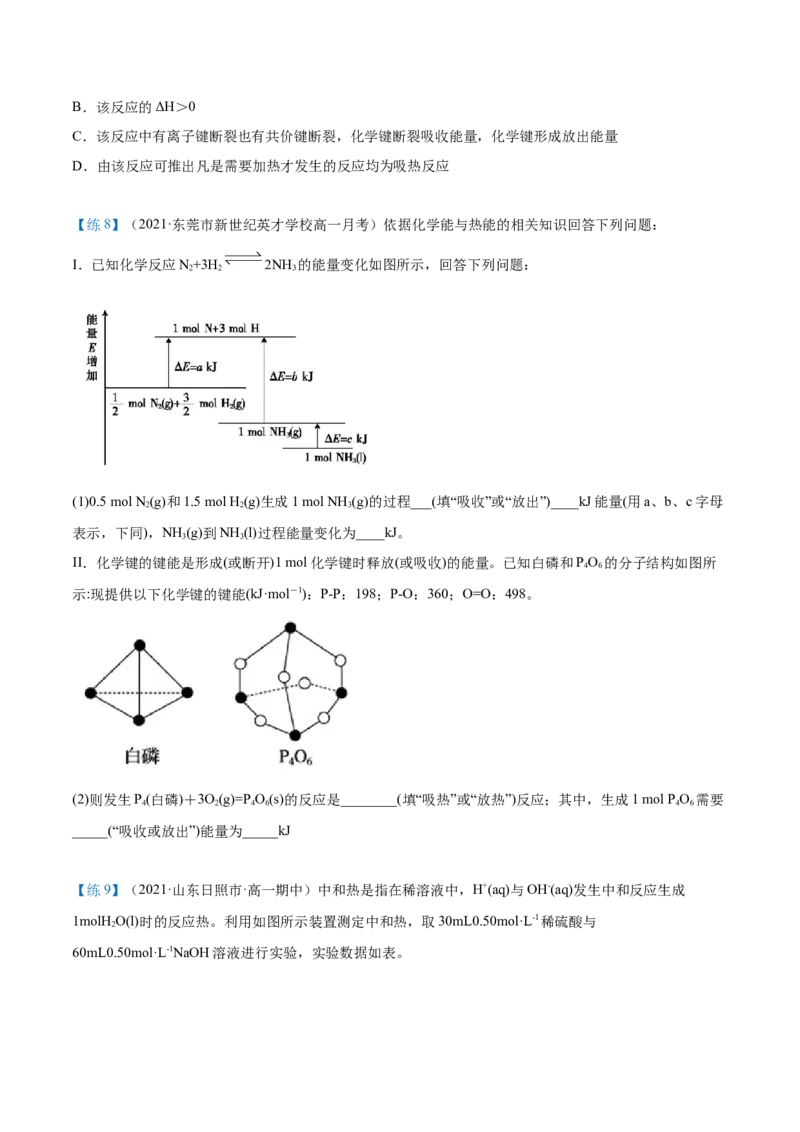
【练8】(2021·东莞市新世纪英才学校高一月考)依据化学能与热能的相关知识回答下列问题:
I.已知化学反应N+3H 2NH 的能量变化如图所示,回答下列问题:
2 2 3 杨sir化学,侵权必究
(1)0.5 mol N (g)和1.5 mol H(g)生成1 mol NH (g)的过程___(填“吸收”或“放出”)____kJ能量(用a、b、c字母
2 2 3
表示,下同),NH (g)到NH (l)过程能量变化为____kJ。
3 3
II.化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量。已知白磷和PO 的分子结构如图所
4 6
示:现提供以下化学键的键能(kJ·mol-1):P-P:198;P-O:360;O=O:498。
(2)则发生P(白磷)+3O(g)=P O(s)的反应是________(填“吸热”或“放热”)反应;其中,生成1 mol P O 需要
4 2 4 6 4 6
_____(“吸收或放出”)能量为_____kJ
【练9】(2021·山东日照市·高一期中)中和热是指在稀溶液中,H+(aq)与OH-(aq)发生中和反应生成
1molH O(l)时的反应热。利用如图所示装置测定中和热,取30mL0.50mol·L-1稀硫酸与
2
60mL0.50mol·L-1NaOH溶液进行实验,实验数据如表。起始温度T/℃
1
温度
终止温度T/℃
实验次数 2
HSO NaOH 平均值
2 4
1 26.2 26.0 26.1 30.2
2 27.0 27.4 27.2 32.3
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.3
回答下列问题:
(1)上述实验中温度变化的平均值为___℃,若近似认为0.50mol·L-1稀硫酸与0.5mol·L-1NaOH溶液的密度均
为1g·cm-3,反应所得溶液的比热容c=4.18J·(g·℃)-1,则中和热ΔH的数值为___kJ·mol-1(保留1位小数)。
(2)上述实验结果与中和热数值57.3kJ·mol-1有偏差,产生偏差的原因不可能是因为___(填标号)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入内筒中
d.测过稀硫酸的温度计未洗净直接用于测定NaOH溶液的温度
(3)本次实验共需NaOH溶液240mL,则配制0.5mol·L-1NaOH溶液时,需称取NaOH固体______g。
(4)若改用30mL0.50mol·L-1稀硫酸与30mL0.5mol·L-1Ba(OH) 溶液进行实验,(填“能”或“不能”)_____据此实
2
验求中和热。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育