文档内容
选择性必修一综合测试(基础)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
1.(2022湖州)书写热化学方程式时不需要标注( )
A.温度 B.压强
C.反应条件 D.物质聚集状态
【答案】C
【解析】由于反应热ΔH与测定的条件(温度、压强)、物质的聚集状态有关,因此书写热化学方程式时应注
明,若是在25 ℃、101 kPa条件下,这时可不注明温度和压强。因此不需要标注的是反应条件。
故答案为:C。
2.(2022云南)下列变化中,不属于吸热反应的是( )
A. 与固体 反应 B. 高温分解反应
C.生石灰跟水反应 D.盐酸与碳酸氢钠溶液反应
【答案】C
【解析】A. 与固体 反应是吸热反应,故A不符合题意;
B.一般分解反应属于吸热反应, 高温分解需要持续加热,是吸热反应,故B不符合题意;
C.一般化合反应属于放热反应,生石灰跟水反应是放热反应,故C符合题意;
D.盐酸与碳酸氢钠溶液反应是吸热反应,故D不符合题意;
故答案为C
3.(2022河南月考)已知 H(g)+Cl (g) 2HCl(g) ∆H=-183kJ∙mol-1,其它相关数据如表:
2 2
物质 H Cl HCl
2 2
1mol分子中的化学键断裂时吸收的能量/kJ 436 a 431
下列说法正确的是( )
A.1L H (g)和1L Cl (g)完全反应生成2L HCl(g)放出183kJ热量
2 2
B.1mol H(g)和1mol Cl (g)的总能量小于2mol HCl(g)的总能量
2 2
C.a=243D.该反应生成2mol HCl(l)时,放出的能量小于183kJ
【答案】C
【解析】A.在热化学方程式中,化学计量数只表示物质的量, 1mol H(g)和1mol Cl (g)完全反应生成
2 2
2mol HCl(g)放出183kJ热量,A不符合题意;
B.由热化学方程式可知,反应放热,则1mol H(g)和1mol Cl (g)的总能量大于2mol HCl(g)的总能量,B不
2 2
符合题意;
C.∆H=E(反应物键能)-E(生成物键能)=436+a-2×431=-183,a=243,C符合题意;
D.物质由气态转变为液态,会放出能量,该反应生成2mol HCl(l)时,放出的能量大于183kJ,D不符合题
意;
故答案为:C。
4.(2022江西)下列能符合题意地表示 燃烧热的热化学方程式是( )
A.
B.
C.
D.
【答案】A
【解析】燃烧热是指1mol可燃物完全燃烧生成稳定化合物放出的热量, 的燃烧热为
,则 完全燃烧生成1mol二氧化碳和2mol液态水放出的热量 ,
所以 燃烧的热化学方程式为:
,故A符合题意。
5.(2022平顶山)下列操作一定能加快相应化学反应速率的是( )
A.延长反应时间 B.增大容积
C.升高体系温度 D.增大浓度【答案】C
【解析】A.延长反应时间,不能加快化学反应速率,A错;
B.对于没有气体参加的反应,增大容积不能改变化学反应速率,对于有气体参与的化学反应,增大容积
减小化学反应速率,B错;
C.升高体系温度,一定能加快反应速率,C对;
D.铁与稀硫酸的反应中,若增大硫酸的浓度,加入浓硫酸,铁与浓硫酸会发生钝化,增大硫酸浓度不能
加快反应速率,D错;
故答案为:C。
6.(2022湖州)通常,平衡常数K越大,反应越完全。一般来说,当 时,反应进行完全。则n为
( )
A.2 B.5 C.10 D.18
【答案】B
【解析】通常,平衡常数K越大,反应越完全,一般来说,当 时,反应进行完全,
故答案为:B。
7.(2022辽宁)反应3H(g)+N(g) 2NH (g) ΔH<0,达到平衡后,将体系的温度降低,下列叙述中正
2 2 3
确的是( )
A.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
B.正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
C.正反应速率和逆反应速率都减小,平衡向逆反应方向移动
D.正反应速率和逆反应速率都减小,平衡向正反应方向移动
【答案】D
【解析】反应3H(g)+N(g) 2NH (g) ΔH<0,该反应的正反应是气体体积减小的放热反应,根据化学
2 2 3
平衡移动原理,当反应达到平衡后,将气体混合物的温度降低,物质的内能减小,反应速率减小,正、逆
反应速率都减小,由于温度对吸热反应影响更大,所以逆反应速率减小的更多,减小反应速率后,放热方
向速率减小的少,正反应速率大于逆反应速率,所以平衡向放热反应方向移动,
故答案为:D。
8.(2022山东)下列关于酸碱中和滴定实验的说法正确的是( )
A.用碱式滴定管量取 的 溶液B.锥形瓶使用前用待测液润洗
C.用标准盐酸滴定某氨水溶液,应选用甲基橙作指示剂
D.用标准盐酸滴定某氨水溶液,滴定终点时俯视读数,导致测定结果偏高
【答案】C
【解析】A.KMnO 溶液具有强氧化性,应用酸式滴定管量取,故A不符合题意;
4
B.锥形瓶使用时不能润洗,否则会导致滴定误差,故B不符合题意;
C.强酸滴定弱碱,应选用甲基橙作指示剂,故C符合题意;
D.达到滴定终点时俯视读数,使读取的标准液的体积偏小,测定结果偏低,故D不符合题意;
故答案为:C。
9.(2021渭滨)在以下各种情形下,下列电离方程式的书写正确的是( )
A.水溶液中NaHSO 电离:NaHSO=Na++H++SO4❑
4 4 2−
B.HCO 的电离:HCO 2H++CO3❑
2 3 2 3 2−
C.Al(OH) 的碱式电离:Al(OH) =Al3++3OH-
3 3
D.亚硫酸氢钠溶液中水的电离:NaHSO Na++HSO3❑
3 −
【答案】A
【解析】A.NaHSO 为强酸的酸式盐,电离方程式为NaHSO=Na++H++SO4❑ ,故A符合题意;
4 4 2−
B.HCO 为二元酸,分步电离:HCO H++HCO3❑,HCO3❑ H++CO3❑ ,故B不符合题意;
2 3 2 3 − − 2−
C.Al(OH) 为两性氢氧化物,其电离可表示为: Al(OH) Al3++3OH-,故C不符
3 3
合题意;
D.亚硫酸氢钠是弱酸的酸式盐,盐是强电解质,溶液中水的电离:NaHSO=Na++HSO3❑, 故D不符合
3 −
题意;
故答案为A。
10.(2021咸阳)25℃时,不断将水滴入 氨水中,下列图像变化合理的是( )A. B.
C. D.
【答案】C
【解析】A.该温度下,加水稀释稀氨水,促进一水合氨电离,溶液的pH减小,但无论任何稀释,溶液的
pH仍然大于7,不能等于7或小于7,故A不符合题意;
B.温度不变时,弱电解质溶液中,浓度越小其电离程度越大,所以一水合氨电离程度随着水的增加而增
大,故B不符合题意;
C.溶液导电能力与离子浓度成正比,加水稀释稀氨水,一水合氨电离增大程度小于溶液体积增大程度,
所以溶液中氢氧根离子和铵根的浓度降低,溶液的导电性减小,故C符合题意;
D.加水稀释稀氨水,溶液中氢离子浓度增大,当溶液接近中性时,氢离子浓度接近10-7mol/L,故D不符
合题意。
故答案为:C。
11.(2022唐山)下列水解的离子方程式正确的是( )
A.NH +2H O NH ·H O+HO+ B.I-+H O HI+OH-
2 3 2 3 2
C.CO +2H O HCO+2OH- D.Al3++3H O=Al(OH) +3H+
2 2 3 2 3
【答案】A
【解析】A.铵根离子水解生成一水合氨和水合氢离子,故A符合题意;
B.碘离子属于强酸阴离子,不水解,故B不符合题意;
C.碳酸根离子为多元弱酸的酸根离子,分步水解,以第一步为主生成碳酸氢根离子和氢氧根离子,CO
+H O +OH-,故C不符合题意;
2D.水解是微弱的,应该用可逆号, Al3++3H O Al(OH) +3H+,故D不符合题意;
2 3
故答案为:A。
12.(2022温州)下列应用与盐类的水解无关的是( )
A.加热蒸干AlCl 溶液,得不到AlCl 固体
3 3
B.FeSO 溶液保存时加入少量铁粉
4
C.热的纯碱溶液可用于清洗餐具上的油污
D.草木灰与铵态氮肥不能混用
【答案】B
【解析】A.由于AlCl +3H O Al(OH) +3HCl,加热HCl挥发,促进AlCl 水解,故加热蒸干AlCl 溶液,
3 2 3 3 3
得不到AlCl 固体,故与水解有关,A不合题意;
3
B.FeSO 溶液保存时加入少量铁粉是防止Fe2+被氧化而变质,与水解无关,B符合题意;
4
C.热的纯碱溶液可用于清洗餐具上的油污是由于 水解使溶液呈碱性,从而促进油脂的水解,故与盐
类的水解有关,C不合题意;
D.草木灰与铵态氮肥不能混用是由于草木灰因水解呈碱性,氨态氮肥因水解呈酸性,二者水解相互促进
将产生NH 逸出,降低氨态氮肥的肥效,与水解有关,D不合题意;
3
故答案为:B。
13.(2022怀仁)用铜片、银片设计成如图所示的原电池。以下有关该原电池的叙述正确的是( )
A.电子通过盐桥从乙池移向甲池
B.盐桥中K+向左移动
C.开始时,银片上发生的反应是Ag-e-=Ag+
D.电路中每转移2mole-,正极材料增重216g
【答案】D
【解析】A.电子从铜片经外电路流向银片,不经盐桥,A不符合题意;
B.盐桥中阳离子向正极移动,则K+向右移动,B不符合题意;C.银片上发生的反应是:Ag++e-=Ag,C不符合题意;
D.每转移2mole-,正极生成2molAg,增重为 ,D符合题意;
故答案为:D。
14.(2022怀仁)下列有关电化学原理的说法正确的是( )
A.铝—空气燃料电池以KOH为电解液时,负极反应为:
B.用电解法精炼铜,阳极反应为:
C.钢铁在中性条件下被腐蚀,正极反应为:
D.电解法冶炼铝时,阳极反应为:
【答案】D
【解析】A. 铝—空气燃料电池以KOH为电解液时,负极上铝失去电子被氧化转变为偏铝酸根离子,负
极反应为: ,A不符合题意;
B. 用电解法精炼铜,阳极粗铜上的铜等金属失电子被氧化,阳极反应为: ,B不符合题
意;
C. 钢铁在中性条件下发生的是吸氧腐蚀,正极反应为: ,C不符合题意;
D.工业上电解熔融的氧化铝来冶炼铝时,阳极氧离子失电子被氧化,阳极反应为: ,
D符合题意;
故答案为:D。
15.(2022越秀)利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列说法错误的是( )
A.电解时以精铜作阳极,发生氧化反应
B.电解时阴极上发生的反应为Cu2++2e- = Cu
C.粗铜连接电源正极,电极反应为Cu-2e- = Cu2+
D.电解后电解槽底部会形成含少量Ag、Pt等金属的阳极泥
【答案】A
【解析】A.电解时粗铜做阳极,发生氧化反应,A符合题意;
B.电解时阴极是溶液中的铜离子得到电子生成铜,B不符合题意;C.粗铜连接电源的正极做阳极,铜失去电子生成铜离子,C不符合题意;
D.比铜活泼性差的金属成为阳极泥,如银或铂等,D不符合题意;
故答案为:A。
16.(2分)(2022高二下·成都期末)下列说法正确的是( )
A.镍镉电池、锂离子电池和碱性锌锰电池都是二次电池
B.黄铜(铜锌合金)制作的铜锣不易生成铜绿与电化学原理有关
C.燃料电池是一种高效但会严重污染环境的新型电池
D.铅蓄电池放电时正极是 ,负极是
【答案】B
【解析】A.碱性锌锰干电池是一次电池,故A不符合题意;
B.铜锌合金,构成原电池,锌是负极,锌失电子被氧化,铜是正极,所以黄铜(铜锌合金)制作的铜锣不易
生成铜绿,与电化学原理有关,故B符合题意;
C.燃料电池如氢氧燃料电池是一种高效但没有污染的新型电池,故C不符合题意;
D.铅蓄电池放电的时候, 被氧化, 为原电池的负极, 被还原,为原电池的正极,D不符合
题意;
故答案为:B。
二、非选择题:共56分。
17.(12分)(2022高二上·天津市期中)完成硫、氮化合物的相关问题
(1)(3分)为减少SO 的排放,常采取的措施有:
2
①将煤转化为清洁气体燃料。写出焦炭与水蒸气反应的热化学方程式。 。
已知:H(g)+ O(g) HO(g) ∆H=-241.8 kJ∙mol-1
2 2 2
C(s)+ O(g) CO(g) ∆H=-110.5 kJ∙mol-1
2
②洗涤含SO 的烟气。以下物质可作洗涤剂的是 。
2
a.Ca(OH) b.NaCO c.CaCl d.NaHSO
2 2 3 2 3
(2)(3分)已知:室温时,氢硫酸(H S): , ;
2
亚硫酸(H SO ): , 。
2 3①HS是有毒气体,可用NaCO 溶液吸收,生成两种酸式盐。写出反应的离子方程式 。
2 2 3
②向饱和HS溶液中通入过量的SO 气体。下列关系图正确的是 。
2 2
a. b.
c. d.
(3)(6分)汽车尾气中NO 和CO的生成及转化
x
①已知汽缸中生成NO的反应为:N(g)+O(g) 2NO(g) △H>0。汽车启动后,汽缸温度越高,单位时
2 2
间内NO排放量越大,原因是: 。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O (g)。已知该反应的
2
△H>0,简述该设想能否实现的依据: 。
③在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为
。
【答案】(1)C(s)+HO(g) CO(g)+H(g) ∆H=+131.3kJ∙mol-1;ab
2 2
(2) ;b
(3)温度升高,反应速率加快,平衡右移;该反应是焓增、熵减的反应,任何温度下均不自发进行;
2NO+2CO N+2CO
2 2
【解析】(1)Ⅰ.H (g)+ O(g) HO(g) ∆H=-241.8 kJ∙mol-1
2 2 2Ⅱ.C(s)+ O(g) CO(g) ∆H=-110.5 kJ∙mol-1
2
①依据盖斯定律,将反应Ⅱ-Ⅰ得:焦炭与水蒸气反应的热化学方程式:C(s)+HO(g) CO(g)+H(g)
2 2
∆H=(-110.5 kJ∙mol-1)-(-241.8 kJ∙mol-1)=+131.3kJ∙mol-1。
②SO 为酸性氧化物,a.Ca(OH) 、b.Na CO 都显碱性,能与SO 发生反应,可作洗涤剂,
2 2 2 3 2
故答案为:ab。答案为:C(s)+HO(g) CO(g)+H(g) ∆H=+131.3kJ∙mol-1;ab;
2 2
(2)①HS是有毒气体,可用NaCO 溶液吸收,生成两种酸式盐为NaHCO 和NaHS,反应的离子方程式
2 2 3 3
。
②向饱和HS溶液中通入过量的SO 气体,起初发生反应2HS+SO=3S↓+2H O,刚好完全反应时溶液呈中
2 2 2 2 2
性,当SO 过量时,发生反应SO +H O HSO 、HSO H++ ,溶液酸性增强,pH减小,则关
2 2 2 2 3 2 3
系图中正确的是b。答案为: ;b;
(3)①对于反应N(g)+O(g) 2NO(g) △H>0,升高温度,平衡正向移动,单位时间内NO排放量越大,
2 2
原因是:温度升高,反应速率加快,平衡右移。
②对于反应2CO(g)=2C(s)+O (g),△H>0,ΔS<0,则△H-TΔS>0,则反应不能自发进行,能否实现的依
2
据:该反应是焓增、熵减的反应,任何温度下均不自发进行。
③在汽车尾气催化转化器中,CO和NO反应,生成N 和CO,其化学反应方程式为2NO+2CO
2 2
N+2CO 。答案为:温度升高,反应速率加快,平衡右移;该反应是焓增、熵减的反应,任何温度下均不
2 2
自发进行;2NO+2CO N+2CO 。
2 2
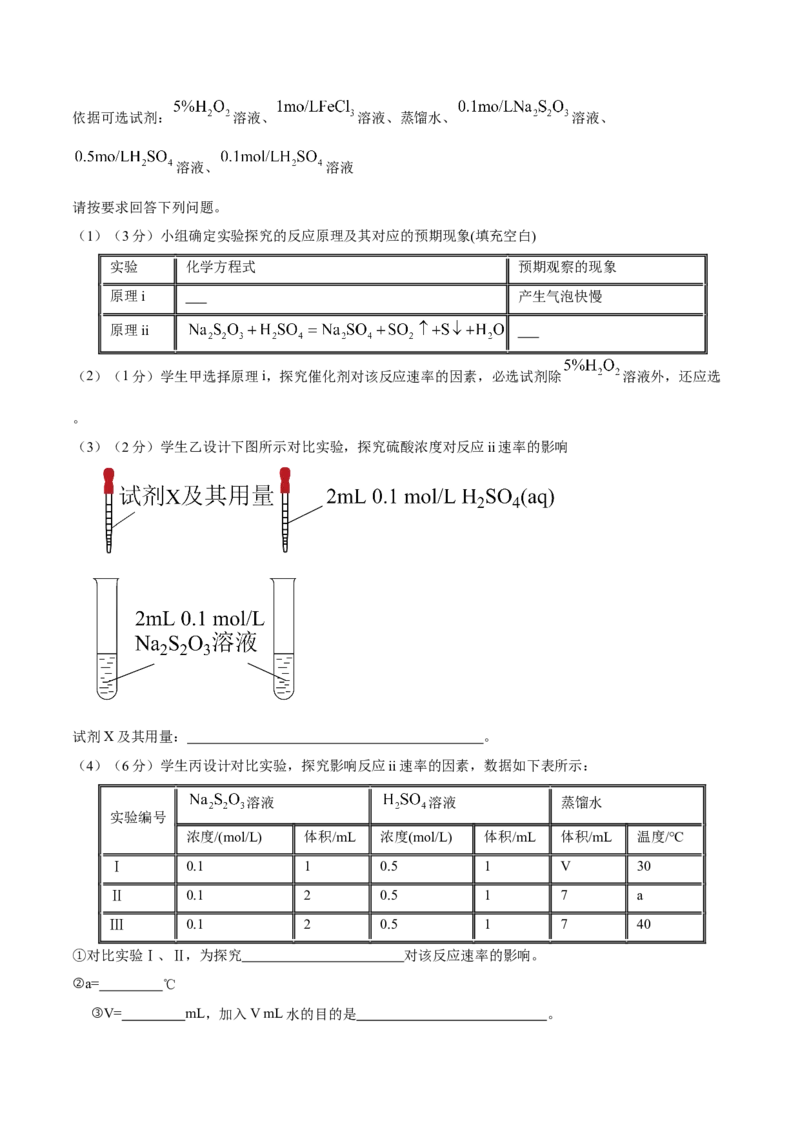
18.(12分)(2022高二上·河西期中)某小组学生设计了如下定性探究影响化学反应速率因素的实验。依据可选试剂: 溶液、 溶液、蒸馏水、 溶液、
溶液、 溶液
请按要求回答下列问题。
(1)(3分)小组确定实验探究的反应原理及其对应的预期现象(填充空白)
实验 化学方程式 预期观察的现象
原理i 产生气泡快慢
原理ii
(2)(1分)学生甲选择原理i,探究催化剂对该反应速率的因素,必选试剂除 溶液外,还应选
。
(3)(2分)学生乙设计下图所示对比实验,探究硫酸浓度对反应ii速率的影响
试剂X及其用量: 。
(4)(6分)学生丙设计对比实验,探究影响反应ii速率的因素,数据如下表所示:
溶液 溶液 蒸馏水
实验编号
浓度/(mol/L) 体积/mL 浓度(mol/L) 体积/mL 体积/mL 温度/℃
Ⅰ 0.1 1 0.5 1 V 30
Ⅱ 0.1 2 0.5 1 7 a
Ⅲ 0.1 2 0.5 1 7 40
①对比实验Ⅰ、Ⅱ,为探究 对该反应速率的影响。
②a= ℃
③V= mL,加入V mL水的目的是 。④对比上述实验数据,推测反应速率最快的是 (填实验编号)。
【答案】(1) ;溶液变浑浊快慢
(2) 溶液
(3) (合理即可给分)
(4) 溶液的浓度;30;8;控制硫酸的起始浓度相同;实验Ⅲ
【解析】(1)原理i 预期的实验现象为产生气泡快慢,结合所给的试剂,选择的反应为
。原理ii 选择的反应为 ,生
成淡黄色沉淀硫单质,故预期的实验现象为溶液变浑浊快慢。
(2) 对反应 具有催化作用,
故选择原理i,探究催化剂对该反应速率的因素,必选试剂除 溶液外,还应选 溶液,
作催化剂。
(3)若要探究硫酸浓度对反应ii速率的影响,两组实验中硫酸的浓度应不同, 溶液的浓度相同,
所加硫酸的体积应相同,故试剂X及其用量为 。
(4)①对比实验Ⅰ、Ⅱ,所加 溶液的体积不同,即 的物质的量不同,所加 溶
液的体积、浓度均相同,则实验Ⅰ、Ⅱ为探究 溶液的浓度对该反应速率的影响。
②实验Ⅰ、Ⅱ为探究 溶液的浓度对该反应速率的影响,则温度应相同,故a=30℃
③实验Ⅰ、Ⅱ所加 溶液的体积、浓度均相同,为保证溶液混合后硫酸的浓度相同,则要加入蒸馏水
控制硫酸的起始浓度相同,由实验可知,溶液混合后总体积为10mL,则V=8mL。
④实验Ⅲ中温度最高, 浓度最大,故推测反应速率最快的是实验Ⅲ。
19.(17分)(2022高二上·河南期中)下列物质中:①CHCOOH②NH ③NH Cl④盐酸
3 3 4⑤NaOH⑥NaHCO 溶液。
3
(1)(2分)属于弱电解质的是 (填序号,下同),属于强电解质且其水溶液呈碱性的是
。
(2)(6分)在氨水中存在电离平衡:NH •H O NH +OH-。将上述六种物质分别配成0.1mol/L的溶液,
3 2
向稀氨水中分别滴加少量六种溶液,能使氨水的电离平衡逆向移动且c(NH )增大的是 (填序号),
此时c(OH-) (填“增大”“减小”或“不变”,下同), = 。
(3)(5分)等体积c(H+)相同的盐酸和醋酸分别与0.1mol•L-1的NaOH溶液恰好完全反应,消耗NaOH体
积较大的是 (填化学式),反应过程中醋酸的电离程度 (填“增大”“减小”或“不
变”,下同),n(CHCOO-) ,水的电离程度逐渐 ,水电离的c(H+)= 。
3
(4)(2分)已知次氯酸(HClO)的电离平衡常数为K=4.0×10-8,向20mL0.1mol•L-1的HClO溶液中滴加少
a
量硫酸,再加水稀释至40mL,此时测得c(H+)=0.05mol•L-1,则溶液中c(ClO-)= mol•L-1。
(5)(2分)已知亚硫酸(H SO )的电离平衡常数为K =1.6×10-2,K =1.0×10-7;碳酸(H CO)的电离平衡常
2 3 a1 a2 2 3
数为K =4.0×10-7,K =4.0×10-11。足量的HSO 溶液和NaHCO 溶液发生反应的主要离子方程式为
a1 a2 2 3 3
。
【答案】(1)①;⑤
(2)③;减小;增大
(3)CHCOOH;增大;增大;增大;增大
3
(4)4.0×10-8
(5)HSO +HCO =HSO +H O+CO↑
2 3 2 2
【解析】(1)①CHCOOH为弱酸,属于弱电解质;⑤NaOH属于强碱,水溶液显碱性;
3
(2)①CHCOOH加入稀氨水中,会消耗氢氧根离子,使平衡向正向移动,不正确;
3
②NH 溶于水显碱性,所以加入稀氨水中,会抑制一水合氨的电离,但不能使c(NH )增大,不正确;
3
③NH Cl加入稀氨水中,增大铵根离子浓度,使平衡逆向移动,且c(NH )增大,正确;此时氢氧根离子浓
4度减小,因为 = ,所以 会增大;
④盐酸会消耗氢氧根离子,使平衡向正向移动,不正确;
⑤NaOH溶于水显碱性,所以加入稀氨水中,会抑制一水合氨的电离,但不能使c(NH )增大,不正确;
⑥NaHCO 溶液溶于水显碱性,所以加入稀氨水中,会抑制一水合氨的电离,但不能使c(NH )增大,不正
3
确;
综上所述,答案为③;减小;增大;
(3)醋酸为一元弱酸,HCl为一元强酸,则等体积c(H+)相同的盐酸和醋酸,醋酸的浓度较大,分别与
0.1mol•L-1的NaOH溶液恰好完全反应,消耗NaOH体积较大的是CHCOOH;反应过程中氢氧化钠不断消
3
耗醋酸电离的氢离子,促进醋酸的电离,即醋酸的电离程度增大,电离生成的醋酸根离子的物质的量增大,
即n(CHCOO-)增大,醋酸对水的抑制作用逐渐减弱,即水的电离程度逐渐增大,水电离的c(H+)增大,故
3
答案为:CHCOOH;增大;增大;增大;增大;
3
(4)次氯酸(HClO)的电离平衡常数为K= =4.0×10-8,向20mL0.1mol•L-1的HClO溶液中
a
滴加少量硫酸,再加水稀释至40mL,则c(HClO)=0.05mol/L,此时测得c(H+)=0.05mol•L-1,依据电离平衡
常数公式可知, =4.0×10-8mol/L;
(5)根据电离平衡常数可知,1.6×10-2>4.0×10-7,HSO 的酸性大于HCO 的酸性,足量的HSO 溶液和
2 3 2 3 2 3
NaHCO 溶液发生反应的主要离子方程式为HSO +HCO =HSO +H O+CO↑。
3 2 3 2 2
20.(15分)(2022高二上·河南期中)高锰酸钾(KMnO)和双氧水(H O)都是常见的消毒试剂,在日常生
4 2 2
活和工业生产中都有广泛的应用。回答下面问题:
(1)(2分)酸性高锰酸钾与双氧水混合有气体产生,经检验产生的气体为氧气。写出反应的离子方程式
。
(2)(3分)HO 是一种二元弱酸,与NaOH反应的化学方程式为NaOH+H O=NaHO +H O,写出HO
2 2 2 2 2 2 2
电离的方程式 (只写第一步)。在酸性条件下HO 的分解速度变大,利用平衡移动
2 2
的原理进行解释: 。
(3)(6分)现有HO-Al燃料电池电解尿素[CO(NH)]制备氢气的装置,b、c、d为石墨电极,电解池
2 2 2 2
中的隔膜只阻止气体通过,如图:①a电极是Al,写出电极反应 ,反应后b电极区溶液的pH (填
“增大”“减小”或“不变”)。
②c电极是 (填“正极”“负极”“阴极”或“阳极”),d电极的电极反应为
。
(4)(4分)某化学兴趣小组为了探究KMnO 与HO 氧化性强弱,设计了如图实验装置:
4 2 2
①当闭合电键K时,电流表指针向左偏转,甲烧杯中溶液颜色逐渐变浅,则石墨电极a上发生反应
(填“氧化”或“还原”),石墨电极b上发生的电极反应为 。
②反应一段时间后,向甲烧杯中滴加KOH溶液,同时向乙烧杯中滴加硫酸溶液,发现电流表指针逐渐翻
转,最后向右偏转,说明KMnO 与HO 氧化性与 有关。
4 2 2
【答案】(1)2MnO +5H O+6H+=2Mn2++5O ↑+8H O
2 2 2 2
(2)HO HO +H+;酸性条件增大了H+浓度,使HO 的电离平衡逆向移动,增大了HO 的浓度,分
2 2 2 2 2 2
解反应速率增大
(3)Al+4OH--3e-=AlO +2H O;增大;阳极;2HO+2e-=H ↑+2OH-
2 2 2
(4)还原;HO -2e-+OH-=O ↑+H O;溶液的酸碱性和浓度
2 2
【解析】(1)酸性高锰酸钾与双氧水混合会发生氧化还原反应,过氧化氢被氧化为氧气,高锰酸钾降低
为锰离子,反应的离子方程式为:2MnO +5H O+6H+=2Mn2++5O ↑+8H O;
2 2 2 2(2)HO 是一种二元弱酸,其第一步电离方程式为:HO HO +H+;酸性条件增大了H+浓度,使
2 2 2 2
HO 的电离平衡逆向移动,增大了HO 的浓度,分解反应速率增大;
2 2 2 2
(3)①HO-Al燃料电池中,Al作负极,在碱性条件下发生失电子的氧化反应转化为偏铝酸根离子,其
2 2
电极反应式:Al+4OH--3e-=AlO +2H O; b电极区HO 发生得电子的还原反应生成OH-,其电极反应式为:
2
,则反应后溶液的pH会增大,故答案为:Al+4OH--3e-=AlO +2H O;增大;
2
②c电极连接的是b电极,为电解池的阳极,d电极为电解池的阴极,水发生得电子的还原反应转化为氢气,
其电极反应式为:2HO+2e-=H ↑+2OH-,故答案为:阳极;2HO+2e-=H ↑+2OH-;
2 2 2 2
(4)①当闭合电键K时,装置为原电池原理,电流表指针向左偏转,说明甲烧杯为正极,溶液颜色逐渐
变浅,高锰酸根离子被还原,化合价降低为锰离子,则石墨电极a上发生的是还原反应;石墨电极b区,
HO 发生氧化反应转化为氧气,b电极上发生的电极反应为:HO -2e-+OH-=O ↑+H O;
2 2
②反应一段时间后,向甲烧杯中滴加KOH溶液,同时向乙烧杯中滴加硫酸溶液,发现电流表指针逐渐翻
转,最后向右偏转,说明高锰酸钾在碱性条件下不能氧化HO ,电子转移方向相反也说明KMnO 与HO
4 2 2
氧化性与溶液的酸碱性和浓度有关。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育