文档内容
选择性必修一综合测试(提升)
满分100分,考试用时75分钟
一、
选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每
小题给出的四个选项中,只有一项是符合题目要求的
1.(2022青海)下列方程式中,属于水解反应的是( )
A. B.
C. D.
2.(2022浙江)下列说法或表示方法中正确的是( )
A.由C(金刚石)=C(石墨) ΔH=-1.9kJ·mol-1可知,金刚石比石墨稳定
B.相同条件下,1molCH (g)的熵大于1molH (g)
4 2
C.在101KPa时,2gH 完全燃烧生成液态水,放出285.8kJ热量,则表示氢气燃烧热的热化学方程式为:
2
2H(g)+O(g)=2HO(1) ΔH=-571.6kJ·mol-1
2 2 2
D.CH(g)+HO(g) CO(g)+3H(g) ΔH>0,低温有利于该反应的自发进行
4 2 2
3.(2022南阳)利用二氧化碳催化加氢合成CHOH是一种实现“双碳”目标的有效方法。
3
已知:①CO(g)+3H(g) CHOH(g)+H O(g) △H =-49.0kJ•mol-1
2 2 3 2 1
②CO (g)+H(g) CO(g)+HO(g) △H =+41.0kJ•mol-1
2 2 2 2
则CO(g)+2H(g) CHOH(g)的△H为( )
2 3
A.+90.0kJ•mol-1 B.+8.0kJ•mol-1
C.-8.0kJ•mol-1 D.-90.0kJ•mol-1
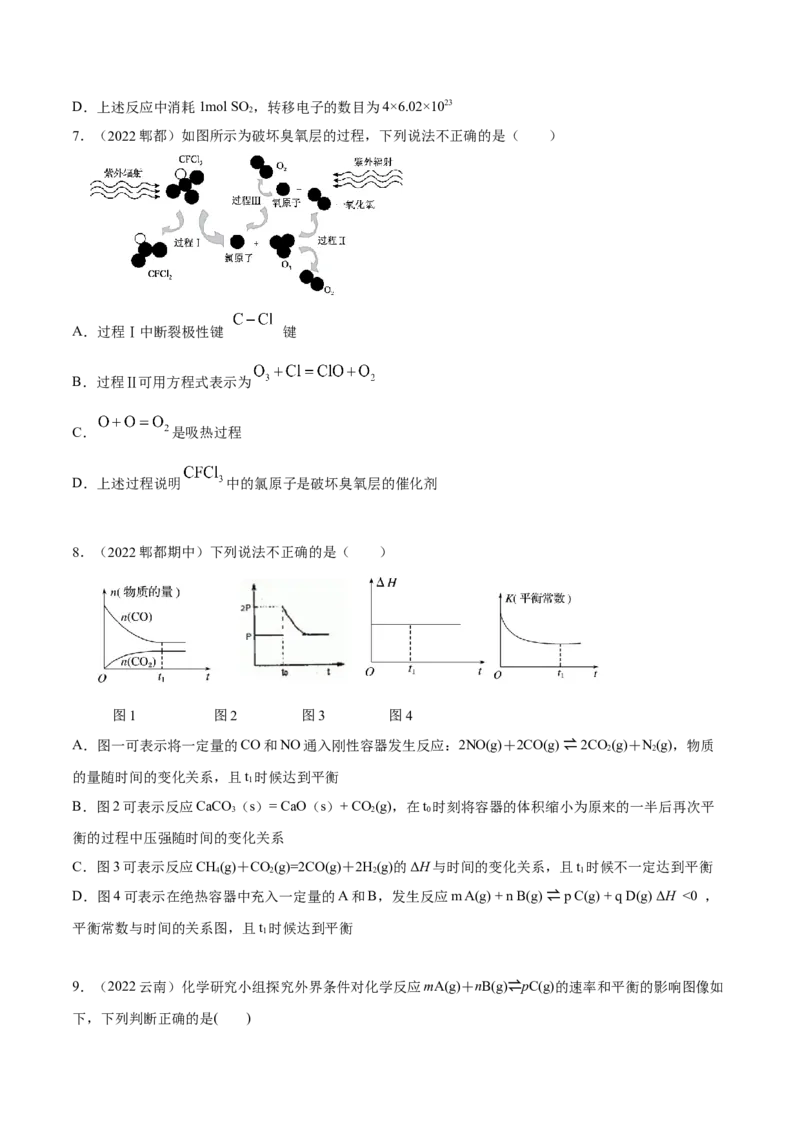
4.(2022南阳)利用如图所示装置,可以模拟铁的电化学腐蚀,下列说法错误的是( )A.若X为碳棒,为减慢铁的腐蚀,开关K应置于N处
B.若X为锌棒,K置于M或N处,均能减慢铁的腐蚀
C.若X为碳棒,将开关K置于M处时铁棒上发生的反应为Fe-2e-=Fe2+
D.若X为锌棒,将开关K置于N处时铁棒上发生的反应为Fe-2e-=Fe2+
5.(2022广东)一定温度下,将浓度为0.1mol/LHF溶液加水不断稀释,始终保持增大的是( )
A. B.
C. D.
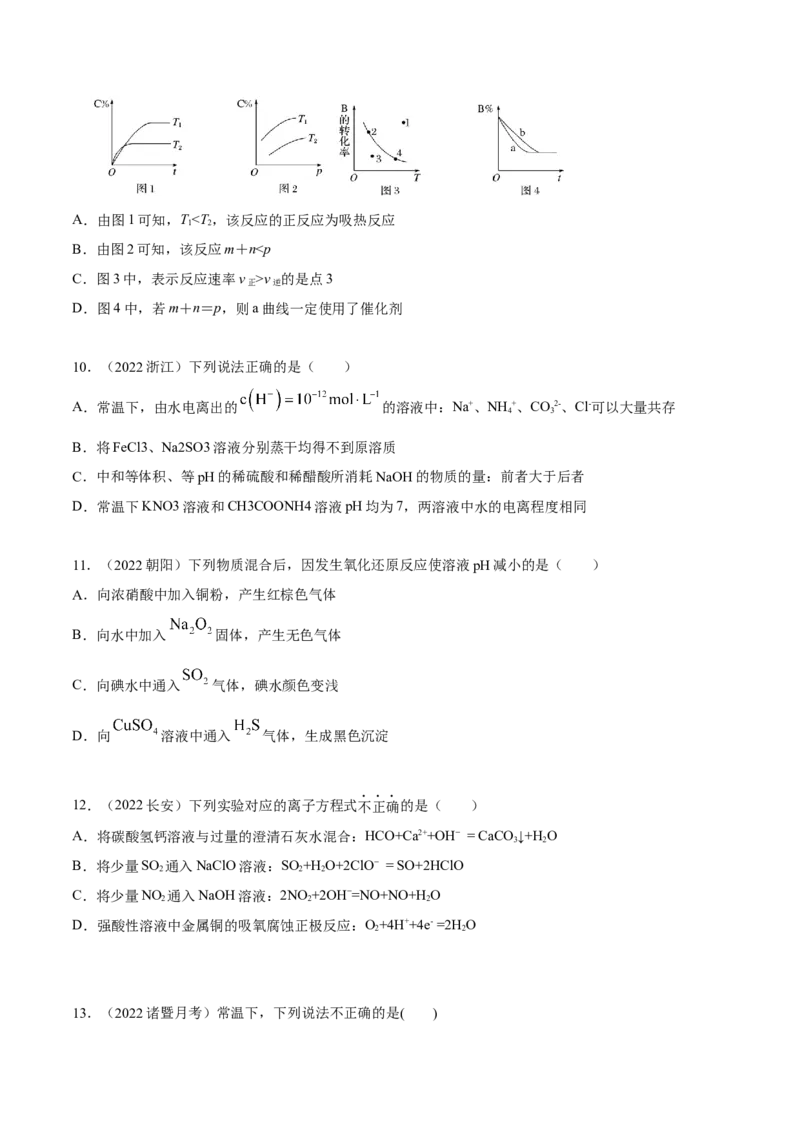
6.(2022苏州期中)反应2SO (g)+O(g) 2SO (g)的能量变化如图所示,下列说法正确的是( )
2 2 3
A.该反应的△H<0,ΔS>0,
B.用VO 催化时,反应①的速率大于反应②
2 5
C.温度升高,上述反应化学平衡常数增大D.上述反应中消耗1mol SO ,转移电子的数目为4×6.02×1023
2
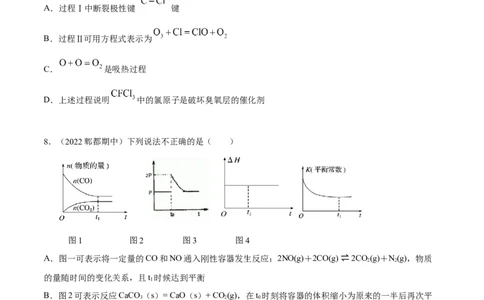
7.(2022郫都)如图所示为破坏臭氧层的过程,下列说法不正确的是( )
A.过程Ⅰ中断裂极性键 键
B.过程Ⅱ可用方程式表示为
C. 是吸热过程
D.上述过程说明 中的氯原子是破坏臭氧层的催化剂
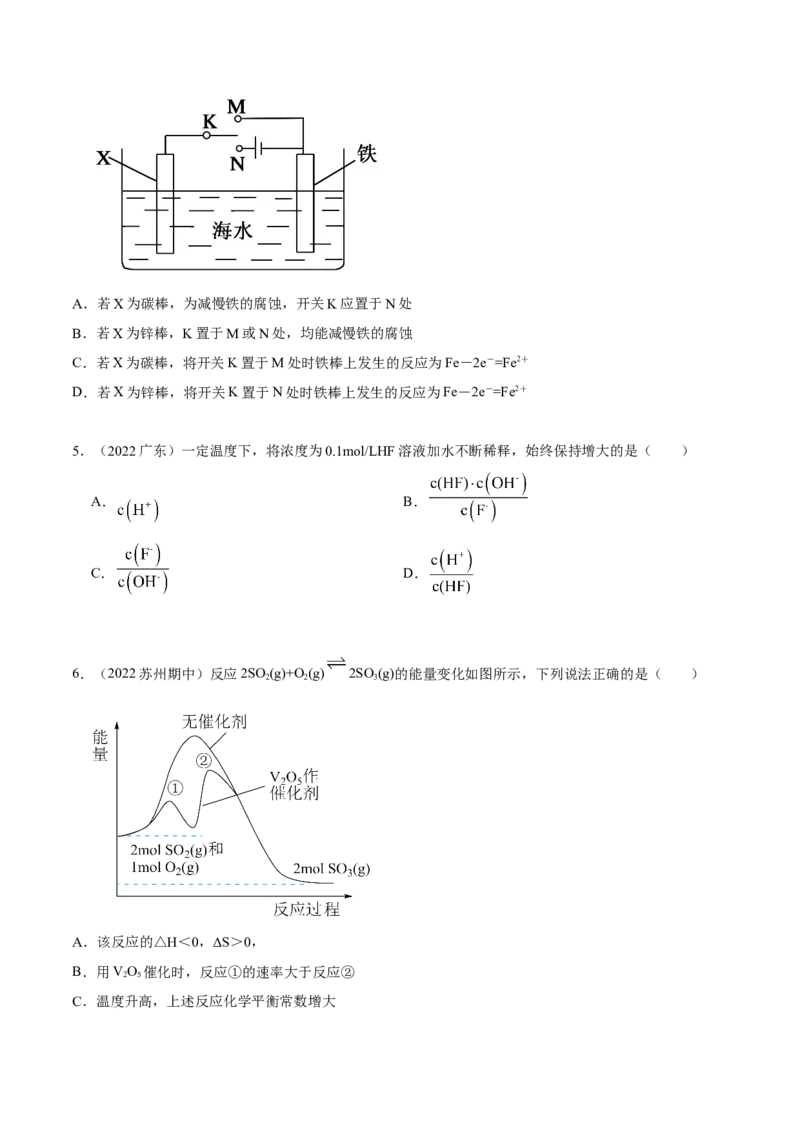
8.(2022郫都期中)下列说法不正确的是( )
图1 图2 图3 图4
A.图一可表示将一定量的CO和NO通入刚性容器发生反应:2NO(g)+2CO(g) ⇌ 2CO (g)+N(g),物质
2 2
的量随时间的变化关系,且t 时候达到平衡
1
B.图2可表示反应CaCO (s)= CaO(s)+ CO(g),在t 时刻将容器的体积缩小为原来的一半后再次平
3 2 0
衡的过程中压强随时间的变化关系
C.图3可表示反应CH(g)+CO(g)=2CO(g)+2H(g)的ΔH与时间的变化关系,且t 时候不一定达到平衡
4 2 2 1
D.图4可表示在绝热容器中充入一定量的A和B,发生反应m A(g) + n B(g) ⇌ p C(g) + q D(g) ΔH <0 ,
平衡常数与时间的关系图,且t 时候达到平衡
1
9.(2022云南)化学研究小组探究外界条件对化学反应mA(g)+nB(g)⇌pC(g)的速率和平衡的影响图像如
下,下列判断正确的是( )A.由图1可知,Tv 的是点3
正 逆
D.图4中,若m+n=p,则a曲线一定使用了催化剂
10.(2022浙江)下列说法正确的是( )
A.常温下,由水电离出的 的溶液中:Na+、NH +、CO2-、Cl-可以大量共存
4 3
B.将FeCl3、Na2SO3溶液分别蒸干均得不到原溶质
C.中和等体积、等pH的稀硫酸和稀醋酸所消耗NaOH的物质的量:前者大于后者
D.常温下KNO3溶液和CH3COONH4溶液pH均为7,两溶液中水的电离程度相同
11.(2022朝阳)下列物质混合后,因发生氧化还原反应使溶液pH减小的是( )
A.向浓硝酸中加入铜粉,产生红棕色气体
B.向水中加入 固体,产生无色气体
C.向碘水中通入 气体,碘水颜色变浅
D.向 溶液中通入 气体,生成黑色沉淀
12.(2022长安)下列实验对应的离子方程式不正确的是( )
A.将碳酸氢钙溶液与过量的澄清石灰水混合:HCO+Ca2++OH− = CaCO↓+H O
3 2
B.将少量SO 通入NaClO溶液:SO +H O+2ClO− = SO+2HClO
2 2 2
C.将少量NO 通入NaOH溶液:2NO +2OH−=NO+NO+H O
2 2 2
D.强酸性溶液中金属铜的吸氧腐蚀正极反应:O+4H++4e- =2H O
2 2
13.(2022诸暨月考)常温下,下列说法不正确的是( )A.已知盐溶液NaX的pH=8,则当升高温度时,溶液的pH可能减小
B.等体积pH=2的HX和HY两种酸分别与足量铁反应生成氢气,若HX放出的氢气多且反应速率快,则
酸性HXNaY, 则酸性:HXc
C.图③可知M点该反应处于平衡状态
D.图④曲线S表示不同压强下达到平衡时A的百分含量,则F点时v(逆)>v(正)
二、非选择题:共56分。
17.(14分)(2022江苏)NOx是形成雾霾天气的主要原因之一,全球空气污染日趋严重,消除氮氧化
物污染对建设宜居环境有重要意义。氮氧化物的处理常用 催化还原,反应原理为:
ΔH
已知:
(1)(3分)用 消除NO污染的反应ΔH= ,则该反应自发进行的条件是
(填“高温”、“低温”或“任何温度”)。
(2)(2分)下列措施可增大NO转化率的是____(填标号)。
A.升高温度 B.将水蒸气从体系中分离出去
C.保持体系压强不变充入He D.增大氨气的浓度
(3)(2分)该反应 时到达平衡。在 时刻保持恒容继续充入一定量NO, 时刻重新到达平衡,请在
图中作出逆反应速率在 ~ 变化的曲线 。
(4)(3分)一定温度下,在2L恒容密闭容器中充入1.2mol NO和0.9mol ,10min时反应达到平衡,此时NO的转化率为50%,体系压强为p MPa,该反应的平衡常 Mpa(用含p的代数式表示,
分压 ,p为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
(5)(4分)不同温度条件下, 与NO的物质的量之比分别为4:1、3:1、1:3,反应经2秒得到
NO脱除率曲线如图所示。曲线a中 的起始浓度为 ,B点NO的脱除速率为
mol/(L·s),在AB所在的曲线上当温度高于900℃时NO脱除率明显降低的原因是
。
18.(15分)(2022高二下·雅安期末)
(1)(4分)I.根据表中数据(常温下),完成下列填空。
物质 CHCOOH NH ∙H O HCN HClO HCO HSO
3 3 2 2 3 2 3
K =4.3×10−7 K =1.5×10−2
电离常数 a1 a1
1.7×10−5 1.7×10−5 4.9×10−10 3×10−8
(K a ) K =5.6×10−11 K =1.0×10−7
a2 a2
常温下,NaCN溶液呈 (填“酸”、“碱”或“中”)性,其原因是 (用
离子方程式表示)。
(2)(2分)常温下,浓度均为0.1 mol∙L−1的下列4种溶液:①CHCOONa溶液,②NaCN溶液,
3
③NaHCO 溶液,④NaClO溶液;这4种溶液pH由大到小的顺序是 (填序号)。
3
(3)(2分)常温下,向NaClO溶液中通入少量CO,发生反应的离子方程式为
2
。(4)(1分)常温下,NaSO 溶液中c(OH-)−c(H+)=c(HSO )+ 。
2 3
(5)(4分)II.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg∙L−1。处理含
镉废水可采用化学沉淀法。K (CdCO)=4.0×10−12,K (CdS)=8.0×10−27;回答下列问题:
sp 3 sp
向某含镉废水中加入NaS,当S2−浓度达到8.0×10−8 mol∙L−1时,废水中Cd2+的浓度为
2
mol∙L−1,此时是否符合生活饮用水卫生标准? (填“是”或“否”)。
(6)(2分)室温下,反应CdCO(s)+S2−(aq) CdS(s)+CO (aq)达到平衡,该反应的平衡常数K=
3
(结果保留两位有效数字)
19.(16分)(2022上海)研究氮氧化物的性质具有重要的意义。
(1)(3分) NO可以催化SO 与O 的反应:
2 2
反应Ⅰ.2NO(g)+O(g) 2NO (g) △H =-114.1 kJ/mol
2 2 1
反应Ⅱ.SO (g)+NO (g) SO (g)+NO(g) △H2=-41.6 kJ/mol
2 2 3
①下列说法正确的是: 。
A.高温下有利于反应Ⅰ的自发进行
B.反应Ⅱ的△S对该反应的自发性影响不大
C.恒温恒容下加入一定量SO 和O,若容器内压强没有明显变化,说明不加催化剂时,SO 和O 的反应
2 2 2 2
不能自发进行
D.NO催化下,一定量SO 和O 反应一段时间后,升高温度,SO 的体积分数可能变大
2 2 3
②据报道,瑞典某工厂利用上述反应制取硫酸。在合成SO 时,向反应容器中适时通入冷激气(冷的原料
3
气),其作用是
(2)(6分)密闭容器中加入一定量NO (g)和SO (g),发生反应Ⅱ(忽略其它反应)。保持常压条件,经过
2 2
相同时间,测得SO 的体积分数随温度的变化如图所示:
2
①由图可知,在M点之前,反应中SO 的体积分数随温度升高而减小,其原因为:
2
②250℃和常压下,等物质的量的SO 和NO 反应后,测得平衡时NO的物质的量分数为40%,则该反应的
2 2
物质的量分数平衡常数Kx= 。(Kx是用平衡时物质的量分数代替平衡浓度计算)
保持上述条件不变,提高原料中NO 的比例,使平衡时SO 的产率为90%。则NO 和SO 的投料比(即起始
2 3 2 2
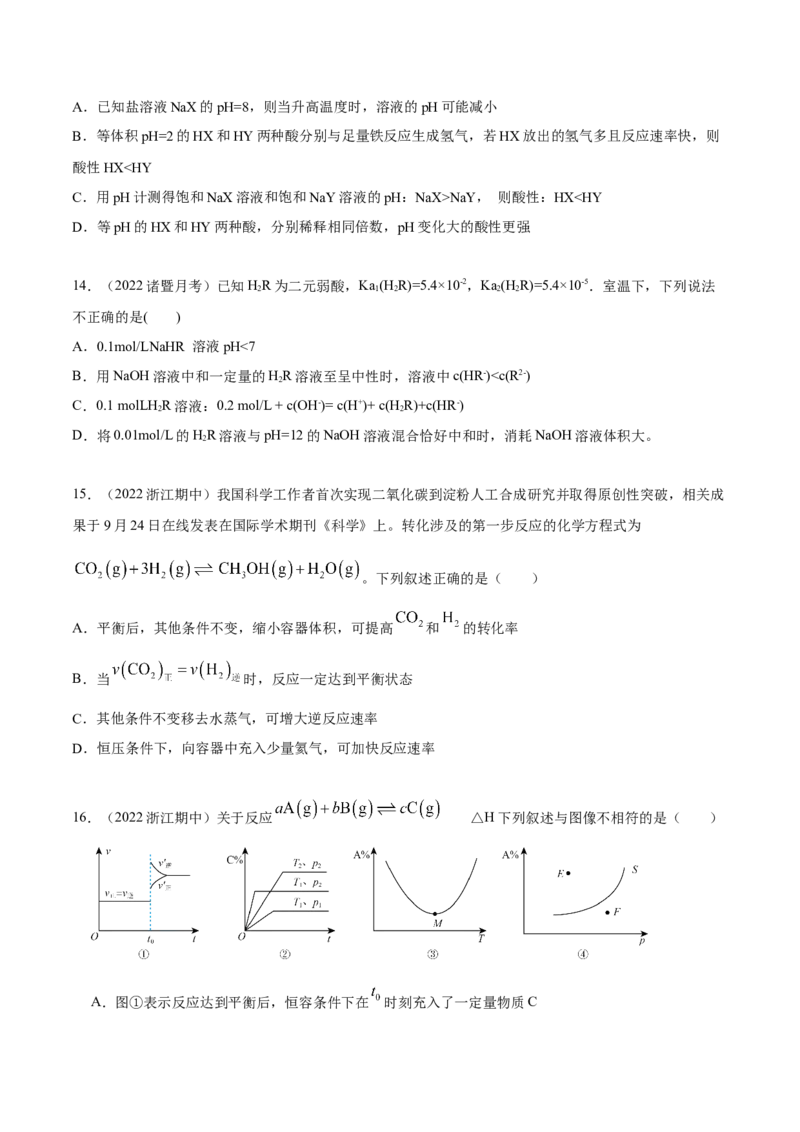
时加入的物质的量之比)为 。(3)(3分)在一定温度下,一定量NO分解成氮气和氧气,同时释放出热量。分解的旁艇均调整据如下
2
表。反应一段时间后,只改变如下一个条件。下列说法正确的是 :
反应时间/ min 0 10 20 30 40 50 60 70 80 90 100
c(NO)/mol·L-1 0.100 0.090 0.080 0.070 0.060 0.050 0.040 0.030 0.020 0.010 0.000
2
A.增大压强,NO分解速率增大
2
B.增大容器的体积,该分解反应平衡右移,c(NO)变小
2
C.减小NO的浓度,该分解反应速率减小
2
D.升高温度,容器内气体的压强一定变大
(4)(4分)以固体催化剂催化CO还原NO生成N 和CO 气体,反应历程如下(*表示吸附态),请补充完
2 2
整。
化学吸附: NO(g) NO*;
表面反应: 2NO* ON-NO*; ;
ON- NO- CO* ON-N* +CO *; 。
2
脱附: N* N(g); CO* CO(g)
2 2 2 2
20.(11分)(2022临汾)进入秋冬季后,有些地区不时会遇到雾霾天气,影响人们的出行。氮氧化物
(NO )是雾霾的主要成分之一,消除氮氧化物有多种方法。回答下列问题:
x
(1)(5分)净化汽车尾气可减少空气中的NO ,净化时的主要原理为
x
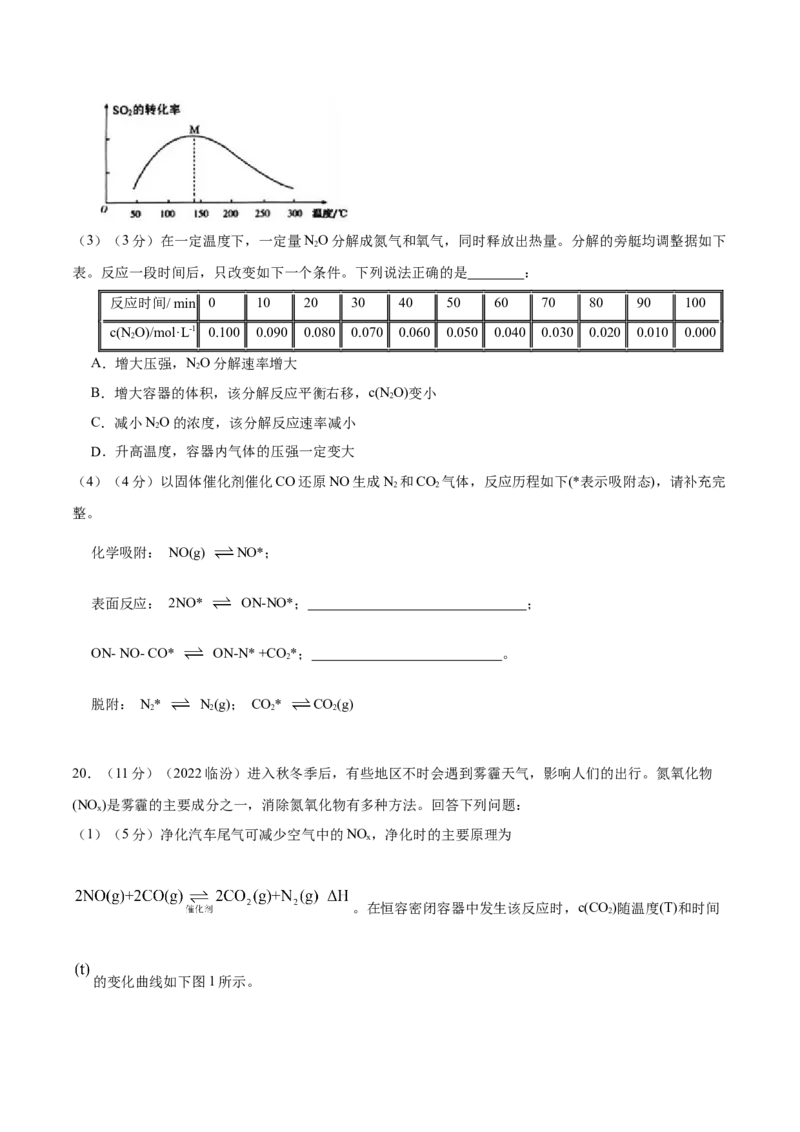
。在恒容密闭容器中发生该反应时,c(CO)随温度(T)和时间
2
的变化曲线如下图1所示。①该反应的△H 0(选填“>”或“<”)。
②在T 温度下,0~2s内的化学反应速率v(N )= 。
2 2
③能判断该反应达到平衡状态的标志是 (填标号)。
A.在单位时间内生成1molCO 的同时消耗了1molCO
2
B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
D.混合气体的压强不再改变
(2)(2分)利用某分子筛作催化剂,NH 可脱除废气中的NO和NO ,生成两种无毒物质,其反应历程
3 2
如下图2所示,则该历程总反应的化学方程式为 。
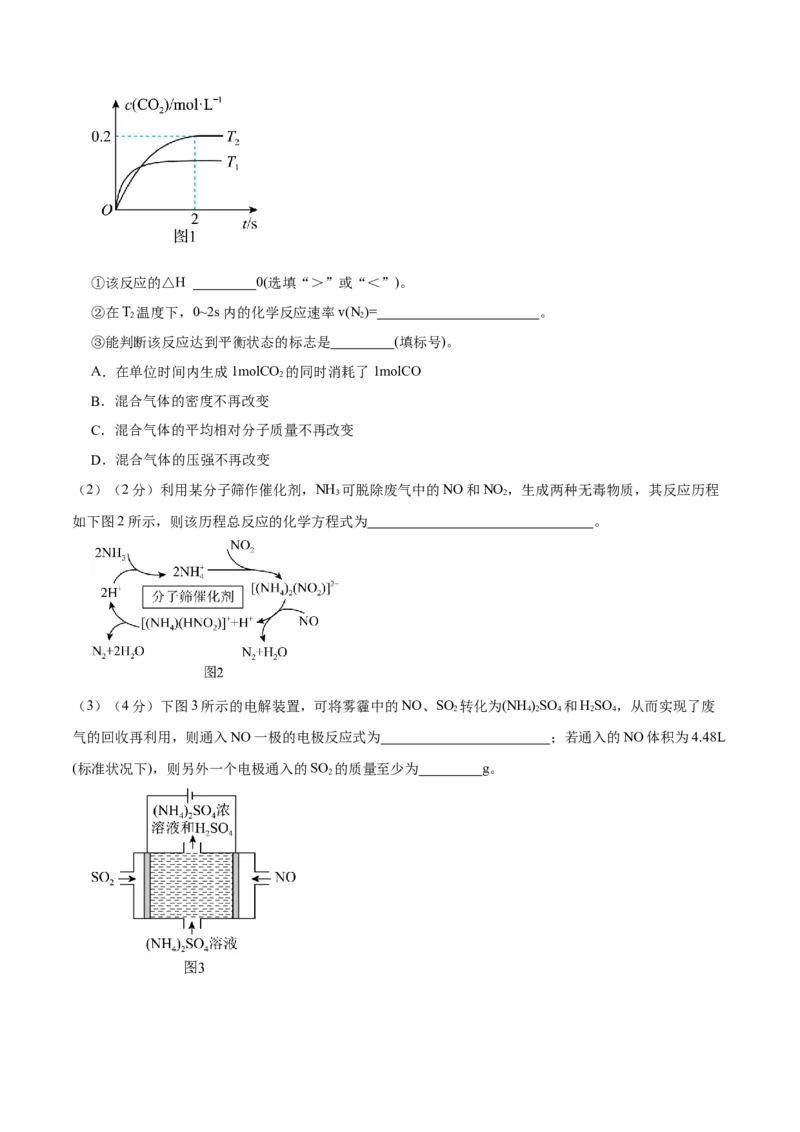
(3)(4分)下图3所示的电解装置,可将雾霾中的NO、SO 转化为(NH )SO 和HSO ,从而实现了废
2 4 2 4 2 4
气的回收再利用,则通入NO一极的电极反应式为 ;若通入的NO体积为4.48L
(标准状况下),则另外一个电极通入的SO 的质量至少为 g。
2倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育