文档内容
期末试卷 02
(能力培优)
一、单项选择题(每小题3分,共16小题,共计48分。)
1.(2021·山东·肥城市教学研究中心高二期中)根据下图所示情况,判断下列说法中正确的是
A.其热化学方程式为CO(g)+HO(g)=CO(g)+H(g) ΔH=41kJ·mol-1
2 2 2
B.该反应为吸热反应
C.1 mol CO具有的能量比1 mol CO 具有的能量高
2
D.当HO为液态时,其反应热大于41 kJ·mol-1
2
【答案】B
【解析】A.将图象中反应的反应物与生成物弄反了,故A错误;B.根据图象,生成物的能量比反应物
的能量高,该反应为吸热反应,故B正确;C.生成物的总能量比反应物的总能量高,但不能判断1 mol
CO与1 mol CO 具有的能量的高低,故C错误;D.水由气态变为液态过程中放热,所以当HO为液态时,
2 2
该反应吸热减少,其反应热的值小于41kJ•mol-1,故D错误;故选B。
2.(2021·山东兰陵·高二期中)在一定温度下的恒容容器中,加入少量A发生反应 == 。
当下列物理量不再发生变化,可以判断达到化学平衡的是
①B的体积分数;②混合气体的压强;③混合气体的总质量;④混合气体的平均相对分子质量;⑤混合气
体的密度
A.仅②③ B.仅②③⑤ C.仅①④⑤ D.①②③④⑤
【答案】B
【解析】①在该反应中只有生成物是气体,每反应产生1 mol B气体,就产生2 mol C气体,所以反应体系
1
原创精品资源学科网独家享有版权,侵权必究!中B的体积分数始终保持不变,因此不能根据B的体积分数判断反应是否达到平衡状态,①不符合题意;
②该反应在恒温、恒容密闭容器中,反应物是固体,若反应未达到平衡状态,则气体的物质的量增加,体
系的压强增大;若反应逆向进行,则气体的物质的量减小,体系的压强减小,因此当进行混合气体的压强
不变时,气体的物质的量不变,反应达到了平衡状态,②符合题意;
③反应混合物不都是气体,若反应正向进行,则混合气体质量增加;若反应逆向进行,则混合气体的质量
会减小,若混合气体的总质量不变,则反应达到了平衡状态,③符合题意;
④反应体系中只有生成物B、C是气体,二者的物质的量的比始终是1:2,因此混合气体的平均相对分子质
量始终保持不变,故不能据此判断反应是否达到平衡状态,④不符合题意;
⑤反应混合物中不都是气体,若反应正向进行,气体的质量增加,气体的密度也会增大;若反应逆向进行,
气体的质量会减小,气体的密度也会减小,因此当混合气体的密度不变时,气体的总质量不变,反应达到
了平衡状态,⑤符合题意;
综上所述可知:可以判断反应达到平衡状态的序号是②③⑤,合理选项是B;选B。
3.(2021·四川·岳池县教研室高二期中)某温度下,将等物质的量的气体A、B混合于1L的密闭容器中,
发生如下反应:A(g)+3B(g) 2C(g)+xD(g)。经2min后测得C的浓度为0.5mol/L,B的物质的量分数为
25%,以D表示2min内的平⇌均反应速率v(D)=0.25mol/L·min),下列说法正确的是
A.2min时,v(A)=0.125mol/L·min
B.2min时,B的物质的量为0.75mol
C.x=1
D.反应前后容器内气体的压强之比为1:2
【答案】B
【解析】2min内的平均速率v(D) = 0.25 mol/(L·min),则c(D) = 0.25 ×2= 0.5 mol/L,根据“三段式”可得:
A(g) + 3B(g) 2C(g) + xD(g)
⇌
,反应后B的物质的量分数=
= 25%,则a= 1.5 mol/L;
A.同一时间段内反应速率之比等于化学计量数之比,此2 min内的平均速率v(A) = 0.125 mo/(L·min),随
着反应进行,浓度逐渐减小,化学反应速率减小,2 min时,v(A)<0.125 mol/(L·min),A错误;B.2 min
2
原创精品资源学科网独家享有版权,侵权必究!后容器内B的物质的量浓度为1.5-0.75=0.75 mol/L,容器体积为1L, B的物质的量为0.75 mol, B正确;
C.同一时间内变化的浓度与化学计量数成正比,则x=2,C错误;D.x=2,则该反应是一个反应前后前
后气体的分子数不变的反应,所有反应前后压强之比为1: 1, D错误; 故选:B。
4.(2021·山东兰陵·高二期中)已知25℃时有关弱酸的电离平衡常数如下:
弱酸化学式
电离平衡常数
则下列有关说法正确的是
A.pH相同的三种溶液,物质的量浓度的关系为c(CHCOOH)>c(H CO)>c(HCN)
3 2 3
B.1 mol/L的醋酸溶液加水稀释,其中醋酸的电离程度先增大后减小
C.NaCN溶液中通入少量CO 发生的化学反应为 ==
2
D.稀释HCN溶液过程中, 减小
【答案】C
【解析】A.酸的电离平衡常数越小,表示该酸越弱,当酸的浓度相等时,其电离产生的H+的浓度就越小,
因此当溶液pH相等时,即c(H+)相等时,电离平衡常数小的酸的浓度就越大。由于电离平衡常数:
K(CHCOOH)>K (H CO)>K(HCN),所以溶液的物质的量浓度c(HCN)>c(H CO)>c(CHCOOH),A错
a 3 a1 2 3 a 2 3 3
误;B.在醋酸溶液在溶液中存在电离平衡:CHCOOH==CH COO-+H+,向溶液中加水稀释时,醋酸的电
3 3
离平衡正向移动,导致更多的醋酸分子发生电离,因此醋酸的电离程度始终是增大,B错误;C.根据电
离平衡常数可知K (H CO)>K(HCN)>K (H CO),根据复分解反应规律:强酸与弱酸盐反应制取弱酸,
a1 2 3 a a2 2 3
所以NaCN溶液中通入少量CO 发生的化学反应为 == ,C正确;D.稀
2
释HCN溶液过程中,HCN的电离平衡正向移动,c(HCN)减小的倍数大于c(CN-)减小的倍数,所以
增大,D错误;故合理选项是C。
5.(2021·湖北天门·高二期中)依据下列实验和现象,得出的结论不正确的是
选项 实验 现象 结论
A 点燃无色气体X,将生成的气体通入澄清石灰水 澄清石灰水先浑浊 X可能为C H
3 6
3
原创精品资源学科网独家享有版权,侵权必究!后澄清
在淀粉和I 的混合溶液中滴加KSCN溶液[已知:
B 2 溶液仍为蓝色 氧化性:(SCN) <I
(SCN) 、SCN-分别与卤素单质、卤素离子性质相似] 2 2
2
将0.1mol/L MgSO 溶液滴入NaOH溶液至不再有沉 先有白色沉淀生成 Cu(OH) 的溶度积比
C 4 2
淀产生,再滴加0.1mol/L CuSO 溶液 后变为浅蓝色沉淀 Mg(OH) 的小
4 2
溶液由无色变为蓝
反应中Cu O既作氧
D 在稀HSO 中加入少量Cu O(s) 色并有红色固体生 2
2 4 2 化剂又作还原剂
成
【答案】B
【解析】A.X可能为C H、甲烷或CO等,燃烧生成的二氧化碳使石灰水变浑浊,A正确;B.溶液仍为
3 6
蓝色,碘可能未完全反应,由操作和现象不能判断(SCN) 、I 的氧化性强弱,B错误;C.由操作和显现可
2 2
知沉淀发生转化,则Cu(OH) 的溶度积比Mg(OH) 的小,C正确;D.酸性溶液中Cu O发生岐化反应生成
2 2 2
Cu铜离子和水,则Cu O既作氧化剂又作还原剂,D正确;答案选B。
2
6.(2021·辽宁·沈阳二中高二期中)常温下,下列溶液中的微粒浓度关系不正确的是
A.常温下,0.1 mol/L NaHB的pH=4,则c(HB-)>c(B2-)>c(H B)
2
B.等物质的量浓度的NaCO 和NaHCO 溶液中:
2 3 3
C.NH HSO 溶液中滴加NaOH溶液至恰好呈中性:
4 4
D.常温下pH相等的①NH Cl、②(NH )SO 、③NH HSO 种溶液中, 由大到小的顺序为:②>①
4 4 2 4 4 4
>③
【答案】D
【解析】A.常温下,0.1 mol/L NaHB的pH=4,c(H+)=10-4 mol/L<0.1 mol/L,说明HB是二元弱酸,在溶
2
液中NaHB电离产生的HB-存在电离平衡和水解平衡,电离产生H+使溶液显酸性;水解产生OH-,使溶液
显碱性。现在0.1 mol/LNaHB溶液pH=4<7,溶液显酸性,说明HB-的电离作用大于其水解作用,所以HB-
电离产生的B2-的浓度大于HB-水解产生的HB的浓度,即浓度:c(B-)>c(H B),但盐电离和水解程度都是
2 2
微弱的,主要以盐电离产生的离子浓存在,所以微粒浓度大小关系为:c(HB-)>c(B-)>c(H B),A正确;
2
B.溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+2c( )+c( ),NaCO 和NaHCO 都是强碱弱酸盐,
2 3 3
水解使溶液显碱性,c(OH-)>c(H+),所以 ,B正确;C.NH HSO 溶液中滴加
4 4
4
原创精品资源学科网独家享有版权,侵权必究!NaOH,NH HSO 中的H+先与OH-反应,都被消耗后,因 水解,溶液显酸性,而此时溶液呈中性,说
4 4
明NH HSO 和NaOH按1:1反应后又多加了一点NaOH,因此c(Na+)>c( ),而 会因水解而消耗,
4 4
因此c( )>c( ),此时溶液中还有大量的 ,远大于水电离产生的OH-的浓度,所以c( )>
c(OH-),因此离子浓度关系为: ,C正确;D.③NH HSO 是强酸的
4 4
酸式盐,电离产生 和H+,起一元强酸是作用,电离产生H+使溶液显酸性,电离产生的H+对 的水
解反应起抑制作用,使其水解程度减弱;①NH Cl、②(NH )SO 是强酸弱碱盐,在溶液中 发生水解反
4 4 2 4
应消耗OH-,使水的电离平衡正向移动,最终达到平衡时溶液中c(H+)>c(OH-),使溶液显酸性,当溶液pH
相等时,c( ):①=②;但盐水解程度是微弱的,水解产生的c(H+)远小于酸电离产生的c(H+),故当溶
液pH相等时,c( ):①=②>③,D错误;故合理选项是D。
7.(2021·江苏·高二月考)下列实验装置,不能完成相应实验的是
A.用甲装置测量稀盐酸和NaOH溶液的反应热
B.用乙装置验证纯水具有微弱的导电性
C.用丙装置制取少量Fe(OH) 沉淀
2
D.用丁装置测定某NaOH溶液的浓度
【答案】B
5
原创精品资源学科网独家享有版权,侵权必究!【解析】A.甲装置是反应热测定装置,可用甲装置测量稀盐酸和NaOH溶液的反应热,A正确;B.纯水
的导电性非常微弱,应将乙装置中的灯泡换为灵敏电流计,才能验证纯水的导电性,B错误;C.丙装置
通电后,阳极 放电生成的Fe2+与溶液中的OH-结合生成Fe(OH) 沉淀,阴极生成的H 为还原性气体,且
2 2
溶液上方的植物油能起到隔绝空气的作用,能够防止Fe(OH) 被氧化,因此可以用丙装置制取少量Fe(OH)
2 2
沉淀,C正确;D.丁装置为酸碱中和滴定的装置,可以用丁装置测定某NaOH溶液的浓度,D正确;故
合理选项是B。
8.(2021·河南开封·高二期中)已知室温时,0.1 mol·L-1 某一元酸HA在水中有0. 2%发生电离,下列叙述
错误的是
A.升高温度,溶液的酸性增强
B.该溶液的c(H+)是2 ×10-4 mol·L-1
C.此一元酸的电离平衡常数约为1×10-7
D.向一元酸HA的溶液中,加水稀释,HA的电离平衡向正反应方向移动,但c(H+)减小
【答案】C
【解析】A.升高温度促进HA电离,溶液中氢离子浓度增大,酸性增强,故A正确;
B.0.1mol/L某一元酸HA在水中有0.2%发生电离,则HA是弱酸,溶液中c(H+)=0.1mol/L×0.2%=2 ×10-
4mol/L,故B正确;C.室温时,电离平衡常数 ,故C错误;
D.越稀越电离,加水稀释,HA的电离平衡向正反应方向移动,n(H+)增大,由于溶液体积增大程度影响
更大,c(H+)减小,故D正确;故选:C。
9.(2021·河南开封·高二期中)下列事实中一定能证明CHCOOH是弱电解质的是
3
①用CHCOOH溶液做导电实验,灯炮很暗
3
②0.1 mol·L-1 CH COOH溶液的pH=2.1
3
③等pH等体积的硫酸、CHCOO- 溶液和足量锌反应,CHCOOH 放出的氢气较多
3 3
④20mL 0. 2 mol·L-1醋酸溶液恰好与20mL 0. 2 mol·L-1NaOH溶液完全反应
⑤pH=1的CHCOOH溶液稀释至1000倍,pH<4
3
A.①②④⑤ B.②③⑤ C.①②③④⑤ D.①②⑤
【答案】B
【解析】①用CHCOOH溶液做导电实验,没有与同浓度的强电解质对比,灯炮很暗不能证明CHCOOH
3 3
是否完全电离,①不符合题意;②0.1 mol·L-1 CH COOH溶液若完全电离则c(H+)=0.1 mol·L-1,pH=2.1则
3
6
原创精品资源学科网独家享有版权,侵权必究!c(H+)=10-2.1 mol·L-1,说明CHCOOH没有完全电离,即证明CHCOOH是弱电解质,②符合题意;③等pH
3 3
等体积的硫酸、CHCOOH溶液和足量锌反应,CHCOOH 放出的氢气较多,说明CHCOOH溶液还能电离
3 3 3
出H+,原来CHCOOH没有完全电离,即证明CHCOOH是弱电解质,③符合题意;④醋酸溶液与NaOH
3 3
溶液反应,反应量与其是否完全电离无关,与其总物质的量有关,20mL 0. 2 mol·L-1醋酸溶液恰好与20mL
0. 2 mol·L-1NaOH溶液完全反应, 不能说明醋酸是否完全电离,即不能证明CHCOOH是弱电解质,④不
3
符合题意;⑤pH=1的CHCOOH溶液稀释至1000倍,pH<4,说明c(H+)没有稀释1000倍,即稀释过程
3
继续电离,说明原CHCOOH溶液没有完全电离,即证明CHCOOH是弱电解质,⑤符合题意;符合题意
3 3
的有②③⑤,故答案选B。
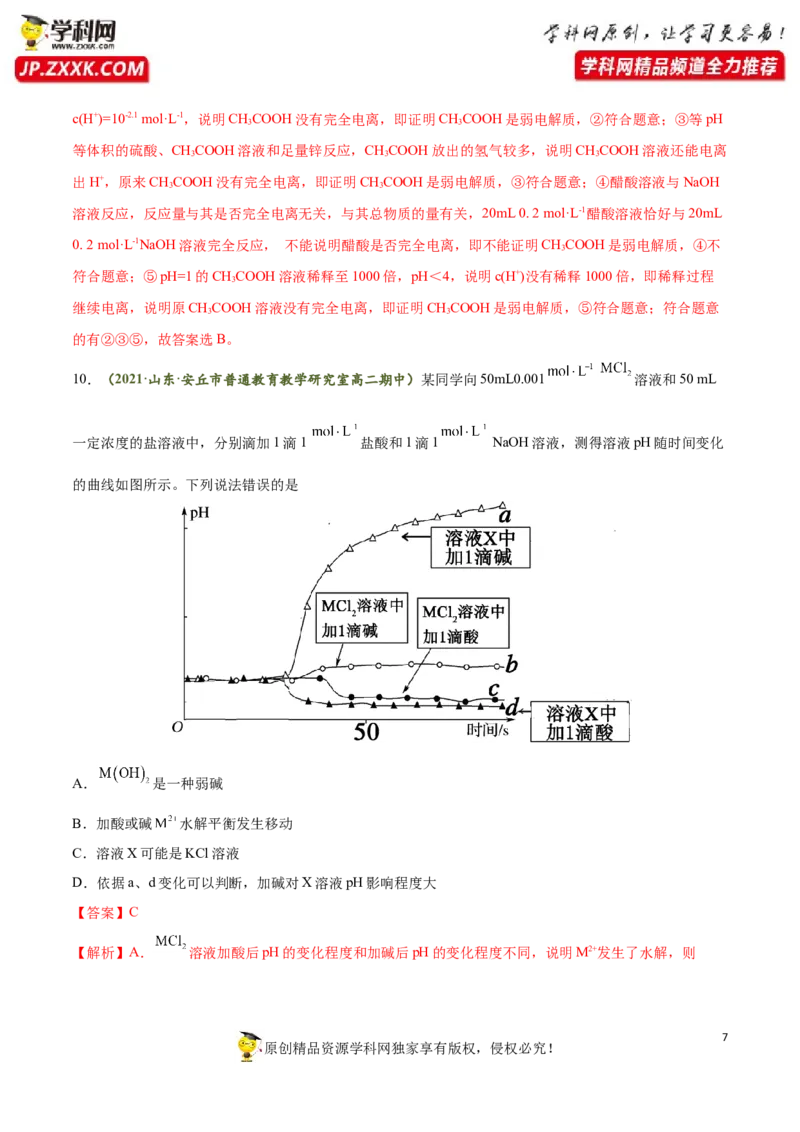
10.(2021·山东·安丘市普通教育教学研究室高二期中)某同学向50mL0.001 溶液和50 mL
一定浓度的盐溶液中,分别滴加1滴1 盐酸和1滴1 NaOH溶液,测得溶液pH随时间变化
的曲线如图所示。下列说法错误的是
A. 是一种弱碱
B.加酸或碱 水解平衡发生移动
C.溶液X可能是KCl溶液
D.依据a、d变化可以判断,加碱对X溶液pH影响程度大
【答案】C
【解析】A. 溶液加酸后pH的变化程度和加碱后pH的变化程度不同,说明M2+发生了水解,则
7
原创精品资源学科网独家享有版权,侵权必究!是一种弱碱,故A正确;B.依据b、c变化可以判断 溶液加酸后pH的变化比加碱后pH的
变化程度大,说明M2+发生了水解,加酸、碱后引起了M2+水解平衡的移动,故B 正确;C.对照组溶液X
加碱后pH的变化程度比加酸后pH的变化程度大,而若对照组溶液X是KCl溶液,则加酸和加碱后溶液的
pH的变化程度应相同,故C错误;D.根据图像,依据a、d变化可以判断,加碱对X溶液pH影响程度大,
故D正确;答案选C。
11.(2021·江苏邗江·高二期中)下图所示的电解装置可实现低电位下高效催化还原CO。下列说法不正
2
确的是
A.a 极连接外接电源的负极
B.b 极的电极反应式为 Cl--2e- + 2OH- = ClO- + H O
2
C.电解过程中 Na+从左池移向右池
D.外电路上每转移1 mol电子,理论可催化还原标准状况下CO 气体 11.2 L
2
【答案】C
【解析】A.根据分析,a极与外电路相连的一极为负极,A正确;B.因右池电解液中含有大量的OH-,
故电极方程式中不能出现H+,正确的电极方程式为Cl--2e-+2OH-=H O+ClO-,B正确; C.根据分析,阴
2
极反应为CO+2e-+H O=CO+2OH-,生成大量阴离子,为平衡电荷,Na+向左边移动,C错误; D.根据B
2 2
选项的电极反应,每转移2mol电子,可还原标况下22.4L的CO,故电路中转移1mol电子,可还原标况
2
下11.2L的CO,D正确;故选C。
2
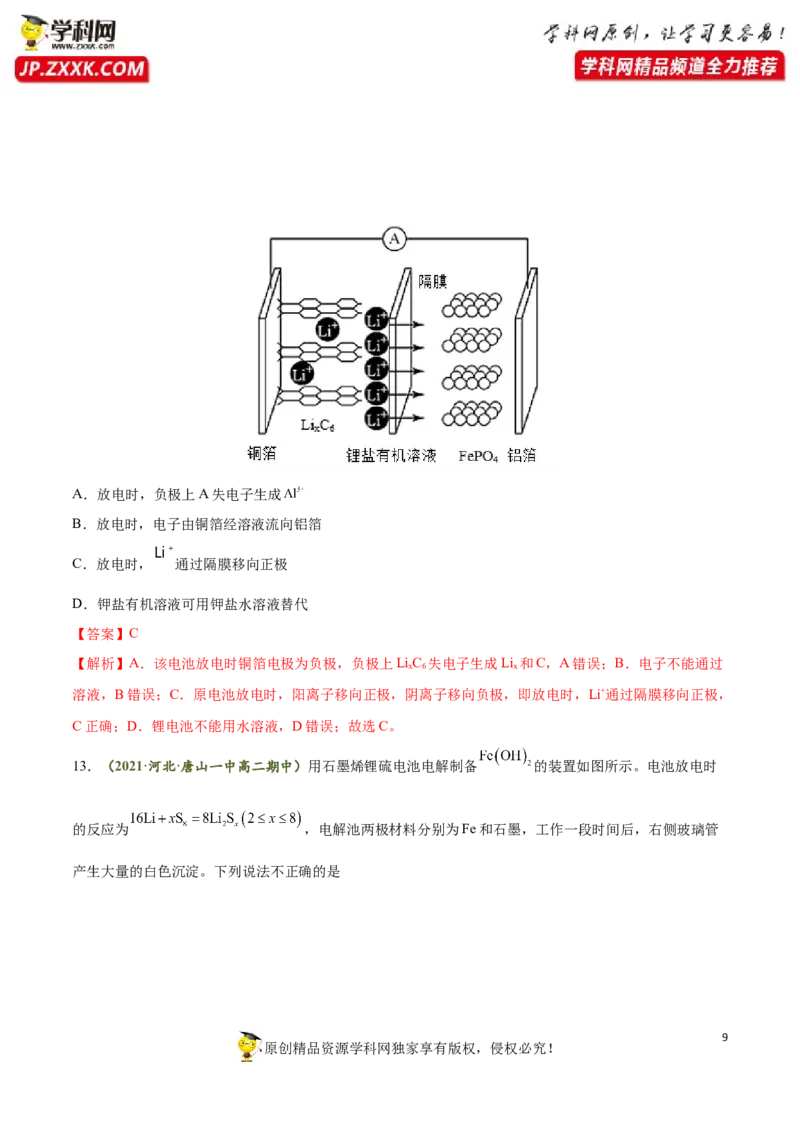
12.(2021·浙江·高二期中)磷酸铁锂电池放电时正极的电极反应式为 ,该电池放电
时的工作原理如图所示,下列叙述正确的是
8
原创精品资源学科网独家享有版权,侵权必究!A.放电时,负极上A失电子生成
B.放电时,电子由铜箔经溶液流向铝箔
C.放电时, 通过隔膜移向正极
D.钾盐有机溶液可用钾盐水溶液替代
【答案】C
【解析】A.该电池放电时铜箔电极为负极,负极上LiC 失电子生成Li 和C,A错误;B.电子不能通过
x 6 x
溶液,B错误;C.原电池放电时,阳离子移向正极,阴离子移向负极,即放电时,Li+通过隔膜移向正极,
C正确;D.锂电池不能用水溶液,D错误;故选C。
13.(2021·河北·唐山一中高二期中)用石墨烯锂硫电池电解制备 的装置如图所示。电池放电时
的反应为 ,电解池两极材料分别为Fe和石墨,工作一段时间后,右侧玻璃管
产生大量的白色沉淀。下列说法不正确的是
9
原创精品资源学科网独家享有版权,侵权必究!A.X是铁电极,发生氧化反应
B.电子流动的方向:
C.正极可发生反应:
D.锂电极减重0.14g时,电解池中溶液减重36g
【答案】D
【解析】A.电解法制备Fe(OH) ,则铁作阳极,发生氧化反应,根据题给总反应可知,金属锂发生氧化反
2
应,作电池的负极,所以Y为阴极,故X是铁电极,A项正确;B.电子从电池的负极流至电解池的阴极,
然后从电解池的阳极流回到电池的正极,即电子从B电极流向Y电极,从X电极流回A电极,B项正确;
C.由图示可知,电极A发生了还原反应,即正极可发生反应 ,C项正确;D.
锂电极减重0.14g,则电路中转移0.02mol电子,电解池中发生的总反应为Fe+2H O Fe(OH) +H ↑,所以
2 2 2
转移0.02mol电子时,电解池中溶液减少0.02mol H O,即减轻0.36g,D项错误;答案选D。
2
14.(2021·河南南阳·高二期中)下列说法正确的是
A.通过构成原电池将反应的化学能全部转化为电能
B.钢铁在潮湿的环境中易腐蚀,是因为钢铁里的铁和少量的碳与表面的水膜形成了无数微小原电池,其
中负极发生的反应为
C.在电解池中电子由阳极流向外接电源的正极,从外接电源的负极流向阴极
10
原创精品资源学科网独家享有版权,侵权必究!D.电解精炼铜时,若阳极质量减少64g,则转移到阴极的电子等于2
【答案】C
【解析】A.通过构成原电池,能将反应的化学能转化为电能,由于存在能量损失,则不可能将化学能全
部转化为电能,A错误;B.钢铁在潮湿的环境中腐蚀时,负极反应是 ,B错误;C.在电解
池中电子由阳极流向外接电源的正极,从外接电源的负极流向阴极,C正确;D.电解精炼铜时,粗铜做
阳极,在阳极参加反应的物质不一定都是铜,也可能是铝或者锌等杂质,故若阳极质量减少64g,转移电
子不一定是2N ,D错误;故选C。
A
15.(2021·河南南阳·高二期中)下图是一套模拟工业生产的电化学装置。丙装置中两电极均为惰性电极,
电解质溶液为KCl溶液,不考虑气体溶解,且钾离子交换膜只允许钾离子通过。下列说法正确的是
A.若甲装置中b为精铜,a为镀件,则可实现a上镀铜
B.丙装置可以制取KOH溶液,制得的KOH可以通过g口排出
C.当d电极消耗标准状况下2.24LO 时,丙装置中阳极室溶液质量减少29.8g
2
D.若甲装置中a、b均为惰性电极,向甲所得溶液中加入0.05molCu (OH) CO 后恰好使溶液复原,则电路
2 2 3
中转移的电子数目为0.2N
A
【答案】C
【解析】A.若装置甲为电镀池,实现镀件上镀铜,阴极为镀件,阳极为精铜,则b极为镀件,a极为精铜,
故A错误;B.由分析可知,丙装置为电解氯化钾溶液的电解池,e极为阳极,f极为阴极,水在阴极上得
到电子发生还原反应生成氢气和氢氧根离子,钾离子通过钾离子交换膜进入阴极区,则高浓度的氢氧化钾
溶液从h口排出,故B错误;C.由分析可知,丙装置为电解氯化钾溶液的电解池,e极为阳极,氯离子在
阳极失去电子发生氧化反应生成氯气,富集的钾离子通过钾离子交换膜进入阴极区,阳极室溶液减少质量
实际为氯化钾的质量,当d电极消耗标准状况下2.24L氧气时,由得失电子数目守恒可知,阳极室溶液减
11
原创精品资源学科网独家享有版权,侵权必究!少质量为 ×4×74.5mol/L=29.8g,故C正确;D.若甲装置中a、b均为惰性电极,该装置为电解
硫酸铜溶液的电解池,向所得溶液中加入碱式碳酸铜后恰好使溶液复原说明电解过程中先电解硫酸铜溶液,
后电解水,由加入的碱式碳酸铜的物质的量为0.05mol可知,参与电解的铜离子为0.1mol、水为0.05mol,
则电路中转移的电子数目为0.1mol×2×N mol—1+0.05mol×2×N mol—1=0.3N ,故D错误;故选C。
A A A
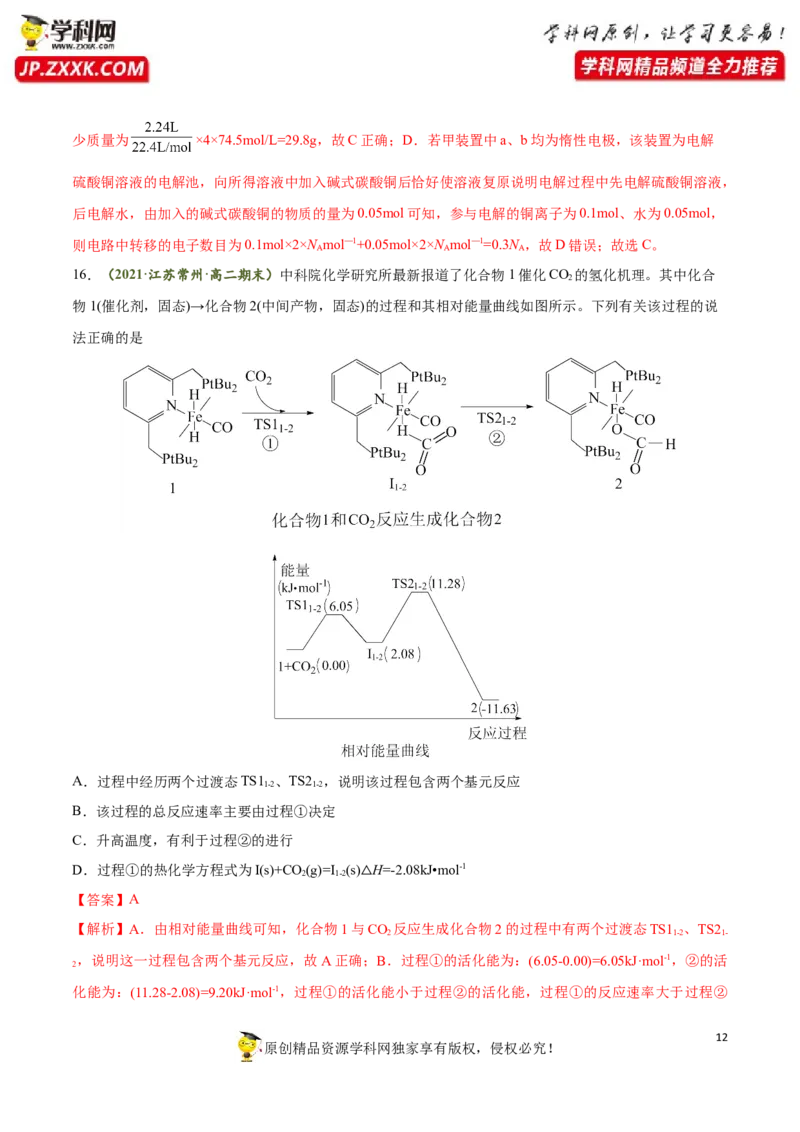
16.(2021·江苏常州·高二期末)中科院化学研究所最新报道了化合物1催化CO 的氢化机理。其中化合
2
物1(催化剂,固态)→化合物2(中间产物,固态)的过程和其相对能量曲线如图所示。下列有关该过程的说
法正确的是
A.过程中经历两个过渡态TS1 、TS2 ,说明该过程包含两个基元反应
1-2 1-2
B.该过程的总反应速率主要由过程①决定
C.升高温度,有利于过程②的进行
D.过程①的热化学方程式为I(s)+CO (g)=I (s) H=-2.08kJ•mol-1
2 1-2
【答案】A △
【解析】A.由相对能量曲线可知,化合物1与CO 反应生成化合物2的过程中有两个过渡态TS1 、TS2
2 1-2 1-
,说明这一过程包含两个基元反应,故A正确;B.过程①的活化能为:(6.05-0.00)=6.05kJ·mol-1,②的活
2
化能为:(11.28-2.08)=9.20kJ·mol-1,过程①的活化能小于过程②的活化能,过程①的反应速率大于过程②
12
原创精品资源学科网独家享有版权,侵权必究!的反应速率,故该过程的总反应速率主要由过程②决定,故B错误;C.过程②为放热反应,升高温度,
反应逆向进行,不利于过程②的进行,故 C 错误;D.过程①的热化学方程式为:I(s)+CO (g)=I
2 1-
(s) H=2.08kJ·mol-1,故D错误;故选A。
2
二、△非选择题(每空2分,共四大题,总计52分。)
17.(2021·四川省绵阳南山中学高二期中)碳、氮元素形成的化合物是人类生产生活中的重要物质。请回
答下列问题:
(1)有机物 经过太阳光照可转化成 ,转化过程如下:
①有机物 中 键和 键的数目之比为___________。
② 、 相比,较稳定的是___________。(填代号)
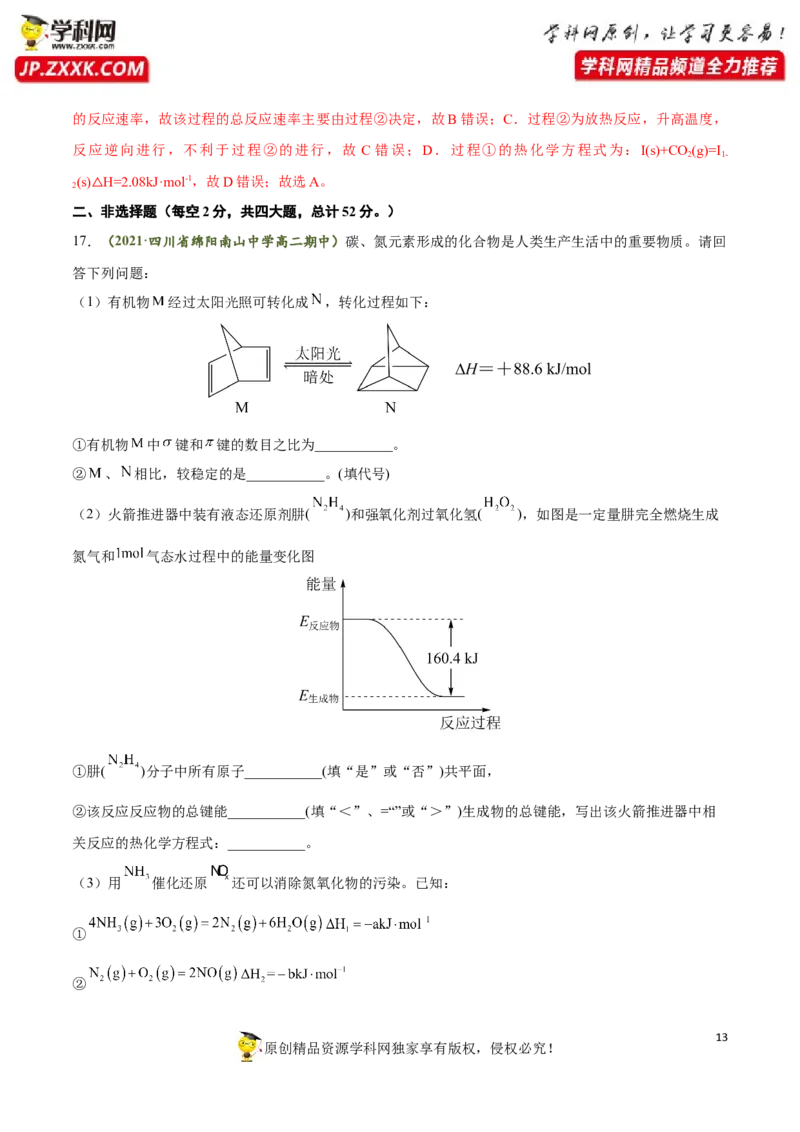
(2)火箭推进器中装有液态还原剂肼( )和强氧化剂过氧化氢( ),如图是一定量肼完全燃烧生成
氮气和 气态水过程中的能量变化图
①肼( )分子中所有原子___________(填“是”或“否”)共平面,
②该反应反应物的总键能___________(填“<”、=“”或“>”)生成物的总键能,写出该火箭推进器中相
关反应的热化学方程式:___________。
(3)用 催化还原 还可以消除氮氧化物的污染。已知:
①
②
13
原创精品资源学科网独家享有版权,侵权必究!若 还原 至 ,则该反应过程中的反应热 ___________ (用含 、 的式子表示)。
【答案】(1) 4:1
(2) 否
(3)
【解析】(1)①有机物 中 键为8, 键的数目为2,两者之比为4:1。
②有机物 经过太阳光照转化成 吸收能量,说明M的能量更低,能量越低越稳定, 、 相比,较稳
定的是M;
(2)①肼( )分子中所有原子不是共平面的,其球棍模型为 ;
②由图可知该反应为放热反应,该反应反应物的总键能小于生成物的总键能,肼( )和强氧化剂过氧化
氢( )生成氮气和水,热化学方程式:
;
(3)
①
②
若 还原 至 ,根据盖斯定律:(①-3②)÷4可得:
。
18.(2021·湖北蕲春·高二期中)肼( )常用于火箭或原电池的燃料。已知:
①
②
14
原创精品资源学科网独家享有版权,侵权必究!③
回答下列问题:
(1)反应 ___________kJ/mol
(2)一定温度下,将 与 以体积比1:1置于10L密闭容器中发生上述反应:
,下列选项不能说明反应达到平衡状态的是________(填编号)。
a.混合气体密度保持不变 b.混合气体颜色保持不变
c. 与 体积之比保持不变 d.体系压强保持不变
(3)在10L的密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:
物质的量(mol)
时间
开始 0.8 1.6 0
2min末 0.6 a 0.3
5min末 0.4 1.2 0.6
6min末 0.4 1.2 0.6
10min末 0.6 1.4 0.3
①前2min内 的平均反应速率为___________。该温度下反应的平衡常数K=___________。
②反应在6min时改变了条件,改变的条件可能是___________(填选项字母)。
A.使用催化剂 B.升高温度 C.减小压强 D.增大 的量
【答案】(1)-1311.7
(2)c
(3) 0.01 9.375 BC
【解析】(1)利用盖斯定律,② 2-①+③ 4得到:(-534kJ/mol) 2-67.7kJ/mol-44kJ/mol 4=-1311.7kJ/
mol;故答案为:-1311.7。
15
原创精品资源学科网独家享有版权,侵权必究!(2)判断达到化学平衡状态的标志,只要看正逆反应速率相等以及各物质浓度保持不变即可。
a.随着反应进行,平衡右移,由于生成液态水,混合气体质量会变小,体积不变,密度会减小,所以当
密度不变,说明平衡不再移动,说明达到平衡状态,故a能说明;
b.NO 为红棕色气体,混合气体颜色不变,说明浓度不变,故b能说明;
2
c.起始时 与 体积之比为1:1,反应消耗的 与 体积之比也是1:1,则二者体积之比始终
是1:1,则体积不变不能说明浓度不变,故c不能说明;
d.由于反应前后体积发生变化,当压强不变,说明混合气体的物质的量不变,说明各物质浓度不变,故d
能说明;
答案选c。
(3)①由图表数据知,反应进行至2min, n(N H)=0.8mol-0.6mol=0.2mol, (N H)=
2 4 2 4
=0.02mol/L, (N H)= =0.01 ,速率之比等于化学计量数之比,则 (NO )=
2 4 2
(N H)=0.01 ;
2 4
由图表数据知,5min~6min时间段内各物质的浓度保持不变,说明该时间段内反应处于平衡状态,平衡常
数K= = =9.375。
②由图表数据知,6min时改变了条件,在10min时N 减少0.3mol,NH 和NO 都增加0.2mol,说明改变
2 2 4 2
条件使平衡逆向移动,且变化量之比等于化学计量数之比,故改变的条件肯定不是使用催化剂和增大NO
2
的量,故A、D不选,该反应是气体体积减小的放热反应,升高温度和减小压强都能使平衡向逆反应方向
移动,符合题意,故选BC。
19.(2021·天津一中高二期中)以FeCl 溶液和不同的强碱弱酸盐溶液作为研究对象,探究盐溶液之间反
3
应的多样性。
实验 现象
I.用 与稀盐酸配制1mol/L 溶液(pH=1);取部分
___________
溶液稀释至0.lmol/L备用
II.取1mL1mol/L 溶液,加入3mL0.5mol/L 溶液 黄色溶液转变为红褐色液体
16
原创精品资源学科网独家享有版权,侵权必究!III.取1mL1mol/L 溶液,加入3mL0.5mol/L 溶液 迅速产生红褐色沉淀和无色气体
加入2滴,出现黑色沉淀,振荡后消
失,溶液澄清;再加2滴,又出现黑色
IV.取10mL0.1mol/L 溶液,滴加0.5mo/L 溶液
沉淀,振荡后消失,同时出现少量淡黄
色沉淀,并有臭鸡蛋味气体产生
(1)①实验I中选用稀盐酸而不用蒸馏水的原因(结合离子方程式解释说明):___________。
②实验I中稀释所得0.1mol/L 溶液的pH___________(选填字母序号)。
a.小于1 b.1~2之间 c.大于2
(2)①用光束照射实验II中红褐色液体有丁达尔现象表明其为___________分散系。
②取少量实验II中红褐色液体加足量盐酸酸化,再加 溶液有白色沉淀,由此推断 溶液与
溶液发生反应的离子方程式是___________。
(3)一些弱酸的电离常数(K)如下表所示
a
化学式
解释实验II和III现象不同的原因:___________。
查阅资料:FeS和 均为难溶于水的黑色固体,其溶度积常数(K )(类似于初中学习过的溶解度,表示物
sp
质的溶解程度)如下表:
化学式 FeS
(4)反思与评价: 溶液和不同的强碱弱酸盐溶液反应的多样性与______有关(至少答出2种影响因
素)。【答案】(1) ,稀盐酸可抑制 的水解 b
(2) 胶体
17
原创精品资源学科网独家享有版权,侵权必究!(3) 水解,溶液呈酸性,加入的 、 水解都使溶液呈碱性,混合后互促水解;
水解程度小、碱性弱、互促程度小,只得到 胶体; 水解程度更大、碱性更强,互促程度更
大,最终有 沉淀和 气体放出; 溶解度小于 ,利于气体逸出(表述出弱的程度不同,促
进不同即可)
(4)强碱弱酸盐溶液的阴离子的水解程度(或碱性强弱)和还原性、 溶液的浓度、生成物的溶解性等
【解析】(1)①Fe3+存在水解反应:Fe3++3H O Fe(OH) +3H+,加酸后H+浓度变大 平衡逆向偏移(即向
2 3
左),抑制铁离子水解,故答案为:Fe3+ 水解:F⇌e3++3H O Fe(OH) +3H+,加酸后H+浓度变大,平衡逆向偏
2 3
移(即向左), 抑制铁离子水解; ⇌
②实验I中是用1mol/L的FeCl 溶液(pH=1)稀释所得0.1mol/L 溶液,即稀释了10倍,由于加水稀释
3
过程中Fe3++3H O Fe(OH) +3H+水解平衡正向移动,故稀释后溶液的pH在1~2之间,故答案为:b;
2 3
(2)①胶体具有丁⇌达尔效应,用光束照射实验II中红褐色液体有丁达尔现象,说明实验II中红褐色液体
为胶体,故答案为:胶体;
②加稀盐酸和氯化钡有白色沉淀,说明溶液中有硫酸根,发生氧化还原反应,反应的离子方程式为:2Fe3+
+ +H O═2Fe2++ +2H+,故答案为:2Fe3++ +H O═2Fe2++ +2H+;
2 2
(3)酸越弱,相应的钠盐越容易水解,溶液的碱性越强,根据电离常数可知,碳酸的K 小于亚硫酸酸的
i2
K ,碳酸钠更易水解,即溶液的碱性更强, 水解,溶液呈酸性,加入的 、 水解都使
i2
溶液呈碱性,混合后互促水解; 水解程度小、碱性弱、互促程度小,只得到 胶体;
水解程度更大、碱性更强,互促程度更大,最终有 沉淀和 气体放出; 溶解度小于 ,
利于气体逸出(表述出弱的程度不同,促进不同即可),故答案为: 水解,溶液呈酸性,加入的
18
原创精品资源学科网独家享有版权,侵权必究!、 水解都使溶液呈碱性,混合后互促水解; 水解程度小、碱性弱、互促程度小,只
得到 胶体; 水解程度更大、碱性更强,互促程度更大,最终有 沉淀和 气体放
出; 溶解度小于 ,利于气体逸出(表述出弱的程度不同,促进不同即可);
(4)结合实验过程及数据分析可知:FeCl 溶液和不同的强碱弱酸盐溶液反应的多样性与盐溶液离子还原
3
性、碱性强弱、反应物的量等有关,故答案为:盐溶液离子还原性、碱性强弱、反应物的量。
20.(2021·天津·耀华中学高二期中)天然气的主要成分为 ,一般还含有 等烃类,是重要的燃料
和化工原料。
(1)乙烷在一定条件可发生如下反应: ,相关物质的燃烧热数据如下表
所示:
物质 (g) (g) (g)
燃烧热 /( ) -1560 -1411 -286
① ___________ 。
②提高该反应平衡转化率的方法有___________、___________。
③容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为α。反应的平衡
常数 ___________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)高温下,甲烷生成乙烷的反应如下: 。反应在初期阶段的速率方程为:
,其中k为反应速率常数。
①设反应开始时的反应速率为v,甲烷的转化率为α时的反应速率为v,则v=___________v
1 2 2 1。
②对于处于初期阶段的该反应,下列说法正确的是___________。
A.增加甲烷浓度,v增大 B.增加 浓度,v增大
C.乙烷的生成速率逐渐增大 D.降低反应温度,k减小
19
原创精品资源学科网独家享有版权,侵权必究!【答案】(1) +137 升高温度 减小压强
(2) 1-α AD
【解析】(1)①燃烧热是指1mol燃料充分燃烧生成稳定氧化物所释放的热量,利用燃烧热写出热化学方
程式:
Ⅰ乙烷的燃烧:C H(g)+3.5O =2CO (g)+3HO(l) H=-1560kJ•mol-1
2 6 2 2 2
Ⅱ乙烯的燃烧:C
2
H
4
(g)+3O
2
=2CO
2
(g)+2H
2
O(l)△H=-1411kJ•mol-1
Ⅲ氢气的燃烧:H
2
(g)+0.5O
2
=H
2
O(l) H=-286kJ△•mol-1
根据盖斯定律,Ⅰ-Ⅱ-Ⅲ得C
2
H
6
(g)═△C
2
H
4
(g)+H
2
(g) H
1
=+137kJ•mol-1;
故答案为:+137; △
②C H(g) C H(g)+H(g) H=137kJ•mol-1是一个气体计量数增大的吸热反应,提高该反应平衡转化率,就
2 6 2 4 2 1
是使化学平⇌衡右移,可以采△用的措施有升高温度、减小压强(增大体积)等,故答案为:升高温度、减小压
强(增大体积);
③设容器中通入乙烷和氢气的物质的量为m,列三段式有:
C H(g) C H(g)+H(g)
2 6 2 4 2
⇌
平衡时的总物质的量=m-αm+αm+m+αm=2m+αm,所以p(H )= = ,同理p(C H)= 、
2 2 4
p(C H)= ,所以K = = ;故答案为: ;
2 6 p
(2)①根据反应在初期阶段的速率方程:v=k×c ,可知v=kc(CH),转化率为α时c′(CH)=(1-α)(CH ),
CH4 1 4 4 4
所以v=kc(CH)(1-α),由于k不受反应物浓度影响,所以v=v(1-α);
2 4 2 1
②A.根据速率方程可知反应速率与甲烷的浓度成正比,增加甲烷浓度,v增大,故A正确;B.根据速率
方程可知反应速率与氢气的浓度成无关,增加H 浓度,v不变,故B错误;C.随着反应的进行,甲烷的
2
浓度减小,反应速率下降,故C错误;D.无论反应是吸热还是放热,速率常数随温度升高增大,随反应
20
原创精品资源学科网独家享有版权,侵权必究!温度降低,k减小,故D正确;故选:AD。
21
原创精品资源学科网独家享有版权,侵权必究!22
原创精品资源学科网独家享有版权,侵权必究!