文档内容
期末模拟测试 02
(时间:75分钟 满分:100分)
可能用到的相对原子质量:H 1 C 12 N14 O16 Si 28 P 31 Cl 35.5 K39 Mn55
第Ⅰ卷 选择题(共60分)
一 选择题 (本题包括20小题,每小题3分,共60分。每小题只有一个选项符合题意)
1.(2023春·宁夏吴忠·高二吴忠中学校考期中)下列物质的化学用语正确的是
A.HO 的电子式:
2 2
B.CO 的结构式:
2
C.中子数为18的 原子:
D.基态碳原子的最外层电子排布图:
【答案】B
【解析】A.HO 分子由H、O原子通过共价键构成,其结构式为H-O-O-H,电子式为
2 2
,A不正确;
B.CO 的电子式为 ,则其结构式为 ,B正确;
2
C.Cl为17号元素,质子数为17,则中子数为18的Cl原子可表示为 ,C不正确;
D.基态碳原子的最外层电子排布式为2s22p2,则其最外层电子排布图为
,D不正确;
故选B。
2.(2023春·福建·高二校联考阶段练习)助力神舟十三号载人飞船顺利飞向太空的运载火
箭发动机以偏二甲肼和液态 为主要燃料,工作时发生的反应为:
。下列有关说法错误的是
A.偏二甲肼 分子中C、N原子的杂化方式不同
B.H、C、N、O电负性依次增大
C.C、N、O第一电离能由大到小的顺序为:N、O、C
D.等物质的量的 、 分子含有相同数目的 键
【答案】A【解析】A.偏二甲肼[ ]分子中C、N原子价层电子对数都为4,其杂化方式
相同,故A错误;
B.根据同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,的H、C、
N、O电负性依次增大,故B正确;
C.根据同周期从左到右第一电离能呈增大趋势,但第IIA族大于第IIIA族,第VA族大于
第VIA族,则C、N、O第一电离能由大到小的顺序为:N、O、C,故C正确;
D.氮气含有氮氮三键,二氧化碳含有两个碳氧双键,因此等物质的量的 、 分子含
有相同数目的 键,故D正确。
综上所述,答案为A。
3.(2023春·山东青岛·高二统考期中)硒化锌(摩尔质量 )是一种重要的半导体材
料,其立方晶胞结构及沿z轴投影如图。已知晶胞参数为 ,O点原子分数坐标为
.下列说法错误的是
A.与 最近且距离相等的 有12个 B. 间距离为
C.Q点原子分数坐标为 D.晶体密度为
【答案】C
【解析】A.以顶点Se原子为对象,面心的Se原子与 最近且距离相等的 有12个,故
A正确;
B.根据晶体结构图可知, 间距离为 对角线的距离,为 ;故B正确;
C.以O原子为原点时,由右图可知,Q点在X轴和Y轴的四分之三处,结合该晶胞的三
维结构,Q点是在Z轴四分之三处,Q点原子分数坐标为 ;故C错误;
D.该晶胞中含有4个硒化锌,所以晶体密度为 ;故D
正确;
故答案选C。
4.(2023春·宁夏银川·高二银川一中校考期中)下列对一些实验事实的理论解释,错误的是
选
实验事实 理论解释
项
电子气中的自由电子在热的作用下与金属原子频繁碰
A 金属的导热性好
撞,从而引起能量的交换。
氟的电负性大于氯的电负性,F-C的极性大于C1-C
酸性: 的极性,使 的极性大于 的极性,导致
B
的羧基中的羟基的极性更大,更易电离出
聚四氟乙烯的化学稳定性高 C-F的键能比C-H的键能大,键能越大,化学性质
C
于聚乙烯 越稳定
D HF的沸点高于HCl HF的相对分子质量小于HCl
A.A B.B C.C D.D
【答案】D
【解析】A.由于自由电子和金属阳离子在热的作用下运动加快,相互碰撞增加,从而引
起能量的交换,所以金属的导热性好,A正确;
B.由于电负性:F>Cl,使得 的极性大于 的极性,因而羟基电子云更偏向O原
子,导致 的羧基中的羟基的极性更大,更易电离出 ,因此酸性:
,B正确;
C.由于F的电负性较大,在与C原子的结合过程中形成的C-F键的键能大于聚乙烯中C-
H键的键能,键能越大,化学性质越稳定,因此聚四氟乙烯的化学稳定性高于聚乙烯,C
正确;
D.由于HF分子间能形成氢键,所以HF的沸点高于HCl,D错误;
答案选D。
5.(2023春·河北·高二统考期中)某离子液体结构如图,Q、R、T、X、Y和Z为原子序
数依次增大的主族元素,基态T原子和Y原子最外层均有两单电子,Q、R、X和Z质子数
均为奇数且和为22。
下列说法错误的是A.该离子液体难挥发,可用作溶剂
B.基态R原子的价层电子的轨道表达式为
C. 分子是极性分子
D. 中含有配位键
【答案】C
【分析】Q、R、T、X、Y和Z为原子序数依次增大的主族元素,基态T原子和Y原子最
外层均有两单电子,结合原子的成键个数,T为C,Y为O,Q、R、X和Z质子数均为奇
数且和为22,Q为H,R为B,X为N,Z为F,据此解答。
【解析】A.该离子液体含离子键,沸点较高,难挥发,可用作溶剂,故A正确;
B.R为B,其基态R原子的价层电子的轨道表达式为 ,故B正确;
C.BF 的分子构型为平面三角形,为对称结构,正负电荷中心重合,是非极性分子,故C
3
错误;
D.B原子最外层只有3个电子,有一个空轨道,故 中含有一个配位键,故
D正确;
故选C。
6.(2023春·宁夏银川·高二银川一中校考期中)下列各组物质,按其晶体的熔点由高到低
排列正确的是
A.NaSO 、SO 、HO、HCl B.MgO、MgCl 、NaCl、Hg
2 4 2 2 2
C.NaCl、HO、BN、CH D.晶体硅、SiC、金刚石、CsCl
2 4
【答案】B
【解析】A.NaSO 是离子晶体熔点高于分子晶体,SO 、HO、HCl均为分子晶体,且
2 4 2 2
HO由于分子间氢键导致熔点升高,SO 的相对分子质量大于HCl,分子间作用力SO 大于
2 2 2
HCl,故熔点由高到低顺序为:NaSO >HO >SO >HCl,A错误;
2 4 2 2
B.已知MgO、MgCl 、NaCl均为离子晶体,而Hg为金属晶体,常温下成液态,且
2
Mg2+所带电荷大于Na+,Mg2+半径小于Na+,O2-所带电荷大于Cl-,O2-半径小于Cl-,故熔点
由高到低的顺序为:MgO>MgCl >NaCl>Hg,B正确;
2
C.已知NaCl为离子晶体,BN为共价晶体, HO、CH 均为分子晶体,故BN熔点最高,
2 4其次为NaCl,CH 呈气态,HO由于分子间氢键导致熔点升高,故熔点由高到低的顺序为:
4 2
BN>NaCl>HO>CH,C错误;
2 4
D.已知晶体硅、SiC、金刚石均为共价晶体,且Si的原子半径大于C的,即Si-Si的键长
大于Si-C大于C-C键,故熔点金刚石>SiC>晶体硅,CsCl是离子晶体,熔点低于共价晶
体,故熔点由高到低的顺序为:金刚石>SiC>晶体硅>CsCl,D错误;
故答案为:B。
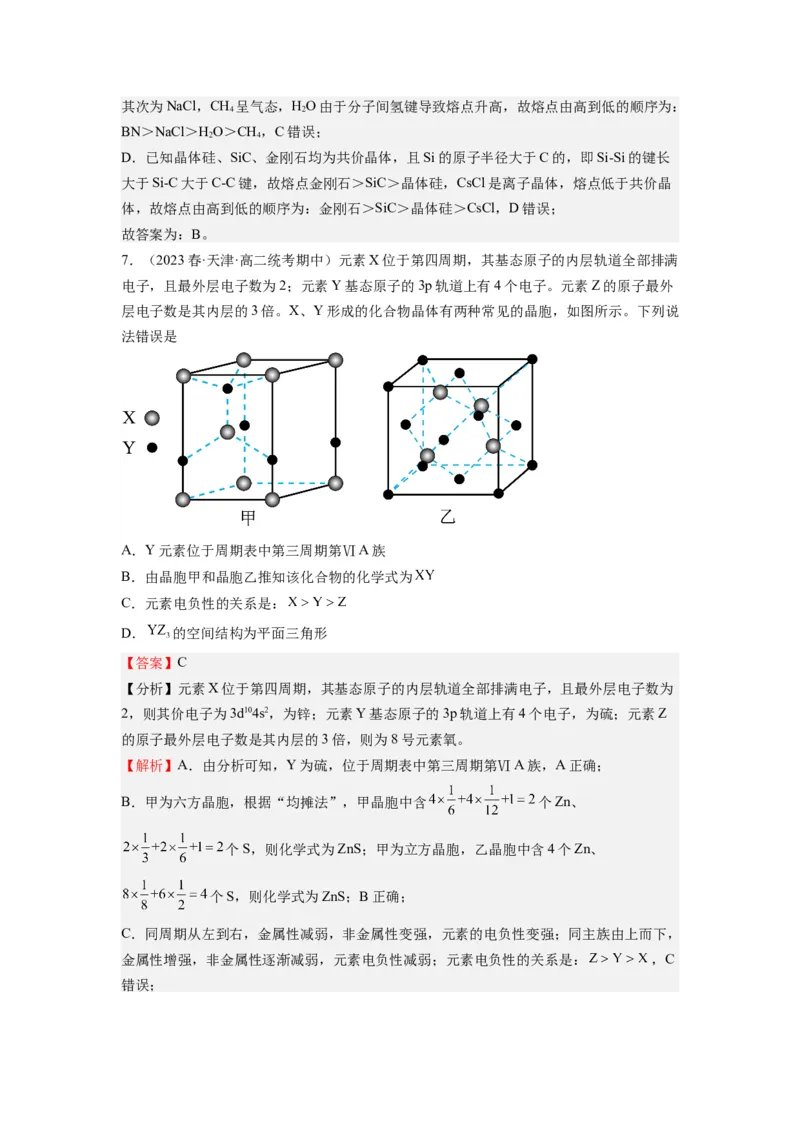
7.(2023春·天津·高二统考期中)元素X位于第四周期,其基态原子的内层轨道全部排满
电子,且最外层电子数为2;元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外
层电子数是其内层的3倍。X、Y形成的化合物晶体有两种常见的晶胞,如图所示。下列说
法错误是
A.Y元素位于周期表中第三周期第ⅥA族
B.由晶胞甲和晶胞乙推知该化合物的化学式为
C.元素电负性的关系是:
D. 的空间结构为平面三角形
【答案】C
【分析】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为
2,则其价电子为3d104s2,为锌;元素Y基态原子的3p轨道上有4个电子,为硫;元素Z
的原子最外层电子数是其内层的3倍,则为8号元素氧。
【解析】A.由分析可知,Y为硫,位于周期表中第三周期第ⅥA族,A正确;
B.甲为六方晶胞,根据“均摊法”,甲晶胞中含 个Zn、
个S,则化学式为ZnS;甲为立方晶胞,乙晶胞中含4个Zn、
个S,则化学式为ZnS;B正确;
C.同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同主族由上而下,
金属性增强,非金属性逐渐减弱,元素电负性减弱;元素电负性的关系是: ,C
错误;D. 的中心原子S原子的价层电子对数为 ,为sp2杂化,空间构型为平面三
角形,D正确;
故选C。
8.(2023春·山东聊城·高二山东聊城一中校考期中)下列关于共价晶体、分子晶体的叙述
中,不正确的是
A.在 晶体中,1个硅原子和4个氧原子形成4个共价键
B.混合晶体石墨的熔点高于金刚石
C. 的相对分子质量大于 ,所以 的沸点高于
D.金刚石为网状结构,由共价键形成的碳原子环中,最小环上最多4个碳原子共面
【答案】C
【解析】A.在 晶体中,1个硅原子和4个氧原子形成4个共价键,A项正确;
B.石墨中的碳碳键的键长小于金刚石中的碳碳键的键长,且石墨融化时不仅要克服共价
键,还要破坏分子间作用力,故熔点大于金刚石,B项正确;
C.虽然 的相对分子质量大于 ,但是由于 分子之间可以形成氢键,所以 的沸
点高于 ,C项错误;
D.金刚石为网状结构,由共价键形成的碳原子环中,最小环上有6个碳原子,最多4个碳
原子共面,D项正确;
答案选C。
9.(2023春·江西·高二统考期中)近日,湖南科技大学和中国科学院上海硅酸盐研究所合
成了磷酸镁(X)/硅酸钙(Y)复合骨水泥,有望用于人体承重部位的骨修复。下列叙述错误的
是
A.X和Y都属于离子晶体 B.Y中阳离子半径大于X中阳离子半径
C.X中基态阳离子最外层电子占据1个轨道 D.X中阴离子空间构型为正四面体形
【答案】C
【解析】A.磷酸镁由镁离子和磷酸根组成,硅酸钙由钙离子和硅酸根形成,二者都属于
离子晶体,故A正确;
B.Y中阳离子为 ,X中阳离子为Mg2+, 有3个电子层,而Mg2+只有2个电子层,
的半径大于Mg2+,故B正确;
C.X中阳离子为Mg2+,电子排布式为1s22s22p6,最外层电子占据2p能级上的3个轨道,
故C错误;
D.X中阴离子为PO ,中心原子价层电子对数为4+ =4,其没有孤电子对,
空间构型为正四面体形,故D正确;
故选C。
10.(2023春·重庆渝中·高三重庆巴蜀中学校考阶段练习)短周期主族元素X、Y、Z、W原子序数依次增大,X原子核外有7个电子,基态Y原子无未成对电子,Z与X为同族元
素,W最高价含氧酸为二元酸,下列说法正确的是
A.原子半径:
B.第一电离能大小:WP>Cu
D.S、P为p区元素,Cu、Zn为d区元素【答案】B
【解析】A.基态Ni原子的简化电子排布式为:[Ar] ,故A错误;
B.基态As原子最高能级为4p,其轨道为哑铃形,故B正确;
C.第一电离能:P>S>Cu,故C错误;
D.S、P为p区元素,Cu、Zn为ds区元素,故D错误;
故答案选:B。
【点睛】本题考查了原子结构与元素性质,明确基态原子核外电子排布规律、熟悉同周期
元素性质递变规律是解题关键,题目难度不大。
14.(2023·湖北·襄阳四中校考模拟预测)DDQ是一种常用的有机氧化剂,其结构式如图
所示,其中X、Y、Z和W是原子序数依次增大的短周期元素,W半径大于Z。下列说法
正确的是
A.简单离子半径:
B.氢化物沸点:
C.元素的电负性:
D.含氧酸的酸性:
【答案】C
【分析】X、Y、Z和W是原子序数依次增大的短周期元素,X有4个价键,Y有三个价键,
Z有2个价键,X、Y、Z和W是原子序数依次增大的短周期元素,W的原子半径大于Z的
原子半径,说明Z在W的上一周期,且W形成1个共价键,则X、Y、Z、W分别是C、
N、O、Cl。
【解析】A.根据同电子层结构核多径小,则半径: ,故A错误;
B.碳可以形成相对分子质量很大的烃,其沸点很好,故碳形成的氢化物的沸点可能高于
氮形成氢化物的沸点,故B错误:
C.同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同主族由上而下,
金属性增强,非金属性逐渐减弱,元素电负性减弱;元素的电负性: ,故C正确;
D.HClO的酸性弱于 的酸性,故D错误。
故选C。
15.(2023春·广东茂名·高三茂名市第一中学校考阶段练习)陈述Ⅰ和Ⅱ均正确且具有因果关系的是
选
陈述Ⅰ 陈述Ⅱ
项
A Al(OH) 能与强碱反应,而Mg(OH) 不能 Al金属性比Mg强
3 2
B 不锈钢含有铬和镍而纯铁中不含 不锈钢比纯铁硬度大,熔点高
C 波尔多液是常见的农药用于除虫害 重金属溶液能使蛋白质变性
D H-F键键能比H-Cl键大 HF沸点比HCl高
A.A B.B C.C D.D
【答案】C
【解析】A. 能与强碱反应,而 不能,但是金属性Mg比Al强,故A错
误;
B. 合金的硬度比纯铁大,但是熔点比纯铁的小,故B错误;
C. 波尔多液含有 ,重金属盐除虫害是蛋白质变性,故C正确;
D. HF沸点比HCl高是物理性质,是因为HF中有氢键,故D错误;
故选C。
16.(2023春·山东青岛·高二统考期中)下列关于物质结构与性质的说法,正确的是
A. 中 键键长比 中 键键长短
B. 石墨中含有 键的物质的量为
C. 和 均为非极性分子
D.乙烯、苯、吡啶( )中碳的杂化方式均相同
【答案】D
【解析】A. 和 空间结构和键角均一致,元素电负性越大,形成的键能也就越大;
键长越长,键能越小;所以 中 键键长比 中 键的键长要长;故A错误;
B.石墨中每个碳原子均摊到的共价键数为 ,所以 石墨中含有 键的物质的
量为 ;故B错误;
C. 为极性分子,故C错误;
D.乙烯、苯、吡啶( )中碳的杂化方式均为sp2杂化,故D正确;
故答案选D。17.(2023春·山东青岛·高二统考期中)反应
曾用于检测司机是否
酒后驾驶。下列说法错误的是
A. 基态核外价电子排布式为
B. 与 互为等电子体
C.反应中碳原子的杂化方式不变
D. 与 可以任意比互溶原因之一为分子间可以形成氢键
【答案】C
【解析】A.基态Cr原子的价电子排布式为 , 基态核外价电子排布式为 ,A
正确;
B.等电子体是指价电子数和原子数相同的分子、离子或原子团, 与 互为等电子
体,B正确;
C.乙醇中C原子的杂化方式为sp3,乙酸中C原子的杂化方式为sp3、sp2,C错误;
D. 与 均含有氧原子,两者可以形成分子间氢键,可以任意比互溶,D正
确;
故选C。
18.(2023春·山东青岛·高二统考期中)部分晶体及分子结构如图所示,下列说法错误的
是
A. 晶胞中有8个 , 配位数是4
B.金刚石晶体中每个碳原子被12个六元环共用,每个六元环最多有4个碳原子共面
C.该气态团簇分子的分子式为 或
D.三种物质对应的晶体熔沸点最高的是
【答案】D
【解析】A.晶胞中钙离子数目为 ,结合晶胞内部的氟离子可知,对应配位
数为4,故A正确;
B.在金刚石晶体中,每个碳原子被12个六元环共同占有,由于C采取sp3杂化,故每个六元环最多有4个碳原子共面,故B正确;
C.该团簇分子,含有F和E的数目均为4,故化学式为 或 ,故C正确;
D.金刚石为共价晶体,三种物质对应的晶体熔沸点最高的是金刚石;故D错误;
故答案选D。
19.(2023春·山东聊城·高二山东聊城一中校考期中)硫化锌是一种优良的宽带隙半导体
锂离子电池负极材料,具有在充电的同时合金化反应的特点。在充电过程中负极材料晶胞
的组成变化如图所示。
下列说法不正确的是
A. 、
B.在 体对角线的一维空间上会出现“ ”的排布规律
C.在 中,硫离子的配位数是4
D.若 的晶胞参数为 ,则 间的距离为
【答案】D
【解析】A.在 晶胞中,由原子个数可得 ,由化合价代数和为零可得
,解得 、 ,A正确;
B.根据 结构,体对角线的一维空间上会出现“ ”的
排布规律,B正确;
C.晶胞 中从图像上可知,硫离子的配位数为4,C正确;
D.若 的晶胞参数为 ,将晶胞切三刀分为8个小立方体,则E在左后上立方体体
心,则 间的距离为 ,D错误;
故选 D。
20.(2023春·山东青岛·高二统考期中)W、X、Y、Z为原子序数依次增大的短周期主族
元素,X与Z位于相邻主族,W、X、Z价电子数之和等于Y的价电子数,它们组成的化合
物结构如图。下列说法正确的是
A.W与Y化合物的化学键不具有方向性和饱和性
B.X的最高价氧化物的水化物为强酸
C.Y所在周期中电负性比Y大的元素有2种
D.W、Y、Z形成的化合物含有离子键和极性共价键
【答案】D
【分析】结合结构图及原子序数大小,Z形成+2价阳离子,则Z为Mg;W只形成1对共
用电子对,且原子序数最小,则W为H;Y形成2对共用电子达到稳定结构,则Y最外层
电子数为6,Y为O;W、X、Z价电子数之和等于Y的价电子数,则X最外层有3个电子,
其原子序数在Mg前,则X为B。
【解析】A.W与Y形成的化合物有水和双氧水,其中O原子利用sp3杂化轨道与H原子
或O原子形成了共价键,sp3杂化轨道有4个不同的伸展方向,有2个孤电子对占据了2个
杂化轨道,只能形成2个成键电子对,因此,W与Y形成的化合物中的化学键有方向性和
饱和性,故A错误;
B.X为B,其最高价氧化物的水化物为HBO,属于弱酸,故B错误;
3 3
C.同周期元素从左到右电负性增强,则比O电负性大的同周期元素只有F一种,故C错
误;
D.Mg、O、H形成Mg(OH) ,镁离子与氢氧根离子之间存在离子键,氢氧根离子中H-O
2
之间存在极性共价键,故D正确;
故选:D。
第Ⅱ卷 非选择题(共40分)
二、填空题
21.(10分)(2023春·山东德州·高二校考阶段练习)铁(Fe)、钴(Co)、镍(Ni)是第四周期
第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
(1)铁系元素能与CO形成Fe(CO) 、Ni(CO) 等金属羰基化合物。已知室温时Fe(CO) 为浅
5 4 5
黄色液体,沸点103℃,则Fe(CO) 中含有的化学键类型包括___________(填字母)。
5
A.极性共价键 B.离子键 C.配位键 D.金属键
(2)镍能形成多种配合物,如Ni(CO) 、[Ni(CN) ]2-、[Ni(NH )]2+等,下列有关说法正确的是
4 4 3 6
___________(填选项字母)。
A.[Ni(NH )]2+中含有共价键和离子键
3 6
B.CO与CN—互为等电子体,其中CO分子内σ键和π键的个数比为1:2
C.NH 中N原子为sp3杂化,其空间构型为正四面体形
3
D.Ni2+在形成配合物时其配位数只能为4,Fe在形成配合物时其配位数只能为6(3)Fe、Co、Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点,Fe、Co、
Ni明显高于Ca,其原因是___________。
(4)Co Ni Fe O 中Co、Ni的化合价都是+2,则Fe的化合价是___________。Fe3+比Fe2+更
x (1-x) 2 4
稳定的原因是___________。
(5)胆矾溶液与氨水在一定条件下可以生成Cu(NH )SO ·H O晶体。在Cu(NH )SO ·H O晶
3 4 4 2 3 4 4 2
体中,含有的原子团或分子有:[Cu(NH )]2+、NH 、SO 、HO,[Cu(NH )]2+为平面正方
3 4 3 2 3 4
形结构,则呈正四面体结构的原子团或分子是___________,其中心原子的杂化轨道类型是
___________。
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO) ,呈正四面体构型,
4
Ni(CO) 易溶于___________(填标号)。
4
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
【答案】(1)AC
(2)B
(3)Fe、Co、Ni的原子半径比Ca的小,价电子数目比Ca的多,金属键比Ca的强,因此熔
点高
(4) +3 Fe3+的价电子排布为3d5,最外层电子半充满,比价电子排布3d6的Fe2+更
稳定
(5) SO sp3杂化
(6)BC
【解析】(1)由物理性质可知,五羰基合铁是沸点低的分子晶体,分子中含有配位键和极
性共价键,不含有离子键和金属键,故选AC;
(2)A. [Ni(NH )]2+配离子中含有配位键和极性共价键,不含有离子键,故A错误;
3 6
B.一氧化碳和氰酸根离子的原子个数都为2、价电子数都为10,互为等电子体,等电子
体具有相同的空间结构,则一氧化碳分子中含有碳氧三键,分子内σ键和π键的个数比为
1:2,故B正确;
C.氨分子中氮原子的价层电子对数为4、孤对电子对数为1,分子的空间构型为三角锥形,
故C错误;
D.Ni2+离子的价电子排布式为3d8,Ni2+在形成配合物时,其配位数可以为4或6,故D错
误;
故选B;
(3)Fe、Co、Ni、Ca四种元素都位于元素周期表第四周期,Fe、Co、Ni 的原子半径都
小于Ca,Fe、Co、Ni位于d区,价电子数多于位于s区的Ca,所以Fe、Co、Ni的金属键
强于Ca,熔点高于Ca,故答案为:Fe、Co、Ni的原子半径比Ca的小,价电子数目比Ca
的多,金属键比Ca的强,因此熔点高;
(4)设化合物中铁元素的化合价为a,由化合价代数和为0可得:2a+2a+2 (1—a )+4×( —2 ) =0,解得a=+3;Fe3+的价电子排布为3d5,最外层电子半充满,比价电子排布3d6
的Fe2+更稳定,故答案为:+3;Fe3+的价电子排布为3d5,最外层电子半充满,比价电子排
布3d6的Fe2+更稳定;
(5)硫酸根离子中硫原子的价层电子对数为4、孤对电子对数为0,硫原子的杂化方式为
sp3杂化,离子的空间构型为正四面体形,故答案为:SO ;sp3杂化;
(6)由题意可知,四羰基合镍为非极性分子,由相似相溶原理可知,四羰基合镍不溶于水,
易溶于有机溶剂四氯化碳和苯,故选BC。
22.(10分)(2023春·江苏无锡·高二江阴市华士高级中学校联考期中)回答下列问题:
(1)已知乙醇在铜的催化下可以被氧化生成乙醛,而具有α-H的醛或酮,在酸或碱的催化作
用下,与另一分子醛或酮发生缩合,生成β-羟基醛或β-羟基酮。以乙醛为例,其过程可表
示如下:
请从元素电负性的角度解释第一步加成反应发生的原理:___________
(2)乙醛也能与甲胺(CHNH )中的-NH 发生类似反应。甲胺常温常压下是一种无色有强刺激
3 2 2
性气味的气体。甲胺极易溶于水除因为它们都是极性分子外,还因为___________。
(3)乙二胺(H NCH CHNH )能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是
2 2 2 2
___________。
(4)化工原料Z是X与HI反应的主产物,X→Z的反应机理如图:
其中中间体Y中碳原子的轨道杂化方式为___________
(5)对羟基苯甲醛 的沸点比邻羟基苯甲醛 的沸点高,其原因是___________。
【答案】(1)CH CHO中α-H带部分正电荷,α-C带部分负电荷,而羰基中碳原子带部分正
3
电荷,加成时碳氧双键打开,带部分正电荷的α-H原子和羰基中带部分负电荷的氧原子结
合,带部分负电荷的α-C原子和羰基中带部分正电荷的碳原子结合
(2)甲胺与水分子间形成氢键
(3)乙二胺的两个N原子提供孤对电子给金属离子形成配位键生成配离子,配离子空间呈较
稳定的五元环状结构
(4)sp2、sp3
(5)对羟基苯甲醛分子间形成氢键,而邻羟基苯甲醛形成的是分子内氢键
【解析】(1)从元素电负性的角度解释第一步加成反应发生的原理为:CHCHO中α-H带
3部分正电荷,α-C带部分负电荷,而羰基中碳原子带部分正电荷,加成时碳氧双键打开,
带部分正电荷的α-H原子和羰基中带部分负电荷的氧原子结合,带部分负电荷的α-C原子
和羰基中带部分正电荷的碳原子结合。
(2)甲胺极易溶于水除因为它们都是极性分子外,还因为:甲胺与水分子间形成氢键。
(3)乙二胺(H NCH CHNH )能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是:
2 2 2 2
乙二胺的两个N原子提供孤对电子给金属离子形成配位键生成配离子,配离子空间呈较稳
定的五元环状结构。
(4)Y中含有-CH 和 ,碳原子的轨道杂化方式为sp3、sp2。
3
(5)对羟基苯甲醛分子间形成氢键,而邻羟基苯甲醛形成的是分子内氢键,则对羟基苯甲
醛 的沸点比邻羟基苯甲醛 的沸点高。
23.(10分)(2023秋·广东深圳·高二统考期末)单质硅是制造太阳能电池板的主要原料,
制备电池板时还需添加硼、氮、钛、钴、钙等多种化学物质。
请回答下列问题:
(1)基态硼原子的电子排布式为______,下列钴原子的价层电子轨道表示式中,不符合洪特
规则的是______(填选项字母)。
A. B.
C. D.
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为______(用元素符号表示),原
因为______。
(3)钛元素位于元素周期表______区;基态钛原子中,最外层电子的电子云轮廓图为______。
(4) 在火焰上灼烧时火焰的颜色为砖红色,从微观角度解释部分金属元素在火焰上灼
烧呈现不同颜色的原因:______。
【答案】(1) B
(2) N>O>C 同周期元素从左向右第一电离能呈增大趋势,N最高能级处于半满
状态,较稳定,所以第一电离能大于O
(3) d 球形
(4)电子从较高能量的激发态跃迁到较低能量的激发态或基态时,以光的形式释放能量
【解析】(1)基态硼原子的电子排布式为 ;
A. 为钴的基态原子的价层电子表示式,A错误;B. ,不符合洪特规则,B正确;
C. ,不符合能量最低原理,C错误;
D. ,不符合泡利原理,D错误;
故选B;
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为:N>O>C,原因为同周
期元素从左向右第一电离能呈增大趋势,N最高能级处于半满状态,较稳定,所以第一电
离能大于O;
(3)基态钛原子的价电子排布式为 ,所以其位于元素周期表d区;基态钛原子的最
外层电子为 ,所以最外层电子的电子云轮廓图为球形;
(4) 在火焰上灼烧时,火焰的颜色为砖红色,原因为电子从较高能量的激发态跃迁
到较低能量的激发态或基态时,以光的形式释放能量。
24.(10分)(2023春·福建莆田·高二莆田一中校考期中)我国磷资源储量丰富。回答下
列问题:
(1)已知亚磷酸(H PO )为二元弱酸,写出亚磷酸与过量 反应的化学方程式
3 3
___________;
(2)磷酸为磷的最高价含氧酸,其空间结构如图1所示:
①键能大小比较:磷氧双键___________(填“大于”“等于”或“小于”)磷氧单键。
②键角大小比较: ___________ (填“大于”“等于”或“小于”)。
③纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是___________。
(3)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图2所示①固态磷化硼属于___________(填“分子”“离子”或“共价”)晶体。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐
标。已知原子分数坐标:M点为(0,0,0)、G点为(1,1,1),则Q点的原子分数坐标为
___________。
③若晶胞参数为acm,则B与P之间的最短距离为___________cm(用含a的代数式表示)。
【答案】(1)
(2) 大于 小于 温度升高,磷酸分子间的氢键被破坏
(3) 共价
【解析】(1)亚磷酸(H PO )为二元弱酸,亚磷酸与过量 反应的化学方程式
3 3
;
(2)①键能大小比较:由图可知磷氧双键键长小于磷氧单键,故磷氧双键键能大于磷氧单
键键能;
②键角大小比较: 含有 键,对其他成键电子对的斥力较大,所以 小于;
③纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是温度升高,磷酸分子间的氢键
被破坏;
(3)①磷化硼(BP)是一种超硬耐磨涂层材料,硬度大,固态磷化硼属于共价晶体;
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐
标。已知原子分数坐标:M点为(0,0,0)、G点为(1,1,1),根据BP立方立方晶胞中相
邻的B与P之间的距离为晶胞体对角线的四分之一分析,则Q点的原子分数坐标为
。
③若晶胞参数为acm,则B与P之间的最短距离为顶点P与B原子的距离,为对角线的四
分之一,则长度为 cm。