文档内容
2023-2024 学年高一化学上学期期末测试卷 01
时间:75分钟 满分:100分 难度:基础
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Fe 56
选择题答题卡
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
答案
第Ⅰ卷(选择题 共 54 分)
一、选择题:本题共18个小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.化学与生产、生活密切相关。下列说法不正确的是
A.节日燃放的五彩缤纷的烟花,所呈现的是不同金属元素的焰色
B.某饮料属于纯天然食品,不含任何化学物质
C.碳酸钠可以用于纺织、造纸、制皂等工业
D.氧化铁是一种红棕色粉末,常用作油漆或涂料的红色颜料
2.(北京市房山区2022-2023学年高一上学期期末)下列物质分别加入水中,主要以离子形式存在的是
A.BaSO B.Cu C.HCl D.Fe O
4 2 3
3.(河北省张家口市2022-2023学年高一上学期期末)钚-239( Pu)裂变速度快,临界密度小,是核武
器重要的核装料。 中的质子数比中子数少
A.51 B.53 C.55 D.57
4.下列实验操作错误的是
A.用滤纸分离提纯氢氧化铁胶体
B.可用干燥的沙土扑灭着火的金属钠
C.制备 Fe(OH) 时将胶头滴管伸入 FeSO 溶液液面下再挤出 NaOH 溶液
2 4
D.将实验后剩余的金属钠块放回原试剂瓶中
5.(山东省聊城市2022-2023学年高一上学期期末)下列有关氯及其化合物的说法正确的是
A.氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白雾生成
B.测定新制氯水的pH操作是用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照
C.向FeCl 溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
2
D.漂白粉在空气中久置变质的原因是漂白粉中的CaCl 与空气中的CO 反应生成CaCO
2 2 3
6.(2023秋·重庆市合川中学高一校考期末)元素周期表是指导化学学习的工具,下列说法正确的是
A.IA族元素全部是金属元素,称为碱金属元素
B.元素周期表纵向看,由16个纵列构成,共16个族
C.元素周期表中元素种类最多的族是第ⅢB族
D.原子最外层有2个电子的元素都在ⅡA族
7.(河北省张家口市2022-2023学年高一上学期期末)下列离子方程式书写正确的是
A.Na与水反应:Na+2HO=Na++OH-+H↑
2 2
B.氢氧化铝和氢氧化钠溶液反应:Al(OH) +OH-= +HO
3 2C.Fe与稀硫酸反应:Fe+2H+=Fe3++H↑
2
D.FeCl 溶液腐蚀铜板:2Fe3++Cu=2Fe2++Cu2+
3
8.(甘肃省酒泉市2022-2023学年高一上学期期末)下列有关化学用语表示正确的是
A.中子数为7的氮原子: N
B.S2-的结构示意图:
C.NaHCO 在水中的电离方程式:NaHCO =Na++H++CO
3 3
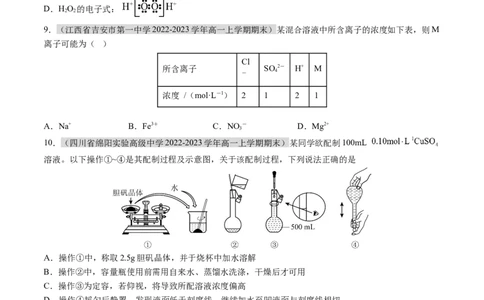
D.HO 的电子式:
2 2
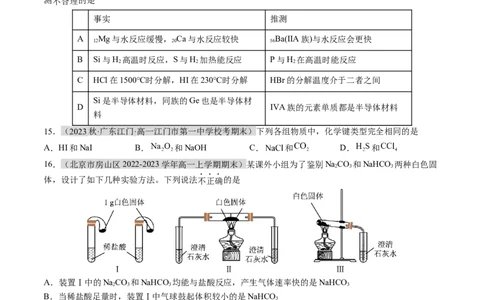
9.(江西省吉安市第一中学2022-2023学年高一上学期期末)某混合溶液中所含离子的浓度如下表,则M
离子可能为( )
Cl
所含离子 SO 2- H+ M
4
-
浓度 /(mol·L-1) 2 1 2 1
A.Na+ B.Fe3+ C.NO - D.Mg2+
3
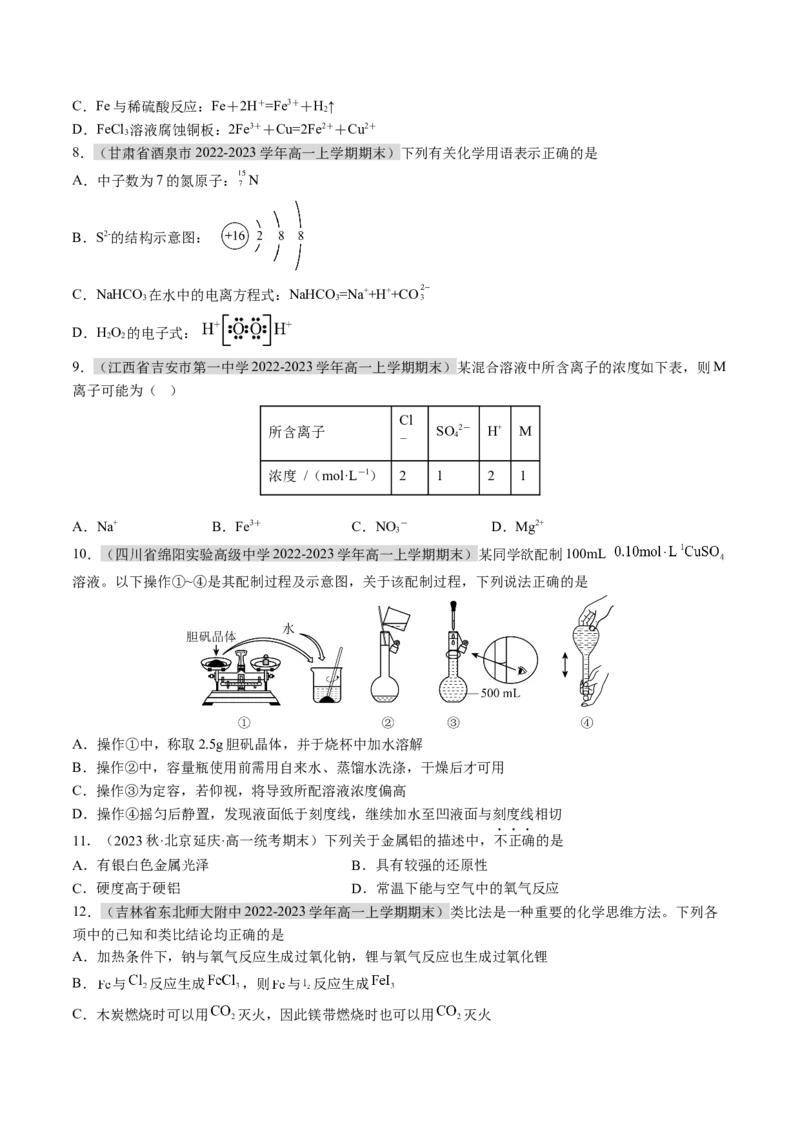
10.(四川省绵阳实验高级中学2022-2023学年高一上学期期末)某同学欲配制100mL
溶液。以下操作①~④是其配制过程及示意图,关于该配制过程,下列说法正确的是
A.操作①中,称取2.5g胆矾晶体,并于烧杯中加水溶解
B.操作②中,容量瓶使用前需用自来水、蒸馏水洗涤,干燥后才可用
C.操作③为定容,若仰视,将导致所配溶液浓度偏高
D.操作④摇匀后静置,发现液面低于刻度线,继续加水至凹液面与刻度线相切
11.(2023秋·北京延庆·高一统考期末)下列关于金属铝的描述中,不正确的是
A.有银白色金属光泽 B.具有较强的还原性
C.硬度高于硬铝 D.常温下能与空气中的氧气反应
12.(吉林省东北师大附中2022-2023学年高一上学期期末)类比法是一种重要的化学思维方法。下列各
项中的已知和类比结论均正确的是
A.加热条件下,钠与氧气反应生成过氧化钠,锂与氧气反应也生成过氧化锂
B. 与 反应生成 ,则 与 反应生成
C.木炭燃烧时可以用 灭火,因此镁带燃烧时也可以用 灭火D. 能与 溶液反应,则 也能与 溶液反应
13.(山东省济宁市2022-2023学年高一上学期期末)已知 为阿伏加德罗常数的值,下列说法错误的是
A. 比 多 个中子
B. 溶液中含有的O原子数目为
C. 和 的固体混合物中含有的阴离子数目为
D.标况下2.24L由 和CO组成的混合气体中含有的质子数为
14.(天津市第一中学2022-2023学年高一上学期期末)根据元素周期律,由下列事实进行归纳推测,推
测不合理的是
事实 推测
A Mg与水反应缓慢, Ca与水反应较快 Ba(ⅡA族)与水反应会更快
12 20 56
B Si与H 高温时反应,S与H 加热能反应 P与H 在高温时能反应
2 2 2
C HCl在1500℃时分解,HI在230℃时分解 HBr的分解温度介于二者之间
Si是半导体材料,同族的Ge也是半导体材
D ⅣA族的元素单质都是半导体材料
料
15.(2023秋·广东江门·高一江门市第一中学校考期末)下列各组物质中,化学键类型完全相同的是
A.HI和NaI B. 和NaOH C. 和 D. 和
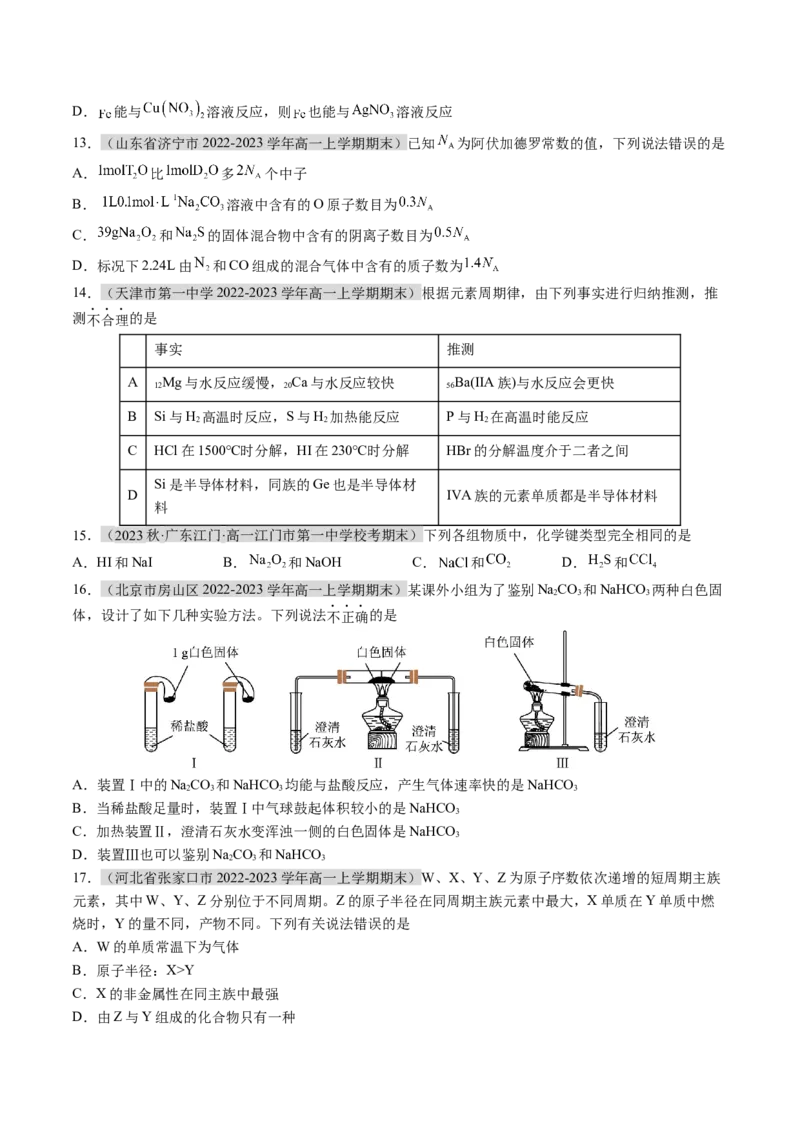
16.(北京市房山区2022-2023学年高一上学期期末)某课外小组为了鉴别NaCO 和NaHCO 两种白色固
2 3 3
体,设计了如下几种实验方法。下列说法不正确的是
A.装置Ⅰ中的NaCO 和NaHCO 均能与盐酸反应,产生气体速率快的是NaHCO
2 3 3 3
B.当稀盐酸足量时,装置Ⅰ中气球鼓起体积较小的是NaHCO
3
C.加热装置Ⅱ,澄清石灰水变浑浊一侧的白色固体是NaHCO
3
D.装置Ⅲ也可以鉴别NaCO 和NaHCO
2 3 3
17.(河北省张家口市2022-2023学年高一上学期期末)W、X、Y、Z为原子序数依次递增的短周期主族
元素,其中W、Y、Z分别位于不同周期。Z的原子半径在同周期主族元素中最大,X单质在Y单质中燃
烧时,Y的量不同,产物不同。下列有关说法错误的是
A.W的单质常温下为气体
B.原子半径:X>Y
C.X的非金属性在同主族中最强
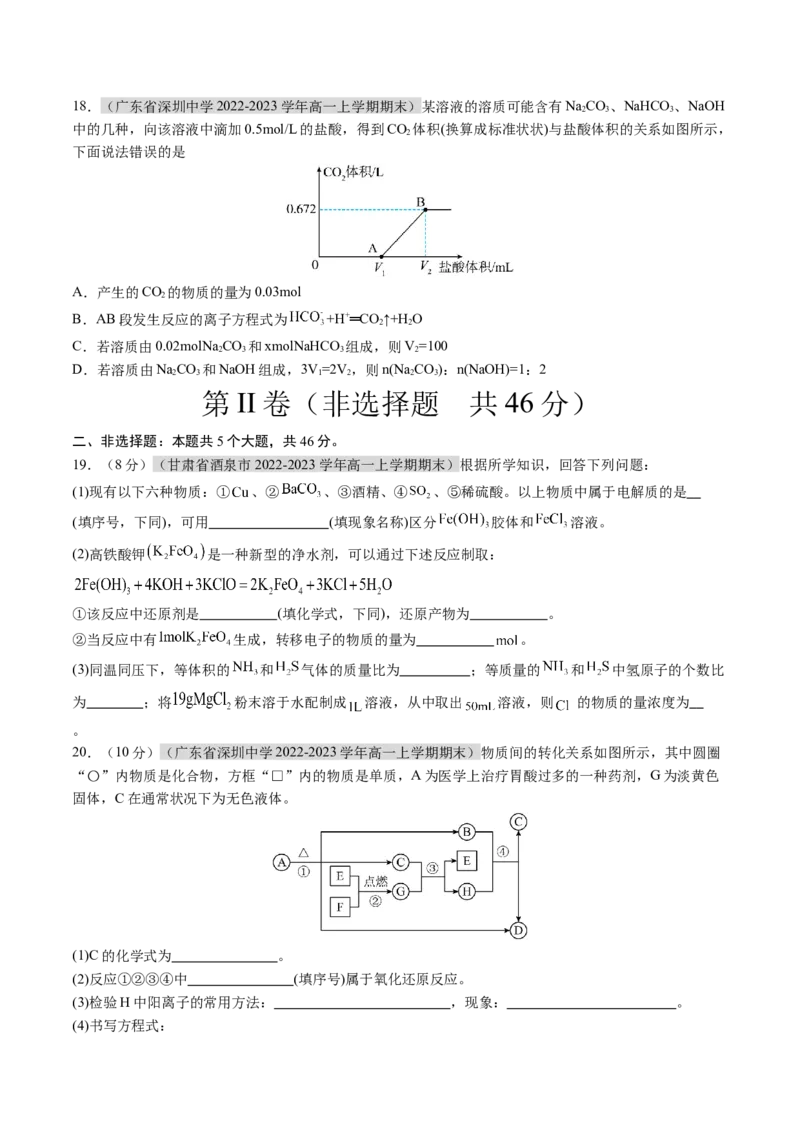
D.由Z与Y组成的化合物只有一种18.(广东省深圳中学2022-2023学年高一上学期期末)某溶液的溶质可能含有NaCO、NaHCO 、NaOH
2 3 3
中的几种,向该溶液中滴加0.5mol/L的盐酸,得到CO 体积(换算成标准状状)与盐酸体积的关系如图所示,
2
下面说法错误的是
A.产生的CO 的物质的量为0.03mol
2
B.AB段发生反应的离子方程式为 +H+═CO ↑+H O
2 2
C.若溶质由0.02molNa CO 和xmolNaHCO 组成,则V=100
2 3 3 2
D.若溶质由NaCO 和NaOH组成,3V=2V ,则n(Na CO):n(NaOH)=1:2
2 3 1 2 2 3
第 II 卷(非选择题 共 46 分)
二、非选择题:本题共5个大题,共46分。
19.(8分)(甘肃省酒泉市2022-2023学年高一上学期期末)根据所学知识,回答下列问题:
(1)现有以下六种物质:① 、② 、③酒精、④ 、⑤稀硫酸。以上物质中属于电解质的是
(填序号,下同),可用 (填现象名称)区分 胶体和 溶液。
(2)高铁酸钾 是一种新型的净水剂,可以通过下述反应制取:
①该反应中还原剂是 (填化学式,下同),还原产物为 。
②当反应中有 生成,转移电子的物质的量为 。
(3)同温同压下,等体积的 和 气体的质量比为 ;等质量的 和 中氢原子的个数比
为 ;将 粉末溶于水配制成 溶液,从中取出 溶液,则 的物质的量浓度为
。
20.(10分)(广东省深圳中学2022-2023学年高一上学期期末)物质间的转化关系如图所示,其中圆圈
“〇”内物质是化合物,方框“□”内的物质是单质,A为医学上治疗胃酸过多的一种药剂,G为淡黄色
固体,C在通常状况下为无色液体。
(1)C的化学式为 。
(2)反应①②③④中 (填序号)属于氧化还原反应。
(3)检验H中阳离子的常用方法: ,现象: 。
(4)书写方程式:①A与少量澄清石灰水反应的离子反应方程式: 。
②由D转化为H的化学反应方程式: 。
(5)若工业制得的D中混有少量A,用化学方程式表示提纯D的方法: 。
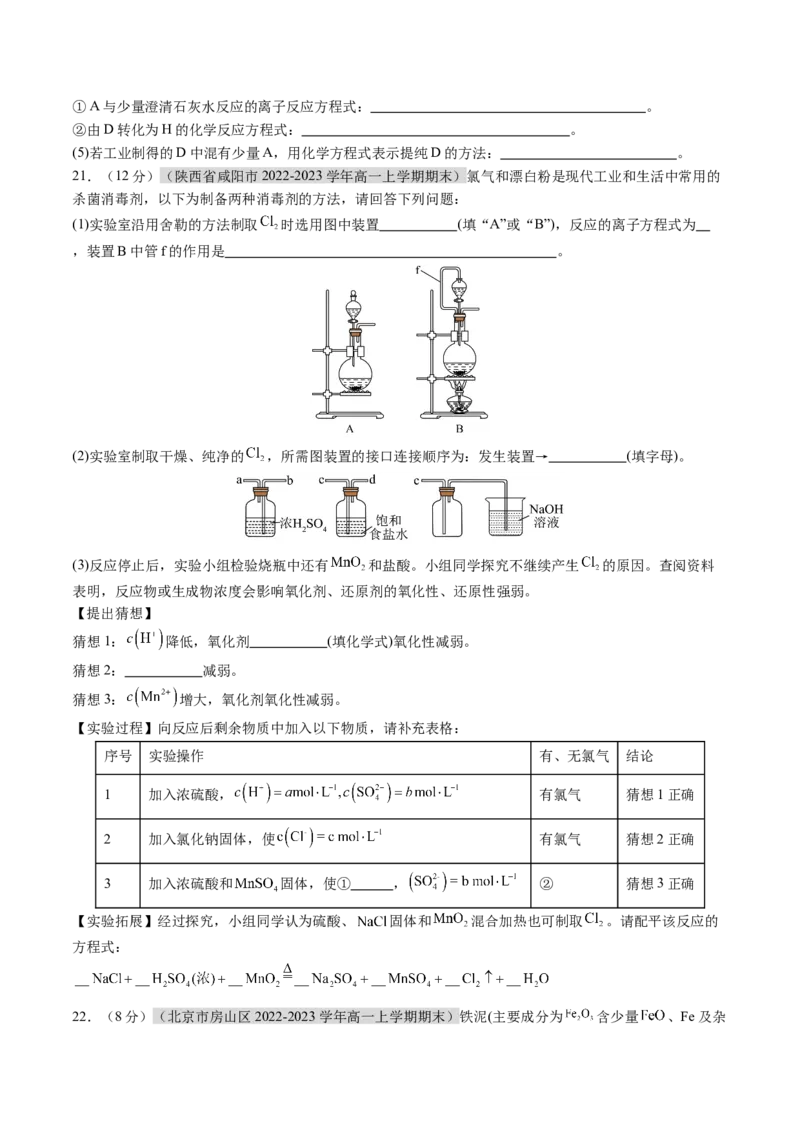
21.(12分)(陕西省咸阳市2022-2023学年高一上学期期末)氯气和漂白粉是现代工业和生活中常用的
杀菌消毒剂,以下为制备两种消毒剂的方法,请回答下列问题:
(1)实验室沿用舍勒的方法制取 时选用图中装置 (填“A”或“B”),反应的离子方程式为
,装置B中管f的作用是 。
(2)实验室制取干燥、纯净的 ,所需图装置的接口连接顺序为:发生装置→ (填字母)。
(3)反应停止后,实验小组检验烧瓶中还有 和盐酸。小组同学探究不继续产生 的原因。查阅资料
表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
【提出猜想】
猜想1: 降低,氧化剂 (填化学式)氧化性减弱。
猜想2: 减弱。
猜想3: 增大,氧化剂氧化性减弱。
【实验过程】向反应后剩余物质中加入以下物质,请补充表格:
序号 实验操作 有、无氯气 结论
1 加入浓硫酸, 有氯气 猜想1正确
2 加入氯化钠固体,使 有氯气 猜想2正确
3 加入浓硫酸和 固体,使① , ② 猜想3正确
【实验拓展】经过探究,小组同学认为硫酸、 固体和 混合加热也可制取 。请配平该反应的
方程式:
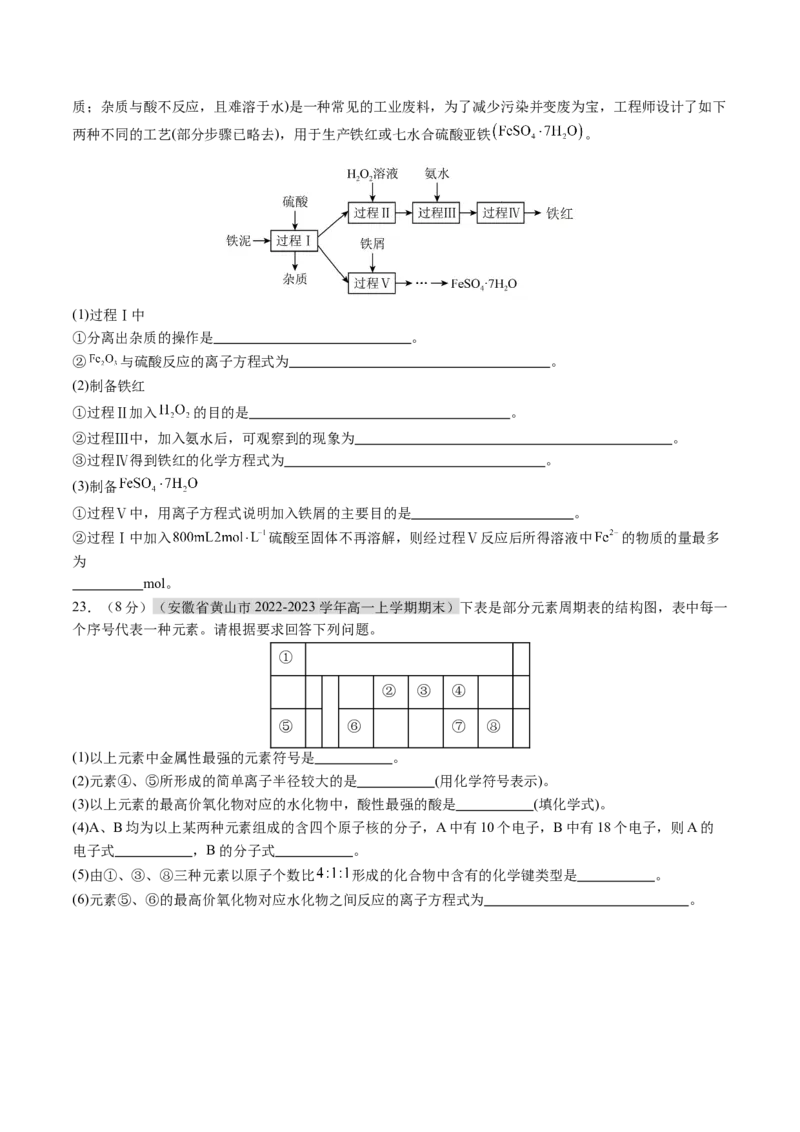
22.(8分)(北京市房山区2022-2023学年高一上学期期末)铁泥(主要成分为 含少量 、Fe及杂质;杂质与酸不反应,且难溶于水)是一种常见的工业废料,为了减少污染并变废为宝,工程师设计了如下
两种不同的工艺(部分步骤已略去),用于生产铁红或七水合硫酸亚铁 。
(1)过程Ⅰ中
①分离出杂质的操作是 。
② 与硫酸反应的离子方程式为 。
(2)制备铁红
①过程Ⅱ加入 的目的是 。
②过程Ⅲ中,加入氨水后,可观察到的现象为 。
③过程Ⅳ得到铁红的化学方程式为 。
(3)制备
①过程Ⅴ中,用离子方程式说明加入铁屑的主要目的是 。
②过程Ⅰ中加入 硫酸至固体不再溶解,则经过程Ⅴ反应后所得溶液中 的物质的量最多
为
mol。
23.(8分)(安徽省黄山市2022-2023学年高一上学期期末)下表是部分元素周期表的结构图,表中每一
个序号代表一种元素。请根据要求回答下列问题。
①
② ③ ④
⑤ ⑥ ⑦ ⑧
(1)以上元素中金属性最强的元素符号是 。
(2)元素④、⑤所形成的简单离子半径较大的是 (用化学符号表示)。
(3)以上元素的最高价氧化物对应的水化物中,酸性最强的酸是 (填化学式)。
(4)A、B均为以上某两种元素组成的含四个原子核的分子,A中有10个电子,B中有18个电子,则A的
电子式 ,B的分子式 。
(5)由①、③、⑧三种元素以原子个数比 形成的化合物中含有的化学键类型是 。
(6)元素⑤、⑥的最高价氧化物对应水化物之间反应的离子方程式为 。