文档内容
期末模拟测试 05
(时间:75分钟 满分:100分)
可能用到的相对原子质量:H 1 C 12 N14 O16 Si 28 P 31 Cl 35.5 K39 Mn55
第Ⅰ卷 选择题(共60分)
一 选择题 (本题包括20小题,每小题3分,共60分。每小题只有一个选项符合题意)
1.(2023春·甘肃兰州·高二兰州一中校考期中)对基态碳原子核外两个未成对电子的描述,
错误的是
A.电子云形状相同 B.自旋方向相同 C.能量相同 D.原子轨道取向相同
2.(2023春·黑龙江齐齐哈尔·高二统考期中)某元素基态原子的价电子排布式为 ,
该元素在周期表中的位置是
A.第三周期第ⅡB族,d区 B.第四周期第ⅡB族,ds区
C.第三周期第ⅦA族,d区 D.第四周期第ⅤB族,d区
3.(2023春·云南昆明·高二云南师大附中校考期中)下列关于Cu的说法正确的是
A.核外电子有29个空间运动状态
B.位于ⅠB族,属于ds区
C.基态Cu原子的价电子轨道表示式为
D.第一电离能比Zn大
4.(2023春·云南昆明·高二云南师大附中校考期中)下列化学用语正确的是
A.质量数为31的磷原子的原子结构示意图: B.顺-2-丁烯的结构简式:
C. 的电子云轮廓图 D. 的空间填充模型:
5.(2023春·北京海淀·高二人大附中校考期中)已知1~18号元素的4种简单离子 、
、 、 都具有相同电子层结构,下列关系正确的是
A.原子半径: B.电负性:
C.氢化物的稳定性: D.第一电离能:
6.(2023春·广东深圳·高二校联考期中)某多孔储氢材料前驱体结构如图,M、W、X、
Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对
电子。下列说法正确的是A.Y的氢化物为HY B.原子半径:MY>XC.W的最高价氧化物对应的水化物具有两性
D.W和Z可形成含有极性共价键的非极性分子
19.(2023春·江西景德镇·高二景德镇一中校考期中)由相邻短周期元素W、X、Y、Z组
成的穴状配体结构如图(部分W和X未标注);X、Y、Z同周期,W原子半径在周期表中最
小,下列说法错误的是
A.第一电离能:Y>Z>X B.W、X、Y三种元素可形成直线型化合物
C.X、Y、Z分别与W形成的简单化合物,其熔沸点在同主族元素中均为最高
D.含W、X、Y、Z元素的化合物,既可以形成分子晶体也可以形成离子晶体
20.(2023春·山东临沂·高二统考期中) 由于核外有空的d轨道,可与一些配体形成
配位数为6的配离子。某同学将淡紫色的 晶体溶于水后再依次加 和
,发现溶液出现下列变化:
已知: 为浅紫色, 为红色, 为无色。
下列说法错误的是
A.向溶液Ⅰ中加一定浓度稀硫酸,溶液颜色可由黄色逐渐变紫色
B. 与 形成配位键时,S原子提供孤电子对
C.溶液Ⅱ加 后溶液由红色变为无色,说明 与 配位键强度不及 与 配
位键强度
D. 中铁的杂化类型为 ,该离子的空间构型为平面正六边形
第Ⅱ卷 非选择题(共40分)
二、填空题
21.(10分)(2023春·全国·高二期中)根据要求填空
(1)选择下列物质填空(填写序号):①金刚石 ②干冰 ③氩晶体 ④白磷 ⑤CaBr ⑥NaH ⑦
2
KC ⑧石墨 ⑨氯化铵 ⑩铜晶体 熔化时不破坏化学键的有_______;含有非极性共价
3 60
键的有_______。
(2)性质比较:(填“>”、“=”或“<”,下同)
①第一电离能Mg_______Al,解释原因_______
②酸性强弱HClO_______HClO,解释原因_______
4 3(3)下图为几种晶体或晶胞的示意图(用名称填写)
①上述晶体中,粒子之间以共价键结合形成的晶体是_______。
②冰、金刚石、MgO、干冰4种晶体的熔点由高到低的顺序为_______。
22.(10分)(2023秋·内蒙古通辽·高二开鲁县第一中学校考期末)回答下列问题
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填标号)。
A.[Ne] B.[Ne] C.[Ne] D.[Ne]
(2)Fe成为阳离子时首先失去_______轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层
电子排布式为_______。
(3)Cu2+基态核外电子排布式为_______。
(4)Mn位于元素周期表中第四周期_______族,基态Mn原子核外未成对电子有_______个。
(5)基态Cl原子有_______种空间运动状态的电子,基态原子价电子排布式_______,属于
_______区(填“s”或“p”或“d”或“f”)
(6)LiBH 由Li+和BH 构成,与BH 互为等电子体的分子为_______,Li、Be、B元素的电
4
离能由大到小排列顺序为_______。
(7)1 mol HCHO分子中含有σ键的数目为_______N ,CS 分子中,存在_______个 键和
A 2
_______个 键。
23.(10分)(2023秋·广东汕头·高二汕头市聿怀中学校考期末)I.2020年12月17日,
我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、
锌、铜、锑、铼等矿物颗粒。
(1)写出铜的基态原子的电子排布式:______。
(2)基态Fe原子有______个未成对电子,Fe3+的电子排布式为______。
(3)Fe在周期表中位于第______周期第______族,属于______区。
Ⅱ.回答下列问题:
(4)p电子的原子轨道呈______形。
(5)基态Al3+核外共有______种不同运动状态的电子。
(6)钒(V)元素广泛用于催化及钢铁工业,其价层电子的轨道表示式为_______。
24.(10分)(2023春·全国·高二期中)卤素单质及其化合物在科研和工农业生产中有着
广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有_______(填标号)。
A. B. C.(2)O、F、Cl电负性由大到小的顺序为_______; 分子的空间构型为_______; 的熔、
沸点低于 ,原因是_______。
(3) (二氟氮烯)分子中,氮原子的杂化类型为 ,则 的结构式为_______。
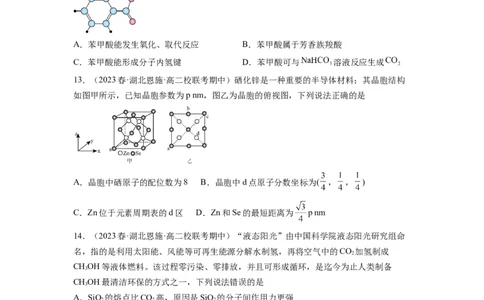
(4)萤石( )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是_______;
若该立方晶胞参数为a pm,正负离子的核间距最小为_______pm。
(5)NiO晶体与NaCl晶体结构相似。
①设阿伏加德罗常数的值为 ,距离最近的两个 间距为a pm,NiO的摩尔质量为M
g/mol,则NiO晶体的密度为_______ (列出计算式)。
②晶体普遍存在各种缺陷。某种NiO晶体中存在如图所示的缺陷:当一个 空缺,会有
两个 被两个 所取代,但晶体仍呈电中性。经测定某氧化镍样品中 与 的离
子数之比为6:91。若该晶体的化学式为 ,则x=_______。