文档内容
期中考测试(基础)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
1.(2023秋·广东河源·高一龙川县第一中学统考期末)在一定条件下,RO 和F 可发生如下反应:RO +
2
F +2OH-=RO +2F-+H O,从而可知在RO 中 ,元素R的化合价是
2 2
A.+4价 B.+5价
C.+6价 D.+7价
2.(2022春·广东深圳 )下列各组物质中符合“酸、碱、盐、酸性氧化物”顺序的是
A.H SO 、Na O、MgCl 、CO
2 4 2 2 2
B.NaHCO 、Ba(OH) 、Na CO 、ZnO
3 2 2 3
C.HNO 、Ca(OH) 、Na CO 、SO
3 2 2 3 3
D.HCl、KOH、Na CO 、MgO
2 3
3.(2023春·广东广州·高一统考开学考试)下列离子能大量共存的是
A.澄清透明的溶液中:Cu2+、 、Cl-、
B.含有大量Fe2+的溶液中:Na+、K+、 、ClO-
C.使酚酞溶液呈红色的溶液中:K+、Mg2+、 、Cl﹣
D.使紫色石蕊溶液呈红色的溶液中:Na+、Ba2+、 、
4.(2022秋·上海黄浦·高一上海市光明中学校考期中)下列关于摩尔质量的说法中,正确的是
A.水的摩尔质量是18g
B.1mol 的质量是32g/mol
C.任何物质的摩尔质量都等于它的相对原子(或分子)质量D.以 为单位时,水的摩尔质量是氢气的摩尔质量的9倍
5.(2023·广东东莞 )下列离子方程式正确的是
A.氢氧化钡溶液与稀硫酸反应 +Ba2++H++OH-=BaSO ↓+H O
4 2
B.铁与稀盐酸反应 2Fe+6H+=2Fe3++3H ↑
2
C.铜片插入硝酸银溶液:Cu+Ag+=Cu2++Ag
D.氧化镁与稀盐酸反应:MgO+2H+=Mg2++H O
2
6.(2023秋·广东 )中华文明源远流长,现代科技也迅猛发展。下列有关我国文明和科技的说法中不涉
及化学变化的是
D.制造“蛟龙”号潜
A.青铜器皿除锈 B.节日燃放烟花 C.利用核反应发电
水器
7.(2022秋·江苏盐城·高一盐城市大丰区新丰中学校考期中)下图是浓盐酸试剂瓶标签上的内容,关于一
定物质的量浓度的盐酸,下列说法正确的
A.0.5mol/L的盐酸溶液中,H+与Cl-的物质的量之和为1mol
B.100mL 0.1mol/L的盐酸中Cl-的物质的量浓度为0.1mol/L
C.将100mL6mol/L盐酸溶液敞口蒸发到体积为50mL后,溶液的浓度为12mol/L
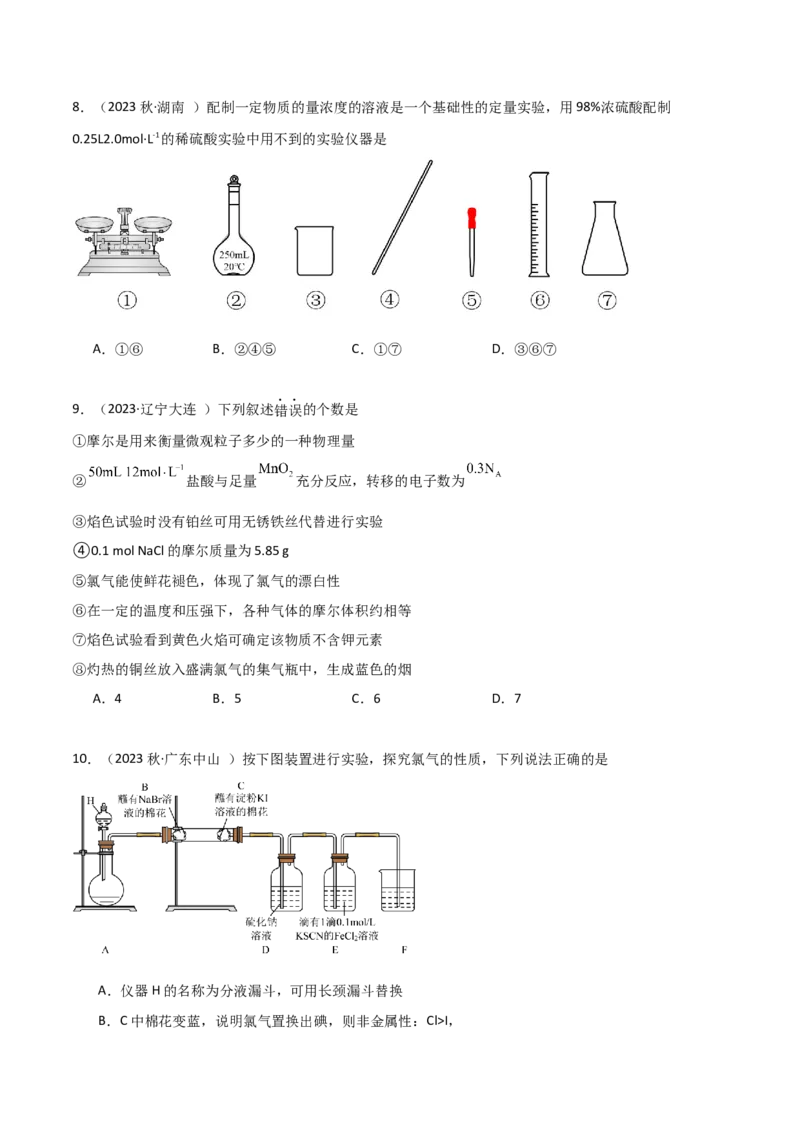
D.实验室用此浓盐酸配制240 mL 1mol/LHCl的盐酸溶液,经计算需要20.3mL浓盐酸8.(2023秋·湖南 )配制一定物质的量浓度的溶液是一个基础性的定量实验,用98%浓硫酸配制
0.25L2.0mol·L-1的稀硫酸实验中用不到的实验仪器是
A.①⑥ B.②④⑤ C.①⑦ D.③⑥⑦
9.(2023·辽宁大连 )下列叙述错误的个数是
①摩尔是用来衡量微观粒子多少的一种物理量
② 盐酸与足量 充分反应,转移的电子数为
③焰色试验时没有铂丝可用无锈铁丝代替进行实验
④0.1 mol NaCl的摩尔质量为5.85 g
⑤氯气能使鲜花褪色,体现了氯气的漂白性
⑥在一定的温度和压强下,各种气体的摩尔体积约相等
⑦焰色试验看到黄色火焰可确定该物质不含钾元素
⑧灼热的铜丝放入盛满氯气的集气瓶中,生成蓝色的烟
A.4 B.5 C.6 D.7
10.(2023秋·广东中山 )按下图装置进行实验,探究氯气的性质,下列说法正确的是
A.仪器H的名称为分液漏斗,可用长颈漏斗替换
B.C中棉花变蓝,说明氯气置换出碘,则非金属性:Cl>I,C.E中溶液先变红后褪色,说明Cl 有漂白性
2
D.F中溶液为NaOH溶液,进行尾气处理
11.(2022秋·广东东莞·高一东莞实验中学校考期中)下列实验操作、现象、结论均正确的是
选
实验操作 现象 结论
项
溶液蓝色褪去,有红色
A 将一小块金属钠加入至CuSO 溶液中 钠比铜还原性强,钠置换出铜
4 固体出现
B 向包裹 Na O 固体的棉花滴入蒸馏水 棉花燃烧起来 Na O 与水反应为放热反应
2 2 2 2
向待测液中先加入稀盐酸酸化,再加入
C 出现白色沉淀 待测液中含有Cl-
硝酸银溶液
向 NaI 溶液中滴加少量新制氯水,再 加入淀粉后溶液变成蓝 该过程主要发生反应:Cl +2I-
D 2
滴加淀粉溶液 色 =2Cl-+I
2
12.(2023·广东韶关 )下列从反应物到生成物能通过化合反应一步制得的是(其他反应物自选)
A.Al O →Al(OH) B.Fe(OH) →Fe(OH) C.Na O →NaOH D.NaAlO →Al(OH)
2 3 3 2 3 2 2 2 3
13.(2023·广东 )下列说法正确的是
A.SO 、Cl 都能使石蕊溶液先变红后褪色,但原理不同
2 2
B.向某溶液中加少量NaOH溶液后,未产生使湿润红色石蕊试纸变蓝的气体,说明溶液中无
C.用玻璃棒蘸取某溶液灼烧,观察到黄色火焰,说明该溶液中含有Na+
D.实验室不能用NH NO 与Ca(OH) 固体共热制氨气
4 3 2
14.(2023春·广东河源 )用如图所示的微型实验装置进行氯气性质探究。②~⑤是滴有相应溶液的滤纸
条,实验时滴几滴浓盐酸。下列说法错误的是A.②③处滤纸均先变红后褪色
B.④处滤纸变蓝色,推测氧化性:
C.⑤处发生反应: 、
D.浓盐酸与 反应体现浓盐酸的还原性和酸性
15.(2023·广东 )古代中国药学著作《开宝本草》中记载了如何提取硝酸钾:“此即地霜也,所在山泽,
冬月地上有霜,扫取以水淋汁后,乃煎炼而成”。下列有关叙述错误的是
A.硝酸钾用在黑火药中是利用了KNO 具有强氧化性,得到的还原产物为二氧化氮
3
B.“煎炼而成”是蒸发浓缩结晶
C.灼烧硝酸钾火焰呈紫色,是硝酸钾的物理性质
D.可用重结晶的方法分离提纯KNO 、NaCl的混合物
3
16.(2023·广东江门 )高铁酸钠 是一种新型绿色消毒剂,工业上制备高铁酸钠其中一种方法
的化学原理为: ,下列有关说法正确的是
A.高铁酸钠中铁元素化合价为+3价
B.上述反应中 作氧化剂
C.还原产物与氧化产物的物质的量之比为2:3
D.每生成 转移3mol电子
二、非选择题:共56分。
17.(2023·河北保定)(16分)根据要求,回答下列问题:
Ⅰ. 从铁、盐酸、氧气、过氧化氢、硝酸银溶液五种物质中选出一种或两种为反应物,按下列反应类型各写出一个化学方程式。
(1)化合反应: 。
(2)分解反应: 。
(3)置换反应: 。
(4)复分解反应: 。
Ⅱ. 按下列要求各写出一个化学方程式。
(5)有水生成的化合反应: 。
(6)生成一种碱性氧化物和一种酸性氧化物的分解反应: 。
(7)有硝酸银参加反应生成硝酸铜的置换反应: 。
(8)生成两种沉淀的复分解反应: 。
18.(2023·湖北黄冈 )(12分)“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品有:①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。将上
述物质分别溶于水,其水溶液具有碱性的是 (填序号,下同),主要成分中属于盐类的是 ,
相互间能发生反应的是 。
(2)生活中遇到下列问题,不涉及到化学变化的是 。
①用四氯化碳可擦去圆珠笔油 ②自来水厂用液氯消毒 ③可用食醋洗掉水垢
(3)当前,环境治理已成为重要的民生工程。
①我国城市发布的“空气质量日报”中,下列物质不列入首要污染物的是 (填字母代号)。
A.二氧化硫 B.二氧化碳 C.二氧化氮 D.可吸入颗粒物
②煤炭直接燃烧会引起多种环境问题。燃煤产生的SO 是导致 (填名称)污染现象形成的原因;处
2
理含CO、SO 烟道气污染的一种方法是将其在催化剂作用下转化为单质S,发生反应的化学方程式为
2
。
(4)向浑浊的水中加入明矾KAl(SO ) •12H O后,水可得到净化。写出明矾在水中的电离方程式 ,往明
4 2 2
矾溶液中逐滴加入Ba(OH) 溶液直至Al3+恰好沉淀完全,发生反应的离子方程式为 。
2
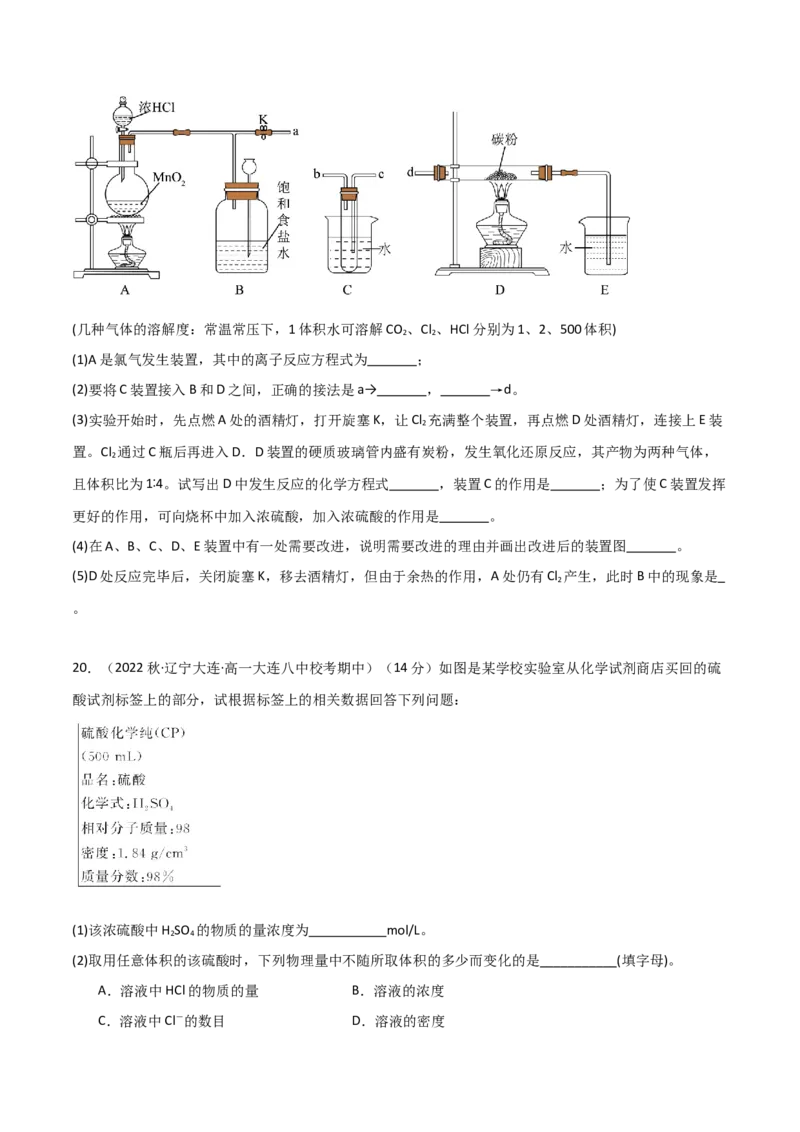
19.(2023秋·高一课时练习)(14分)如图是一个制取氯气并以氯气为原料进行特定反应的装置:(几种气体的溶解度:常温常压下,1体积水可溶解CO 、Cl 、HCl分别为1、2、500体积)
2 2
(1)A是氯气发生装置,其中的离子反应方程式为 ;
(2)要将C装置接入B和D之间,正确的接法是a→ , →d。
(3)实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl 充满整个装置,再点燃D处酒精灯,连接上E装
2
置。Cl 通过C瓶后再进入D.D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为两种气体,
2
且体积比为1∶4。试写出D中发生反应的化学方程式 ,装置C的作用是 ;为了使C装置发挥
更好的作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是 。
(4)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由并画出改进后的装置图 。
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl 产生,此时B中的现象是
2
。
20.(2022秋·辽宁大连·高一大连八中校考期中)(14分)如图是某学校实验室从化学试剂商店买回的硫
酸试剂标签上的部分,试根据标签上的相关数据回答下列问题:
(1)该浓硫酸中H SO 的物质的量浓度为 mol/L。
2 4
(2)取用任意体积的该硫酸时,下列物理量中不随所取体积的多少而变化的是___________(填字母)。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度实验室欲用上述浓硫酸和蒸馏水配制80 mL 2.2 mol·L-1的稀硫酸:
(3)完成本实验所必需的仪器有:托盘天平(或电子天平)、药匙、烧杯、玻璃棒、量筒、① 、胶头滴
管以及称量纸等。
(4)配制溶液前必须进行的操作是 。
(5)操作步骤如下:用100 mL量筒量取18.4 mol·L-1的浓硫酸 mL,将浓硫酸沿烧杯内壁缓缓注
入盛有蒸馏水的烧杯中,并不断用玻璃棒搅拌。搅拌均匀后立即沿玻璃棒注入①中,用蒸馏水洗涤烧杯和
玻璃棒,洗涤液转移至①中,重复操作2~3次,继续用烧杯向①中加入蒸馏水,使溶液的凹液面恰好与刻
度线相切,盖上瓶塞后摇匀,装入试剂瓶中。实验操作中存在的错误有 处。
(6)下列操作会使所配溶液浓度偏低的是 (填字母)。
A.定容时仰视读数
B.量筒量取浓硫酸时俯视读数
C.容量瓶用蒸馏水洗净后仍残留有蒸馏水
D.量取浓硫酸的量筒没洗涤
E.定容摇匀后,发现液面低于刻度线,再加水至刻度线
(7)若把配制好的硫酸与等质量的水混合所得溶液的物质的量分数 (填大于,等于或小于)1.1
mol·L-1。