文档内容
2023−2024 学年上学期期中模拟考试 01
高一化学
时间:75分钟 满分:100分 测试范围:第五、六章
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5
第Ⅰ卷(选择题 共 60 分)
一、选择题:本题共20个小题,每小题3分,共60分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.(22-23高一下·广东茂名·期中)我国在科技上不断取得重大成果。下列各项中使用的材料不属于无机
非金属材料的是
A.“神舟十四 B.“嫦娥五号”探测器
C.用于吊装港珠澳大桥的 D.应用于5G手机中
号”上搭载的石英 使用的砷化镓太阳能电
超高分子量聚乙烯纤维吊绳 的石墨烯导热膜
挠性加速度计 池板
2.(23-24高一上·重庆·期中)下列溶液中,能大量共存的离子组是
A.含有 的溶液中:
B.加入足量 的溶液中:
C.在透明的溶液中:
D.强碱性溶液中:
3.(23-24高一上·广东深圳·期中)下列描述对应的离子方程式正确的是
A.钠投入冷水中:Na+HO=Na+ + OH− + H ↑
2 2
B.硫酸氢钠在水中的电离:NaHSO=Na+ + HSO
4
C.氢硫酸中滴加双氧水:HO + 2H+ +S2−=2HO + S↓
2 2 2
D.少量CO 通入澄清石灰水中:Ca2+ + 2OH− + CO=CaCO ↓ + H O
2 2 3 2
4.(22-23高一下·贵州铜仁·期中)氮是生命的基础,氮及其化合物在生产生活中具有广泛应用。实验室
可选用下列装置和试剂制备氨气,并干燥、收集和处理尾气,下列说法正确的是
A.①和②均可用于实验室制备氨气
B.③中盛有碱石灰或无水氯化钙可用于干燥氨气C.④可用于收集氨气,气流方向为a进b出
D.⑤中盛有稀硫酸可用于氨气的尾气处理
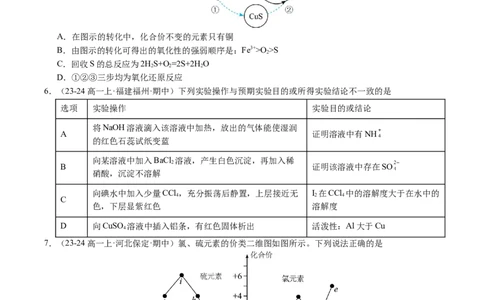
5.(23-24高一上·上海·期中)将HS和空气的混合气体通入FeCl 、FeCl 、CuCl 的混合溶液中反应回收
2 3 2 2
S,如图所示,下列说法正确的是
A.在图示的转化中,化合价不变的元素只有铜
B.由图示的转化可得出的氧化性的强弱顺序是:Fe3+>O >S
2
C.回收S的总反应为2HS+O=2S+2H O
2 2 2
D.①②③三步均为氧化还原反应
6.(23-24高一上·福建福州·期中)下列实验操作与预期实验目的或所得实验结论不一致的是
选项 实验操作 实验目的或结论
将NaOH溶液滴入该溶液中加热,放出的气体能使湿润
A 证明溶液中有NH
的红色石蕊试纸变蓝
向某溶液中加入BaCl 溶液,产生白色沉淀,再加入稀
2
B 证明该溶液中存在SO
硝酸,沉淀不溶解
向碘水中加入少量CCl ,充分振荡后静置,上层接近无 I 在CCl 中的溶解度大于在水中的
4 2 4
C
色,下层显紫红色 溶解度
D 向CuSO 溶液中插入铝条,有红色固体析出 活泼性:Al大于Cu
4
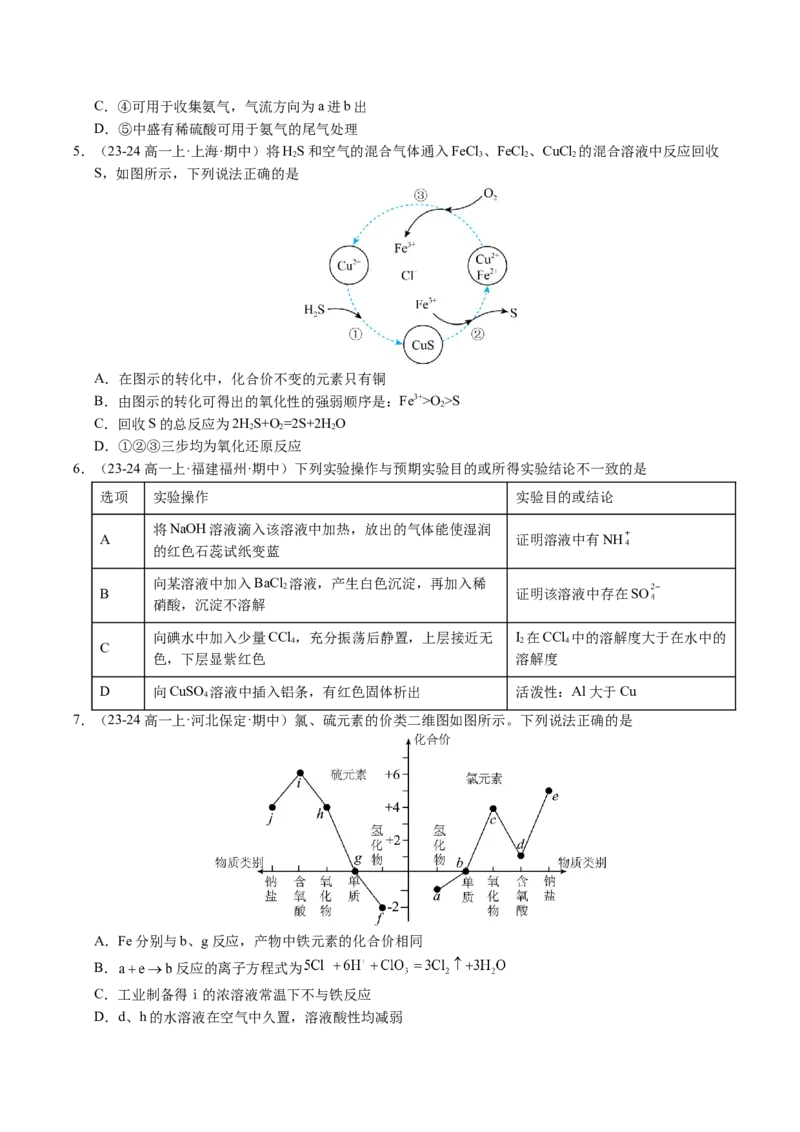
7.(23-24高一上·河北保定·期中)氯、硫元素的价类二维图如图所示。下列说法正确的是
A.Fe分别与b、g反应,产物中铁元素的化合价相同
B. 反应的离子方程式为
C.工业制备得ⅰ的浓溶液常温下不与铁反应
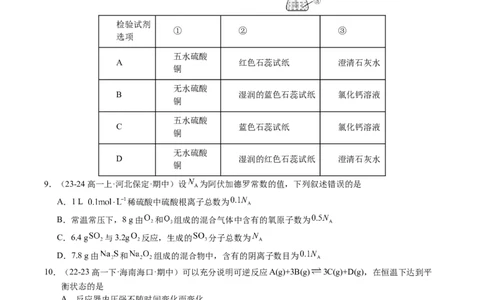
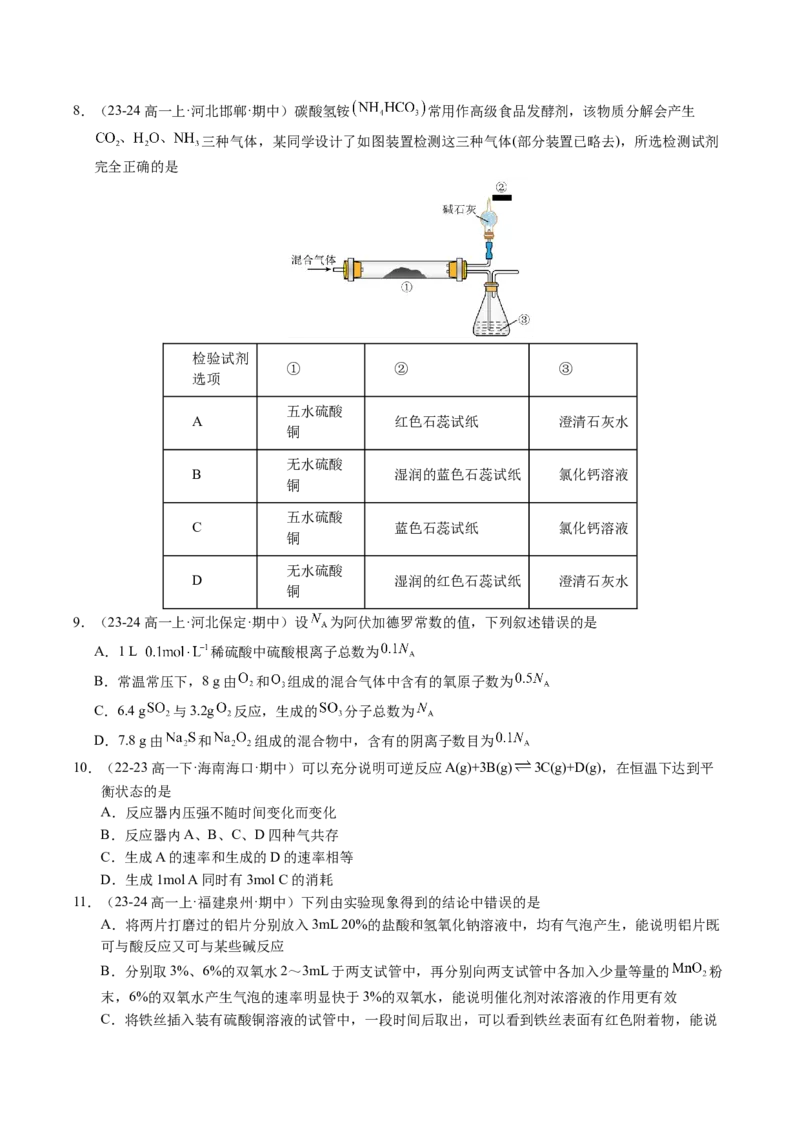
D.d、h的水溶液在空气中久置,溶液酸性均减弱8.(23-24高一上·河北邯郸·期中)碳酸氢铵 常用作高级食品发酵剂,该物质分解会产生
三种气体,某同学设计了如图装置检测这三种气体(部分装置已略去),所选检测试剂
完全正确的是
检验试剂
① ② ③
选项
五水硫酸
A 红色石蕊试纸 澄清石灰水
铜
无水硫酸
B 湿润的蓝色石蕊试纸 氯化钙溶液
铜
五水硫酸
C 蓝色石蕊试纸 氯化钙溶液
铜
无水硫酸
D 湿润的红色石蕊试纸 澄清石灰水
铜
9.(23-24高一上·河北保定·期中)设 为阿伏加德罗常数的值,下列叙述错误的是
A.1 L 稀硫酸中硫酸根离子总数为
B.常温常压下,8 g由 和 组成的混合气体中含有的氧原子数为
C.6.4 g 与3.2g 反应,生成的 分子总数为
D.7.8 g由 和 组成的混合物中,含有的阴离子数目为
10.(22-23高一下·海南海口·期中)可以充分说明可逆反应A(g)+3B(g) 3C(g)+D(g),在恒温下达到平
衡状态的是
A.反应器内压强不随时间变化而变化
B.反应器内A、B、C、D四种气共存
C.生成A的速率和生成的D的速率相等
D.生成1mol A同时有3mol C的消耗
11.(23-24高一上·福建泉州·期中)下列由实验现象得到的结论中错误的是
A.将两片打磨过的铝片分别放入3mL 20%的盐酸和氢氧化钠溶液中,均有气泡产生,能说明铝片既
可与酸反应又可与某些碱反应
B.分别取3%、6%的双氧水2~3mL于两支试管中,再分别向两支试管中各加入少量等量的 粉
末,6%的双氧水产生气泡的速率明显快于3%的双氧水,能说明催化剂对浓溶液的作用更有效
C.将铁丝插入装有硫酸铜溶液的试管中,一段时间后取出,可以看到铁丝表面有红色附着物,能说明铁比铜更活泼
D.取15%的双氧水2~3mL于试管中,只有少量气泡产生,如果将试管置于75℃的热水中,气泡会
明显增多,能说明温度升高反应会加快
12.(22-23高一下·河北衡水·期中)在 的反应中,下列选项表示的化学反
应速率最快的是
A.v(X)=0.6mol·L-1·min-1 B.v(Z)=0.1mol·L-1·s-1
C.v(Y)=0.2mol·L-1·min-1 D.v(Q)=0.15nmol·L-1·min-1
13.(22-23高一下·广东东莞·期中)一种NO-空气燃料电池的工作原理如图所示,该电池工作时,下列说
法正确的是
A.负极的电极反应式为NO-3e-+2H O=NO +4H+
2
B.H+通过质子交换膜向左侧多孔石墨棒移动
C.若产生lmolHNO ,则通入O 的体积应大于16.8L
3 2
D.电子的流动方向:负极→电解质溶液→正极
14.(23-24高一上·江苏盐城·期中)某固体可能含有Na+、Ba2+、 、Cl-、 、 中的几种离子,
取等质量的两份该固体,进行如下实验:
(1)一份固体溶于水,加入足量BaCl 溶液,得沉淀2.33g;过滤后加盐酸沉淀不溶解。
2
(2)另一份固体溶于水,与过量NaOH溶液混合后充分加热,只产生使湿润的红色石蕊试纸变蓝色
的气体(NH )0.672L(标准状况)。已知 +OH- NH +H O。下列说法正确的是
3 3 2
A.该固体中一定含有NH 、Cl-、SO 、Na+
B.根据以上实验,无法确定该固体中是否含有CO
C.Cl-一定存在且n(Cl-)≥0.01mol
D.该固体中一定没有Na+、CO
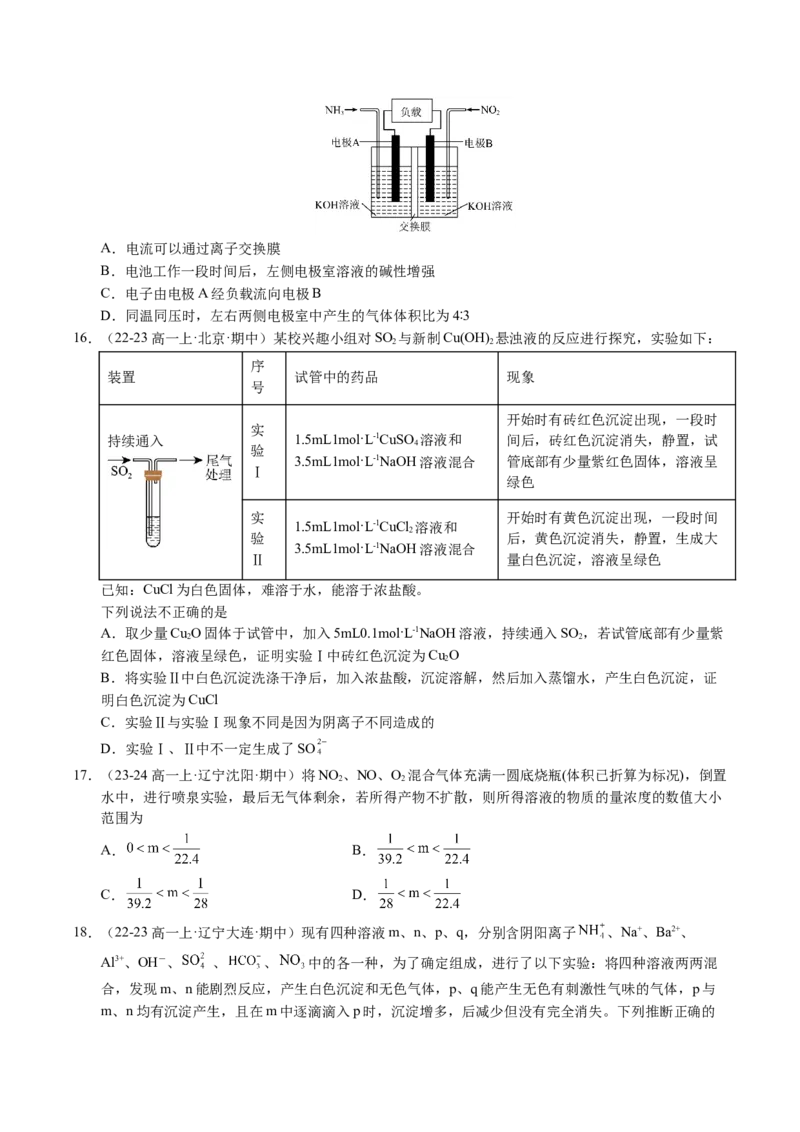
15.(22-23高一下·山东青岛·期末)为有效降低含氮化物的排放量,又能充分利用化学能,合作小组利用
反应 设计如图所示电池(离子交换膜对溶液里的离子具有选择透过能力)。
下列说法错误的是A.电流可以通过离子交换膜
B.电池工作一段时间后,左侧电极室溶液的碱性增强
C.电子由电极A经负载流向电极B
D.同温同压时,左右两侧电极室中产生的气体体积比为4∶3
16.(22-23高一上·北京·期中)某校兴趣小组对SO 与新制Cu(OH) 悬浊液的反应进行探究,实验如下:
2 2
序
装置 试管中的药品 现象
号
开始时有砖红色沉淀出现,一段时
实
持续通入 1.5mL1mol·L-1CuSO 溶液和 间后,砖红色沉淀消失,静置,试
4
验
3.5mL1mol·L-1NaOH溶液混合 管底部有少量紫红色固体,溶液呈
Ⅰ
绿色
实 开始时有黄色沉淀出现,一段时间
1.5mL1mol·L-1CuCl 溶液和
2
验 后,黄色沉淀消失,静置,生成大
3.5mL1mol·L-1NaOH溶液混合
Ⅱ 量白色沉淀,溶液呈绿色
已知:CuCl为白色固体,难溶于水,能溶于浓盐酸。
下列说法不正确的是
A.取少量Cu O固体于试管中,加入5mL0.1mol·L-1NaOH溶液,持续通入SO ,若试管底部有少量紫
2 2
红色固体,溶液呈绿色,证明实验Ⅰ中砖红色沉淀为Cu O
2
B.将实验Ⅱ中白色沉淀洗涤干净后,加入浓盐酸,沉淀溶解,然后加入蒸馏水,产生白色沉淀,证
明白色沉淀为CuCl
C.实验Ⅱ与实验Ⅰ现象不同是因为阴离子不同造成的
D.实验Ⅰ、Ⅱ中不一定生成了SO
17.(23-24高一上·辽宁沈阳·期中)将NO 、NO、O 混合气体充满一圆底烧瓶(体积已折算为标况),倒置
2 2
水中,进行喷泉实验,最后无气体剩余,若所得产物不扩散,则所得溶液的物质的量浓度的数值大小
范围为
A. B.
C. D.
18.(22-23高一上·辽宁大连·期中)现有四种溶液m、n、p、q,分别含阴阳离子 、Na+、Ba2+、
Al3+、OH-、 、 、 中的各一种,为了确定组成,进行了以下实验:将四种溶液两两混
合,发现m、n能剧烈反应,产生白色沉淀和无色气体,p、q能产生无色有刺激性气味的气体,p与
m、n均有沉淀产生,且在m中逐滴滴入p时,沉淀增多,后减少但没有完全消失。下列推断正确的是
A.p是Ba(OH) B.q 是NH HCO C.n是Al (SO ) D.m 是Al(NO )
2 4 3 2 4 3 3 3
19.(23-24高一上·河北衡水·期中)一定温度下,10mL0.8 溶液发生催化分解。不同时刻测
得生成的 的体积(已折算为标准状况下)如表。
t/min 0 2 4 6 8 10
0.0 9.9 17.2 22.4 26.5 29.9
下列叙述正确的是(溶液体积变化忽略不计)
A.反应到6min时,
B.第4min时的瞬时速率小于第6min时的瞬时速率
C.反应至6min时, 分解率为50%
D.0~6min的平均反应速率:
20.(22-23高一下·广东东莞·期中)一种NO-空气燃料电池的工作原理如图所示,该电池工作时,下列说
法正确的是
A.负极的电极反应式为NO-3e-+2H O=NO +4H+
2
B.H+通过质子交换膜向左侧多孔石墨棒移动
C.若产生lmolHNO ,则通入O 的体积应大于16.8L
3 2
D.电子的流动方向:负极→电解质溶液→正极
第 II 卷(非选择题 共 40 分)
三、非选择题:本题共4个大题,共40分。
21.(10分)(22-23高一下·山东青岛·期末)图一所示是一个燃料电池的示意图,a、b表示通入的气体,
当此燃料电池工作时:
(1)如果a极通入H,b极通入O,HSO 溶液作电解质溶液,则相同时间内,正极和负极通入的气
2 2 2 4体的体积比为: 。(设气体为同温、同压)
(2)如果a极通入CH,b极通入O,NaOH溶液作电解质溶液,则通CH 的电极上的电极反应为:
4 2 4
。
(3)如果a极通入乙烯,b极通入O,HSO 溶液作电解质溶液,则通乙烯的电极上的电极反应为:
2 2 4
。
(4)某原电池装置初始状态如图二所示,交换膜两侧的溶液体积均为2L,该电池总反应为 ,
当电路中转移1mol电子时,共有 mol离子通过交换膜,交换膜右侧溶液中c(HCl)=
mol•L-1(忽略溶液体积变化和Cl 溶于水)。
2
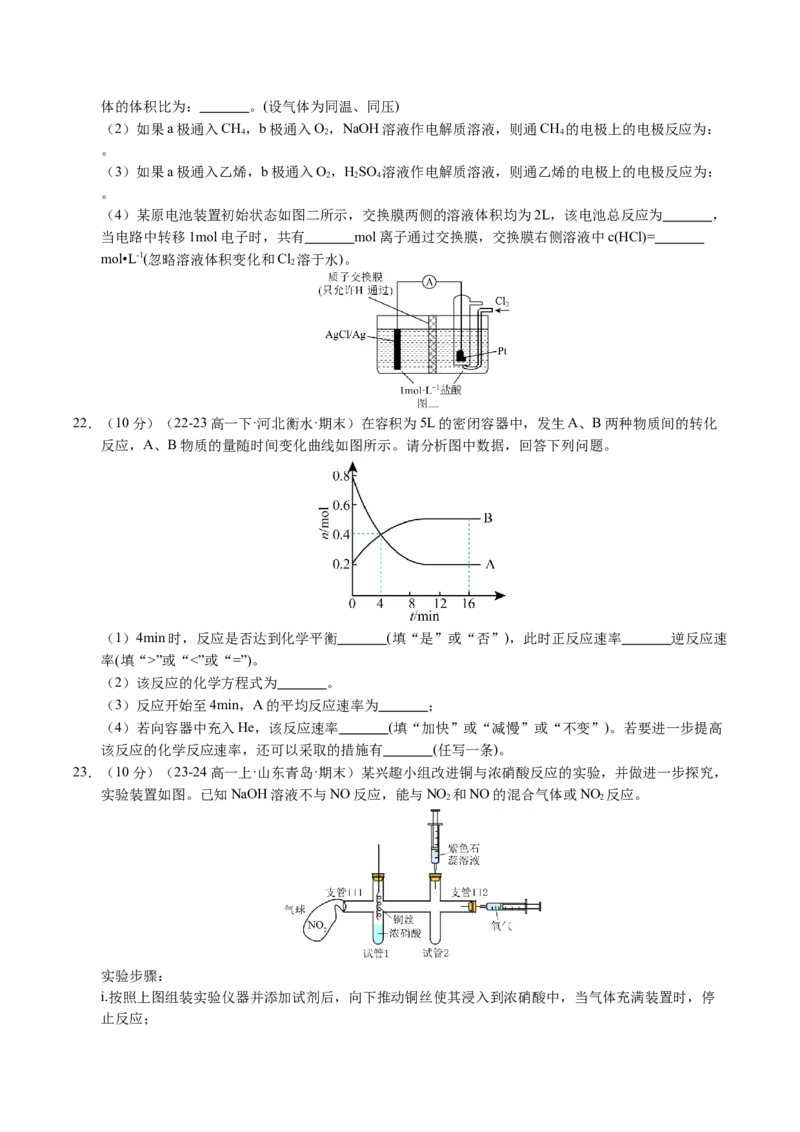
22.(10分)(22-23高一下·河北衡水·期末)在容积为5L的密闭容器中,发生A、B两种物质间的转化
反应,A、B物质的量随时间变化曲线如图所示。请分析图中数据,回答下列问题。
(1)4min时,反应是否达到化学平衡 (填“是”或“否”),此时正反应速率 逆反应速
率(填“>”或“<”或“=”)。
(2)该反应的化学方程式为 。
(3)反应开始至4min,A的平均反应速率为 ;
(4)若向容器中充入He,该反应速率 (填“加快”或“减慢”或“不变”)。若要进一步提高
该反应的化学反应速率,还可以采取的措施有 (任写一条)。
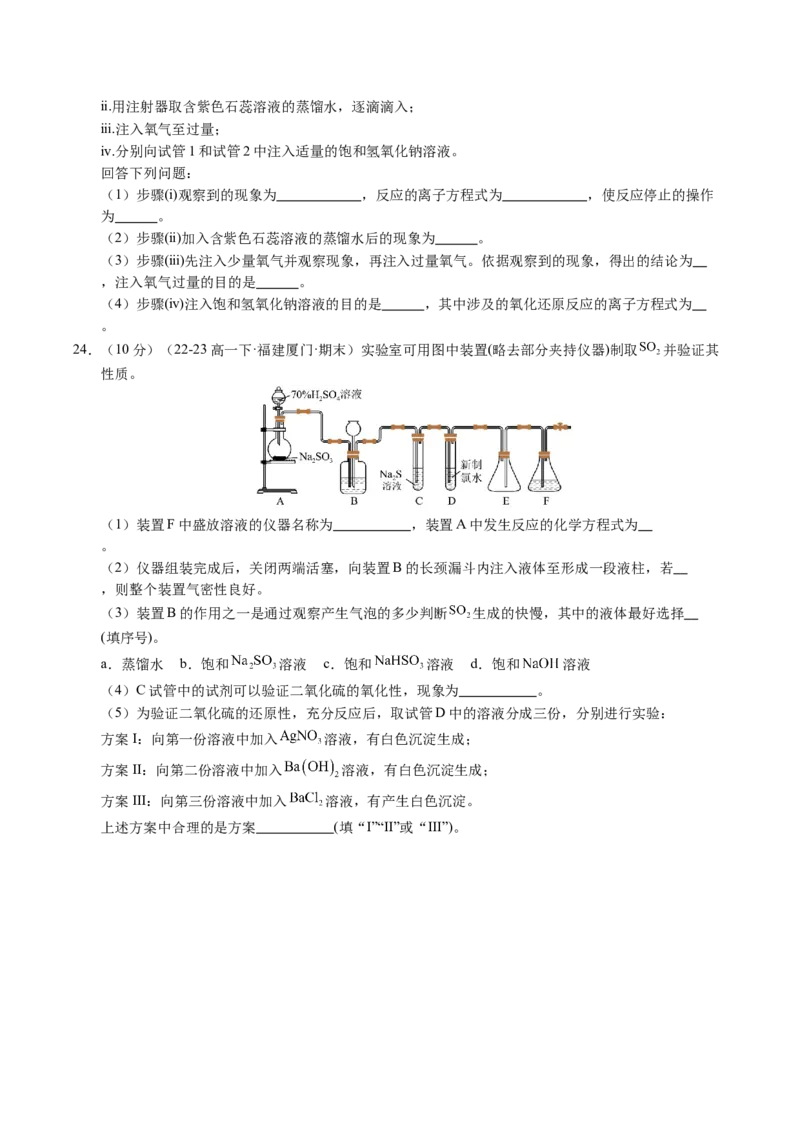
23.(10分)(23-24高一上·山东青岛·期末)某兴趣小组改进铜与浓硝酸反应的实验,并做进一步探究,
实验装置如图。已知NaOH溶液不与NO反应,能与NO 和NO的混合气体或NO 反应。
2 2
实验步骤:
ⅰ.按照上图组装实验仪器并添加试剂后,向下推动铜丝使其浸入到浓硝酸中,当气体充满装置时,停
止反应;ⅱ.用注射器取含紫色石蕊溶液的蒸馏水,逐滴滴入;
ⅲ.注入氧气至过量;
ⅳ.分别向试管1和试管2中注入适量的饱和氢氧化钠溶液。
回答下列问题:
(1)步骤(ⅰ)观察到的现象为 ,反应的离子方程式为 ,使反应停止的操作
为 。
(2)步骤(ⅱ)加入含紫色石蕊溶液的蒸馏水后的现象为 。
(3)步骤(ⅲ)先注入少量氧气并观察现象,再注入过量氧气。依据观察到的现象,得出的结论为
,注入氧气过量的目的是 。
(4)步骤(ⅳ)注入饱和氢氧化钠溶液的目的是 ,其中涉及的氧化还原反应的离子方程式为
。
24.(10分)(22-23高一下·福建厦门·期末)实验室可用图中装置(略去部分夹持仪器)制取 并验证其
性质。
(1)装置F中盛放溶液的仪器名称为 ,装置A中发生反应的化学方程式为
。
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若
,则整个装置气密性良好。
(3)装置B的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择
(填序号)。
a.蒸馏水 b.饱和 溶液 c.饱和 溶液 d.饱和 溶液
(4)C试管中的试剂可以验证二氧化硫的氧化性,现象为 。
(5)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入 溶液,有白色沉淀生成;
方案II:向第二份溶液中加入 溶液,有白色沉淀生成;
方案III:向第三份溶液中加入 溶液,有产生白色沉淀。
上述方案中合理的是方案 (填“I”“II”或“III”)。