文档内容
2023−2024 学年上学期期中模拟考试 02
高一化学
时间:75分钟 满分:100分 测试范围:第五、六章
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5
第Ⅰ卷(选择题 共 60 分)
一、选择题:本题共20个小题,每小题3分,共60分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.(22-23高一下·云南丽江·期中)生活与能量转化息息相关,下列能量转化是由化学能直接转化为电能
的是
A.燃料电池电动车 B.风力发电 C.使用天然气燃气灶 D.火力发电
2.(22-23高一下·陕西商洛·期中)在四个不同的容器中,不同条件下进行的合成氨反应N+3H
2 2
2NH ,其中生成氨气速率最快的是
3
A.v(N )=0.3 mol·L-1·min-1 B.v(NH )=0.5 mol·L-1·min-1
2 3
C.v(H )=0.01 mol·L-1·s-1 D.v(N )=0.2 mol·L-1·min-1
2 2
3.(22-23高一下·山东济南·期中)利用太阳光在新型复合催化剂表面实现高效分解水,其主要过程如图
所示:
下列说法错误的是
A.整个过程实现了光能向化学能的转换
B.过程Ⅰ是氧化还原反应
C.过程Ⅰ吸收能量,过程Ⅱ放出能量
D.反应物总能量小于生成物的总能量
4.(22-23高一下·海南海口·期中)将镁带投入盛放在敞口容器内的盐酸里,反应速率用产生的氢气的速
率表示,在下列因素中:①盐酸的浓度②镁带的表面积③溶液的温度④盐酸的体积⑤氯离子的浓度,
影响反应速率的因素是
A.①④ B.③⑤ C.①②③⑤ D.①②③
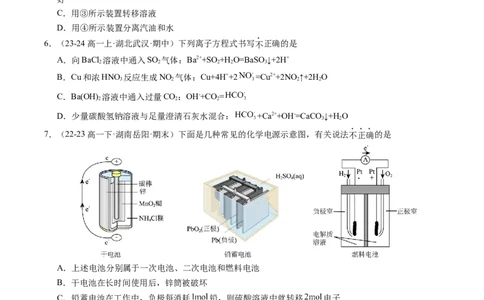
5.(23-24高一上·福建福州·期中)下列有关实验装置或操作说法正确的是A.用①所示装置检验样品中是否含有
B.装置②中,向长颈漏斗中加一定量水,并形成水柱,随后水柱下降至与瓶中液面相平,说明气密性
好
C.用③所示装置转移溶液
D.用④所示装置分离汽油和水
6.(23-24高一上·湖北武汉·期中)下列离子方程式书写不正确的是
A.向BaCl 溶液中通入SO 气体:Ba2++SO+H O=BaSO↓+2H+
2 2 2 2 3
B.Cu和浓HNO 反应生成NO 气体:Cu+4H++2 =Cu2++2NO↑+2H O
3 2 2 2
C.Ba(OH) 溶液中通入过量CO:OH-+CO =
2 2 2
D.少量碳酸氢钠溶液与足量澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
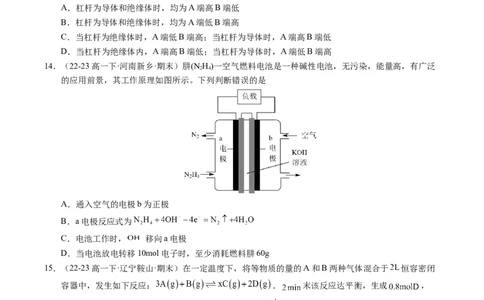
7.(22-23高一下·湖南岳阳·期末)下面是几种常见的化学电源示意图,有关说法不正确的是
A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,锌筒被破坏
C.铅蓄电池在工作中,负极每消耗 铅,则硫酸溶液中就转移 电子
D.氢氧燃料电池具有清洁、安全、高效等特点
8.(23-24高一上·广东东莞·期中)下列各组离子在给定条件下能大量共存的是
A.在常温pH=1的溶液中:NH 、Fe2+、 、
B.有 存在的溶液中:Na+、Mg2+、Ca2+、Br-
C.能使酚酞溶液变红的溶液中:Na+、Ba2+、Cl-、
D.无色透明的水溶液中:K+、Fe3+、Cl-、
9.(22-23高一下·河南开封·期末)下列有关化学反应速率或限度的说法中正确的是A.常温下,Al片分别与浓硝酸和稀硝酸接触2min,与浓硝酸接触收集的气体更多
B.铝片与过量的稀硫酸反应,加入 溶液可减缓速率且不影响 的产量
C.用双氧水制氧气时,加入少量 粉末可显著加快反应速率
D.工业合成氨时,使用过量的氮气、有可能使 的转化率达到100%
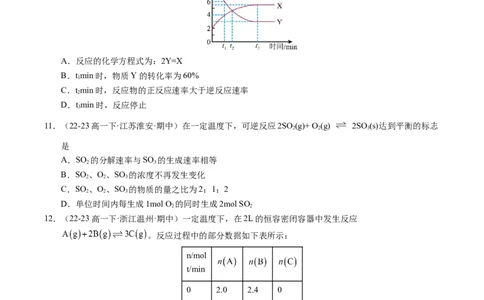
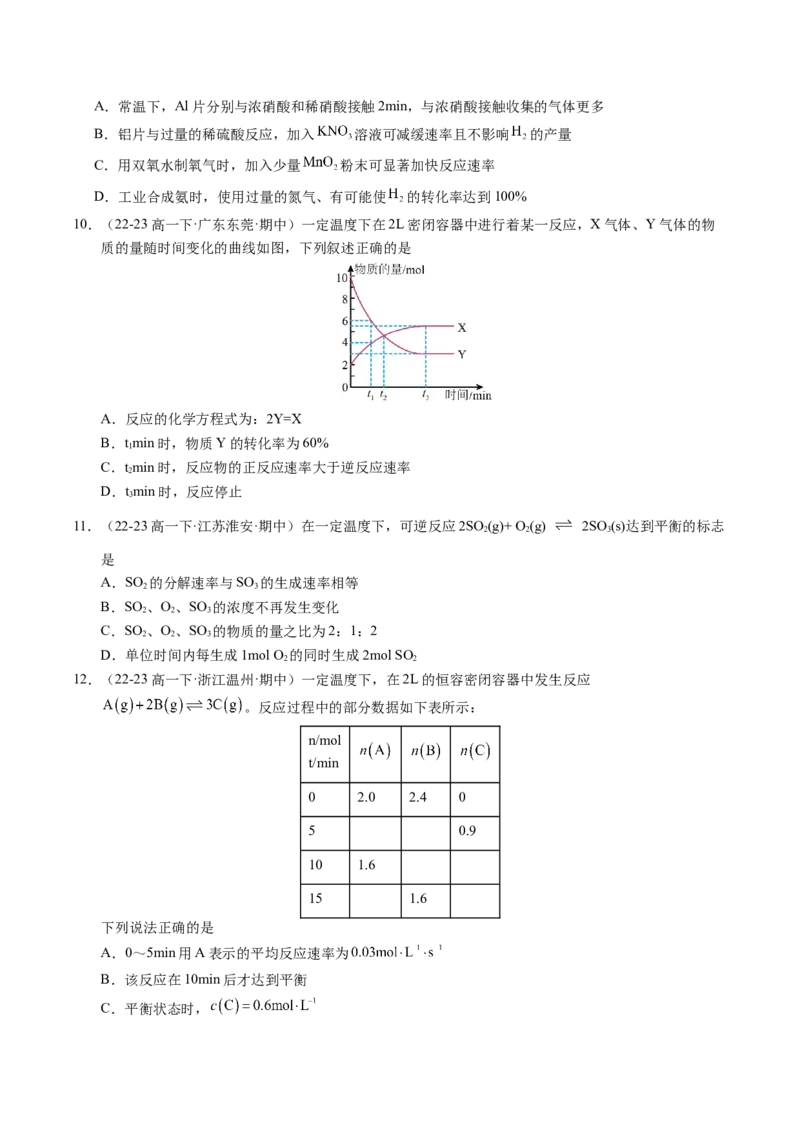
10.(22-23高一下·广东东莞·期中)一定温度下在2L密闭容器中进行着某一反应,X气体、Y气体的物
质的量随时间变化的曲线如图,下列叙述正确的是
A.反应的化学方程式为:2Y=X
B.tmin时,物质Y的转化率为60%
1
C.tmin时,反应物的正反应速率大于逆反应速率
2
D.tmin时,反应停止
3
11.(22-23高一下·江苏淮安·期中)在一定温度下,可逆反应2SO (g)+ O (g) 2SO (s)达到平衡的标志
2 2 3
是
A.SO 的分解速率与SO 的生成速率相等
2 3
B.SO 、O、SO 的浓度不再发生变化
2 2 3
C.SO 、O、SO 的物质的量之比为2:1:2
2 2 3
D.单位时间内每生成1mol O 的同时生成2mol SO
2 2
12.(22-23高一下·浙江温州·期中)一定温度下,在2L的恒容密闭容器中发生反应
。反应过程中的部分数据如下表所示:
n/mol
t/min
0 2.0 2.4 0
5 0.9
10 1.6
15 1.6
下列说法正确的是
A.0~5min用A表示的平均反应速率为
B.该反应在10min后才达到平衡
C.平衡状态时,D.物质B的平衡转化率为20%
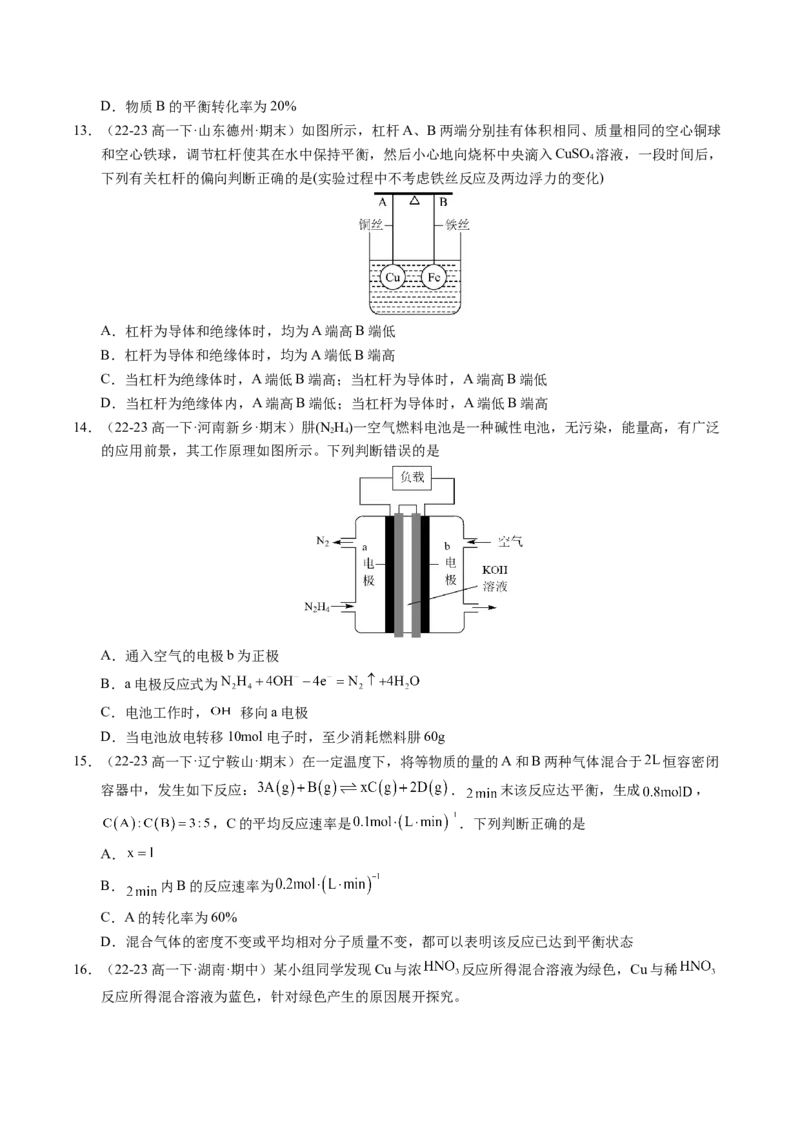
13.(22-23高一下·山东德州·期末)如图所示,杠杆A、B两端分别挂有体积相同、质量相同的空心铜球
和空心铁球,调节杠杆使其在水中保持平衡,然后小心地向烧杯中央滴入CuSO 溶液,一段时间后,
4
下列有关杠杆的偏向判断正确的是(实验过程中不考虑铁丝反应及两边浮力的变化)
A.杠杆为导体和绝缘体时,均为A端高B端低
B.杠杆为导体和绝缘体时,均为A端低B端高
C.当杠杆为绝缘体时,A端低B端高;当杠杆为导体时,A端高B端低
D.当杠杆为绝缘体内,A端高B端低;当杠杆为导体时,A端低B端高
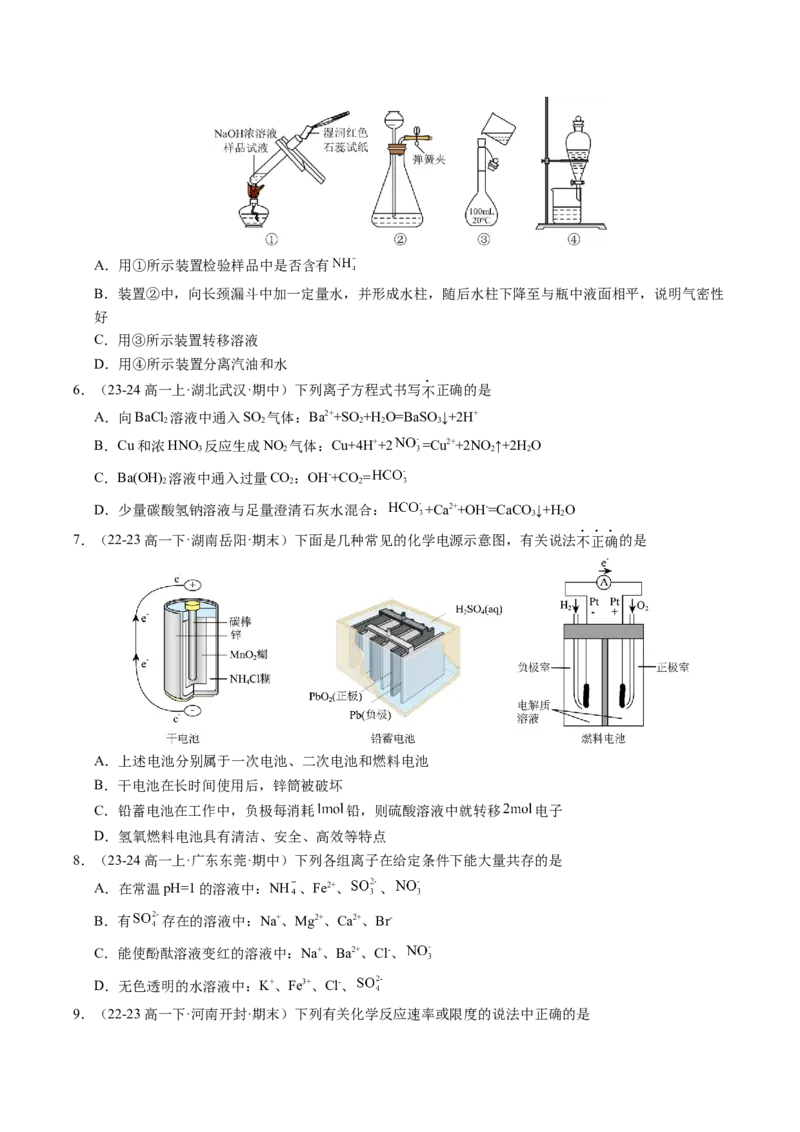
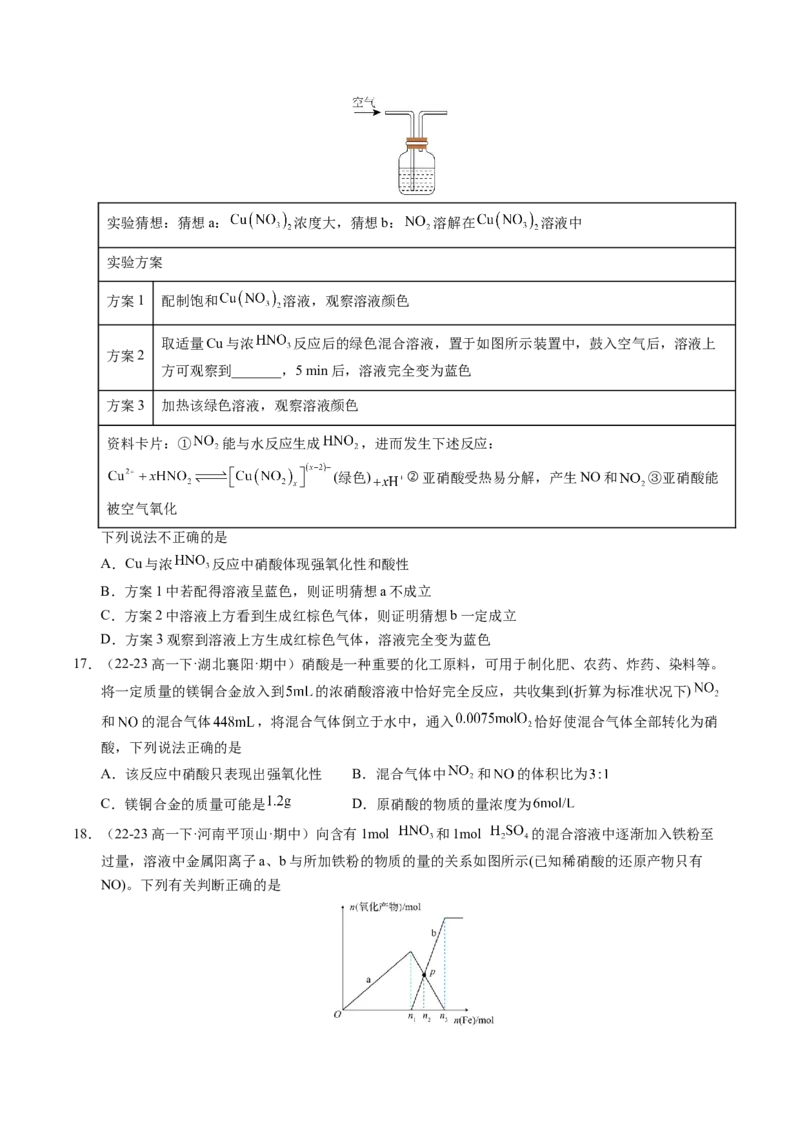
14.(22-23高一下·河南新乡·期末)肼(N H)一空气燃料电池是一种碱性电池,无污染,能量高,有广泛
2 4
的应用前景,其工作原理如图所示。下列判断错误的是
A.通入空气的电极b为正极
B.a电极反应式为
C.电池工作时, 移向a电极
D.当电池放电转移10mol电子时,至少消耗燃料肼60g
15.(22-23高一下·辽宁鞍山·期末)在一定温度下,将等物质的量的A和B两种气体混合于 恒容密闭
容器中,发生如下反应: . 末该反应达平衡,生成 ,
,C的平均反应速率是 .下列判断正确的是
A.
B. 内B的反应速率为
C.A的转化率为60%
D.混合气体的密度不变或平均相对分子质量不变,都可以表明该反应已达到平衡状态
16.(22-23高一下·湖南·期中)某小组同学发现Cu与浓 反应所得混合溶液为绿色,Cu与稀
反应所得混合溶液为蓝色,针对绿色产生的原因展开探究。实验猜想:猜想a: 浓度大,猜想b: 溶解在 溶液中
实验方案
方案1 配制饱和 溶液,观察溶液颜色
取适量Cu与浓 反应后的绿色混合溶液,置于如图所示装置中,鼓入空气后,溶液上
方案2
方可观察到_______,5 min后,溶液完全变为蓝色
方案3 加热该绿色溶液,观察溶液颜色
资料卡片:① 能与水反应生成 ,进而发生下述反应:
(绿色) ②亚硝酸受热易分解,产生NO和 ③亚硝酸能
被空气氧化
下列说法不正确的是
A.Cu与浓 反应中硝酸体现强氧化性和酸性
B.方案1中若配得溶液呈蓝色,则证明猜想a不成立
C.方案2中溶液上方看到生成红棕色气体,则证明猜想b一定成立
D.方案3观察到溶液上方生成红棕色气体,溶液完全变为蓝色
17.(22-23高一下·湖北襄阳·期中)硝酸是一种重要的化工原料,可用于制化肥、农药、炸药、染料等。
将一定质量的镁铜合金放入到 的浓硝酸溶液中恰好完全反应,共收集到(折算为标准状况下)
和 的混合气体 ,将混合气体倒立于水中,通入 恰好使混合气体全部转化为硝
酸,下列说法正确的是
A.该反应中硝酸只表现出强氧化性 B.混合气体中 和 的体积比为
C.镁铜合金的质量可能是 D.原硝酸的物质的量浓度为
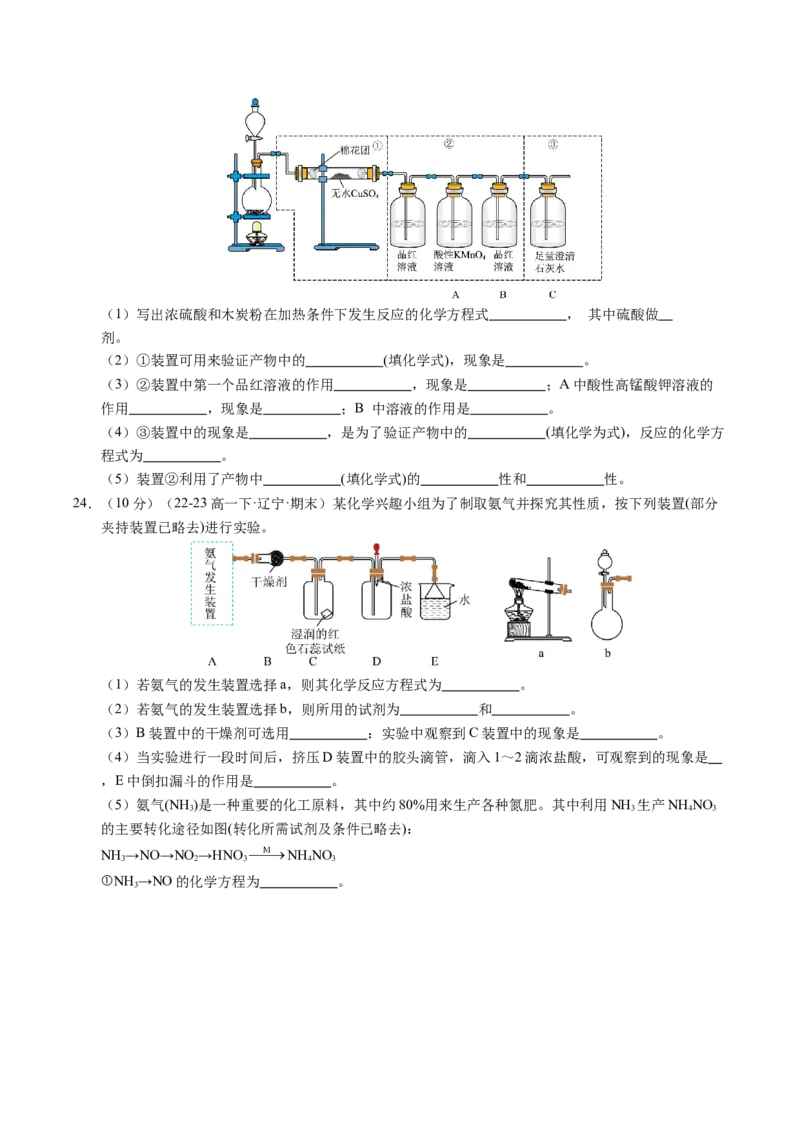
18.(22-23高一下·河南平顶山·期中)向含有1mol 和1mol 的混合溶液中逐渐加入铁粉至
过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有
NO)。下列有关判断正确的是A. B.a表示 的关系曲线
C.P点时, D.向P点溶液中加入铜粉,最多可溶解14.4g
19.(22-23高一下·河北衡水·期中)某学习小组为了探究酸性高锰酸钾溶液与NaHSO 溶液反应速率的影
3
响因素,该小组设计如下实验方案。
0.2 mol·L-1 0.1 mol·L-1 0. 1 mol·L-1
0.6 mol·L-1 混合溶液褪
实验 NaHSO 溶 KMnO 溶 MnSO 溶 V(H O)/mL
3 4 4 2
HSO 溶液/mL 色时间/min
2 4
液/mL 液/mL 液/mL
1 3.0 2.0 1.0 0 2.0 8
2 3.0 2.0 2.0 0 a 6
3 4.0 2.0 2.0 0 0 4
4 3.0 2.0 1.0 0.5 b 3
下列说法错误的是
A.该反应的离子方程式为
B.实验3从反应开始到反应结束这段时间内反应速率v(MnO -)=0.0625mol·L-1·min-1
4
C.a=1.0、b=1.5
D.实验4与实验1相比,说明Mn2+可能是该反应的催化剂
20.(22-23高一下·河南郑州·期中)关于如图的微生物原电池相关叙述中错误的是
A.电池工作时,电流由a流向b
B.微生物所在电极区放电时发生氧化反应
C.放电过程中,H+穿过质子交换膜向右侧迁移
D.正极反应式为:MnO +4H++2e-=Mn2++2H O
2 2
第 II 卷(非选择题 共 40 分)
三、非选择题:本题共4个大题,共40分。
21.(10分)(22-23高一下·吉林辽源·期末)一定温度下,在 的密闭容器中, 两种气体的物质
的量随时间变化的曲线如图所示:(1)反应的化学方程式为 。
(2)反应达到最大限度的时间是 ,该时间内的平均反应速率 ,N
的转化率为 。
(3)判断该反应达到平衡状态的依据是___________(填序号)
A.该条件下,正、逆反应速率都为零
B.该条件下,混合气体的密度不再发生变化
C.该条件下,混合气体的压强不再发生变化
D.该条件下,单位时间内消耗 的同时,消耗
(4)能加快反应速率的措施是_________(填序号)
A.升高温度
B.容器容积不变,充入惰性气体
C.容器压强不变,充入惰性气体
D.使用催化剂
22.(10分)(22-23高一下·河北衡水·期末)根据原电池原理,人们研制出性能各异的化学电池。
(1)锌铜原电池装置示意图如图所示,Zn片作 (填“正极”或“负极”)。
(2)铜片上观察到的实验现象是 ,锌片上的电极反应式为 。
(3)电流表指针发生偏转,说明该装置实现了化学能向 的转化。
(4)若把反应 仿照上图设计成原电池,则两个电极分别为铜、 (填材料
名称),电解质溶液为 (填化学式)。
(5)镁、海水、溶解氧可构成原电池,为水下小功率设备长时间供电,结构示意图如图所示,其总
反应为: 。下列说法正确的是 (填字母序号)。
a.Mg作电池的负极 b. 发生氧化反应
23.(10分)(22-23高一下·上海徐汇·期末)如图所示虚线框中的装置可用来检验浓硫酸与木炭粉在加热
条件下反应产生的所有气体产物。填写下列空白:(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式 , 其中硫酸做
剂。
(2)①装置可用来验证产物中的 (填化学式),现象是 。
(3)②装置中第一个品红溶液的作用 ,现象是 ;A中酸性高锰酸钾溶液的
作用 ,现象是 ;B 中溶液的作用是 。
(4)③装置中的现象是 ,是为了验证产物中的 (填化学为式),反应的化学方
程式为 。
(5)装置②利用了产物中 (填化学式)的 性和 性。
24.(10分)(22-23高一下·辽宁·期末)某化学兴趣小组为了制取氨气并探究其性质,按下列装置(部分
夹持装置已略去)进行实验。
(1)若氨气的发生装置选择a,则其化学反应方程式为 。
(2)若氨气的发生装置选择b,则所用的试剂为 和 。
(3)B装置中的干燥剂可选用 :实验中观察到C装置中的现象是 。
(4)当实验进行一段时间后,挤压D装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
,E中倒扣漏斗的作用是 。
(5)氨气(NH )是一种重要的化工原料,其中约80%用来生产各种氮肥。其中利用NH 生产NH NO
3 3 4 3
的主要转化途径如图(转化所需试剂及条件已略去):
NH →NO→NO →HNO NH NO
3 2 3 4 3
①NH →NO的化学方程为 。
3