文档内容
下学期期中模拟考试 01
高二化学
时间:75分钟 满分:100分 测试范围:选必2+选必3第1~3章第4节
可能用到的相对原子质量:H 1 C 12 B 11 N 14 O 16 Na 23
第Ⅰ卷(选择题 共 48 分)
一、选择题:本题共16个小题,每小题3分,共48分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.悠久的历史创造了灿烂的华夏文明。下列文化典籍中标注的物品不涉及有机物的是
A.凡酿酒必资曲药成信 B.收取种茧……近上则丝薄,近地则子不生也
C.镇戎军有一铁甲……强弩射之,不能入 D.松脂出陇西,松胶者善
【答案】C
【解析】A.酒的主要成分为乙醇,属于有机物,A不符合题意;
B.蚕丝的主要成分是蛋白质,属于有机物,B不符合题意;
C.铁甲的主要成分是铁,含有少量的碳,它们都属于无机物,C符合题意;
D.松脂的主要成分是油脂,属于有机物,D不符合题意;
故选C。
2.化学与科技、生活密切相关,下列说法正确的是
A.航天器使用的太阳能电池帆板的主要成分是
B.现代化学常利用原子光谱的特征谱线来鉴定元素
C.通过红外光谱仪可以测定分子的相对分子质量
D.焰火、激光都与原子核外电子跃迁吸收能量有关
【答案】B
【解析】A.太阳能电池帆板的主要成分是Si单质,故A错误;
B.不同元素原子的吸收光谱或发射光谱不同,常利用原子光谱的特征谱线可以鉴定元素,故B正确;
C.通过红外光谱仪可以测定分子中的官能团和化学键,通过质谱仪可以测定分子的相对分子质量,故C
错误;
D.焰火、激光都与原子核外电子跃迁释放能量有关,故D错误;
选B。
3.下列哪种电子排布不属于激发态
A. B.
C. D.
【答案】C4.下列关于原子结构及元素周期表的说法错误的是
A.所含元素种类最多的族是第ⅢB族
B.同一原子中,2p、3p、4p能级的能量依次升高
C.在元素周期表中,ds区只有6种自然形成的元素,且均为金属元素
D.基态原子价层电子排布式为ns2的元素一定是第IIA族元素(n为周期数)
【答案】D
【解析】A.所含元素种类最多的族是第ⅢB族,共有32种元素,故A正确;
B.同一原子中,能级的能量:2p<3p<4p,因此2p、3p、4p能级的能量依次升高,故B正确;
C.在元素周期表中,ds区只有6种自然形成的元素(4、5、6三个周期,每个周期2种元素共6种),且均
为金属元素,故C正确;
D.基态原子价层电子排布式为ns2的元素可能为第IIA族元素(n为周期数),也可能是0族元素(比如He),
故D错误。
综上所述,答案为D。
5.下列有关化学用语表示正确的是
A.CSO的电子式: B.甲烷分子的球棍模型:
C.原子核内有20个中子的氯原子:20 Cl D.HClO分子的结构式:H-Cl-O
17
【答案】A
【解析】A.CSO中C原子分别与S、O原子形成2对共用电子对,故CSO的电子式为 ,A正
确;
B.甲烷分子的比例模型是: ,B错误;
C.原子核内有20个中子的氯原子,质量数是37,故表示为: ,C错误;
D. HClO分子中O原子分别与H、Cl原子形成共价键,结构式:H-O-Cl,D错误;
故合理选项是A。
6.下列实验中,所采取的分离或提纯方法与对应原理都正确的是
选项 实验目的 分离或提纯方法 原理
A 分离食用油和汽油 分液 食用油和汽油的密度不同
B 分离溶于水中的溴 乙醇萃取 溴在乙醇中的溶解度较大
C 除去乙烷中的乙烯 通过酸性KMnO 溶液洗 乙烯与酸性KMnO 溶液反
4 4气 应
D 除去碘中的NaCl 加热、升华 NaCl的熔点高,碘易升华
【答案】D
【解析】A.汽油和食用油互溶,不能分液分离,应选蒸馏法,A错误;
B.乙醇与水互溶,则乙醇不能作萃取剂,B错误;
C.乙烯被酸性高锰酸钾溶液氧化生成二氧化碳,引入新杂质,不能除杂,C错误;
D.碘受热易升华,NaCl受热难升华,则可以通过加热的方法分离,D正确;
故答案为:D。
7.含氯、硫、磷等元素的化合物是重要的化工原料,有关比较中不正确的是
A.原子半径:P > S > Cl B.第一电离能:P < S < Cl
C.电负性: P < S < Cl D.最简单氢化物的热稳定性:P < S < Cl
【答案】B
【解析】A.同周期元素,从左到右,原子半径逐渐减小,所以原子半径:P > S > Cl,故A正确;
B.P核外电子排布为半充满稳定结构,第一电离能大于S,故B错误;
C.同周期元素,从左到右,远点复兴逐渐增大,所以电负性: P < S < Cl,故C正确;
D.元素非金属性越强,最简单氢化物越稳定,所以最简单氢化物的热稳定性:P < S < Cl,故D正确;
答案选B。
8.价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是
A. 和 的VSEPR模型均为四面体
B. 和 的空间构型均为三角锥形
C. 和 均为非极性分子
D. 与 的键角相等
【答案】B
【解析】A. 中P的价层电子对数为: ,VSEPR模型为三角双锥, 种O原子的价层电子
对数为: ,VSEPR模型为四面体,A错误;
B. 中S原子的价层电子对数为: ,空间构型为三角锥形, 中Cl原子的价层电子对数为:
,空间构型为三角锥形,B正确;
C. 中C原子的价层电子对为: ,正四面体构型,为非极性分子, 中S原子的价层电子对
为: ,空间构型不对称,为极性分子,C错误;D. 中Xe的价层电子对数为: , 中Sn的价层电子对数为: ,两者键角不相等,
D错误;
故选B。
9.已知 As与 P位于同一主族。下列说法正确的是
33 15
A.酸性:HAsO < H PO < H SO
3 4 3 4 2 4
B.第一电离能:As < P < S
C.As在元素周期表中位于第五周期VA族
D.沸点:AsH > PH > NH
3 3 3
【答案】A
【解析】A.由于非金属性:S>P>As,故最高价氧化物对应水化物酸性: ,A项正
确;
B.同周期从左到右第一电离能逐渐增大,第五主族最外层半充满结构,比较稳定,第一电离能出现反常,
则P >S,同主族从上到下,第一电离能逐渐减小,则P>As,即第一电离能:As < S < P,B项错误;
C.As在元素周期表中位于第四周期VA族,C项错误;
D. 含有氢键,沸点最高, 都不含氢键,相对分子质量越大,沸点越高,故沸点:
,D项错误;
答案选A。
10.学会分类使化学学习事半功倍。下列关于有机化合物的分类正确的是
A. 属于脂环化合物 B. 属于芳香烃
C. 属于链状化合物 D. 属于烃的衍生物
【答案】D
【解析】A.脂环化合物是有机化学分类通过碳骨架排列不同所得到的一类有机化合物。其分子中含有由
3个或者3个以上碳原子连接成的碳环,该分子中的环中含有O、B原子,故不属于脂环化合物,A错误;
B.分子中含有氮原子,不属于烃类,B错误;
C.分子中含有碳环,属于环状化合物,C错误;
D.分子含有N、O、Br原子,属于烃的衍生物,D正确;
故选D。11. 是一种有机烯醚,可以用烃A通过下列路线制得:
则下列说法正确的是( )
A. 的分子式为C HO
4 4
B.A的结构简式是CH=CHCHCH
2 2 3
C.①②③的反应类型分别为卤代、水解、消去
D.A能使酸性高锰酸钾酸性溶液褪色
【答案】D
【分析】醇羟基之间脱水可生成醚键,因此由 可知C的结构简式为HOCH CH=CHCH OH;由
2 2
A(烃)生成B,显然发生的是加成反应,B的结构中含有2个Br原子;那么由B生成C即发生卤代烃的水
解反应,由C的结构可得B的结构简式为BrCHCH=CHCH Br,所以A为1,3-丁二烯;由A生成B,发生
2 2
的是1,3-丁二烯的1,4-加成反应。
【解析】A.由 的结构可知,其不饱和度为2,分子式为C HO,A项错误;
4 6
B.通过分析可知,A为1,3-丁二烯,其结构简式为CH=CH-CH=CH ,B项错误;
2 2
C.通过分析可知,反应①为加成反应,反应②为水解反应,反应③为取代反应,C项错误;
D.通过分析可知,A为1,3-丁二烯,分子结构中含有碳碳双键,可以使酸性高锰酸钾溶液褪色,D项正确;
答案选D。
【点睛】由有机物的结构书写其分子式时,可以先判断有机物的不饱和度,再根据不饱和度的计算公式,
计算分子式中H的个数。
12.下列卤代烃中,既能发生取代反应又能发生消去反应的是
A.CHCl B.CHCHCHBr
3 3 2 2
C. D.
【答案】B
【解析】A.CHCl分子中含有Cl原子,属于卤代烃,在碱性条件下能够发生取代反应;由于Cl原子连接
3
的C原子无邻位C原子,因此不能发生消去反应,A不符合题意;B.CHCHCHBr分子中含有Br原子,属于卤代烃,在碱性条件下能够发生取代反应;由于Br原子连接
3 2 2
的C原子有邻位C原子,且邻位C原子上有H原子,因此也能发生消去反应,B符合题意;
C.该物质分子中含有Cl原子,属于卤代烃,在碱性条件下能够发生取代反应;由于Cl原子取代对二甲苯
的甲基上的H原子,苯环具有特殊的稳定性,因此不能发生消去反应,C不符合题意;
D.该物质分子中含有Br原子,属于卤代烃,能够在碱性条件下发生取代反应;由于Br原子连接的C原
子有邻位C原子,但邻位C原子上没有H原子,因此不能发生消去反应,D不符合题意;
故合理选项是B。
13.某有机物可发生下列变化
已知C为羧酸,且C、E均不发生银镜反应,则A的可能结构有
A.1种 B.2种 C.3种 D.4种
【答案】B
【分析】A 能在碱性条件下反应生成 B 和 D , B 与酸反应,应为盐, D 能在 Cu 催化作用下发生氧
化,应为醇,则 A 应为酯, C 和 E 都不能发生银镜反应,说明 C 、 E 不含醛基,如 C 为乙酸,则
D 为 CHCHOHCH CH ,如 C 为丙酸,则 D 为 CHCHOHCH ,据此进行解答。
3 2 3 3 3
【解析】A 的分子式为 C H O, A 能在碱性条件下反应生成 B 和 D , B 与酸反应, B 应为盐,
6 12 2
D 能在 Cu 催化作用下发生氧化, D 应为醇,则 A 属于酯, C 和 E 都不能发生银镜反应,说明 C
、 E 不含醛基,则 C 不可能为甲酸,
若 C 为乙酸,则 D 为 CHCH(OH)CHCH,
3 2 3
若 C 为丙酸,则 D 为 CHCH(OH)CH,
3 3
若 C 为丁酸,则 D 为乙醇、 E 为乙醛,不可能,
所以 A 只能为: CHCOOCH(CH) CHCH 或CHCHCOO CH(CH),总共有两种可能的结构,
3 3 2 3 3 2 2 3 2
答案选 B。
【点睛】本题考查有机物的推断,题目难度不大,本题注意 C和 E都不能发生银镜反应的特点,为解答
该题的关键,以此推断对应的酸或醇的种类和推断出 A 的可能结构。
14.益母草中的提取物益母草碱具有活血化瘀、利水消肿的作用,其分子结构如图。下列说法不正确的是
A.存在3种含氧官能团 B.能发生取代、加成和氧化反应
C.既能与NaOH溶液反应又能与盐酸反应 D.分子中N原子的杂化方式都是sp3
【答案】D【解析】A.益母草碱中存在醚键、酚羟基和酯基3种含氧官能团,选项A正确;
B.益母草碱中存在酯基、氨基可发生取代反应,碳氮双键及苯环可发生加成反应,酚羟基易发生氧化反
应,选项B正确;
C.益母草碱中存在酚羟基及酯基,能与氢氧化钠溶液反应,含有氨基,能与盐酸反应,选项C正确;
D.分子中N原子有两个只含有单键,杂化方式为sp3,但有一个氮原子存在碳氮双键,杂化方式为sp2,
选项D不正确;
答案选D。
15.下列实验方案设计、现象和结论都正确的是
选项 方案设计 现象和结论
将CHCHCHCl与NaOH水溶液共热,
3 2 2
A 有沉淀产生,说明CHCHCHCl发生了水解
3 2 2
冷却后,取少量溶液,加入AgNO 溶液
3
葡萄糖溶液用硝酸酸化后加入新制氢氧
B 未产生砖红色沉淀,说明葡萄糖分子中不含有醛基
化铜并加热
C 往苯酚钠溶液中通入CO 溶液变浑浊,说明苯酚的酸性比碳酸弱
2
往CH=CHCHO溶液中滴加酸性高锰酸 酸性高锰酸钾溶液褪色,说明含有碳碳双键的有机
2
D
钾溶液 物能使酸性高锰酸钾溶液褪色
【答案】C
【解析】A.NaOH溶液会与AgNO₃溶液反应产生沉淀,不能确定CH₃CH₂CH₂Cl是否发生水解,故A错
误;
B.稀硝酸会与新制氢氧化铜反应,干扰实验,不能确定葡萄糖分子中是否含有醛基,故B错误;
C.往苯酚钠溶液中通入CO,两者反应生成的苯酚微溶于水使溶液变浑浊,原理是较强酸制备较弱酸,
2
能说明苯酚的酸性比碳酸弱,故C正确;
D.醛基也能使酸性高锰酸钾溶液褪色,故D错误;
故选C。
16.2-甲基-2-氯丙烷是重要的化工原料,实验室中可由叔丁醇与浓盐酸反应制备,路线如下:
下列说法不正确的是
A.叔丁醇的系统命名为2-甲基-2-丙醇
B.无水CaCl 的作用是除去有机相中残存的少量水
2
C.进行操作1时,用到的玻璃仪器有漏斗、烧杯、玻璃棒D.蒸馏时产物比叔丁醇先蒸馏出来
【答案】C
【分析】叔丁醇与浓盐酸反应生成2-甲基-2-氯丙烷和水,分液后向有机相中加入水进行洗涤分液,继续向
有机相中加入5%的碳酸钠溶液洗涤分液,再次向有机相中加入水进行洗涤分液,由于有机物2-甲基-2-氯
丙烷的密度小于水,分液后获得上层有机相,有机相中加入少量无水氯化钙干燥,蒸馏即得到有机物2-甲
基-2-氯丙烷。
【解析】A.叔丁醇的系统命名为2-甲基-2-丙醇,A正确;
B.无水氯化钙能吸收有机相中残留的水,从而使蒸馏时得到纯净的2-甲基-2-氯丙烷,B正确;
C.操作1为分液,需要用到的玻璃仪器有分液漏斗、烧杯,C错误;
D.2-甲基-2-氯丙烷比叔丁醇的沸点低,蒸馏时先得到产物2-甲基-2-氯丙烷,D正确;
故答案选C。
第 II 卷(非选择题 共 52 分)
二、非选择题:本题共4个大题,共52分。
17.(14分)X、Y、Z、W、Q五种元素,它们在周期表中的相对位置如下表所示(虚线部分表示省略了
部分族),回答下列问题:
(1)已知元素的第一电离能X>Y,则X原子最高能级电子云轮廓图是 形状;Y的简单氢化物中,Y
原子的杂化轨道类型为 。
(2)W核外电子有15种空间运动状态且电子运动状态数目最少,则W原子价层电子排布图为 ;五
种元素中,第一电离能最小的是元素 (填元素名称),X、Y、Q三种元素电负性由大到小的顺序为
(用元素符号表示)。
(3)Q形成的氢化物分子的空间结构为 ,ZY 中化学键类型为 。
2 2
【答案】(每空2分)
(1)哑铃形 sp3
(2) 钠 O>N>As
(3)三角锥形 共价键(或非极性共价键)、离子键
【分析】Z是第三周期第ⅠA族元素,Z是Na元素;X、Y是第二周期的元素,同周期元素从左到右第一
电离能有增大趋势,N原子2p能级半充满,结构稳定,第一电离能大于同周期相邻元素,第一电离能
X>Y,则X是N、Y是O元素;Q与N同主族,Q是As元素;W核外电子有15种空间运动状态且电子运
动状态数目最少,说明有15个原子轨道,且有6个未成对电子,则W是Cr元素。【解析】(1)X是N、Y是O元素,N原子最高能级是2p,电子云轮廓图是哑铃形;O的简单氢化物是
HO,O原子价电子对数为4,杂化轨道类型为sp3。
2
(2)W是Cr元素,Cr原子价层电子排布图为 ;金属性越强,
第一电离能越小,五种元素中,第一电离能最小的是元素钠;同周期元素从左到右电负性增大,同主族从
上到下电负性减小, N、O、As三种元素电负性由大到小的顺序为O>N>As;
(3)Q是As元素,形成的氢化物是AsH ,As原子价电子对数为4,有1个孤电子对,空间结构为三角锥
3
形,NaO 由Na+、 构成,化学键类型为离子键、共价键。
2 2
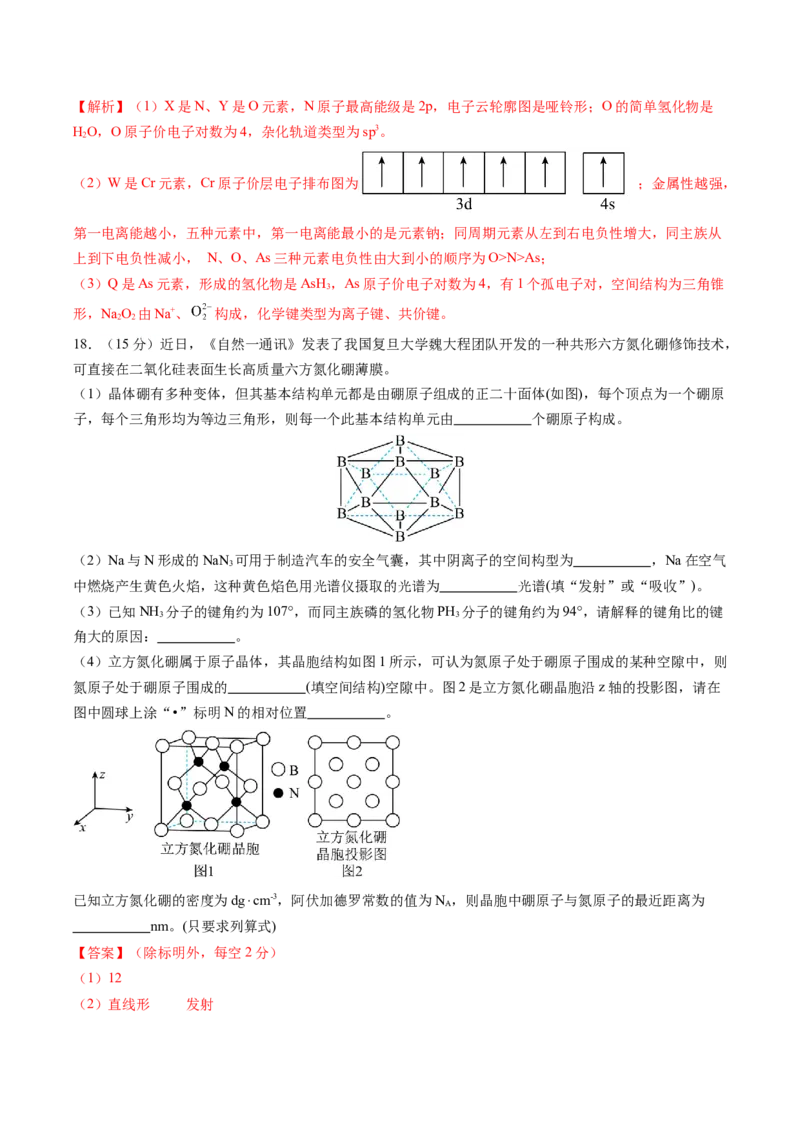
18.(15分)近日,《自然一通讯》发表了我国复旦大学魏大程团队开发的一种共形六方氮化硼修饰技术,
可直接在二氧化硅表面生长高质量六方氮化硼薄膜。
(1)晶体硼有多种变体,但其基本结构单元都是由硼原子组成的正二十面体(如图),每个顶点为一个硼原
子,每个三角形均为等边三角形,则每一个此基本结构单元由 个硼原子构成。
(2)Na与N形成的NaN 可用于制造汽车的安全气囊,其中阴离子的空间构型为 ,Na在空气
3
中燃烧产生黄色火焰,这种黄色焰色用光谱仪摄取的光谱为 光谱(填“发射”或“吸收”)。
(3)已知NH 分子的键角约为107°,而同主族磷的氢化物PH 分子的键角约为94°,请解释的键角比的键
3 3
角大的原因: 。
(4)立方氮化硼属于原子晶体,其晶胞结构如图1所示,可认为氮原子处于硼原子围成的某种空隙中,则
氮原子处于硼原子围成的 (填空间结构)空隙中。图2是立方氮化硼晶胞沿z轴的投影图,请在
图中圆球上涂“•”标明N的相对位置 。
已知立方氮化硼的密度为dg⋅cm-3,阿伏加德罗常数的值为N ,则晶胞中硼原子与氮原子的最近距离为
A
nm。(只要求列算式)
【答案】(除标明外,每空2分)
(1)12
(2)直线形 发射(3)N原子半径小于P,NH 中成键电子对离中心原子近,成键电子对之间的排斥作用强
3
(4)正四面体 (3分)
【解析】(1)每个顶点为一个硼原子,每个三角形均为等边三角形,根据均摊原则,每个面占用 个B
原子,则每一个此基本结构单元由 个硼原子构成。
(2) 与CO 属于等电子体,CO 是直线型分子, 的空间构型为直线形,Na在空气中燃烧产生黄色
2 2
火焰,这种黄色焰色是电子由高能级跃迁到低不能形成的发射光谱。
(3)N原子半径小于P,NH 中成键电子对离中心原子近,成键电子对之间的排斥作用强,所以NH 的键
3 3
角比PH 的键角大。
3
(4)根据图示,氮原子处于硼原子围成的正四面体空隙中。图2是立方氮化硼晶胞沿z轴的投影图,在图
中圆球上涂“•”标明N的相对位置为 。
根据均摊原则,晶胞中N原子数为4、B原子数为 ,立方氮化硼的密度为dg⋅cm-3,阿伏加
德罗常数的值为N ,则晶胞的边长为 ,则晶胞中硼原子与氮原子的最近距离为体对角线的
A
,硼原子与氮原子的最近距离为 nm。
19.(10分)有机物X(C HO)是一种应用最早、最广的药物之一,也是重要的合成中间体。有机物X的
9 8 4
仪器分析如下:
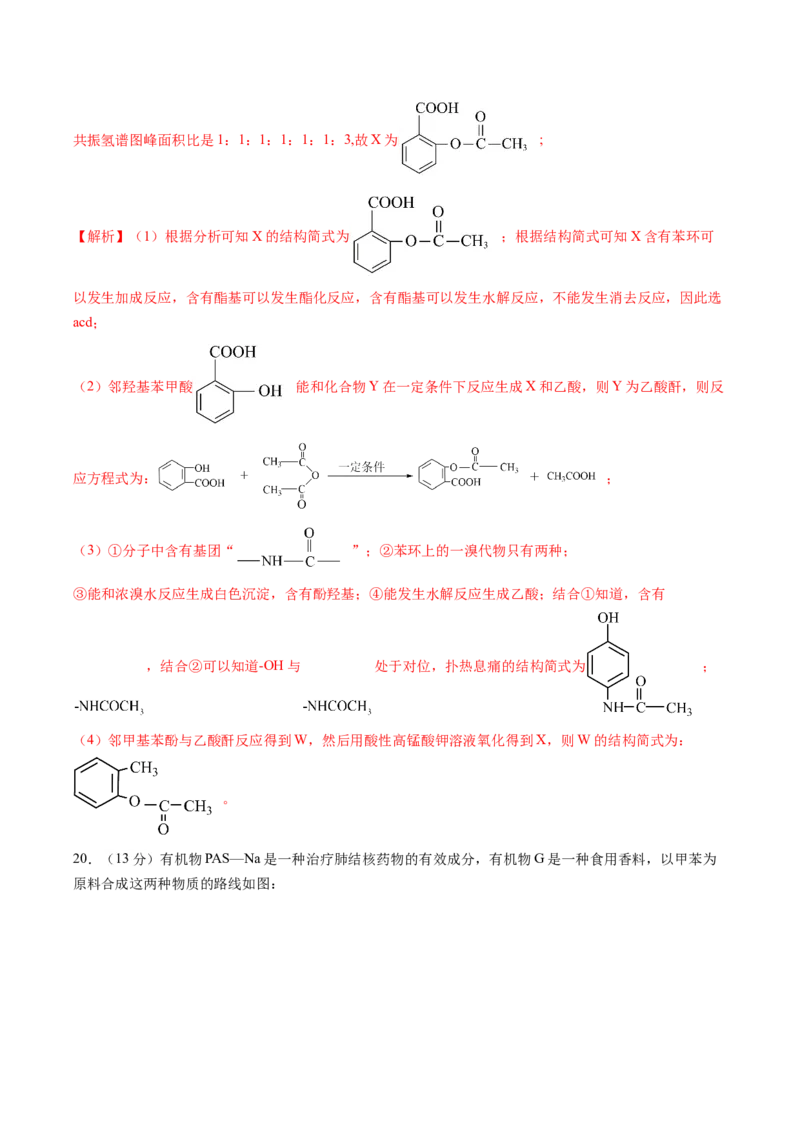
① 有机物X的红外光谱②有机物X的核磁共振氢谱图峰面积比是1:1:1:1:1:3
回答下列问题:
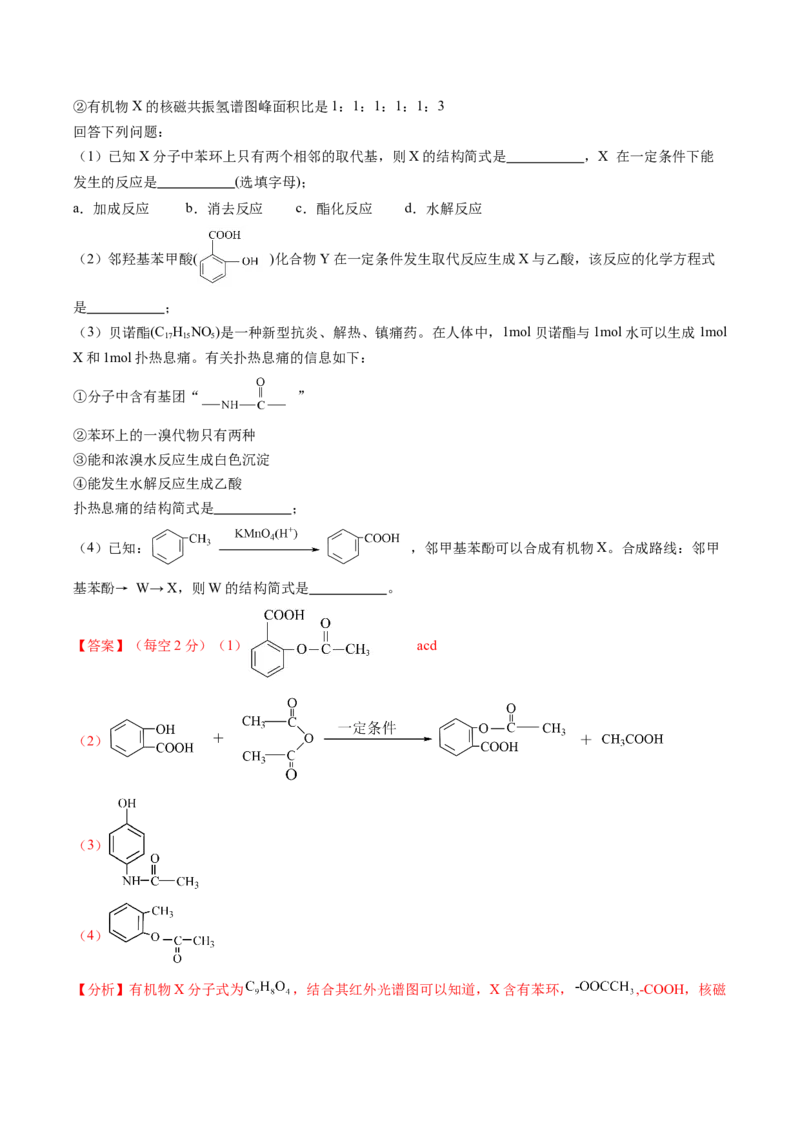
(1)已知X分子中苯环上只有两个相邻的取代基,则X的结构简式是 ,X 在一定条件下能
发生的反应是 (选填字母);
a.加成反应 b.消去反应 c.酯化反应 d.水解反应
(2)邻羟基苯甲酸( )化合物Y在一定条件发生取代反应生成X与乙酸,该反应的化学方程式
是 ;
(3)贝诺酯(C H NO )是一种新型抗炎、解热、镇痛药。在人体中,1mol贝诺酯与1mol水可以生成1mol
17 15 5
X和1mol扑热息痛。有关扑热息痛的信息如下:
①分子中含有基团“ ”
②苯环上的一溴代物只有两种
③能和浓溴水反应生成白色沉淀
④能发生水解反应生成乙酸
扑热息痛的结构简式是 ;
(4)已知: ,邻甲基苯酚可以合成有机物X。合成路线:邻甲
基苯酚→ W→ X,则W的结构简式是 。
【答案】(每空2分)(1) acd
(2)
(3)
(4)
【分析】有机物X分子式为 ,结合其红外光谱图可以知道,X含有苯环, ,-COOH,核磁共振氢谱图峰面积比是1:1:1:1:1:1:3,故X为 ;
【解析】(1)根据分析可知X的结构简式为 ;根据结构简式可知X含有苯环可
以发生加成反应,含有酯基可以发生酯化反应,含有酯基可以发生水解反应,不能发生消去反应,因此选
acd;
(2)邻羟基苯甲酸 能和化合物Y在一定条件下反应生成X和乙酸,则Y为乙酸酐,则反
应方程式为: ;
(3)①分子中含有基团“ ”;②苯环上的一溴代物只有两种;
③能和浓溴水反应生成白色沉淀,含有酚羟基;④能发生水解反应生成乙酸;结合①知道,含有
,结合②可以知道-OH与 处于对位,扑热息痛的结构简式为 ;
(4)邻甲基苯酚与乙酸酐反应得到W,然后用酸性高锰酸钾溶液氧化得到X,则W的结构简式为:
。
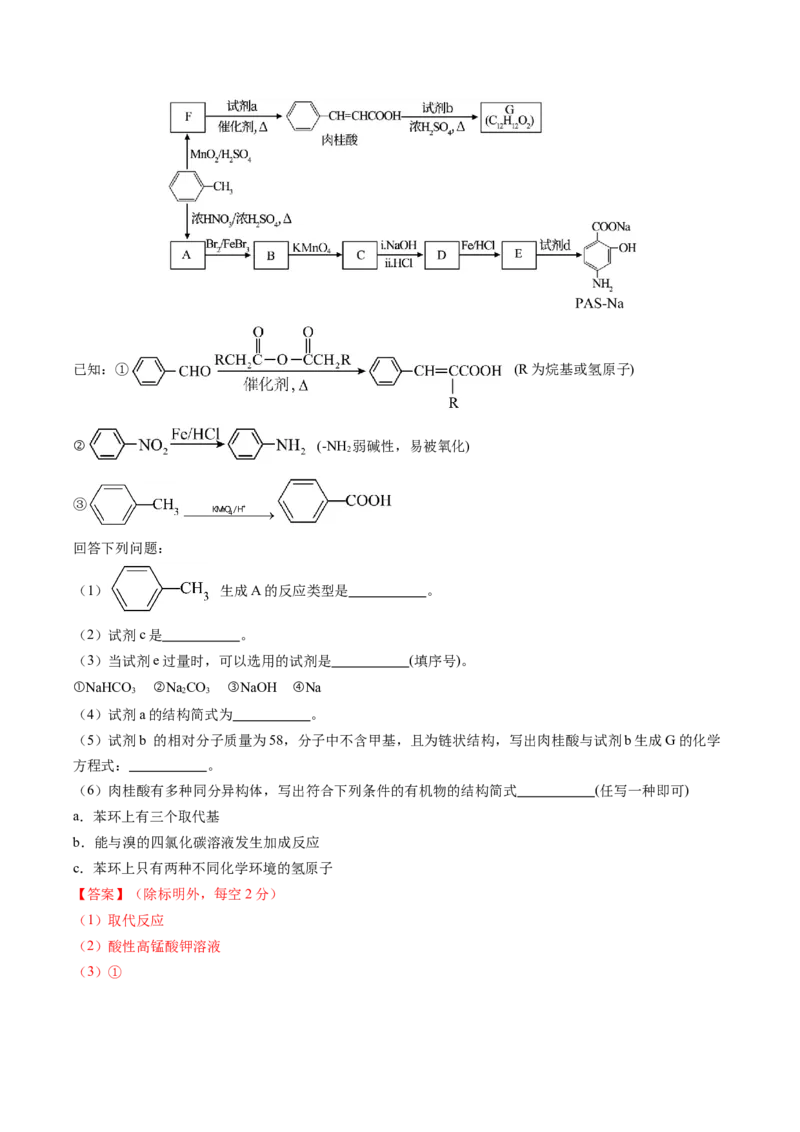
20.(13分)有机物PAS—Na是一种治疗肺结核药物的有效成分,有机物G是一种食用香料,以甲苯为
原料合成这两种物质的路线如图:已知:① (R为烷基或氢原子)
② (-NH 弱碱性,易被氧化)
2
③
回答下列问题:
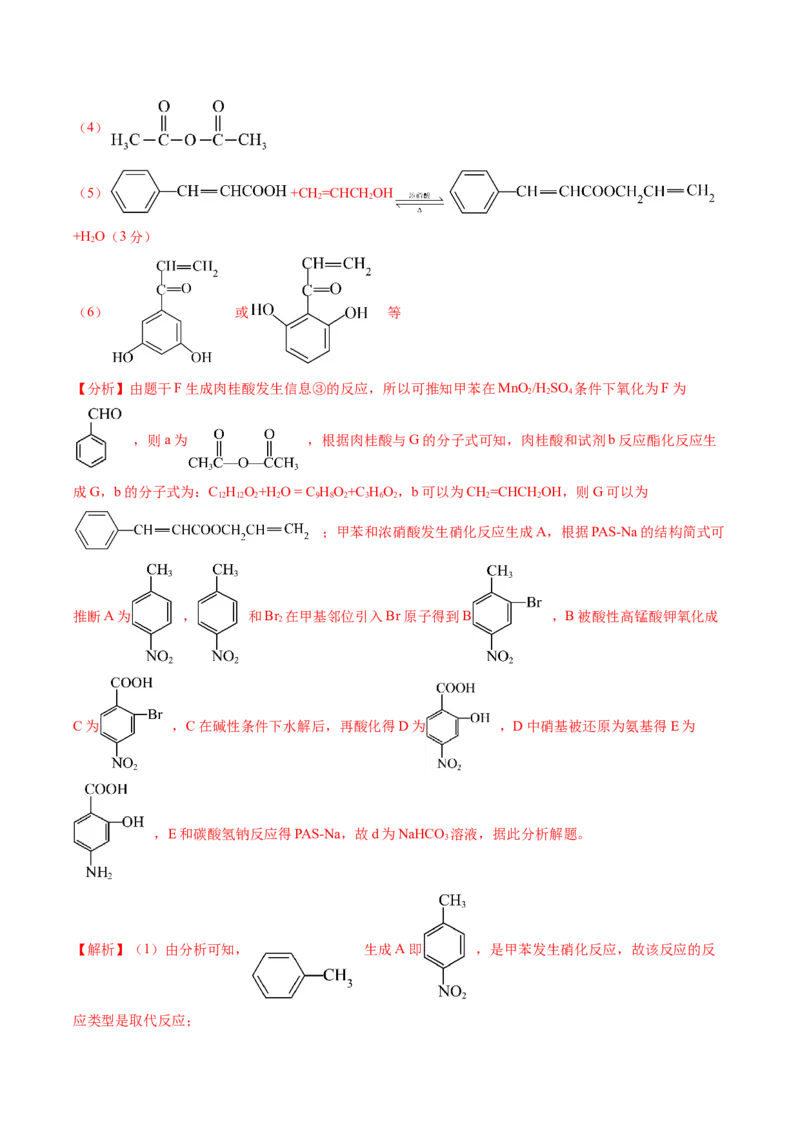
(1) 生成A的反应类型是 。
(2)试剂c是 。
(3)当试剂e过量时,可以选用的试剂是 (填序号)。
①NaHCO ②Na CO ③NaOH ④Na
3 2 3
(4)试剂a的结构简式为 。
(5)试剂b 的相对分子质量为58,分子中不含甲基,且为链状结构,写出肉桂酸与试剂b生成G的化学
方程式: 。
(6)肉桂酸有多种同分异构体,写出符合下列条件的有机物的结构简式 (任写一种即可)
a.苯环上有三个取代基
b.能与溴的四氯化碳溶液发生加成反应
c.苯环上只有两种不同化学环境的氢原子
【答案】(除标明外,每空2分)
(1)取代反应
(2)酸性高锰酸钾溶液
(3)①(4)
(5) +CH =CHCHOH
2 2
+H O(3分)
2
(6) 或 等
【分析】由题干F生成肉桂酸发生信息③的反应,所以可推知甲苯在MnO /H SO 条件下氧化为F为
2 2 4
,则a为 ,根据肉桂酸与G的分子式可知,肉桂酸和试剂b反应酯化反应生
成G,b的分子式为:C H O+H O = C HO+C HO,b可以为CH=CHCHOH,则G可以为
12 12 2 2 9 8 2 3 6 2 2 2
;甲苯和浓硝酸发生硝化反应生成A,根据PAS-Na的结构简式可
推断A为 , 和Br 在甲基邻位引入Br原子得到B ,B被酸性高锰酸钾氧化成
2
C为 ,C在碱性条件下水解后,再酸化得D为 ,D中硝基被还原为氨基得E为
,E和碳酸氢钠反应得PAS-Na,故d为NaHCO 溶液,据此分析解题。
3
【解析】(1)由分析可知, 生成A即 ,是甲苯发生硝化反应,故该反应的反
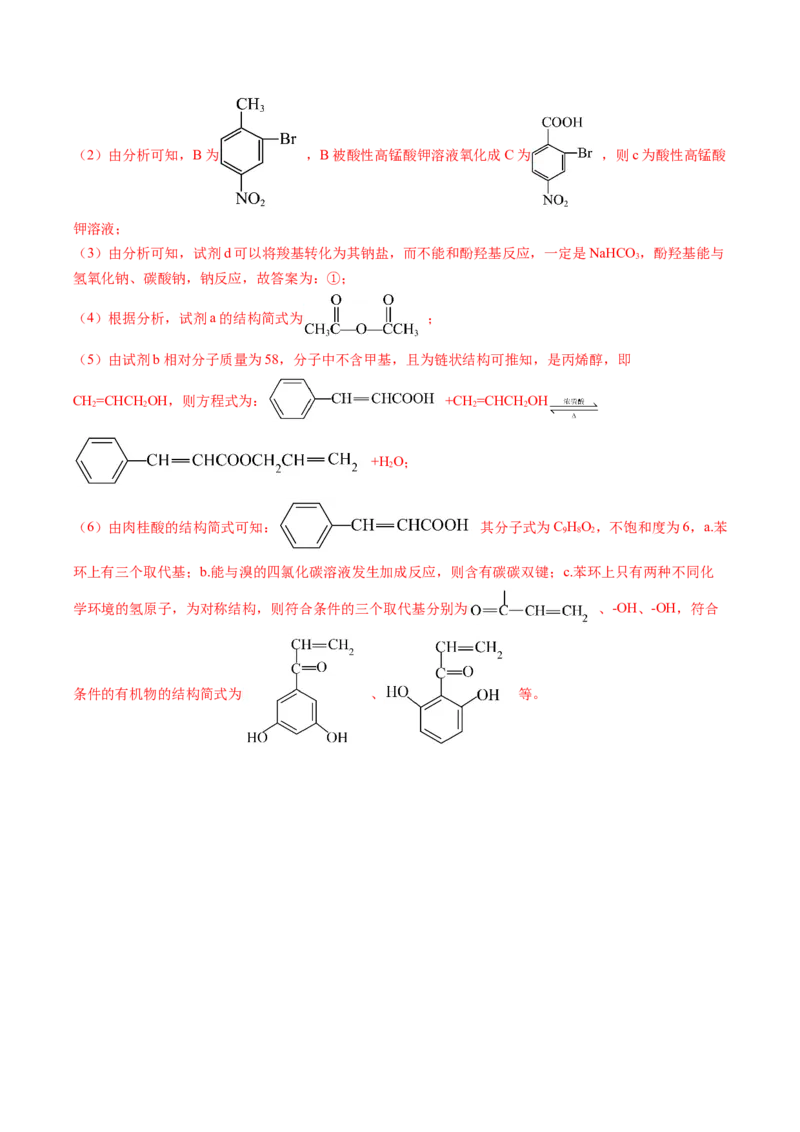
应类型是取代反应;(2)由分析可知,B为 ,B被酸性高锰酸钾溶液氧化成C为 ,则c为酸性高锰酸
钾溶液;
(3)由分析可知,试剂d可以将羧基转化为其钠盐,而不能和酚羟基反应,一定是NaHCO ,酚羟基能与
3
氢氧化钠、碳酸钠,钠反应,故答案为:①;
(4)根据分析,试剂a的结构简式为 ;
(5)由试剂b相对分子质量为58,分子中不含甲基,且为链状结构可推知,是丙烯醇,即
CH=CHCHOH,则方程式为: +CH =CHCHOH
2 2 2 2
+H O;
2
(6)由肉桂酸的结构简式可知: 其分子式为C HO,不饱和度为6,a.苯
9 8 2
环上有三个取代基;b.能与溴的四氯化碳溶液发生加成反应,则含有碳碳双键;c.苯环上只有两种不同化
学环境的氢原子,为对称结构,则符合条件的三个取代基分别为 、-OH、-OH,符合
条件的有机物的结构简式为 、 等。